Paul Eduardo Lada1 ID· Paula Frávega2 ID· Fabián Caballero3 ID· Martín Sánchez3 ID· Christian Janikow3 ID· Julián Martínez Peluaga3 ID· Selene Molina2 ID· Florencia Matcosky2 ID· María Rosa Defago4 ID
1Titular Encargado del Servicio de Cirugía General Sala 3/5 “Pablo Luis Mirizzi”. Hospital Nacional de Clínicas. UNC. Córdoba. Argentina.
2Residente de Cirugía General de la Sala 3/5 “Pablo Luis Mirizzi”. Hospital Nacional de Clínicas. UNC. Córdoba. Argentina.
3Profesor Asistente del Servicio de Cirugía General Sala 3/5 “Pablo Luis Mirizzi”. Hospital Nacional de Clínicas. UNC. Córdoba. Argentina.
4Servicio de Gastroenterología del Instituto Humana. Córdoba. Argentina.
Acta Gastroenterol Latinoam 2024;54(4):341-345
Recibido: 29/04/2024 / Aceptado: 11/11/2024 / Publicado online el 30/12/2024 /
https://doi.org/10.52787/agl.v54i4.411
Resumen
Introducción. La ganglioneuromatosis intestinal es una enfermad neoplásica benigna poco frecuente. Se describe en general en niños, en asociación con la neoplasia endocrina múltiple tipo 2b, en asociación con la neoplasia endocrina múltiple tipo 2b y la neurofibromatosis tipo 1. La ganglioneuromatosis es rara en adultos, en los que suele presentarse de forma esporádica y aislada. Caso clínico. Presentamos una paciente con ganglioneuromatosis intestinal, en la que los hallazgos clínicos y radiográficos iniciales simulaban una enfermedad de Crohn. Se realizó la resección de un segmento del intestino delgado debido a la oclusión de la cápsula endoscópica. El estudio inmunohistoquímico de dicho segmento sugirió el diagnóstico de ganglioneuroma. Conclusión. La presentación clínica de la ganglioneuromatosis intestinal es variable. El paciente puede ser oligosintomático o tener una presentación atípica. Este diagnóstico debe considerarse cuando se han excluido las causas más frecuentes de anemia por deficiencia de hierro. El diagnóstico definitivo es posible después de la resección y el análisis patológico del segmento involucrado.
Palabras claves. Ganglioneuromatosis intestinal, hemorragia digestiva, anemia, enfermedad de Crohn.
Ganglioneuroma of the Small Intestine Mimicking Crohn’s Disease
Summary
Introduction. Intestinal ganglioneuromatosis is a rare benign neoplastic disease. It is usually described in children, in association with multiple endocrine neoplasia type 2b and neurofibromatosis type 1. Ganglioneuromatosis is rare in adults, where it usually occurs sporadically and in isolation. Case report. We present a patient with intestinal ganglioneuromatosis in whom the initial clinical and radiographic findings simulated Crohn’s disease. A small bowel resection was performed due to endoscopic capsule occlusion. The immunohistochemical study of the resected segment suggested the diagnosis of small bowel ganglioneuroma. Conclusion. The clinical presentation of intestinal ganglioneuromatosis is variable. The patient may be oligosymptomatic or have an atypical presentation. This diagnosis should be considered when the most common causes of iron deficiency anemia have been excluded. Definitive diagnosis is possible after resection and pathologic analysis of the segment involved.
Keywords. Intestinal ganglioneuromatosis, gastrointestinal bleeding, anemia, Crohn’s disease.
Abreviaturas
GN: Ganglioneuroma.
NEM: Neoplasia endocrina múltiple.
GNM: Ganglioneuromatosis.
TC: Tomografía computada.
CE: Cápsula endoscópica.
Introducción
Los ganglioneuromas (GN) son tumores poco frecuentes que se asocian habitualmente con la neurofibromatosis tipo 1 y la neoplasia endocrina múltiple (NEM) tipo 2 b (en conjunto con el cáncer medular de tiroides y el feocromocitoma), pero también pueden presentarse de forma esporádica y aislada.1 Rara vez se ubican en el tracto gastrointestinal, donde pueden manifestarse como una lesión solitaria o como múltiples pólipos en el colon o en el íleon terminal.2-4
Debe realizarse el diagnóstico diferencial con otras lesiones de intestino delgado que se presentan con estenosis, como enfermedad de Crohn, tuberculosis, ingesta crónica de AINEs, isquemia, infecciones y tumores.5
El objetivo de este trabajo es presentar el caso clínico de una paciente con ganglioneuromatosis (GNM) intestinal cuyos hallazgos clínicos y radiográficos iniciales simulaban una enfermedad de Crohn.
Caso clínico
Una paciente de sexo femenino, de 62 años de edad, es internada por presentar hematoquezia, dolor abdominal, pérdida de peso y diarrea. Desde hacía 4 meses había comenzado con dos evacuaciones diarreicas por día, acompañadas de dolor epigástrico de tipo cólico, pérdida de peso de 8 kg y sangre en materia fecal. Examen físico: palidez mucocutánea; frecuencia cardíaca: 100/ min; TA: 100/70 mm Hg; afebril; abdomen blando y depresible, con ruidos hidroaéreos normales, percusión normal. Laboratorio: hemoglobina: 6,5 g/dL; hematocrito: 24%; albúmina 2,8 g/dL; PCR elevada.
Con respecto a las imágenes, la radiografía directa de abdomen y la telerradiografía de tórax fueron normales. Se realizó una tomografía computada (TC) de abdomen que mostró asas de intestino delgado de paredes engrosadas sin estenosis, ausencia de líquido libre y presencia de divertículos en el colon. Se administraron hidratación y alimentación parenterales, y dos transfusiones de sangre. Se solicitó una videoendoscopía digestiva alta que evidenció gastropatía antral. En la videocolonoscopía hasta ciego se observó diverticulosis sigmoidea. Se constató la presencia de sangre fresca a través de la válvula íleocecal pero no se logró canular el íleon. Se solicitó una cápsula endoscópica (CE) donde se observó la presencia de sangre fresca y coágulos desde el yeyuno medio hasta íleon, con múltiples úlceras lineales, cicatrices y vasos de neo formación que alternaban con mucosa de aspecto normal (Figuras 1-3).
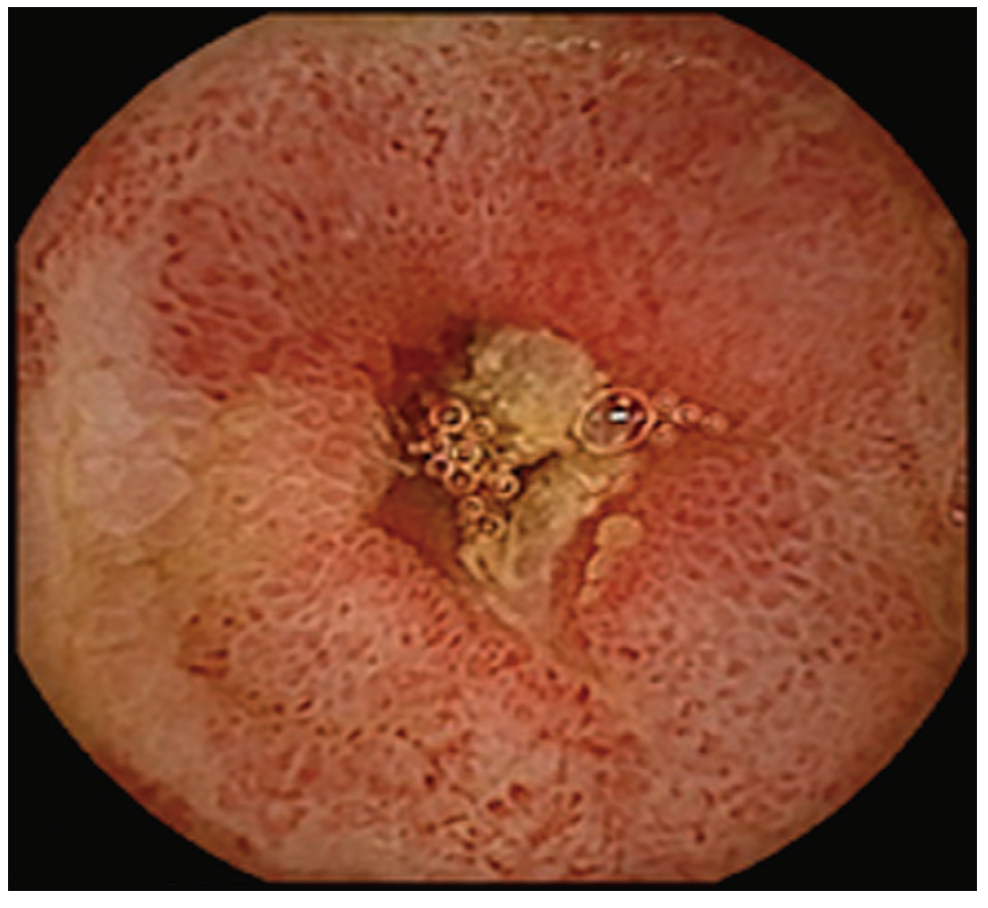
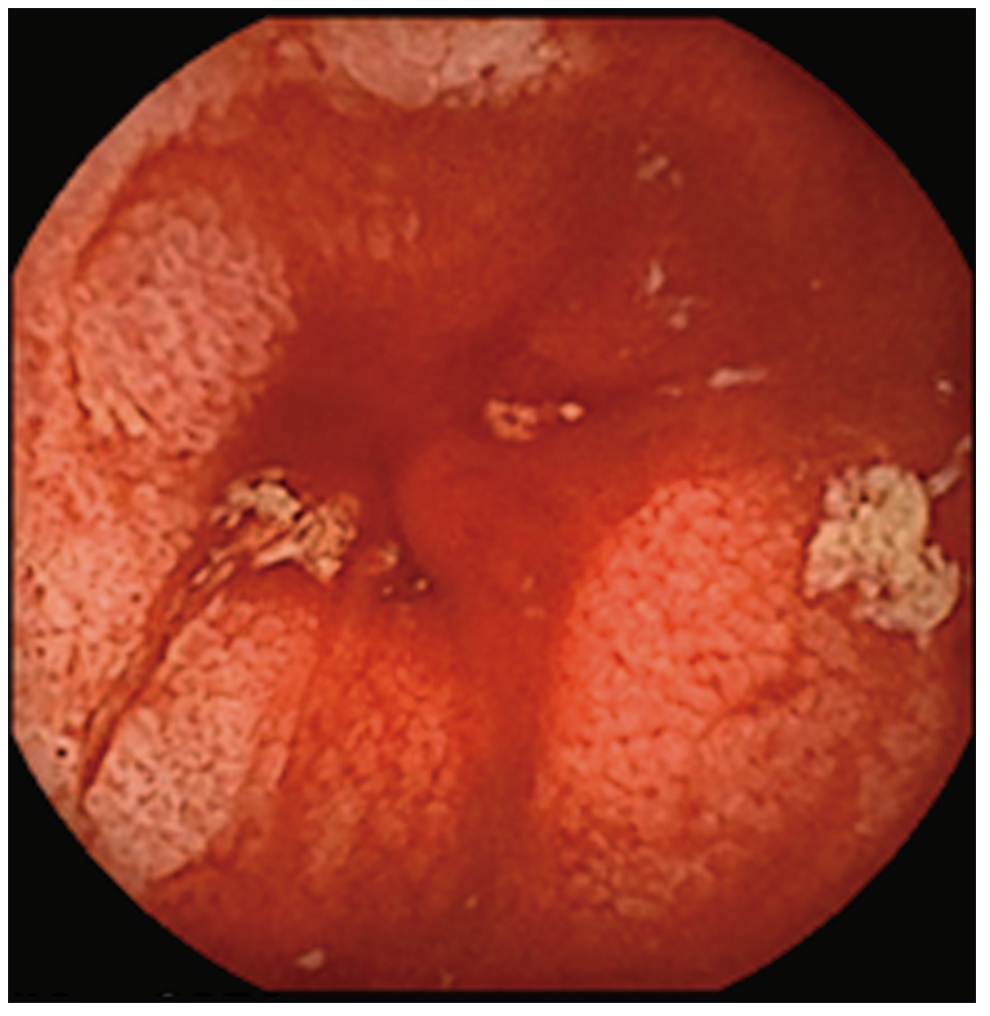
Figura 1. Úlceras. Disminución del calibre
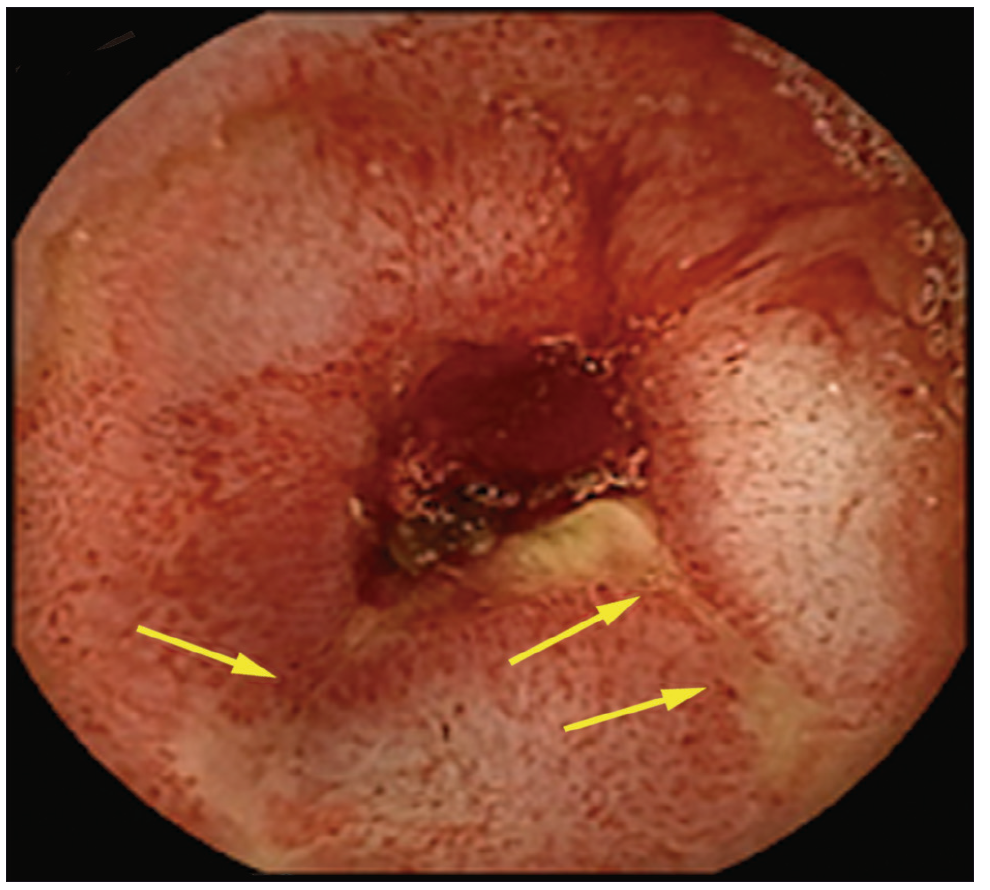
Las zonas afectadas presentaban disminución del calibre de la luz intestinal. Dichos hallazgos eran compatibles con enfermedad de Crohn. No se observó el pasaje de la cápsula a colon a través de la válvula íleo cecal.
A las 12 horas del estudio la paciente presentó un cuadro de suboclusión intestinal. La radiografía directa de abdomen mostró asas del intestino delgado dilatadas y la sospecha de que la CE se encontraba en el hipogastrio. La TC de abdomen con sustracción de imágenes demostró la ubicación de la cápsula en el intestino delgado. Se decidió realizar una laparotomía exploradora en la que se examinó el intestino delgado desde el ángulo duodenoyeyunal, donde se observaron asas dilatadas con las paredes engrosadas. A los 80 cm de la válvula íleocecal se encontró la CE en funcionamiento (Figura 4). Se realizó una ileostomía con extracción de la CE. A 10 cm del sector proximal de la ubicación de la CE se observaron varias estenosis y una fístula entero-entérica, por lo que se decidió realizar la resección de 40 cm de intestino delgado aproximadamente, con anastomosis termino-terminal (Figura 5).
Figura 4. Obstrucción intestinal por cápsula endoscópica
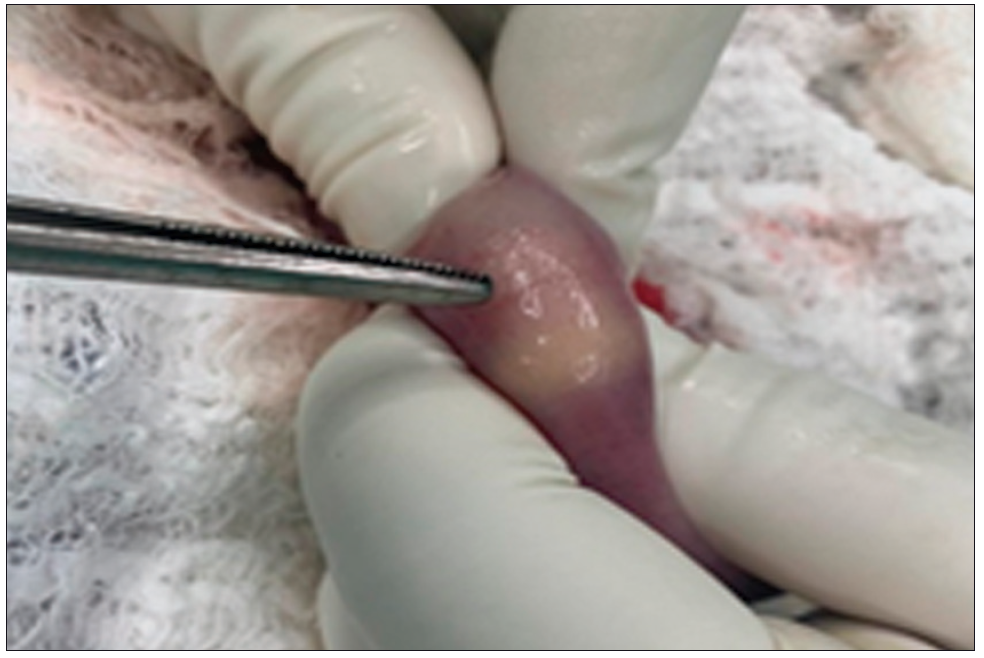
Figura 5. Pieza quirúrgica de resección intestinal
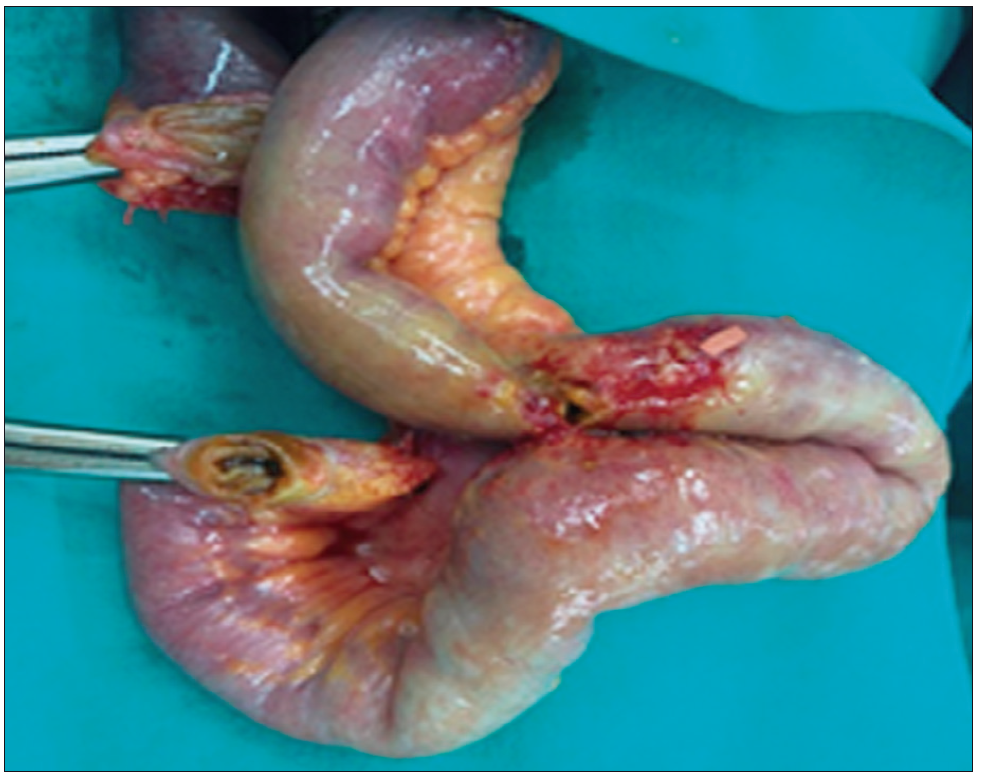
La paciente presentó buena evolución postoperatoria y fue dada de alta a los 8 días de la cirugía. El estudio histopatológico de la pieza quirúrgica informó un ganglioneuroma de intestino delgado con pruebas S 100 (+), ASMA (-), CD20 (-) y CD3 (-) (Figura 6). Los límites quirúrgicos estaban libres de lesión.
Figura 6. Prueba de inmunohistoquímica que muestra intensa expresión difusa de nervios
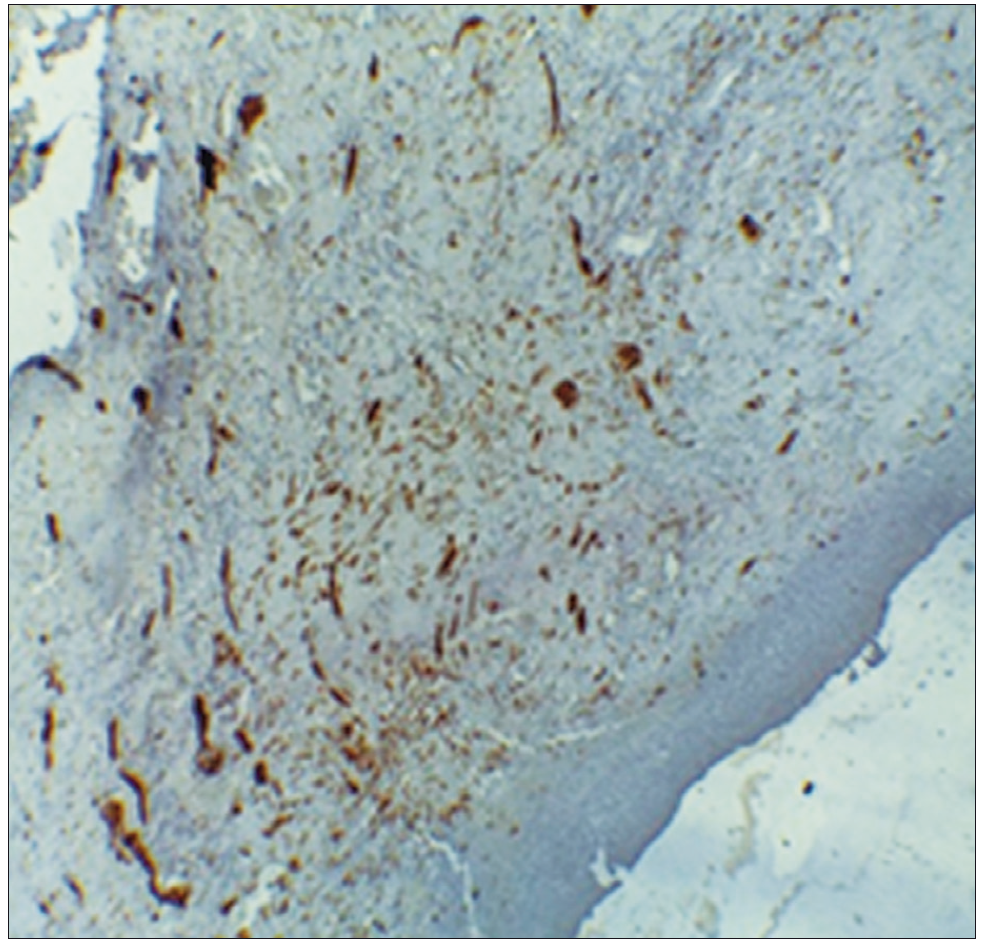
Discusión
La GNM intestinal es una enfermedad neoplásica benigna poco frecuente caracterizada por una marcada proliferación de células ganglionares, células de Schwann y fibras nerviosas en la pared del intestino.6 Se describe en general en niños, en asociación con NEM tipo 2b y neurofibromatosis tipo 1. En adultos es una condición rara que suele presentarse de forma esporádica y aislada.7
Su presentación puede ser de tres formas:5
1.- Polipoidea. Se manifiesta por pólipos colónicos solitarios compuestos por células fusiformes y células ganglionares.
2.- Pólipos múltiples. Se encuentran en colon e íleon.
3.- Difusa. Se caracteriza por hiperplasia del plexo mientérico y proliferación infiltrativa mal circunscripta de tejido ganglioneuromatoso en la pared del intestino. Puede ser transmural, afectando incluso asas intestinales adyacentes, como en nuestra paciente. Afecta con mayor frecuencia el colon, el íleon terminal y el apéndice.8-9 Cuando afecta el íleon distal puede provocar un marcado engrosamiento de la pared intestinal, proliferaciones submucosas nodulares y formación de estenosis extensa,8 simulando una enfermedad de Crohn.1,5,10-11
La presentación clínica de la GNM intestinal es variable y depende de la ubicación y extensión de la lesión. Los síntomas más frecuentes son los cambios en el hábito intestinal, el dolor abdominal y los episodios oclusivos por formación de estenosis, como en nuestro caso. Algunos pacientes pueden permanecer asintomáticos durante décadas.12 La hemorragia oculta o la anemia ferropénica secundaria a la ulceración de la mucosa intestinal son complicaciones raras, lo que hace que el proceso de diagnóstico sea desafiante.13 El diagnóstico diferencial de segmentos con estenosis y engrosamiento de la pared intestinal en el íleon distal incluyen isquemia crónica, lesiones por radioterapia, citomegalovirus, enfermedad de injerto contra huésped, enteropatía por AINEs, linfoma y amiloidosis.14-15
En las formas difusas de GNM intestinal, en la TC de abdomen se puede observar engrosamiento de la pared de un tramo del intestino delgado que puede simular una enfermedad de Crohn, como ha sido descripto en la literatura.5, 10-11
La apariencia endoscópica de la GNM intestinal depende de la naturaleza focal o difusa de las lesiones. A medida que las lesiones se profundizan en el epitelio, se manifiestan como masas subepiteliales únicas o múltiples de tamaño y distribución variable.15 Los cambios en la inervación de la pared intestinal debido a la hiperplasia del plexo mientérico y otras estructuras del sistema nervioso autónomo, determinan cambios segmentarios de la contracción intestinal, dando lugar a un aspecto tubular de la luz.7
Se ha descripto la ulceración de las lesiones debido a la erosión del epitelio sobre su superficie, particularmente en las lesiones solitarias grandes. Histológicamente hay proliferación de fibras nerviosas y células ganglionares, lo que determina una expansión hiperplástica fusiforme del plexo mientérico o incluso una proliferación ganglioneuromatosa transmural, los cuales distorsionan el plexo mientérico e infiltran la pared intestinal adyacente. La inmunorreactividad de las células ganglionares a la proteína S100, proteína ácida fibrilar glial, vimentina, NSE y sinaptofisina confirman el origen nervioso de la proliferación celular,7 como en nuestra paciente.
La realización de una laparotomía exploradora parece justificada en algunos pacientes con duda diagnóstica o complicaciones. En este caso se realizó laparotomía por atascamiento de la CE en íleon, lo que permitió llegar al diagnóstico y adoptar una conducta terapéutica. En la GNM intestinal difusa limitada a un segmento digestivo, como en nuestra paciente, el tratamiento de elección es la resección quirúrgica.1 En aquellos pacientes que requieren resecciones más extensas, la decisión quirúrgica es más difícil, debido al riesgo de un síndrome de intestino corto.
La relación entre la GNM intestinal y las neoplasias malignas no ha sido bien establecida. Sin embargo, se ha publicado la coexistencia con adenocarcinoma del intestino delgado y colon.7 Un hecho a destacar es que la mayoría de estos casos no se asociaron con neurofibromatosis tipo 1.
Conclusión
La GNM intestinal difusa es una afección poco frecuente, particularmente en adultos, en ausencia de síndromes sistémicos como neurofibromatosis tipo 1 o NEM 2b. La presentación clínica es variable. El paciente puede ser oligosintomático o tener una presentación atípica. Este diagnóstico debe considerarse cuando se han excluido las causas más frecuentes de anemia por deficiencia de hierro. El diagnóstico definitivo sólo es posible después de la resección y el análisis patológico del segmento involucrado. La estrategia terapéutica óptima es la cirugía para las lesiones sintomáticas o con sospecha de neoplasia maligna, pero no se ha definido el mejor protocolo de seguimiento.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos y las figuras presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2024 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Lada P E, Frávega P, Caballero F y col. Ganlioneuroma del intestino delgado simulando una enfermedad de crohn. Acta Gastroenterol Latinoam. 2024;54(4):341-345. https://doi.org/10.52787/agl.v54i4.411
Referencias
- Fernandes A, Ferreira AM, Serra P, Carvalho L. Intestinal ganglioneuromatosis: An unusual aetiology for occult gastrointestinal bleeding. BMJ Case Rep 2015. DOI: 10.1136/bcr-2015-211764
- Abraham G, Prakash SR. Solitary colonic ganglioneuroma: A rare incidental finding of hematochezia. Case Rep Gastrointest. Med. 2015. DOI: 10.1155/2015/794985
- Badrinath M, Mandru R, Lowe D, Manocha D, Achufusi T. Isolated Intestinal Ganglioneuroma Mimicking Small Bowel Crohn’s Disease. ACG. Case Rep. J. 2019.6:1-3. DOI:10.14309/crj.0000000000000114
- Anuradha Calicut KR, Sushmitha MG, Kudva R, Shenoy R, Kumar S. Intestinal ganglioneuromatosis with peri-intestinal neurofibroma limited to the gastrointestinal tract clinically and morphologically mimicking Crohn’s disease. J. Interdiscip. Histopathol. 2017. 5(3): 99-102.
- Charagundla SR, Levine MS, Torigian DA, Campbell MS, Furth EE, Rombeau J. Diffuse intestinal ganglioneuromatosis mimicking Crohn’s disease. Am. J. Roentgenol. 2004. 182(5): 1166-1168. DOI:10.2214/ajr.182.5.1821166
- Haggitt RC, Reid BJ. Hereditary gastrointestinal polyposis syndromes. Am. J. Surg. Patho.l 1986. 10: 871-887.
- Chambonnière ML, Porcheron J, Scoazec JY, Audigier JC, Mosnier JF. Intestinal ganglioneuromatosis diagnosed in adult patients. Gastroenterol. Clin. Biol. 2003. 27: 219-224.
- Shekitka KM, Sobin LH. Ganglioneuromas del tracto gastrointestinal: relación con la enfermedad de Von Reckling-hausen y otros síndromes tumorales múltiples. Am. J. Surg. Pathol. 1994.18: 250-257.
- Fenoglio-Preiser CM, Noffsinger AE, Stemmermann GN, Lantz PE, Listrom MB, Rilke FO. Gastrointestinal pathology: an atlas and text. 3rd ed Philadelphia, PA: Lippincott Williams and Wilkins, 2008: 555-559.
- Tobler A, Maurer R, Klaiber C. Stenosing ganglioneuromatosis of the small intestine with ileus and ileal rupture. Schweiz. Med. Wochenschr. 1981.111: 684-688.
- Urbano U, Farina P. Ganglioneuromatosis intestinal en un caso de ileítis terminal. Pathologica 1967.59: 547-550
- Herman M, Abed J, Shi W, Buyuk A, Mankal PK, Kotler D, Ionescu G. A case of ganglioneuroma of the colon during routine colonoscopy. Int. J. Case. Rep. Images. 2015.6(9): 560-563.
- Tatemichi M, Nagata H, Morinaga S, Kaneda S. Protein-losing enteropathy caused by mesenteric vascular involvement of neurofibromatosis. Dig. Dis. Sci. 1993.38: 1549-1553.
- Normann T, Otnes B. Ganglioneuromatosis intestinal, diarrea y carcinoma medular de tiroides. Scand. J. Gastroenterol. 1969.4: 553-559.
- Rubesin SE, Herlinger H. Intestino delgado: diagnóstico diferencial. En: Gore RM, Levine MS, eds. Libro de texto de radiología gastrointestinal, 2ª ed. Filadelfia, PA: Saunders, 2000: 884-890.
Correspondencia: Paul Eduardo Lada
Correo electrónico: pauleduardolada@yahoo.es
Acta Gastroenterol Latinoam 2024;54(4):341-345
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE