Pamela Ruth Daffra,1 Juan Andrés De Paula,1 María Josefina Etchevers,1 Ramiro Cruz González Sueyro,1 María Josefina Sobrero,1 Germán Luis Rainero,2 Franck Carbonnel,3 Mariano Martín Marcolongo1
1 Servicio de Gastroenterología, Hospital Italiano de Buenos Aires. Ciudad Autónoma de Buenos Aires, Argentina.
2 Servicio de Gastroenterología, Hospital Austral. Provincia de Buenos Aires, Argentina.
3 Servicio de Gastroenterología, Bicetre Hospital. Le Kremlin-Bicetre, Francia.
Acta Gastroenterol Latinoam 2019;49(2):161-165
Recibido: 06/08/2018 / Aprobado: 06/02/2019 / Publicado en www.actagastro.org el 17/06/2019
Resumen
No existe un acuerdo unánime acerca de cuál es el abordaje terapéutico más adecuado para el manejo de la enfermedad inflamatoria (EII) después del trasplante hepático por colangitis esclerosante primaria (CEP). Un tercio de estos pacientes presentará mala evolución de la EII después del trasplante, mientras que un quinto de los pacientes desarrollará EII en un plazo de cuatro años después del trasplante por CEP. El manejo de esta situación implica un desafío complejo debido a la necesidad de sumar drogas inmunosupresoras. Informamos el primer caso en América Latina de colitis ulcerosa que por recidivar después del trasplante hepático fue tratado con vedolizumab con buena respuesta terapéutica. Este fármaco ejerce su acción de manera selectiva en el tracto digestivo y representa una opción terapéutica interesante por su especificidad y buen perfil de seguridad en pacientes receptores de trasplante hepático que ya están recibiendo regímenes inmunosupresores.
Palabras claves. Colitis ulcerosa, vedolizumab, trasplante hepático, enfermedad inflamatoria intestinal.
Vedolizumab for ulcerative colitis in a liver transplant patient. First case report in Argentina
Summary
There is much debate about the most adequate therapeutic approach for the management of inflammatory bowel disease (IBD) after liver transplant due to primary sclerosing cholangitis (PSC). One third of those patients will worsen their IBD after transplantation, while one fifth of the patients will develop IBD within four years after transplantation due to PSC. Managing this situation involves a complex challenge due to the need to add immunosuppressant drugs. We report the first case of relapsing ulcerative colitis after liver transplantation treated with vedolizumab in Latin America. This drug exerts its action selectively in the digestive tract and provides an interesting therapeutic option for its specificity and good safety profile in liver transplant recipients already receiving anti-rejection immunosuppressive regimens.
Key words. Ulcerative colitis, vedolizumab, liver transplantation, inflammatory bowel disease.
Abreviaturas
PR. planticola: Raoultella planticola.
SBP: spontaneous bacterial peritonitis.
No existe un acuerdo unánime acerca de cuál es el abordaje terapéutico más adecuado para tratar la enfermedad inflamatoria intestinal (EII), incluida la colitis ulcerosa (CU), después del trasplante hepático. Si bien se han evaluado diversos tratamientos farmacológicos en esta población particular, los resultados están lejos de ser óptimos. Durante los últimos años, los agentes biológicos han surgido como una opción promisoria. Entre ellos, el vedolizumab, un anticuerpo monoclonal humanizado que actúa sobre la integrina α4β7, ejerciendo actividad antiinflamatoria selectiva a nivel intestinal y que ha sido aprobado para la inducción de la remisión y el mantenimiento de la EII moderada a severa en pacientes que nunca recibieron agentes anti-TNF o que han demostrado ser refractarios a los mismos. Sin embargo, existe información limitada acerca del uso del vedolizumab en pacientes que han sido sometidos a un trasplante hepático.1 En este informe de caso, presentamos el primer paciente con EII y trasplante hepático tratado con vedolizumab en un centro de referencia de trasplante hepático en América Latina.
Caso clínico
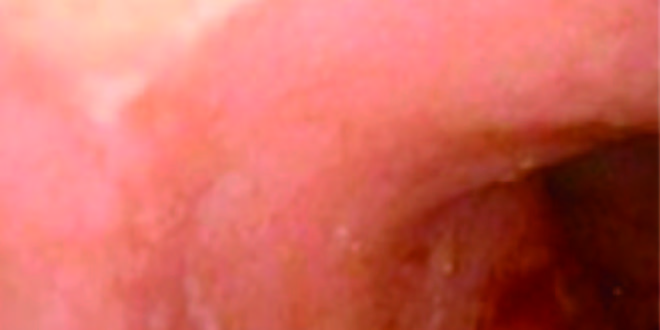
Se trata de un paciente de sexo masculino, de 20 años, con antecedentes de CU y colangitis esclerosante primaria (CEP), ambas entidades diagnosticadas durante la niñez. Tiene diagnóstico de pancolitis ulcerosa desde los 6 meses de edad tratado con mesalazina y corticosteroides que ha presentado recidivas frecuentes de la enfermedad (Figuras 1 y 2). En mayo de 2012, a los 14 años, el paciente fue derivado a nuestro hospital para trasplante hepático. Tres años después del trasplante, en tratamiento con tacrolimus, deltisona y mesalazina, en septiembre de 2015, experimentó una exacerbación severa de la CU mientras se encontraba en Francia, a raíz de lo cual se inició tratamiento con infliximab. Sin embargo, en diciembre de 2015, dos meses después del inicio del tratamiento, se constató pérdida de la respuesta por lo cual se decidió cambiar su tratamiento a vedolizumab, con respuesta clínica y endoscópica. Los análisis de sangre realizados después del inicio de vedolizumab mostraron una mejora en los parámetros inflamatorios y enzimas hepáticas estables en comparación con los valores basales. En abril de 2016, el paciente regresó a la Argentina y se le realizó una colonoscopía de seguimiento que mostró remisión de la CU (puntaje endoscópico de Mayo: 1). El paciente aún continúa con vedolizumab, con una buena evolución sin complicaciones. El tratamiento se administra a través de un régimen especial de uso compasivo, ya que este fármaco aún no ha sido aprobado por las autoridades regulatorias locales, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT).
Figura 1. Colonoscopía que muestra eritema leve y pérdida del patrón vascular.
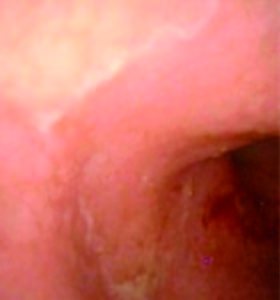
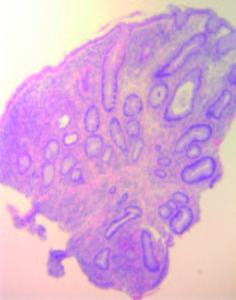
Figura 2. Vista microscópica (40X) que muestra glándulas quiescentes y cambios epiteliales reactivos típicos de la colitis crónica. Se puede observar criptitis focal y abscesos crípticos, con distorsión de la arquitectura glandular.
Discusión
El manejo terapéutico de la EII después del trasplante hepático es difícil. Se estima que un tercio de los pacientes con EII que reciben un trasplante debido a CEP tendrán una mala evolución de su EII y requerirán intensificación del tratamiento médico y/o tratamiento quirúrgico.2 Además, aproximadamente una quinta parte de los pacientes trasplantados debido a CEP desarrollarán una EII en el plazo de cuatro años después del trasplante.3
La información es escasa acerca del uso de vedolizumab en pacientes con trasplante hepático. La capacidad de este fármaco para ejercer su acción de manera selectiva en el tracto digestivo representa una opción terapéutica para los receptores de trasplante hepático que ya están recibiendo regímenes inmunosupresores anti-rechazo.
Recientemente se publicó una serie de casos de diez pacientes pre y postrasplante hepático, cinco de los cuales recibieron vedolizumab después del trasplante, en la que se observó que el vedolizumab fue bien tolerado, mostrando una buena tasa de respuesta con mejoría de los síntomas, de los marcadores objetivos de inflamación intestinal y de la calidad de vida.4
Una publicación más reciente de diez pacientes trasplantados reportó que el vedolizumab fue seguro y efectivo para el tratamiento de la CU moderada a severa.5 Se observó mejoría clínica en 7/10 y 6/10 pacientes después de 6 y 12 meses de tratamiento, respectivamente. A los 12 meses, 6/10 pacientes lograron reducir significativamente o interrumpir los corticoides para la EII. Si bien cinco de esos pacientes experimentaron un total de once infecciones tras el inicio de vedolizumab, la mayoría de las infecciones fueron preexistentes (Clostridium difficile: 4 recidivas en 2 pacientes que ya habían tenido infecciones previas, y colangitis: en 3 de 4 casos se asociaron con el tubo de colangiografía transhepática percutánea). Se calculó que los datos mencionados representan una tasa de 0,95 infecciones por personas/año de exposición al vedolizumab, y se informó en esta serie de pacientes que todas las infecciones respondieron al tratamiento antibiótico, no registrándose muertes.
Adicionalmente se observó buena evolución de la EII en otros case reports y series pequeñas, presentados como manuscritos o como resúmenes en congresos, que incluyen pacientes, que como el caso reportado, no eran naïve de otro biológico.6-8 También se reportó la eficacia y la seguridad para la EII en series estudiadas con el objetivo primario de investigar el efecto del vedolizumab sobre la enfermedad hepática.9, 10
Conclusión
Según nuestra experiencia y basado en los pocos casos informados en la bibliografía, el vedolizumab podría constituir una opción segura para tratar la colitis ulcerosa refractaria en pacientes con trasplante hepático. Sin embargo, se necesitan estudios clínicos para determinar la eficacia y la seguridad de este fármaco en este grupo particularmente complejo de pacientes.
Sostén financiero. Takeda Pharma S.A. proporcionó los fondos para la traducción y la edición lingüística de este artículo.
Referencias
- Feagan BG, Rutgeerts P, Sands BE, Hanauer S, Colombel JF, Sandborn WF, Van Assche G, Axler J, Kim HJ, Danese S, Fox I, Milch C, Sankoh S, Wyant T, Xu J, Parikh A; GEMINI 1 Study Group. Vedolizumab as induction and maintenance therapy for ulcerative colitis. N Engl J Med 2013; 369: 699-710.
- Singh S, Loftus EV Jr, Talwalkar JA. Inflammatory bowel disease after liver transplantation for primary sclerosing cholangitis. Am J Gastroenterol 2013; 108: 1417-1425.
- Schnitzler F, Friedrich M, Stallhofer J, Schönermarck U, Fischereder M, Habicht A, Karbalai N, Wolf C, Angelberger M, Olszak T, Beigel F, Tillack C, Göke B, Zachoval R, Denk G, Guba M, Rust C, Grüner N, Brand S. Solid organ transplantation in patients with inflammatory bowel diseases (ibd): Analysis of Transplantation Outcome and IBD Activity in a Large Single Center Cohort. PLoS One 2015; 10: e0135807.
- Lim TY, Pavlidis P, Gulati S, Pirani T, Samaan M, Chung-Faye G, Dubois P, Irving P, Heneghan M, Hayee B. Vedolizumab in inflammatory bowel disease associated with autoimmune liver disease pre and post liver transplantation: a case series. Inflamm Bowel Dis 2016; 22: E39-E40.
- Wright AP, Fontana RJ, Stidham RW. Vedolizumab is safe and effective in moderate-to-severe inflammatory bowel disease following liver transplantation. Liver Transpl 2017; 23: 968-997.
- Olmedo Martín RV, Amo Trillo V, González Grande R, Jiménez Pérez M. Efficacy and safety of vedolizumab as a treatment option for moderate to severe refractory ulcerative colitis in two patients after liver transplant due to primary sclerosing cholangitis. Rev Esp Enferm Dig 2017; 109: 659-662.
- Meszaros M, Pageaux GP, Altwegg R. Management of Ulcerative Colitis Using Vedolizumab after liver transplantation for primary sclerosing cholangitis. J Crohns Colitis 2016; 10: 236.
- Hartery K, O’Reilly S, Houlihan D, Doherty G, Mulcahy H, Cullen G, Sheridan J. Letter: vedolizumab for the management of inflammatory bowel disease in patients after liver transplantation for primary sclerosing cholangitis. Aliment Pharmacol Ther 2017; 45: 376-378.
- Christensen B, Micic D, Gibson PR, Yarur A, Bellaguarda E, Corsello P, Gaetano JN, Kinnucan J, Rao VL, Reddy S, Singh S, Pekow J, Rubin DT. Vedolizumab in patients with concurrent primary sclerosing cholangitis and inflammatory bowel disease does not improve liver biochemistry but is safe and effective for the bowel disease. Aliment Pharmacol Ther 2018; 47: 753-762.
- Caron B, Peyrin-Biroulet L, Nachury M, Bouhnik Y, Seksik P, Bouguen G, Caillo L, Laharie D, Carbonnel F, Altwegg R, Reenaers C, Serrero M, Boureille A, Nancey S, Filippi J, Abitbol V, Savoye G, Vuitton L, Viennot S, Fumery M, Reymond M, Bronowicki JP, Reimund J-M, Amiot A. Vedolizumab for primary sclerosing cholangitis associated with inflammatory bowel disease: A multicenter cohort study from the GETAID. Journal of Crohn’s and Colitis 2018; 12: S278-S278.
Correspondencia: Pamela Ruth Daffra Eduardo
Acevedo 227, 4to A, CABA 1405, Argentina
Tel.: +54-911-2191-9736
Correo electrónico: pamela.daffra@hospitalitaliano.org.ar
Acta Gastroenterol Latinoam 2019;49(2):162-165
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE