José Daniel Bosia,1 María Virginia D´Ascenzo,1 Silvia Mabel Borzi,1 Ezequiel Barán,2 María Cecilia Calzona1
1 Servicio de Gastroenterología.
2 Servicio de Neumonología – Unidad de Fibrosis Quística de Adultos.
Hospital Profesor Rodolfo Rossi, Ciudad de La Plata. Provincia de Buenos Aires. Argentina.
Acta Gastroenterol Latinoam 2021;51(1):84-86
Recibido: 03/04/2020 / Aceptado: 02/02/2021 / Publicado en www.actagastro.org el 22/03/2021 / https://doi.org/10.52787/tzdh9217
Resumen
El desarrollo de nuevos fármacos antivirales de acción directa para el tratamiento de la infección por el virus de Hepatitis C ha permitido obtener una excelente tasa de curación y extender las indicaciones de erradicación del virus de Hepatitis C a poblaciones muy difíciles de tratar anteriormente, como los pacientes con fibrosis quística, en quienes el tratamiento con los regímenes clásicos basados en Interferón pegilado más ribavirina podría favorecer el empeoramiento de la función pulmonar. Presentamos el caso de un varón de 41 años de edad con fibrosis quística, diagnosticado de infección por virus de Hepatitis C, genotipo 1a, no cirrótico, tratado con antivirales de acción directa durante doce semanas, obteniéndose respuesta virológica sostenida, sin efectos adversos. Un año después, hallándose en lista de espera, el paciente fue sometido a trasplante bipulmonar.
Palabras claves. Fibrosis quística, Hepatitis C, adultos, antivirales de acción directa, trasplante bipulmonar.
Treatment of Chronic Hepatitis C Virus with Direct-Acting Antiviral Drugs in a Patient with Cystic Fibrosis
Summary
The development of new direct acting antiviral drugs for the treatment of Hepatitis C virus infection, has made it possible to obtain an excellent cure rate and extend the indications for eradication of Hepatitis C virus to previously very difficult populations to treat like cystic fibrosis, in whom treatment with classic regimens based on pegylated Interferon plus ribavirin could favor worsening lung function. We present a case of a 41-year-old man with cystic fibrosis, diagnosed with Hepatitis C virus infection, genotype 1a, non-cirrhotic, treated with direct acting antiviral drugs for twelve weeks, obtaining a sustained viral response, without adverse effects. One year later, being on the waiting list, underwent a bipulmonary transplant.
Keywords. Cystic fibrosis, C hepatitis, adults, acting antivirals drugs, bipulmonary transplant.
Abreviaturas
HCV: Virus de Hepatitis C.
CHC: Carcinoma hepatocelular.
HBV: Virus de hepatitis B.
VIH: Virus de Inmunodeficiencia Humana.
AAD: Antivirales de acción directa.
PEG IFN: Interferón Pegilado.
RB: Ribavirina.
FQ: Fibrosis quística.
RVS: Respuesta virológica sostenida.
VEF1: Volumen respiratorio forzado en el primer segundo.
CVF: Capacidad vital forzada.
Introducción
La infección por el virus de Hepatitis C (HCV) constituye una de las principales causas de enfermedad hepática crónica a nivel mundial.1 El impacto de esta enfermedad puede ser variable, desde el desarrollo de hepatitis crónica o cirrosis hasta carcinoma hepatocelular (CHC). Se estima que existen aproximadamente más de 71 millones de personas infectadas con esta enfermedad en el mundo,1, 2 la mayoría de las cuales desconoce su infección. En la Argentina la prevalencia es de aproximadamente el 2% de la población.3
Si bien la progresión de la enfermedad hepática crónica puede demorar varias décadas, esta puede ser acelerada por algunos cofactores tales como el consumo de alcohol, la diabetes, la coinfección con el virus de Hepatitis B (HBV) y la coinfección con el Virus de Inmunodeficiencia Humana (VIH), con un 40% de progresión a cirrosis hepática, dependiendo de la presencia de estos cofactores.4 En los pacientes con cirrosis hepática constituye una de las principales causas predisponentes al CHC.
El advenimiento de nuevos fármacos antivirales de acción directa (AAD), más efectivos, seguros y con mejor tolerancia que los regímenes clásicos basados en Interferón pegilado (PEG IFN) más ribavirina (RB), ha permitido obtener una excelente tasa de curación luego de ocho a doce semanas de tratamiento, que supera el 95%.5 Además, ha permitido extender las indicaciones de erradicación del HCV a poblaciones muy difíciles de tratar anteriormente, entre otros, como los pacientes con fibrosis quística (FQ), en quienes el tratamiento con (PEG IFN) (RB) puede aumentar las infecciones respiratorias con el consiguiente empeoramiento de la función pulmonar.6 En estos pacientes resulta importante realizar el tratamiento antiviral previo a un eventual trasplante pulmonar.
Actualmente el objetivo final del tratamiento para HCV es lograr la respuesta virológica sostenida (RVS), definida por un RNA del HCV en sangre no detectable a las doce semanas después de haber finalizado el tratamiento.7
Los estudios de seguimiento a largo plazo han demostrado que la RVS corresponde a la cura definitiva de la infección por HCV en más del 99% de los casos.8
Presentamos el caso de un varón de 41 años de edad con FQ, diagnosticado de infección por HCV, tratado con AAD durante doce semanas, obteniéndose respuesta viral sostenida, sin evidenciarse efectos adversos. Un año después, hallándose en lista de espera, el paciente fue sometido a trasplante bipulmonar.
Caso
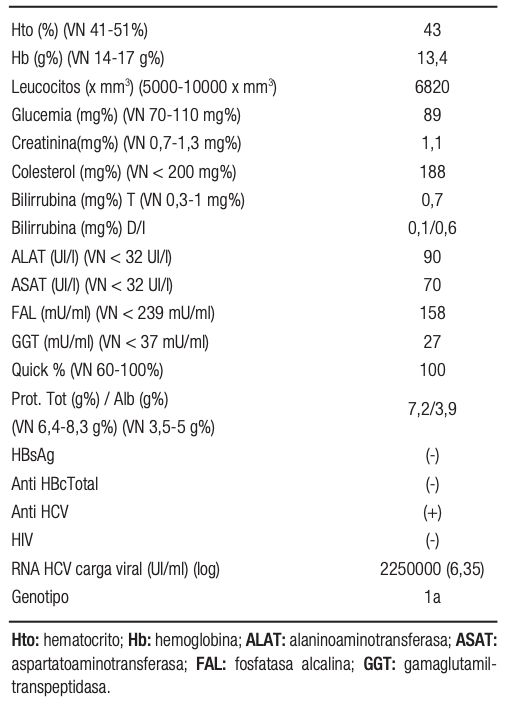
Varón de 41 años de edad, peso 67 Kg, talla 185 cm, IMC 19,5 Kg/m2, con diagnóstico de FQ realizado a los 9 años, presentando un compromiso pulmonar severo por infección crónica por Pseudomona Aeruginosa y Staphilococus Aureus meticilino resistente, asistido en la Unidad de Fibrosis Quística de adultos de HIGA R Rossi de la ciudad de La Plata, Argentina. Ante la evidencia de un progresivo deterioro de la función respiratoria (VEF1: 17%, CVF 35%), requirió internación en sala general. Los resultados de las pruebas bioquímicas y hematológicas realizadas durante la internación están detalladas en la Tabla 1. Se solicitó RNA HCV carga viral 2250000 UI/ml (log 6,35) y genotipo 1a.
Tabla 1. Valores de laboratorio y serología viral
La ecografía doppler espleno portal abdominal mostró signos de afectación hepática crónica (esteatosis grado I), sin signos de hipertensión portal ni imágenes focales hepáticas.
A los efectos de valorar la afectación hepática se realizó Fibroelastografia Hepática (Fibroscan), hallándose una mediana de 11,9 kPa, lo cual correlaciona con un estadio de Metavir F3.
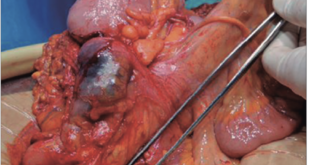
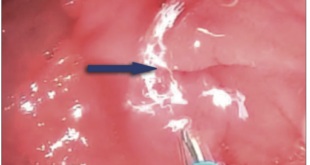
Se decide iniciar tratamiento con un esquema de AAD (paritaprevir-ritonavir-ombitasvir y dasabuvir), durante doce semanas. Durante el tratamiento el paciente presentó buena evolución y no se observaron efectos secundarios ni exacerbación respiratoria. A las doce semanas de finalizado el tratamiento se solicitó RNA HCV, hallándose no detectable y considerándose como RVS. Un año después, hallándose en lista de espera, presentó un mayor deterioro de la función respiratoria y fue sometido a trasplante bipulmonar.
Discusión
El advenimiento de los AAD, con elevadas tasas de curación, ha producido un cambio radical en el paradigma de la hepatitis C, poniendo en evidencia dos desafíos muy significativos: por una parte, identificar a los pacientes asintomáticos, y por otro, el acceso al tratamiento, incluso en pacientes con FQ, en los cuales ha sido demostrado que con el tratamiento con (PEG IFN) (RB) resulta esperable un deterioro de la función respiratoria.6 Además, permite tratar a estos pacientes con mayor seguridad y casi sin efectos colaterales antes de que sean sometidos a un trasplante bipulmonar.
Actualmente la infección por HCV es considerada una contraindicación relativa para el trasplante bipulmonar,9 aunque esto no es seguido uniformemente en todas las unidades de trasplante, teniendo en cuenta que no existe un consenso acerca del manejo de los pacientes infectados por HCV en el pretrasplante bipulmonar.
Un estudio reciente10 publicó el caso de un paciente con FQ e infección por HCV que recibió tratamiento previo con un esquema pangenotípico de AAD y se sometió exitosamente al trasplante bipulmonar de un donante virémico de HCV, con reinfección y subsiguiente curación de su HCV. Coincidentemente, nuestro paciente recibió tratamiento con AAD previo al trasplante bipulmonar, sin hallarse exacerbación de los parámetros de función respiratoria intratratamiento y obteniéndose RVS, lo que favoreció el trasplante bipulmonar realizado un año después.
Conclusión
Consideramos relevante la comunicación de este caso en el contexto del nuevo desafío que constituye la mayor sobrevida de los pacientes con FQ, resultado de la evaluación por parte de equipos especializados junto con la emergencia de nuevos y más exitosos tratamientos.
Aviso de derechos de autor
 © 2021 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
© 2021 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Bosia JD, D´Ascenzo MV, Borzi SM y col. Tratamiento de hepatitis crónica por virus de Hepatitis C con drogas antivirales de acción directa en un paciente con fibrosis quística. Acta Gastroenterol Latinoam. 2021;51(1):84-6. https://doi.org/10.52787/tzdh9217
Referencias
- Polaris Observatory HCV Collaborators. Global prevalence and genotype distribution of hepatitis C virus infection in 2015: a modelling study. Lancet Gastroenterol Hepatol. 2017;2:161-76.
- European Union HCV Collaborators. Hepatitis C virus prevalence and level of intervention required to achieve the WHO targets for elimination in the European Union by 2030: a modelling study. Lancet Gastroenterol Hepatol. 2017;2:325-36.
- Descalzi V, Rey J, Bessone F, Mengarelli S, Ramadan A. Prevalencia de la Hepatitis C en población general y en donantes de sangre. Consenso Argentino de Hepatitis C. 2007:39-45.
- Afdhal NH. The natural History of Hepatitis C. Semin Liver Dis. 2004;24:3-8.
- Falade-Nwulia O, Suarez-Cuervo C, Nelson DR, Fried MW, Segal JB, Sulkowski MS. Oral direct-acting agent therapy for hepatitis C virus infection: a systematic review. Ann Intern Med. 2017;166:637-48.
- Adán-Merino L, Olveira-Martín A, Prados C, Gea-Rodríguez F, Castillo-Grau P, Martín-Arranz E, Sáenz JC, Segura-Cabral J. Chronic hepatitis C treatment in a cystic fibrosis patient in the pulmonary pre-transplant stage. Rev Esp Enferm Dig. 2010;102(10):587-90.
- Chevaliez S, Pawlotzky JM. Diagnosis and magnagement of chonical viral hepatitis: antigens, antibodies, viral genomes. Best Prod Res Clin Gastroenterol. 2008;22:1031-48.
- European Association for the Study of the Liver. EASL Recommendations on Treatment of Hepatitis C 2018. J Hepatol. 2018;69(2):461-511.
- Weill D. Lung transplantation: indications and contraindications. Journal of Thoracic Disease. 2018;10(7).
- Harano T, Haidar G, Schaheen L, Morrell MR, Pilewski JM, D’Cunha J. Successful lung transplantation from a hepatitis C RNA-positive donor to a hepatitis C treatment-experienced recipient with cystic fibrosis. J Thorac Cardiovasc Surg. 2019;158(4):e155-e157.
Correspondencia: José Daniel Bosia
Calle 158 Nº 610 Berisso (C.P. 1923). Buenos Aires, Argentina
Tel.: 54 221 4612553 / Cel.: 221154091506
Correo electrónico: bosia@intramed.net
Acta Gastroenterol Latinoam 2021;51(1):84-86
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE