Lourdes Mollard ID· Rodrigo A Gasque ID· Magalí Chahdi Beltrame ID· Marcelo E Lenz ID
Francisco J Mattera ID· Emilio G Quiñonez ID
Unidad de Cirugía Hepatobiliar Compleja y Trasplante Hepático.
Hospital El Cruce. Florencio Varela, Provincia de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2025;55(4):358-370
Recibido: 23/09/2025 / Aceptado: 15/12/2025 / Publicado online el 23/12/2025 / https://doi.org/10.52787/agl.v55i4.547
Resumen
Introducción. Los avances en la cirugía hepática oncológica han mejorado la radicalidad de los procedimientos y ampliado los criterios de resecabilidad. Las transaminasas pueden ser indicadores de injuria hepatocelular postoperatoria. Objetivos. Evaluar la relación entre las transaminasas del primer día postoperatorio y la morbimortalidad en las hepatectomías por patología maligna. Materiales y métodos. Análisis retrospectivo de hepatectomías por patología maligna entre marzo de 2015 y febrero de 2023. Se evaluaron variables demográficas, intraoperatorias y postoperatorias. Se determinaron los valores de corte óptimos de transaminasas y su relación con las complicaciones y la mortalidad mediante curvas ROC y cálculos de sensibilidad y especificidad. Resultados. Realizamos 273 hepatectomías en nuestra institución, 118 por patología maligna. Hallamos una relación estadísticamente significativa entre los valores elevados de las transaminasas en el primer día postoperatorio y el desarrollo de la morbimortalidad. Los puntos de corte para predecir mortalidad fueron 856 UI/L para la transaminasa glutámico-oxalacética y 1341 UI/L para la transaminasa glutámico-pirúvica (AUC: 0,714 y 0,579, respectivamente), y 530 UI/L y 257 UI/L para predecir la ocurrencia de complicaciones (AUC: 0,700 y 0,663). Los valores de transaminasas glutámico-oxalacética elevados se asociaron a insuficiencia hepática postoperatoria, con un punto de corte > 856 UI/L (AUC: 0,834). Conclusión. Los valores elevados de transaminasas al primer día postoperatorio se asociaron con mayor ocurrencia de complicaciones, necesidad de hemoderivados y uso de drogas vasoactivas. Una transaminasa glutámico-oxalacética elevada indica un riesgo mayor de insuficiencia hepática postoperatoria y mortalidad a 90 días. Las transaminasas son marcadores pronósticos útiles en las hepatectomías por patología maligna.
Palabras claves. Hepatectomía, complicaciones postoperatorias, mortalidad, aspartato aminotransferasa, alanina aminotransferasa.
Transaminases on the First Day After Hepatectomy and Prediction of Outcomes in Malignant Disease
Summary
Introduction. Advances in oncological liver surgery have improved the radicality of procedures and broadened the criteria for resectability. Transaminases can be indicators of postoperative hepatocellular injury. Objectives. Evaluate the relationship between transaminase levels on the first postoperative day and morbidity and mortality in hepatectomies for malignant disease. Materials and methods. A retrospective analysis was conducted on hepatectomies for malignant disease between March 2015 and February 2023. Demographic, intraoperative, and postoperative variables were evaluated. Optimal transaminase cutoff values and their relationship with complications and mortality were determined using ROC curves and sensitivity and specificity calculations. Results. We performed 273 hepatectomies at our institution, 118 of which were for malignant pathology. We found a statistically significant relationship between elevated transaminase levels on the first postoperative day and the development of morbidity and mortality. The cutoff points for predicting mortality were 856 IU/L for glutamic-oxaloacetic transaminase and 1341 IU/L for glutamic-pyruvic transaminase (AUC: 0,714 and 0,579, respectively), and 530 IU/L and 257 IU/L for predicting the occurrence of complications (AUC: 0,700 and 0,663, respectively). Elevated glutamic-pyruvic transaminase values were associated with postoperative liver failure, with a cutoff point > 856 IU/L (AUC: 0,834). Conclusion. Elevated transaminase values on the first postoperative day are associated with a higher occurrence of complications, the need for blood products and the use of vasoactive drugs. Elevated glutamic-pyruvic transaminase indicates a higher risk of postoperative liver failure and 90-day mortality. Transaminases are useful prognostic markers in hepatectomies for malignant pathology.
Keywords. Hepatectomy, postoperative complications, mortality, aspartate aminotransferase, alanine aminotransferase.
Abreviaturas
MELD: Model for end-stage liver disease.
BCLC: Barcelona Clinic Liver Cancer.
ALPPS: Associating liver partition and portal vein ligation for staged hepatectomy.
AINES: Antiinflamatorios no esteroideos.
GOT: Transaminasa glutámico-oxalacética.
GPT: Transaminasa glutámico-pirúvica.
BT: Bilirrubina total.
TP: Tiempo de protrombina.
ICC: Índice de Comorbilidad de Charlson.
RIN: Radio internacional normalizado.
UTI: Unidad de terapia intensiva.
DS: Desvío estándar.
IQR: Rango intercuartil.
ROC: Receiver operating characteristic.
S: Sensibilidad.
E: Especificidad.
AUC: Area under the curve.
CCR: Cáncer colorrectal.
TNE: Tumor neuroendócrino.
GIST: Tumor del estroma gastrointestinal.
ICG R15: Índice de Retención de Verde de Indocianina a los 15 minutos.
Introducción y objetivos
Los avances en cirugía hepática oncológica en las últimas décadas han sido notables, reflejándose en la mayor radicalidad de los procedimientos y en la expansión de los criterios de resecabilidad de los pacientes. Si bien la tendencia global apunta a un descenso en la mortalidad perioperatoria, con tasas reportadas menores al 5%, la morbilidad se mantiene dentro de valores altos, que varían del 36 al 56% en diferentes centros,1-5 por lo que continúa siendo una preocupación sustancial. Esto es particularmente cierto en las resecciones hepáticas por patología maligna, debido a que los pacientes frecuentemente presentan un peor estado general y algún grado de hepatotoxicidad en los casos en los que se realiza quimioterapia previa a la cirugía.6 Esta área temática se ha investigado extensivamente en un esfuerzo por reducir la morbimortalidad, dando lugar a múltiples estudios de benchmarking.7, 8 Se han identificado diversos factores de riesgo independientes relacionados con el desarrollo de complicaciones en las resecciones hepáticas. Entre los preoperatorios, se encuentran la edad, las comorbilidades y la funcionalidad hepática; mientras que los intraoperatorios incluyen, entre otros, el requerimiento de transfusiones sanguíneas y la extensión de la resección hepática.1, 9, 10 Los valores de transaminasas son considerados indicadores fidedignos de injuria hepatocelular postoperatoria, y es habitual su dosaje en forma rutinaria. Se ha estudiado su relación con el desarrollo de complicaciones postoperatorias, pero los resultados disponibles en la bibliografía no han sido concluyentes.11-15 La determinación temprana de parámetros bioquímicos adecuados podría ayudar a detectar en forma precoz a aquellos pacientes en riesgo de desarrollar complicaciones postoperatorias, y así mejorar los resultados a corto plazo. El objetivo de este trabajo es evaluar la relación entre los valores de transaminasas en el primer día postoperatorio y el desarrollo de la morbilidad y la mortalidad en las hepatectomías llevadas a cabo por patología maligna.
Materiales y métodos
El estudio fue aprobado por el Comité de Ética de nuestra institución y se respetaron los principios de la Declaración de Helsinki. Se realizó un análisis retrospectivo de todas las hepatectomías efectuadas por patología maligna en el período comprendido entre marzo de 2015 y febrero de 2023 en nuestro servicio, registradas en una base de datos institucional completada de forma prospectiva. Debido al tamaño reducido de la muestra y el grupo de interés específico se utilizó un muestreo censal. No fue necesaria la obtención de consentimiento informado por la naturaleza retrospectiva del estudio. Los criterios de inclusión fueron: pacientes mayores a 18 años, confirmación anatomopatológica de malignidad y seguimiento postoperatorio mínimo de 90 días. En cuanto a los pacientes cirróticos, sólo fueron incluidos aquellos con cirrosis compensada, valorada mediante la Clasificación pronóstica de D’Amico (etapas 1 y 2), el Score Child-Pugh (A), y el Score MELD (≤ 9 puntos); un valor de plaquetas mayor a 80000/µL; y un estadio tumoral de la Barcelona Clinic Liver Cancer (BCLC) muy temprano (0) o temprano (A), para garantizar la seguridad de las intervenciones conforme a la evidencia vigente.16-19 Se excluyeron las biopsias excisionales, los pacientes con seguimiento discontinuo, los casos en los que no se dispusiera de laboratorio al primer día postoperatorio, y aquellos pacientes que requirieron técnicas de modulación del flujo portal (hepatectomía en dos tiempos, ALPPS y sus variantes, y embolización portal preoperatoria) por su mayor morbimortalidad inherente a las técnicas utilizadas.20-22 Se plantearon y analizaron todos los casos en el comité multidisciplinario de tumores.
Los procedimientos fueron realizados bajo anestesia general. Se utilizó un protocolo de fluidoterapia restrictiva para mantener una presión venosa central menor a 5 mmHg y disminuir el riesgo de sangrado. Los fármacos utilizados en forma habitual fueron propofol, midazolam, rocuronio o atracurio, fentanilo o remifentanilo, de acuerdo al criterio y preferencia del profesional a cargo. En cuanto al abordaje laparoscópico o convencional, la decisión fue tomada individualizando cada caso, considerando el tamaño y la localización tumoral. Se utilizó ecografía sistemáticamente para el mapeo intraoperatorio de las lesiones y sus relaciones con los elementos vasculobiliares. La transección parenquimatosa fue realizada con bisturí armónico, sellador de vasos, aspirador ultrasónico, y suturas mecánicas vasculares. Los fármacos utilizados en forma rutinaria en el postoperatorio fueron protectores gástricos (omeprazol) y analgésicos. De acuerdo al tipo de abordaje se administraron antiinflamatorios no esteroideos (AINES) en forma inicial y luego opiáceos (fentanilo, morfina o tramadol), o únicamente AINES en las intervenciones por vía laparoscópica. Se realizaron determinaciones consecutivas de transaminasas, bilirrubina total y tiempo de protrombina desde el primer día postoperatorio y hasta el quinto día inclusive. Los valores de referencia de laboratorio fueron: transaminasa glutámico-oxalacética (GOT) ≤ 34 UI/L, transaminasa glutámico-pirúvica (GPT) ≤ 55 UI/L, bilirrubina total (BT) ≤ 1,4 mg/dl y tiempo de protrombina (TP) 70-100%.
Se analizaron datos demográficos como edad, sexo, antecedentes patológicos y diagnóstico de cirrosis. Se estratificó a los pacientes en función de sus comorbilidades preexistentes utilizando el Índice de Comorbilidad de Charlson (ICC). Se utilizó un punto de corte igual o mayor a 5 para identificar a aquellos con una sobrevida estimada a 10 años menor al 50%.23 Se analizó la indicación del procedimiento, la realización preoperatoria de quimioterapia y el tipo de resección según la terminología de Brisbane 2000, que define como hepatectomía mayor a la exéresis de 3 o más segmentos.24 En cuanto a las variables intraoperatorias, se analizó el tiempo quirúrgico, la utilización de la maniobra de Pringle, el requerimiento transfusional, y la resección concomitante de otros órganos. Las variables postoperatorias analizadas fueron: requerimiento de drogas vasoactivas en el postoperatorio inmediato; dosaje de transaminasas al primer día postoperatorio; transfusión de hemoderivados; estadía en UTI y estadía hospitalaria. Las complicaciones postoperatorias fueron registradas con la escala de Dindo-Clavien, considerando complicaciones menores a aquellas inferiores al grado III.25 La insuficiencia hepática postoperatoria se definió de acuerdo a 3 modelos validados. El modelo del International Study Group of Liver Surgery (ISGLS) la define como la incapacidad del hígado para mantener sus funciones de síntesis, excreción y detoxificación, caracterizadas por un aumento del radio internacional normalizado (RIN) y la bilirrubina sérica a partir del quinto día postoperatorio inclusive; clasifica su severidad en 3 grados: A, donde se produce una alteración en los parámetros bioquímicos que no condiciona cambios en el manejo postoperatorio habitual, B, que conlleva cambios no agresivos en el manejo postoperatorio habitual, y C, aquella que por su severidad requiere de tratamientos invasivos.26, 27 El trabajo de Mullen y cols. establece la presencia de insuficiencia hepática postoperatoria a partir de un valor pico de bilirrubina mayor a 7 mg/dl.28 Por último, se consideraron los criterios 50-50, -que consideran la presencia concomitante de un tiempo de protrombina menor a 50% y bilirrubina sérica total mayor a 50 μmol/L (equivalente a 2,92 mg/dl) al quinto día postoperatorio.29 Se registró la mortalidad perioperatoria a los
90 días del procedimiento, teniendo en cuenta la evidencia creciente sobre la subestimación de este parámetro cuando se utilizan períodos menores.30-32
El análisis estadístico se realizó mediante el programa Stata Versión 14.2 (StataCorp®, 2016). Las variables continuas se describieron utilizando mediana y rango, o media y desvío estándar, según correspondiera. Las variables discretas fueron descritas mediante valores absolutos y porcentajes. Se utilizaron el t-test para muestras independientes, el test Mann-Whitney U y el test de correlación de Spearman para las variables continuas; y el test de Chi2 para las categóricas. Se analizaron las variables relacionadas con el desarrollo de complicaciones y la mortalidad. Se examinaron las variables asociadas al aumento de las transaminasas en el primer día postoperatorio. Se construyó una curva ROC para determinar el valor de corte óptimo de GOT y GPT en relación al desarrollo de complicaciones y a la mortalidad; con este valor se calculó sensibilidad (S) y especificidad (E). Se midió el área bajo la curva para evaluar la capacidad diagnóstica del test.
Resultados
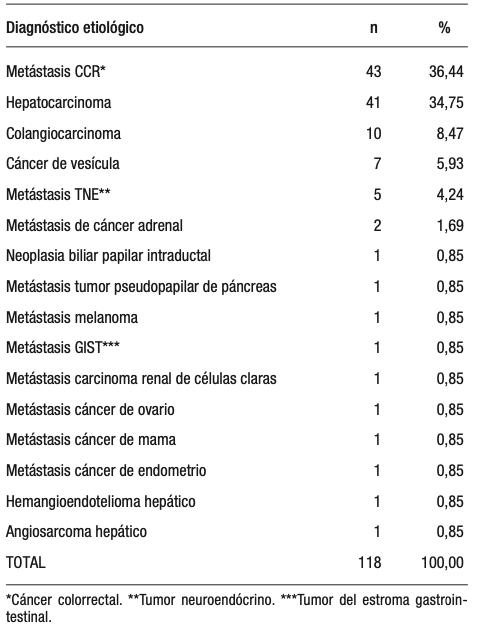
En el período estudiado, sobre un total de 273 hepatectomías, 118 (43,2%) fueron por patología maligna. Las indicaciones quirúrgicas más frecuentes fueron metástasis de cáncer colorrectal (36,4%) seguidas de hepatocarcinoma (34,8%). Las principales etiologías pueden observarse en la Tabla 1. Hubo predominio masculino (n = 65, 55,1%). La media de edad fue de 58 ± 13,4 años.
En 26 casos (22%) se trató de pacientes cirróticos, siendo la principal etiología la infección por hepatitis C (61,5%), seguida del alcohol (15,4%).
Tabla 1. Indicaciones quirúrgicas
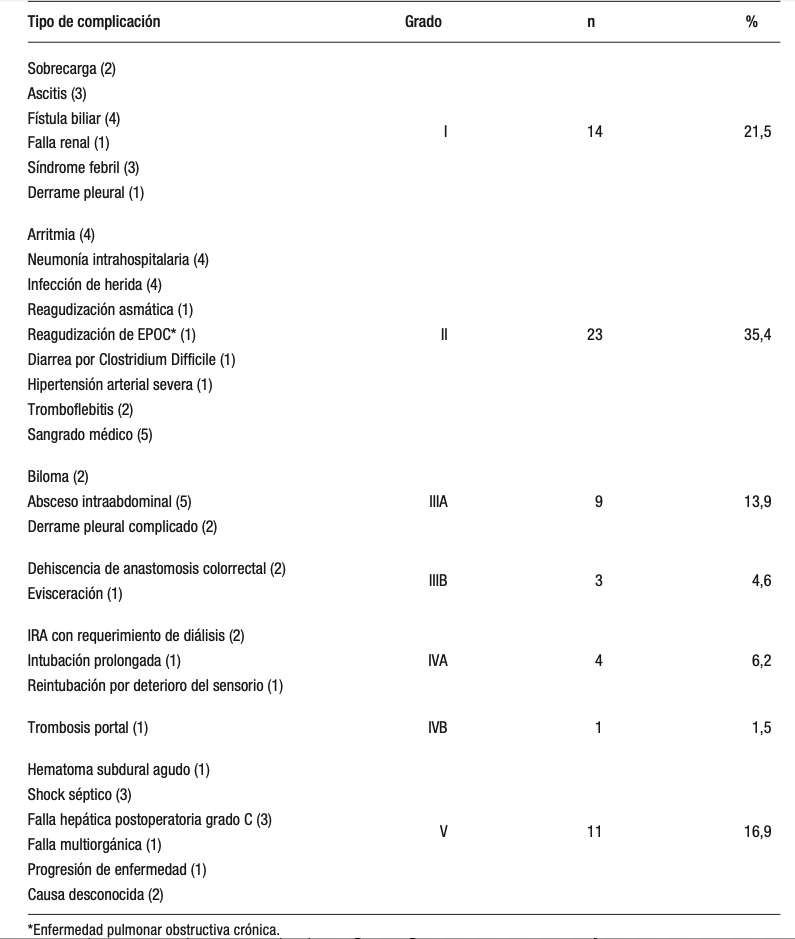
Veinte pacientes (76,9%) correspondieron al estadio BCLC A, mientras que 6 (23,1%) al estadio BCLC 0. Ochenta y cinco pacientes (72%) presentaron un ICC ≥ 5 puntos. Treinta y cinco pacientes (29,7%) habían realizado quimioterapia previamente. El abordaje fue convencional en 98 casos (83,1%) y laparoscópico en 20 (16,9%), con 8 conversiones (6,8%). Las cirugías efectuadas fueron hepatectomías mayores en 56 casos (47,5%). En 16 pacientes (13,6%) se llevaron a cabo resecciones combinadas de otros órganos. La mediana de tiempo quirúrgico fue de 240 minutos (r: 180-300). La mediana de estadía en UTI fue de 3 días (r: 2-5), y la de días de internación fue de 6 (r: 4-11). Cuarenta y cuatro pacientes (37,3%) requirieron transfusiones intraoperatorias de hemoderivados, mientras que 21 (17,8%) las recibieron en el postoperatorio. Cinco pacientes (4,2%) requirieron vasopresores en el postoperatorio inmediato. La morbilidad fue del 55,1% (65 pacientes), y la incidencia de complicaciones mayores fue de 23,7%. Las complicaciones estratificadas por grado pueden observarse en la Tabla 2. La incidencia de insuficiencia hepática postoperatoria fue de 4,2%, correspondiendo dos casos al Grado A y tres al Grado C.
Tabla 2. Complicaciones por grado
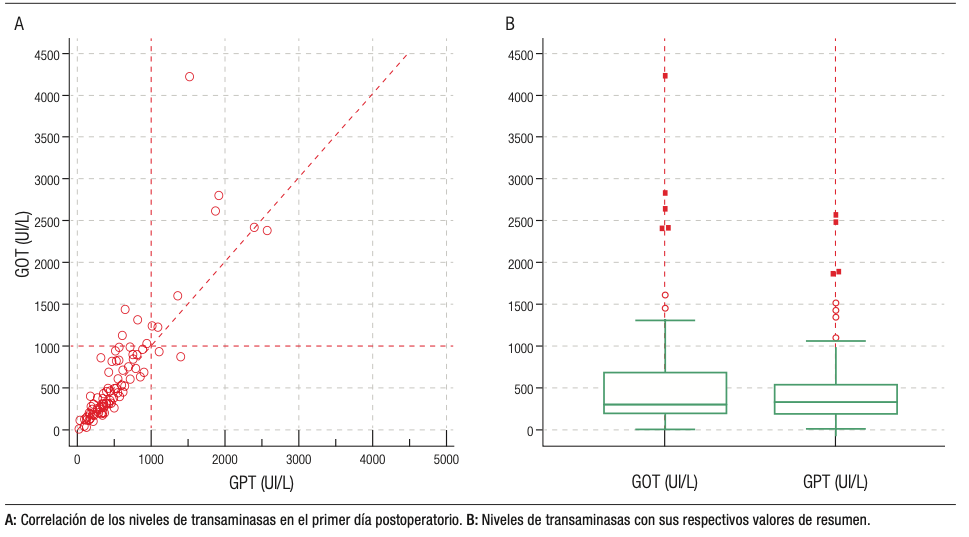
Once pacientes fallecieron, siendo la mortalidad global del 9,3%. Los valores de transaminasas y su correlación se ilustran en la Figura 1.
Figura 1.
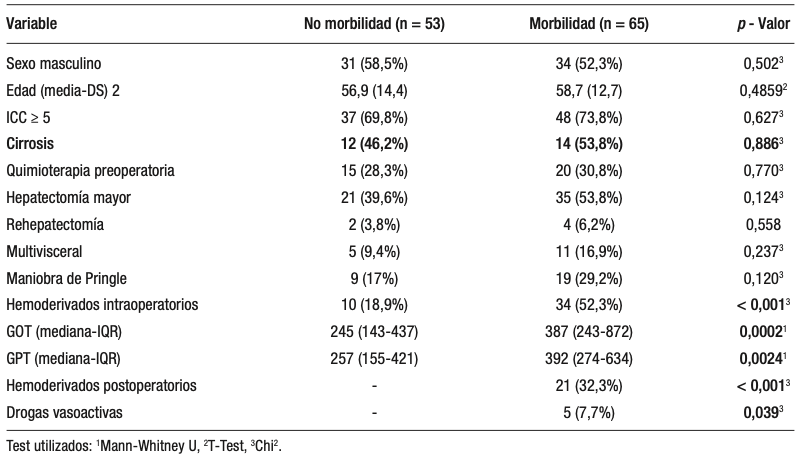
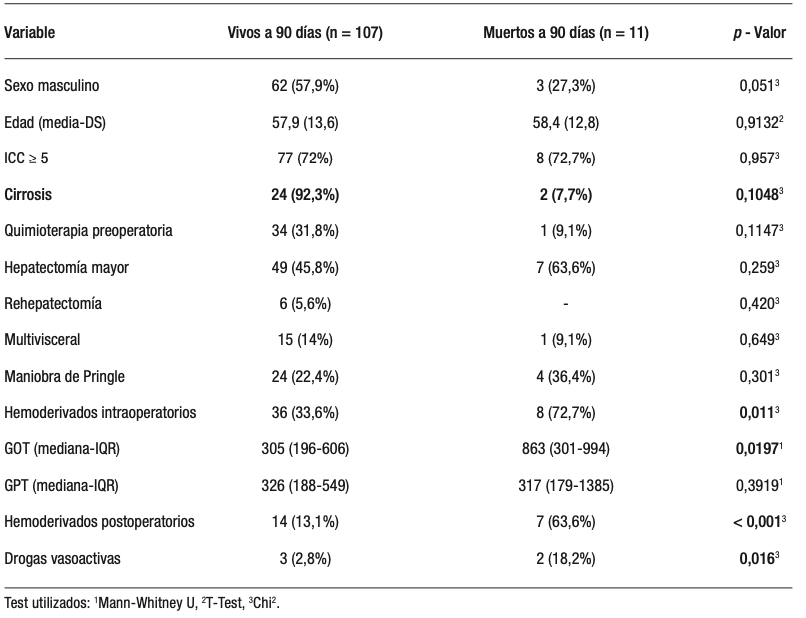
El análisis estadístico halló una relación significativa entre el desarrollo de complicaciones y los valores de GOT (mediana 387, r: 243-872 vs. mediana 245, r: 143-437, p = 0,0002) y GPT (mediana 392 r: 274-634 vs. 257 r: 155-421, p = 0,0024), el requerimiento intra y postoperatorio de hemoderivados (ambas p << 0,001) y el requerimiento de drogas vasoactivas en el postoperatorio inmediato (p = 0,039). No se hallaron diferencias significativas en cuanto a edad, sexo, comorbilidades, diagnóstico de cirrosis, tratamiento quimioterápico previo, magnitud de la hepatectomía, resección combinada de otros órganos y rehepatectomía (Tabla 3).
Tabla 3. Factores relacionados con el desarrollo de complicaciones
Respecto a la mortalidad, los resultados arrojaron diferencias estadísticamente significativas en los valores de GOT (mediana 863, r: 301-994 vs. mediana 305, r: 196-606, p = 0,0197), el requerimiento intra y postoperatorio de hemoderivados (p = 0,011 y p << 0,001, respectivamente), y el requerimiento de drogas vasoactivas en el postoperatorio inmediato (p = 0,016).
No se hallaron otras diferencias estadísticamente significativas (Tabla 4).
Tabla 4. Factores relacionados con mortalidad a 90 días
Se halló una asociación estadísticamente significativa entre los valores de GOT al primer día postoperatorio y el desarrollo de insuficiencia hepática postoperatoria (mediana 947, r: 863-994 vs. mediana 305, r: 200-606, p = 0,0118), no así para los valores de GPT (mediana 516, r: 307-544 vs. mediana 324, r: 179-549, p = 0,3531).
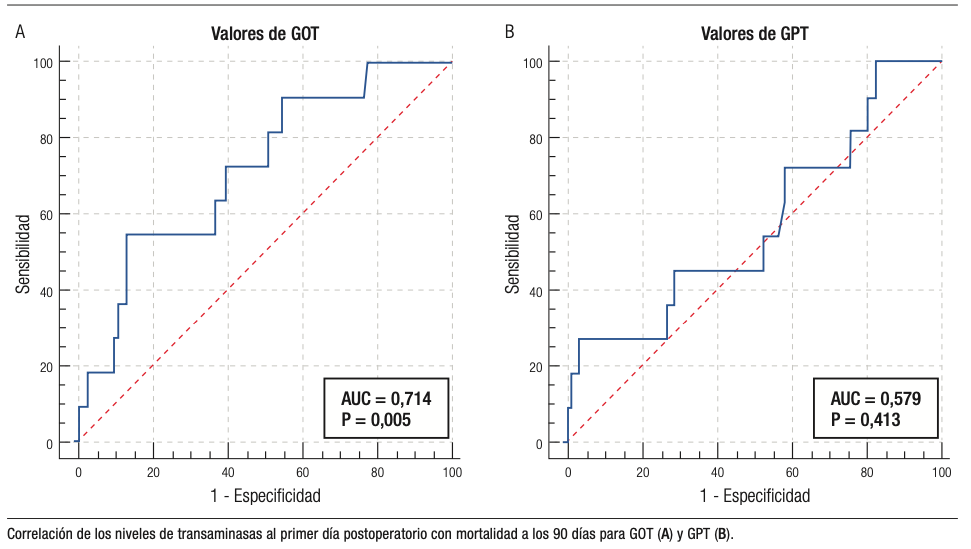
Se realizó un análisis de la curva ROC (Figura 2) para examinar el valor predictivo de los niveles de GOT y GPT en el primer día postoperatorio como indicadores de mortalidad quirúrgica a los 90 días. Los valores del área bajo la curva (AUC) para GOT y GPT predictores de mortalidad fueron 0,714 y 0,579, respectivamente; siendo el primero clasificado como aceptable y el segundo como regular. Se determinaron los valores de corte óptimos para la predicción de mortalidad postoperatoria utilizando los niveles de GOT y GPT en toda la cohorte, los cuales fueron de 856 (sensibilidad 54,6%, especificidad 93%) y 1341 (sensibilidad 27,3%, especificidad 97,2%) UI/L, respectivamente.
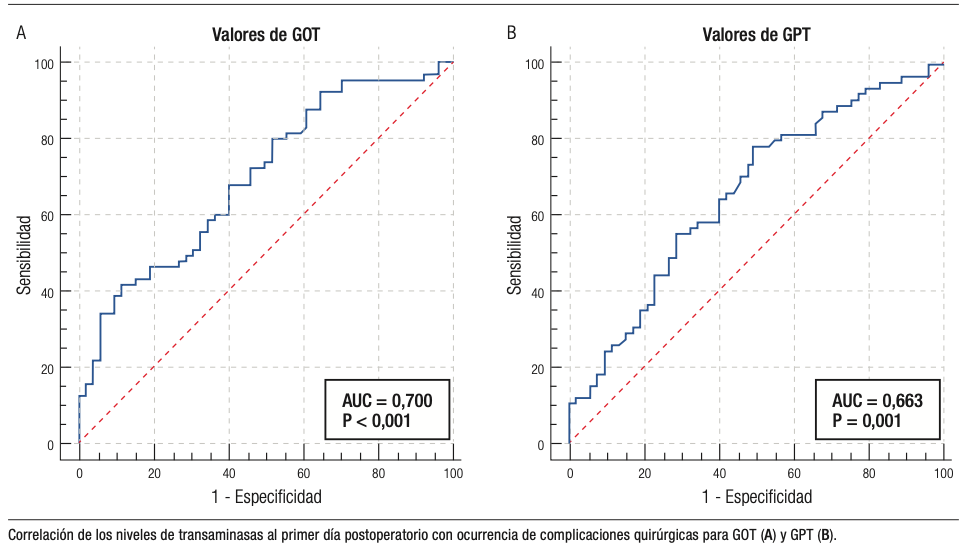
Se llevó a cabo un análisis de la curva ROC (Figura 3) para examinar el valor predictivo de los niveles de GOT y GPT en el primer día postoperatorio como indicadores de ocurrencia de complicaciones quirúrgicas. Los valores del área bajo la curva para GOT y GPT predictores de morbilidad fueron 0,700 y 0,663, respectivamente, siendo el primero clasificado como valor predictivo aceptable y el segundo como regular. Se determinaron los valores de corte óptimos para la predicción de ocurrencia de complicaciones postoperatorias utilizando los niveles de GOT y GPT en toda la cohorte, los cuales fueron de 530 (sensibilidad 41,5%, especificidad 88,7%) y 257 (sensibilidad 78,5%, especificidad 50,9%) UI/L, respectivamente.
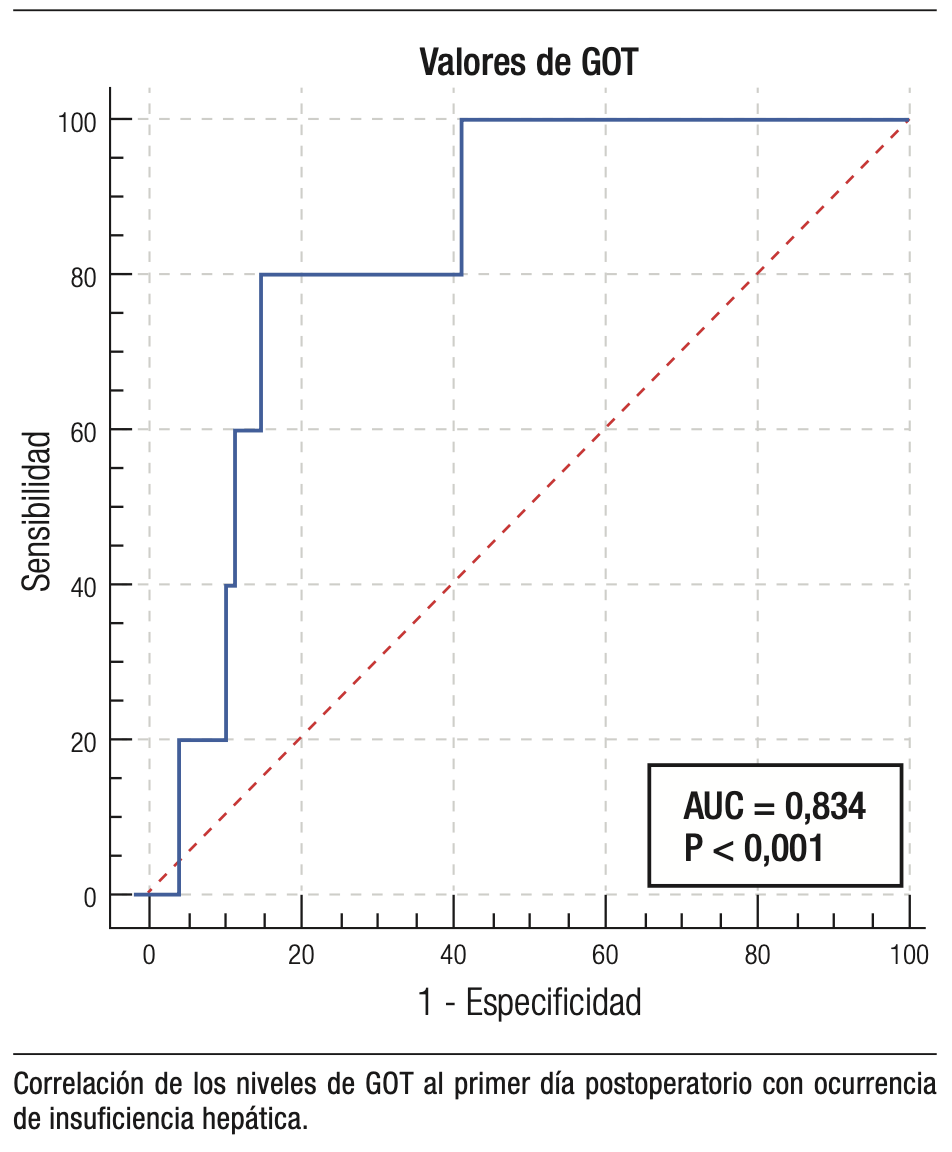
El análisis de la curva ROC (Figura 4) para evaluar el poder predictivo de GOT en el primer día postoperatorio como indicador de insuficiencia hepática reveló un área bajo la curva de 0,834, que se traduce en un valor predictivo sobresaliente. Se determinó un valor de corte óptimo para GOT > 856 UI/L (sensibilidad 80%, especificidad 85%).
Figura 2.
Figura 3.
Figura 4.
Se analizaron las variables relacionadas a los niveles elevados de GOT. El test de correlación de Spearman evidenció una relación positiva entre los valores de GOT al primer día postoperatorio y el tiempo quirúrgico (rho: 0,4663, p << 0.001). Otros factores que se asociaron a mayores niveles de la enzima fueron las hepatectomías mayores (mediana 492,5 r: 303,5 vs. mediana 223,5 r: 156-387, p << 0,001), el requerimiento de drogas vasoactivas en el postoperatorio inmediato (mediana 1604 r: 1314-2388 vs. mediana 305 r: 200-530, p = 0,004), la realización de la maniobra de Pringle (mediana 477 r: 273-884 vs. mediana 302,5 r: 178-528, p = 0,0046), las transfusiones de hemoderivados intra (mediana 483 r: 269-982,5 vs. mediana 270 r: 157-437, p = 0,0001) y postoperatorias (mediana 492 r: 306-947 vs. mediana 299 r:184-528, p = 0,009) y la ausencia de cirrosis (mediana 346,5 r: 221,5-708,5 vs. mediana 214 r: 156-324, p = 0,0154).
Los valores de GPT al primer día postoperatorio también mostraron una relación positiva con el tiempo quirúrgico (rho: 0.3984, p << 0.001), las hepatectomías mayores (mediana 437,5 r: 308-692 vs. mediana
255 r: 139-365, p << 0,01), el uso de drogas vasoactivas en el postoperatorio inmediato (mediana 1341
r: 803-1905 vs. mediana 137 r: 179-517, p = 0,0008), la realización de maniobra de Pringle (mediana 437,5 r: 307-757,5 vs. mediana 311 r: 163-517, p = 0,0029), la ausencia de cirrosis (mediana 355,5 r: 256,5-605 vs. mediana 191 r:109-324, p = 0,0005) y la transfusión de hemoderivados intraoperatorios (mediana: 437,5 r: 297,5-735 vs. mediana 299,5 r: 155-471, p = 0,0007), no así con los hemoderivados postoperatorios (mediana 410 r: 289-544 vs. 317 r: 188-549, p = 0,1930).
Discusión
Al analizar los resultados globales de nuestra serie, llama la atención el valor de mortalidad postoperatoria, que es aproximadamente el doble de lo reportado en la bibliografía.2,5 Atribuimos esto a varios factores: por un lado, se trata de una población con múltiples comorbilidades, como evidencia el hecho de que 72% de los pacientes presentaban un ICC ≥ 5. Además, la muestra estuvo conformada exclusivamente por patología neoplásica maligna, lo que acarrea un peor estado nutricional y performance status. Por otro lado, al ser nuestro centro una institución pública, la gran mayoría de la población hospitalaria presenta un bajo nivel socioeconómico, que frecuentemente conlleva demoras en el acceso a la atención y diagnóstico, lo que impacta directamente en el estadio y el pronóstico de su patología. Finalmente, esta muestra es heterogénea, e incluye casos de cirugía hepática extrema, que requirieron exclusión vascular total y reconstrucción venosa, los cuales se asocian a una mayor mortalidad.33
Luego de una resección hepática, las transaminasas experimentan una elevación en sus niveles, que habitualmente alcanza su pico en el primer día postoperatorio, para luego disminuir paulatinamente.34 Esta elevación es considerada un marcador de daño hepatocelular y, como tal, probablemente tenga una etiología multifactorial. La lesión por isquemia-reperfusión juega un rol conocido, siendo el paradigma de esto la realización de la maniobra de Pringle. Aunque el clampeo intermitente del pedículo ha demostrado contribuir en la elevación de transaminasas,35 es probable que por sí solo tenga un efecto menor en los niveles máximos de las enzimas. Este efecto resulta más pronunciado en asociación con la esteatosis hepática;36 sin embargo, en la bibliografía disponible no es habitual que se detalle el aspecto macroscópico o las características histológicas del hígado de los pacientes operados. El tiempo quirúrgico también ha demostrado ser un elemento condicionante de estos valores.34 Además, la manipulación del hígado en sí misma puede provocar lesión hepatocelular, como se ha informado anteriormente, lo cual probablemente sea un factor determinante más importante en las cirugías hepáticas más largas y complejas, debido a una manipulación hepática más extensa.37-38 En nuestra serie, esto se pone de manifiesto en la relación positiva hallada entre los valores crecientes de transaminasas con el tiempo quirúrgico y la realización de hepatectomías mayores. Todos estos factores podrían contribuir a los resultados contradictorios en varios informes sobre el valor predictivo de los niveles de GOT y GPT.
De todos modos, la bibliografía disponible sobre esta temática es reducida. En un estudio de Olthof y cols.,15 donde se incluyeron 539 resecciones hepáticas, se encontró que los niveles pico de transaminasas postoperatorias estuvieron asociados a complicaciones de grado III o superiores en la escala de Dindo-Clavien y a mayor requerimiento de transfusiones intraoperatorias. En esta cohorte se estableció como punto de corte de GOT para predecir la mortalidad 828 UI/L, con un área bajo la curva de 0,81 (0,73 – 0,89); el mismo fue un predictor independiente de mortalidad postoperatoria
(p < 0,01). Grat y cols.13 observaron, en una serie retrospectiva de 236 pacientes sometidos a resección hepática por metástasis de cáncer colorrectal, una asociación entre los valores de GOT y la mortalidad a 90 días, con un punto de corte de GOT a partir de 798 U/l (S 62,5%,
E 90,4%); sin embargo, hallaron como mejor predictor de morbilidad el valor de bilirrubina al primer día postoperatorio. Un estudio publicado en 2021 por De Klein y cols.14 demostró que la GOT, pero no la GPT, es un factor predictivo independiente de morbilidad mayor (p = 0,017) y que la probabilidad de complicaciones mayores aumenta significativamente en relación a los aumentos de GOT. Bhogal y cols.12 estudiaron exclusivamente los valores de GPT al primer día postoperatorio como predictor de morbimortalidad en pacientes con metástasis de origen colorrectal, pero tampoco pudieron demostrar su correlación. Estos hallazgos se encuentran en sintonía con los resultados del presente estudio. Analizando el área bajo la curva, encontramos que los valores predictivos de morbilidad y mortalidad para GOT resultan aceptables, no así los de GPT, cuya capacidad discriminatoria es regular; por este motivo no consideramos que la GPT sea un parámetro confiable para clasificar a los pacientes en bajo o alto riesgo. Por otro lado, observamos que el punto de corte óptimo de GOT para predecir mortalidad en nuestra serie fue de 856 UI/L, similar al reportado por Olthof y cols.
En el subgrupo de pacientes cirróticos, no hallamos diferencias en cuanto al desarrollo de complicaciones y mortalidad, aunque tanto la mediana de GOT como la de GPT fueron menores respecto a los no cirróticos, con una diferencia estadísticamente significativa. Suponemos que esto puede deberse a dos factores: por un lado, en su mayoría se trató de hepatectomías menores; por otro, la liberación de transaminasas postoperatoria responde a la injuria hepatocitaria. En un hígado cirrótico, donde gran parte del parénquima está sustituido por tejido fibrocicatrizal, sería lógico suponer que esta liberación de enzimas y, por lo tanto, su valor absoluto, sea menor. Esta teoría podría respaldarse considerando los hallazgos de Giovannini y cols.,34 que analizan los componentes de la hipertransaminasemia luego de una resección hepática, y muestran una relación inversa entre los picos de transaminasas y la presencia de cirrosis. Asimismo, un estudio de Fung y cols.,39 que analiza la utilidad del Índice de Retención de Verde de Indocianina a los 15 minutos (ICG R15) en la ocurrencia de complicaciones, mostró valores postoperatorios pico de transaminasas menores en pacientes que tenían un ICG R15 mayor a 10%, es decir, con menor reserva funcional hepática (GOT 294 UI/L vs. 521 UI/L, p = 0,029 y GPT 154 UI/L vs. 481 UI/L, p = 0,002). De cualquier manera, inferimos que la medición de enzimas como predictor de morbimortalidad probablemente presente una menor sensibilidad en cirróticos, y por ende sus valores deberían ser interpretados con cautela en este grupo.
Otro hallazgo relevante en nuestra serie fue la asociación entre los valores de GOT y el desarrollo de insuficiencia hepática postoperatoria. Esta relación ya había sido reportada por Vassanasiri y cols.40 que, en una población de 890 pacientes, demostraron que los puntos de corte para GOT de 260 UI/L y GPT de 270 UI/L fueron predictores independientes de insuficiencia hepática postoperatoria. En nuestro caso, el punto de corte difiere considerablemente, siendo de 856 UI/L. Sin embargo, el área bajo la curva refleja valores predictivos óptimos. Dado que las definiciones actuales de insuficiencia hepática postoperatoria toman como referencia los parámetros bioquímicos a partir del quinto día postoperatorio, consideramos que puede ser de suma utilidad disponer de un indicador temprano, como lo son las enzimas al primer día postoperatorio. Teniendo en cuenta la potencial severidad de esta entidad, y siendo su tratamiento fundamentalmente clínico y de soporte, una alerta precoz puede cambiar el pronóstico sustancialmente, favoreciendo el monitoreo minucioso de la evolución del paciente y evitando dilaciones en la toma de conductas agresivas.
Boissel y cols.41 describieron las tres principales características para considerar adecuado un marcador subrogado. La primera es la conveniencia, es decir, debe ser accesible y presentarse con mayor frecuencia que la variable de resultado en cuestión. La segunda es la relación entre el marcador y la variable de resultado; ésta debe ser bien establecida, cualitativa y cuantitativamente, a través de estudios epidemiológicos relevantes. Por último, se encuentra la estimación del beneficio clínico, es decir, los marcadores subrogados deben poder producir estimaciones de riesgo y beneficio paralelas a las variables de resultado que sustituyen. Consideramos que el dosaje de transaminasas en el primer día postoperatorio cumple con los postulados enunciados, al tratarse de una determinación de laboratorio fácilmente reproducible, de bajo costo, y cuya asociación con el desarrollo de complicaciones y mortalidad ha sido evidenciada en los resultados de nuestra serie. Sabemos, no obstante, que la estimación de riesgo debe ser mejor establecida mediante la realización de ensayos clínicos aleatorizados. Por otro lado, reconocemos algunas limitaciones en el presente estudio. En primer lugar, debido a su naturaleza retrospectiva, puede haber existido un sesgo de selección. En segundo lugar, las características de los pacientes sometidos a hepatectomía pueden ser heterogéneas. Finalmente, la población en estudio era pequeña, lo que resultó en un número relativamente reducido que podría haber afectado el poder del análisis. Sin embargo, esperamos que este trabajo pueda oficiar como punto de partida para profundizar los estudios en este campo de investigación.
Conclusión
En conclusión, encontramos una asociación significativa entre niveles elevados de GOT y GPT y la aparición de complicaciones quirúrgicas, así como la necesidad de hemoderivados y el uso de drogas vasoactivas en el postoperatorio inmediato. Además, los niveles altos de GOT se relacionaron con un mayor riesgo de insuficiencia hepática postoperatoria y mortalidad a los
90 días. Los valores predictivos de GOT para la mortalidad y las complicaciones fueron moderados, pero óptimos para la insuficiencia hepática postoperatoria. De estos resultados se desprende que los niveles de transaminasas son útiles como marcadores pronósticos en pacientes sometidos a hepatectomías por patología maligna.
Propiedad intelectual. Los autores declaran que los datos, las figuras y las tablas presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Mollard L, Gasque R A, Chahdi Beltrame M y col. Transaminasas en el primer día poshepatectomía y predicción de resultados en patología maligna. Acta Gastroenterol Latinoam. 2025;55(4):358-370. https://doi.org/10.52787/agl.v55i4.547
Referencias
- Jarnagin WR, Gonen M, Fong Y, DeMatteo RP, Ben-Porat L, Little S, Corvera C, Weber S, & Blumgart LH. Improvement in perioperative outcome after hepatic resection: analysis of 1,803 consecutive cases over the past decade. Ann Surg. 2002; 236(4):397-407.
- Botea F, Ionescu M, Braşoveanu V, Hrehoreţ D, Alexandrescu S, Grigorie M, Stanciulea O, Nicolaescu D, Tomescu D, Droc G, Ungureanu D, Fota R, Croitoru A, Gheorghe L, Gheorghe C, Lupescu I, Grasu M, Boroş M, Dumitru R, Toma M, Herlea V, Popescu I. Liver Resections in a High-Volume Center: Form Standard Procedures to Extreme Surgery and Ultrasound-guided Resections. Chirurgia (Bucur). 2017 May-Jun;112(3):259-277.
- Dokmak S, Ftériche FS, Borscheid R, Cauchy F, Farges O, Belghiti J. 2012 Liver resections in the 21st century: we are far from zero mortality. HPB (Oxford). 2013 Nov;15(11):908-15.
- Franken LC, Schreuder AM, Roos E, van Dieren S, Busch OR, Besselink MG, van Gulik TM. Morbidity and mortality after major liver resection in patients with perihilar cholangiocarcinoma: A systematic review and meta-analysis. Surgery. 2019 May;165(5):918-928.
- Azoulay D, Bhangui P, Pascal G, Salloum C, Andreani P, Ichai P, Saliba F, Lim C. The impact of expanded indications on short-term outcomes for resection of malignant tumours of the liver over a 30 year period. HPB (Oxford). 2017 Jul;19(7):638-648.
- Mahlmann JC, Wirth TC, Hartleben B, Schrem H, Mahlmann JF, Kaltenborn A, Klempnauer J, Kulik U. Chemotherapy and Hepatic Steatosis: Impact on Postoperative Morbidity and Survival after Liver Resection for Colorectal Liver Metastases. Visc Med. 2021 Jun;37(3):198-205.
- Bagante F, Ruzzenente A, Beal EW, Campagnaro T, Merath K, Conci S, Akgül O, Alexandrescu S, Marques HP, Lam V, Shen F, Poultsides GA, Soubrane O, Martel G, Iacono C, Guglielmi A, Pawlik TM. Complications after liver surgery: a benchmark analysis. HPB (Oxford). 2019 Sep;21(9):1139-1149.
- Rössler F, Sapisochin G, Song G, Lin YH, Simpson MA, Hasegawa K, Laurenzi A, Sánchez Cabús S, Nunez MI, Gatti A, Beltrame MC, Slankamenac K, Greig PD, Lee SG, Chen CL, Grant DR, Pomfret EA, Kokudo N, Cherqui D, Olthoff KM, Shaked A, García-Valdecasas JC, Lerut J, Troisi RI, De Santibanes M, Petrowsky H, Puhan MA, Clavien PA. Defining Benchmarks for Major Liver Surgery: A multicenter Analysis of 5202 Living Liver Donors. Ann Surg. 2016 Sep;264(3):492-500.
- Aloia TA, Fahy BN, Fischer CP, Jones SL, Duchini A, Galati J, Gaber AO, Ghobrial RM, Bass BL. Predicting poor outcome following hepatectomy: analysis of 2313 hepatectomies in the NSQIP database. HPB (Oxford). 2009 Sep;11(6):510-5.
- Vasavada B, Patel K. Postoperative Morbidity after Liver Resection – A Systemic Review, Meta-analysis and Metaregression of Factors Affecting Them. Surg Chron 2022; 27(2): 143-149
- Boleslawski E, Vibert E, Pruvot FR, Le Treut YP, Scatton O, Laurent C, Mabrut JY, Régimbeau JM, Adham M, Cosse C, Farges O. Relevance of postoperative peak transaminase after elective hepatectomy. Ann Surg. 2014 Nov;260(5):815-20; discussion 820-1.
- Bhogal RH, Nair A, Papis D, Hamady Z, Ahmad J, Lam FT, Khan S, Marangoni G. Postoperative day one serum alanine aminotransferase does not predict patient morbidity and mortality after elective liver resection in non-cirrhotic patients. Hepatobiliary Pancreat Dis Int. 2016 Dec;15(6):655-659.
- Grąt M, Hołówko W, Lewandowski Z, Kornasiewicz O, Barski K, Skalski M, Zieniewicz K, Krawczyk M. Early post-operative prediction of morbidity and mortality after a major liver resection for colorectal metastases. HPB (Oxford). 2013 May;15 (5):352-8.
- de Klein GW, Brohet RM, Liem MSL, Klaase JM. Post-operative Day 1 Serum Transaminase Levels in Relation to Morbidity After Liver Resection. World J Surg. 2022;46(2):433-440.
- Olthof PB, Huiskens J, Schulte NR, Wicherts DA, Besselink MG, Busch OR, Heger M, van Gulik TM. Postoperative peak transaminases correlate with morbidity and mortality after liver resection. HPB (Oxford). 2016 Nov;18(11):915-921.
- D’Amico G, Garcia-Tsao G, Pagliaro L. Natural history and prognostic indicators of survival in cirrhosis: a systematic review of 118 studies. J Hepatol. 2006 Jan;44(1):217-31.
- Lee JS, Choi HW, Kim JS, Lee TY, Yoon YC. Update on Resection Strategies for Hepatocellular Carcinoma: A Narrative Review. Cancers (Basel). 2024 Dec 6;16(23):4093.
- Delis SG, Bakoyiannis A, Biliatis I, Athanassiou K, Tassopoulos N, Dervenis C. Model for end-stage liver disease (MELD) score, as a prognostic factor for post-operative morbidity and mortality in cirrhotic patients, undergoing hepatectomy for hepatocellular carcinoma. HPB (Oxford). 2009 Jun;1
(4):351-7. - Elshaarawy O, Aman A, Zakaria HM, Zakareya T, Gomaa A, Elshimi E, Abdelsameea E. Outcomes of curative liver resection for hepatocellular carcinoma in patients with cirrhosis. World J Gastrointest Oncol. 2021 May 15;13(5):424-439.
- Torzilli G, Viganò L, Cimino M, Imai K, Vibert E, Donadon M, Mansour D, Castaing D, Adam R. Is Enhanced One-Stage Hepatectomy a Safe and Feasible Alternative to the Two-Stage Hepatectomy in the Setting of Multiple Bilobar Colorectal Liver Metastases? A Comparative Analysis between Two Pioneering Centers. Dig Surg. 2018;35(4):323-332.
- Torzilli G, Serenari M, Viganò L, Cimino M, Benini C, Massani M, Ettorre GM, Cescon M, Ferrero A, Cillo U, Aldrighetti L, Jovine E. Outcomes of enhanced one-stage ultrasound-guided hepatectomy for bilobar colorectal liver metastases compared to those of ALPPS: a multicenter case-match analysis. HPB (Oxford). 2019 Oct;21(10):1411-1418.
- Ironside N, Bell R, Bartlett A, McCall J, Powell J, Pandanaboyana S. Systematic review of perioperative and survival outcomes of liver resections with and without preoperative portal vein embolization for colorectal metastases. HPB (Oxford). 2017 Jul;19(7):559-566.
- Charlson ME, Pompei P, Ales KL, MacKenzie CR. A new method of classifying prognostic comorbidity in longitudinal studies: development and validation. J Chronic Dis. 1987;40(5):373-83.
- Pang YY. The Brisbane 2000 terminology of liver anatomy and resections. HPB 2000; 2:333-39. HPB (Oxford). 2002;4(2):99; author reply 99-100
- Dindo D, Demartines N, Clavien PA. Classification of surgical complications: a new proposal with evaluation in a cohort of 6336 patients and results of a survey. Ann Surg. 2004;240(2)
:205-213. - Rahbari NN, Garden OJ, Padbury R, Brooke-Smith M, Crawford M, Adam R, Koch M, Makuuchi M, Dematteo RP, Christophi C, Banting S, Usatoff V, Nagino M, Maddern G, Hugh TJ, Vauthey JN, Greig P, Rees M, Yokoyama Y, Fan ST, Nimura Y, Figueras J, Capussotti L, Büchler MW, Weitz J. Posthepatectomy liver failure: a definition and grading by the International Study Group of Liver Surgery (ISGLS). Surgery. 2011 May;149(5):713-24.
- Sultana A, Brooke-Smith M, Ullah S, Figueras J, Rees M, Vauthey JN, Conrad C, Hugh TJ, Garden OJ, Fan ST, Crawford M, Makuuchi M, Yokoyama Y, Büchler M, Padbury R. Prospective evaluation of the International Study Group for Liver Surgery definition of post hepatectomy liver failure after liver resection: an international multicentre study. HPB (Oxford). 2018 May;20(5):462-469.
- Mullen JT, Ribero D, Reddy SK, Donadon M, Zorzi D, Gautam S, Abdalla EK, Curley SA, Capussotti L, Clary BM, Vauthey JN. Hepatic insufficiency and mortality in 1,059 noncirrhotic patients undergoing major hepatectomy. J Am Coll Surg. 2007 May;204(5):854-62; discussion 862-4.
- Balzan S, Belghiti J, Farges O, Ogata S, Sauvanet A, Delefosse D, Durand F. The «50-50 criteria» on postoperative day 5: an accurate predictor of liver failure and death after hepatectomy. Ann Surg. 2005 Dec;242(6):824-8, discussion 828-9.
- Mayo SC, Shore AD, Nathan H, Edil BH, Hirose K, Anders RA, Wolfgang CL, Schulick RD, Choti MA, Pawlik TM. Refining the definition of perioperative mortality following hepatectomy using death within 90 days as the standard criterion. HPB (Oxford). 2011 Jul;13(7):473-82.
- Egger ME, Ohlendorf JM, Scoggins CR, McMasters KM, Martin RC 2nd. Assessment of the reporting of quality and outcome measures in hepatic resections: a call for 90-day reporting in all hepatectomy series. HPB (Oxford). 2015 Sep;17(9):839-45.
- Schiergens TS, Dörsch M, Mittermeier L, Brand K, Küchenhoff H, Lee SM, Feng H, Jauch KW, Werner J, Thasler WE. Thirty-day mortality leads to underestimation of postoperative death after liver resection: A novel method to define the acute postoperative period. Surgery. 2015 Dec;158(6):1530-7.
- Azoulay D, Pascal G, Salloum C, Adam R, Castaing D, Tranecol N. Vascular reconstruction combined with liver resection for malignant tumours. Br J Surg. 2013 Dec;100(13):1764-75.
- Giovannini I, Chiarla C, Giuliante F, Vellone M, Ardito F, Sarno G, Nuzzo G. Analysis of the components of hypertransaminasemia after liver resection. Clin Chem Lab Med. 2007;45
(3):357-60. - Gurusamy KS, Sheth H, Kumar Y, Sharma D, Davidson BR. Methods of vascular occlusion for elective liver resections. Cochrane Database Syst Rev. 2009 Jan 21;(1):CD007632.
- Belghiti J, Noun R, Malafosse R, Jagot P, Sauvanet A, Pierangeli F, Marty J, Farges O. Continuous versus intermittent portal triad clamping for liver resection: a controlled study. Ann Surg. 1999 Mar;229(3):369-75.
- van den Broek MA, Shiri-Sverdlov R, Schreurs JJ, Bloemen JG, Bieghs V, Rensen SS, Dejong CH, Olde Damink SW. Liver manipulation during liver surgery in humans is associated with hepatocellular damage and hepatic inflammation. Liver Int. 2013 Apr;33(4):633-41.
- van de Poll MC, Derikx JP, Buurman WA, Peters WH, Roelofs HM, Wigmore SJ, Dejong CH. Liver manipulation causes hepatocyte injury and precedes systemic inflammation in patients undergoing liver resection. World J Surg. 2007 Oct;31(10):2033-8.
- Fung J, Poon RT, Yu WC, Chan SC, Chan AC, Chok KS, Cheung TT, Seto WK, Lo CM, Lai CL, Yuen MF. Use of liver stiffness measurement for liver resection surgery: correlation with indocyanine green clearance testing and post-operative outcome. PLoS One. 2013 Aug 28;8(8):e72306.
- Vassanasiri W, Rungsakulkij N, Suragul W, Tangtawee P, Muangkaew P, Mingphruedhi S, Aeesoa S. Early postoperative serum aspartate aminotransferase for prediction of post-hepatectomy liver failure. Perioper Med (Lond). 2022 Oct 7;11(1):51.
- Boissel JP, Collet JP, Moleur P, Haugh M. Surrogate endpoints: a basis for a rational approach. Eur J Clin Pharmacol. 1992;43(3):235-44.
Correspondencia: Lourdes Mollard
Correo electrónico: lourdes.mollard@gmail.com
Acta Gastroenterol Latinoam 2025;55(4):358-370
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE