José María Alvarez Gallesio,1 Maximiliano Bun,1, 2 Lisandro Pereyra,2 Francisco Schlottmann,1 José Manuel Mella,2 Carlos Peczan,1, 2 Daniel Gustavo Cimmino,2 Nicolás Agustín Rotholtz1, 2
1 Servicio de Cirugía General.
2 Servicio de Endoscopía.
Hospital Alemán de Buenos Aires, Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2018;48(2):117-123
Recibido: 19/06/2017 / Aprobado: 08/01/2018 / Publicado en www.actagastro.org el 18/06/2018
Resumen
La obstrucción colorrectal aguda neoplásica es una situación frecuente que requiere clásicamente un tratamiento quirúrgico de urgencia. El uso de stents auto-expansibles ha surgido como una alternativa terapéutica. Objetivos. Evaluar la eficacia y la seguridad de la colocación de prótesis auto-expansibles en el tratamiento de la obstrucción colorrectal neoplásica. Comparar los resultados según la causa sea intrínseca o extrínseca. Material y métodos. Estudio retrospectivo de una serie consecutiva de pacientes con obstrucción colorrectal neoplásica y colocación de stent endoscópico auto-expansible, entre 2005 y 2017. Fueron analizadas las variables demográficas, clínicas, el éxito en la colocación, el éxito clínico (paliación y/o puente a la cirugía), las complicaciones tempranas y las alejadas. Se realizó el análisis comparativo según la obstrucción colorrectal fuera de tipo intrínseca grupo1 (G1) o extrínseca grupo 2 (G2). Resultados. Se realizaron 33 procedimientos en 34 pacientes. Edad mediana 66 años (rango: 29-98). El éxito en la colocación fue del 88,2%, con un tiempo promedio de 49,4 minutos (rango: 20-120) y sin complicaciones durante el procedimiento. La mediana de seguimiento fue de 5 meses (0,3-26). En 10 pacientes se colocó el stent como puente a la cirugía. El éxito clínico fue del 93%. La tasa de migración fue de 8,8% y la de perforación 2,9%. El éxito en la colocación fue superior en G1 (100% vs. 42,8%; p = 0,001) y el éxito clínico fue similar en ambos grupos (G1 100% vs. G2 93%; p = 0,6). Conclusiones. La utilización de stents auto-expansibles constituye una alternativa eficaz y segura en el tratamiento de la obstrucción colorrectal neoplásica. El éxito en la colocación es mayor en los pacientes con obstrucción neoplásica intrínseca.
Palabras claves. Cáncer colorrectal, prótesis colónica, obstrucción colorrectal, éxito en la colocación, éxito clínico.
Outcomes of self-expandable stent for the treatment of acute neoplasic colorectal obstruction. Intrinsic vs. extrinsic neoplasia
Summary
Acute malignant colorectal obstruction is a common situation that usually requires emergency surgical treatment. Self-expanding stents has emerged as a therapeutic alternative. Aim. To evaluate the efficacy and safety of self-expandable colonic stents for the treatment of colorectal neoplastic obstruction. Comparative analysis is performed according to the type of obstruction. Material and methods. A retrospective study of a consecutive series of patients with malignant colorectal obstruction and endoscopic placement of self-expanding stent, between 2005 and 2017. Demographic and clinical variables, technical success, clinical success (palliation and / or bridge to surgery), early and late complications were analyzed. A comparative analysis was performed according to the type of obstruction, intrinsic (G1) or extrinsic (G2). Results. 34 procedures were performed in 33 patients. Median age was 66 years (range: 29-98). Technical success was 88.2%, with a mean procedure time of 49.4 minutes (range: 20-120). No complications were registered during stent placement. Median follow up was 5 months (range: 0.3-26). The stent as a bridge to surgery was placed in 10 patients. Clinical success was 93%. Stent migration and perforation rates were 8.8% and 2.9% respectively. Technical success was higher in G1 (100% vs. 42.8%; p = 0.001). Clinical success was similar between groups (G1 100% vs. G2 93%, p = 0.6). Conclusion. The use of self-expanding stents is effective and safe in the treatment of neoplastic colorectal obstruction. The technical success is higher in patients with intrinsic neoplastic obstruction.
Key words. Colorectal cancer, colonic stent, colorectal obstruction, technical success, clinical success.
Abreviaturas
SCA: stent colónico auto-expansible.
G1: Grupo 1.
G2: Grupo 2.
El cáncer colorrectal presenta una incidencia global de 1 millón de nuevos casos por año, es la tercera en frecuencia en mujeres y cuarta en hombres.1 Su presentación clínica como cuadro de obstrucción intestinal ocurre entre el 10 y el 25 % de los pacientes.2 El tratamiento estándar para este tipo de síndromes suele ser la cirugía, siendo la misma paliativa o potencialmente curativa.
La cirugía de urgencia en pacientes en mal estado general y sin preparación colónica posee una morbimortalidad significativamente mayor que la cirugía electiva.1-3 Es por ello que habitualmente el tratamiento quirúrgico ante una obstrucción colónica neoplásica se realiza en dos tiempos. En primer lugar, se intenta aliviar la sintomatología mediante una ostomía descompresiva (con o sin resección del tumor primario), para luego restablecer el tránsito intestinal en un segundo tiempo quirúrgico. Sin embargo, en aproximadamente un 50% de los pacientes ostomizados nunca se realiza la reconstrucción del tránsito con la consecuente pérdida en la calidad de vida y complicaciones asociadas.1-4
En este contexto, la prótesis (stent) colónica auto-expansible (SCA) podría ser una alternativa terapéutica para la obstrucción colónica neoplásica.5 De esta manera se aliviarían los síntomas obstructivos evitando la morbimortalidad asociada a la cirugía de urgencia.
Inicialmente, la colocación de SCA se postuló como una alternativa únicamente paliativa;6 no obstante, diversos estudios muestran la utilidad del SCA en pacientes con cáncer colorrectal resecable como puente a la cirugía.7-9 De esta manera se logra mejorar el estado clínico del paciente, con la posibilidad de realizar una resección quirúrgica electiva y anastomosis primaria con mejores resultados posoperatorios.7-10
Sin embargo, no existen muchos reportes que describan factores asociados al fracaso del SCA, dado que son difíciles de detectar en pequeñas series donde las tasas de éxito globales (técnico y clínico) suelen ser altas.
El único factor ya descripto asociado con una menor tasa de éxito técnico fue la presencia de carcinomatosis. Las fallas técnicas suelen relacionarse con complicaciones de procedimiento tales como perforación o la incapacidad para desplegar un stent o falla en la expansión de este. El éxito clínico presenta una tendencia a ser mayor en pacientes donde la prótesis actúa como puente a la cirugía. Cuando el stent se realiza para una obstrucción secundaria a una neoplasia colorrectal primaria, la tasa de éxito clínico descripta es mayor.11
El objetivo primario de este estudio fue evaluar la eficacia y seguridad de la colocación de SCA para el tratamiento de las obstrucciones colorrectales de origen neoplásico. En forma secundaria, comparar los resultados del SCA entre aquellos pacientes con obstrucciones según la causa fuera intrínseca o extrínseca.
Material y métodos
Se realizó un estudio observacional, analítico y retrospectivo sobre una base de datos cargada en forma prospectiva en el período comprendido entre junio de 2005 y marzo de 2017. Se incluyeron todos los pacientes sometidos en forma consecutiva a colocación de SCA para tratamiento de obstrucciones colónicas agudas neoplásicas. El diagnóstico de obstrucción neoplásica se efectuó mediante parámetros clínicos, bioquímicos, radiológicos (Rx de abdomen de pie, TC de abdomen y pelvis, colon por enema según fuera necesario).
El SCA se indicó con criterio paliativo en estadios avanzados de enfermedad o bien como puente a la cirugía. Se definió “puente a la cirugía” a aquellos pacientes considerados potenciales candidatos a resección quirúrgica, donde la colocación del stent permitiría resolver la oclusión, optimizar la condición clínica del paciente y estadificar correctamente la enfermedad. La colocación del SCA fue realizada por cirujanos colorrectales y gastroenterólogos utilizando colonoscópios (CV-180, Olympus, Tokio, Japón) en la sala de endoscopía. La técnica utilizada en todos los casos se efectuó bajo guía endoscópica-radiológica y con sedación. Una vez alcanzada la estenosis se realizó un estudio radiológico con contraste para evaluar el pasaje a proximal y la longitud de la lesión. Luego se progresó una guía de alambre a través de la obstrucción, seguida de la progresión de la endoprótesis a través del canal de trabajo, con posterior apertura y expansión en el sitio de la estenosis. Se utilizaron stents auto-expansibles de nitinol no recubiertos (Boston Wallflex, Boston, Massachusetts, Estados Unidos) con longitudes entre 9 y 12 cm y con un diámetro de 22 a 25 mm según la extensión de la estenosis. Luego de la colocación se realizó un control radiológico entre las 24 y 48 horas posteriores para evaluar el correcto posicionamiento de la prótesis.
Se analizaron variables demográficas, topografía de la obstrucción e intención terapéutica (paliación o puente a la cirugía). Además, se evaluó el éxito en la colocación, el éxito clínico y las complicaciones luego del procedimiento. El éxito técnico fue definido como el correcto posicionamiento y expansión del stent en el sitio de obstrucción neoplásica.
El éxito clínico fue determinado como el restablecimiento de la ingesta oral asociado a un tránsito intestinal normal en todos aquellos pacientes donde la colocación del stent fue exitosa. Las complicaciones se dividieron en tempranas o tardías según fueran dentro de los primeros 30 días de colocado el stent o luego de dicho período respectivamente.
Se realizó un análisis comparativo de las variables en estudio de acuerdo a si la obstrucción neoplásica colónica fuera de tipo intrínseca G1 (neoplasia primaria de colon) o extrínseca G2 (neoplasia extracolónica).
Los datos fueron estadísticamente valorados a través de las pruebas Chi², test t de Student según fuera necesario utilizando el paquete SPSS v20. Todos los métodos consideraron significativa a una p < 0,05.
Resultados
Durante el período de estudio, se realizaron 34 procedimientos de colocación de SCA en 33 pacientes (un paciente requirió 2 stents) con obstrucción colorrectal de origen neoplásico. Veintidós fueron hombres (65%) y con una edad mediana de 68 años (rango: 29-98). En 21 casos la obstrucción se localizó en colon (11 sigmoides, 6 ángulo esplénico, 2 ángulo hepático, 2 descendente), 4 en la unión rectosigmoidea, 4 en recto superior y 4 en recto medio. La etiología de la obstrucción fue adenocarcinoma colorrectal en 27 pacientes (82%) y en 7 casos (18%) la oclusión fue causada por neoplasias extracolónicas (1 próstata, 1 ovario, 2 endometrio, 2 páncreas y 1 vesícula) (Tabla 1). El éxito en la colocación del stent fue del 88,2% y el tiempo promedio del procedimiento 49,4 minutos (rango: 20-120). Dos procedimientos (5,8 %) requirieron dilatación con balón previa a la colocación por dificultad de progresión de dispositivo previo a la apertura del stent. No se registraron complicaciones durante las intervenciones.
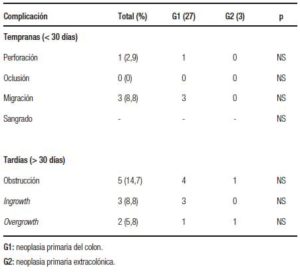
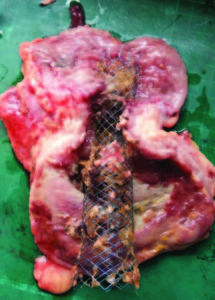
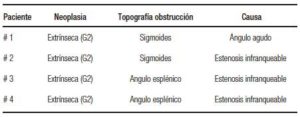
Con una mediana de seguimiento de 5 meses (rango: 0,3-26), el éxito clínico de la totalidad de la serie fue del 93% (Tabla 2). En 10 pacientes con CCR el SCA fue utilizado como puente a la cirugía con intencionalidad curativa, logrando en 9 casos (90%) resecciones colónicas con anastomosis primaria sin ostomía en forma programada. El tiempo promedio entre la colocación del stent y la cirugía programada fue de 9 meses (rango: 6-20). En 8 casos el abordaje fue laparoscópico. En el otro paciente donde el objetivo fue el puente a la cirugía, el stent migró sin necesidad de recolocación o cirugía de urgencia (Figura 1). Luego de la colocación de la prótesis, cinco pacientes presentaron obstrucción con requerimiento de cirugía de urgencia con confección de ostomía (2 pacientes al mes, 2 a los 2 meses y el otro a los 3 meses). Tres pacientes (8,8%) presentaron migración del stent, uno de los cuales requirió la recolocación. Los dos casos restantes no manifestaron nuevamente síntomas obstructivos luego de la migración, pudiendo cumplir el tratamiento quimioterápico sin necesidad de cirugía. La tasa de perforación luego de colocado el stent fue del 2,9% (1 paciente). Este caso recibió tratamiento quimioterápico previo con FOLFOX (leucovorina cálcica, fluorouracilo y oxaliplatino) más anticuerpo monoclonal Bevacizumab. Las tasas de complicaciones tempranas y tardías fueron similares entre los pacientes con neoplasia primaria de colon y aquellos con compresión extrínseca (G1: 33% vs. G2: 30%; p = NS) (Tabla 3). El éxito en la colocación del stent fue superior en pacientes con neoplasia primaria de colon (G1: 100% vs. G2: 42.8%; p = 0,006). El fracaso en la colocación de los 4 pacientes en G2 se debió a una angulación a nivel del colon sigmoides en un paciente, e imposibilidad de progresar el alambre guía distal a la obstrucción en tres pacientes (Tabla 4). El éxito clínico fue similar en ambos grupos (G1 93% vs. G2 100%) (Tabla 5).
Tabla 2. Variables de la colocación del stent colónico auto-expansible.
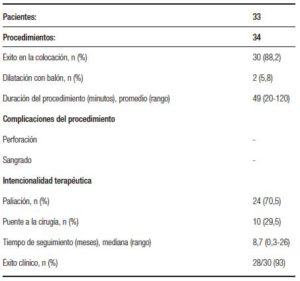
Tabla 4. Obstrucción primaria (G1) vs. obstrucción secundaria (G2).
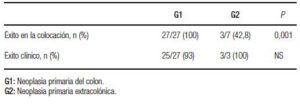
Tabla 5. Falla en la colocación del SCEA.
Discusión
La cirugía de urgencia por obstrucción colónica neoplásica conlleva un elevado riesgo para los pacientes en términos de morbilidad y mortalidad.12 En un escenario de enfermedad neoplásica avanzada y tratamientos paliativos, los pacientes deben recuperarse de una cirugía al mismo tiempo que familiarizarse con la ostomía en los últimos meses de su vida. En aquellos casos con enfermedad resecable la propia distensión colónica y el mal estado general del paciente pueden hacer improbable una anastomosis primaria posterior a la resección colónica. A esto se suma la dificultad para realizar un abordaje laparoscópico con la consiguiente pérdida de los beneficios del método. En otros casos con enfermedad metastásica potencialmente resecable (por ej. secundarismo hepático bilobar), la colocación de un SCA permite comenzar un tratamiento quimioterápico sistémico y evaluar respuesta para luego planificar la resección de las metástasis y del tumor primario en forma programada ante una respuesta favorable. Es por ello que el empleo de SCA en diferentes escenarios de obstrucción colónica por cáncer puede brindar beneficios.
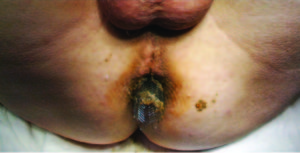
La utilización de SCA ha demostrado reducción de la morbilidad, mortalidad y estadía hospitalaria en comparación con la cirugía.13 Si bien el éxito del procedimiento es variable según los diversos centros, Watt y col. evaluaron mediante una revisión sistemática la colocación de SCA en 1785 pacientes con obstrucción intrínseca, y reportaron un éxito técnico y clínico del 96,2% y 92% respectivamente.14 En nuestra serie en dicha población, el éxito técnico y clínico fue 100% y 93% respectivamente. El procedimiento resultó seguro, sin complicaciones durante la colocación y con una tasa de migración del 8,8%, homologable a lo descripto en 2 revisiones sistemáticas donde la tasa de migración fue entre 10 y 12%.15, 16 Entre las potenciales complicaciones posteriores al procedimiento se describen el dolor, el sangrado, la reestenosis y la perforación, siendo esta última la más grave. La tasa de perforación en la literatura es de un 4%, equiparable al 2,9% de la presente serie.15 Los factores conocidos asociados a la perforación son la dilatación con balón y la quimioterapia con drogas antiangiogénicas,17 siendo esta última un factor posiblemente asociado a la única perforación encontrada en esta serie (Figura 2). No obstante, ninguno de los pacientes con dilataciones con balón sufrió esta complicación.
Teniendo en cuenta lo previamente mencionado, en centros con experiencia en procedimientos endoscópicos terapéuticos, la utilización de SCA es segura y efectiva en la mayoría de los casos.
Por otro lado, el SCA ha surgido como una opción de descompresión temporaria y puente hacia una cirugía electiva.18-20 Esta alternativa, no solo mejora el estado general del paciente, pudiendo evitar una ostomía al realizar una cirugía diferida con anastomosis primaria, sino que también permitiría un estudio más exhaustivo para detectar lesiones colorrectales sincrónicas o bien metástasis a distancia, que cambiarían el abordaje terapéutico de la patología.21-23 No obstante, la colocación de SCA como puente a una cirugía es controvertido. La Sociedad Europea de Gastroenterología y Endoscopia (ESGE) no recomienda el SCA como puente a la cirugía, sin embargo, lo defiende como una alternativa a la cirugía de emergencia en aquellos pacientes con elevado riesgo quirúrgico.24 Empero en nuestra experiencia, en diez pacientes con cáncer colorrectal como causa de obstrucción se utilizó el stent como puente a la cirugía con intencionalidad curativa. Dentro de ellos, en ocho (80%) se realizó una cirugía laparoscópica posterior y en nueve (90%) se logró confeccionar una anastomosis primaria sin ostomía. Como contrapartida, el uso de un stent conlleva el riesgo de perforación tumoral con la consecuente siembra tumoral e impacto negativo en la supervivencia.25 Sumado a esto, se ha planteado que la prótesis colónica podría provocar una reacción inflamatoria con liberación de células tumorales al torrente sanguíneo, diseminando la enfermedad.26 Malgras y col. identificaron en un modelo murino el proceso metastásico inducido por el stent con una marcada elevación de LDH plasmática y menor sobrevida.27 Sin embargo, no existe hasta el momento evidencia suficiente de que el empleo de SCA como puente a la cirugía empeore el pronóstico oncológico de los pacientes.28
El origen de la obstrucción neoplásica podría influir en la factibilidad de la colocación, siendo las obstrucciones extrínsecas más dificultosas de paliar con el stent. Keswani y col.29 evaluaron factores asociados al éxito de la colocación del SCA y el único predictor de falla técnica resultó la obstrucción colónica extrínseca. En nuestra cohorte, al comparar los resultados entre aquellos pacientes con obstrucciones intrínsecas y aquellos con compresiones extracolónicas, obtuvimos una diferencia significativa en el éxito en la colocación a favor de los pacientes con neoplasia colónicas (100% vs. 42,8%; p = 0,001).
El presente trabajo presenta ciertas limitaciones. En primer lugar, la naturaleza retrospectiva podría generar un sesgo de selección de pacientes. El corto período de seguimiento obedece a que la mayoría de los pacientes presentaron enfermedad neoplásica avanzada. Por otro lado, no existió grupo control de pacientes sometidos a cirugía, lo que imposibilita la comparación de resultados entre aquellos sometidos a una cirugía de urgencia y a los que se les colocó un SCA ante una obstrucción colónica neoplásica. Sin embargo, el correcto registro de historia clínica informatizada permitió obtener detalladamente los resultados técnicos y clínicos y las complicaciones asociadas al procedimiento. Serán necesarios trabajos prospectivos, randomizados y con mayor número de pacientes para confirmar los buenos resultados del SCA para la resolución de obstrucción colorrectal de origen neoplásico, y particularmente para evaluar su utilización como puente a la cirugía.
En conclusión, el empleo de stents auto-expansibles constituye una alternativa eficaz y segura para el tratamiento paliativo de la obstrucción colorrectal neoplásica y el éxito en su colocación sería mayor en los pacientes con obstrucción neoplásica intrínseca. En casos seleccionados, el stent podría ser utilizado como puente a una cirugía para obtener mejores resultados quirúrgicos.
Referencias
- Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin 2005; 55: 74-108.
- Ohman U. Prognosis in patients with obstructing colorectal carcinoma. Am J Surg 1982; 143: 742-747.
- Iversen LH, Bülow S, Christensen IJ, Laurberg S, Harling H. Postoperative medical complications are the main cause of early death after emergency surgery for colonic cancer. Br J Surg 2008; 95: 1012-1019.
- Wong RW, Rappaport WD, Witzke DB, Putnam CW, Hunter GC. Factors influencing the safety of colostomy closure in the elderly. J Surg Res 1994; 57: 289-292.
- Deans GT, Krukowski ZH, Irwin ST. Malignant obstruction of the left colon. Br J Surg 1994; 81: 1270-1277.
- Dohmoto M. New method-endoscopic implantation of rectal stent in palliative treatment of malignant stenosis. Endoscopy Digest 1991; 3: 1507-1512.
- Law WL, Choi HK, Chu KW. Comparison of stenting with emergency surgery as palliative treatment for obstructing primary left-sided colorectal cancer. Br J Surg 2003; 91: 1429-1433.
- Tan CJ, Dasari BV, Gardiner K. Systematic review and meta-analysis of randomized clinical trials of self-expanding metallic stents as a bridge to surgery versus emergency surgery for malignant left-sided large bowel obstruction. Br J Surg 2012; 99: 469-476.
- Kim JS, Hur H, Min BS, Sohn SK, Cho CH, Kim NK. Oncologic outcomes of self-expanding metallic stent insertion as a bridge to surgery in the management of left-sided colon cancer obstruction: comparison with non-obstructing elective surgery. World J Surg 2009; 33: 1281-1286.
- Ng KC, Law WL, Lee YM, Choi HK, Seto CL, Ho JW. Self-expanding metallic stent as a bridge to surgery versus emergency resection for obstructing left-sided colorectal cancer: a case-matched study. J Gastrointest Surg 2006; 10: 798-803.
- Abbas MA, Kharabadze GG, Ross EM, Abbass MA. Predictors of outcome for endoscopic colorectal stenting: a decade experience. International Journal of Colorectal Disease 2016; 32: 375-382.
- Tekkis PP, Kinsman R, Thompson MR, Stamatakis JD. The Association of Coloproctology of Great Britain and Ireland study of large bowel obstruction caused by colorectal cancer. Ann Surg 2004; 240: 76-81.
- Tilney HS, Lovegrove RE, Purkayastha S, Sains PS, Weston- Petrides GK, Darzi AW, Tekkis PP, Heriot AG. Comparison of colonic stenting and open surgery for malignant large bowel obstruction. Surg Endosc 2007; 21: 225-233.
- Watt AM, Faragher IG, Griffin TT, Rieger NA, Maddern GJ. Self-expanding metallic stents for relieving malignant colorectal obstruction: a systematic review. Ann Surg 2007; 246: 24-30.
- Khot UP, Lang AW, Murali K, Parker MC. Systematic review of the efficacy and safety of colorectal stents. Br J Surg 2002; 89: 1096-1102.
- Sebastian S, Johnston S, Geoghegan T, Torreggiani W, Buckley M. Pooled analysis of the efficacy and safety of self-expanding metal stenting in malignant colorectal obstruction. Am J Gastroenterol 2004; 99: 2051-2057.
- Van hooft JE, Fockens P, Marinelli AW, Timmer R, Berkel A, Bossuyt P, Bemelman W. Early closure of a multicenter randomized clinical trial of endoscopic stenting versus surgery for stage IV left-sided colorectal cancer. Endoscopy 2008; 40: 184-191.
- Jiménez Pérez J, Casellas J, García Cano J, Vandervoort J, Roncero García-Escribano O, Barcenilla J, Alvarez Delgado A, Goldberg P, Gonzalez-Huix F, Vázquez-Astray E, Meisner S. Colonic stenting as a bridge to surgery in malignant large-bowel obstruction: a report from two large multinational registries. Am J Gastroenterol 2011; 106: 2174-2180.
- Alcantara M, Serra X, Bombardó J, Falcó J, Perandreu J, Ayguavi¬ves I, Mora L, Hernando R, Navarro S. Colorectal stenting as an effective therapy for preoperative and palliative treatment of large bowel obstruction: 9 years’ experience. Tech Coloproctol 2007; 11: 316-322.
- Tan CJ, Dasari BV, Gardiner K. Systematic review and meta-analysis of randomized clinical trials of self-expanding metallic stents as a bridge to surgery versus emergency surgery for malignant left-sided large bowel obstruction. Br J Surg 2012; 99: 469-476.
- Young CD, Kim JY, Hong SP, Jung MK, Ye BD, Kim SG, Kim JH, Lee KM, Kim KH, Baik GH, Kim HG, Eun CS, Kim TI, Kim SW, Kim CD, Yang CH. Outcome and safety of self-expandable metallic stents for malignant colon obstruction: a Korean multicenter randomized prospective study. Surg Endosc 2012; 11: 3106-3113.
- Vemulapalli R, Lara LF, Sreenarasimhaiah J, Harford WV, Siddi¬qui AA. A comparison of palliative stenting or emergent surgery for obstructing incurable colon cancer. Dig Dis Sci 2010; 55: 1732-1737.
- Tilney HS, Lovegrove RE, Purkayastha S, Sains PS, Weston- Petrides GK, Darzi AW, Tekkis PP, Heriot AG. Comparison of colonic stenting and open surgery for malignant large bowel obs¬truction. Surg Endosc 2007; 21: 225-233.
- Van Hooft J, Van Halsema E, Vanbiervliet G, Beets-Tan R, DeWitt J, Donnellan F, Repici A. Self-expandable metal stents for obstructing colonic and extracolonic cancer: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline. En¬doscopy 2014; 46: 990-1053.
- Avlund TH, Erichsen R, Ravn S, Ciplys Z, Andersen JC, Laur¬berg S, Iversen LH. The prognostic impact of bowel perforation following self-expanding metal stent as a bridge to surgery in colo¬rectal cancer obstruction. Surgical Endoscopy 2017; 22: 328-336.
- Maruthachalam K, Lash GE, Shenton BK, Horgan AF. Tumour cell dissemination following endoscopic stent insertion. Br J Surg 2007; 94: 1151-1154.
- Malgras B, Brullé L, Dico RL, Marjou FE, Robine S, Therwath PA, Pocard PM. Insertion of a stent in obstructive colon cancer can induce a metastatic process in an experimental murine model. Annals of Surgical Oncology 2015; 22: 1475-1480.
- Knight AL, Trompetas V, Saunders MP, Anderson HJ. Does stenting of left-sided colorectal cancer as a “bridge to surgery” adversely affect oncological outcomes? A comparison with non-obstructing elective left-sided colonic resections. International Journal of Colorectal Disease 2012; 27: 1509-1514.
- Keswani RN, Azar RR, Edmundowicz SA, Zhang Q, Ammar TA, Banerjee B, Early DS, Jonnalagadda SS. Stenting for malignant colonic obstruction: a comparison of efficacy and complications in colonic versus extracolonic malignancy. Gastrointestinal endos¬copy 2009; 69: 675-680.
Correspondencia: José María Alvarez Gallesio
Pueyrredón 1640. Ciudad Autónoma de Buenos Aires, Argentina
Tel.: (+5411) 4827-7000 (interno 2808) /Fax: (+5411) 4827-7000 (interno 2807)
Correo electrónico: jalvarezgallesio@gmail.com
Acta Gastroenterol Latinoam 2018;48(2): 117-123
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE