Jesús Chang-Hermida1 ID· Fernando Miñán-Arana1 ID· Arantza Gabriela Carriel-Mendoza1 ID
Leonardo Aveiga-Cedeño2 ID· Miguel Puga-Tejada3 ID
1 Instituto Oncológico Nacional (ION) Dr. Juan Tanca Marengo, Sociedad de Lucha contra el Cáncer del Ecuador (SOLCA). Guayaquil, Ecuador.
2 Hospital El Cruce (HEC), Florencio Varela. Provincia de Buenos Aires, Argentina.
3 Instituto Ecuatoriano de Enfermedades Digestivas (IECED). Guayaquil, Ecuador.
Acta Gastroenterol Latinoam 2025;55(2):136-147
Recibido: 30/05/2025 / Aceptado: 30/06/2025 / Publicado online: 30/06/2025 / https://doi.org/10.52787/agl.v55i2.498
Resumen
Introducción. La información sobre morbimortalidad tras una gastrectomía subtotal o total es limitada en países en vías de desarrollo, especialmente ante el cambio epidemiológico del cáncer gástrico. Objetivo. Identificar factores asociados a morbimortalidad en pacientes con cáncer gástrico operados con intención curativa en un centro oncológico de Ecuador. Materiales y métodos. Estudio de cohorte histórica realizado en el Instituto Oncológico Nacional “Dr. Juan Tanca Marengo” (Guayaquil, 2019-2021). Se incluyeron adenocarcinomas gástricos operados con intención curativa. Se evaluaron eventos adversos y mortalidad (30, 90 días y global). Se estimaron factores asociados mediante regresión logística. Resultados. Se incluyeron 111 pacientes (87 gastrectomía subtotal, 24 total). Hubo ≥ 1 evento adverso en 15,4% (subtotal) y 17,9% (total). La mortalidad a 30, 90 días y global tras la gastrectomía subtotal fue, respectivamente, del 1,1%, 2,3% y 34,5%; tras la total fue de 0%, 4,2% y 54,2%, respectivamente. La presencia de eventos adversos se asoció con tumor Bormann III/IV (OR 9.6; IC95% 1,8 – 79,7; p = 0,0175) y una mayor estancia hospitalaria (OR 2,3; IC95% 1,4 – 5.1; p < 0,001). La mortalidad se asoció con Bormann III/IV (p = 0,0038) y dehiscencia gastro-duodenal (p = 0,0383). Conclusión. Las tasas de morbimortalidad a 90 días fueron menores a lo reportado en otras series. Bormann III/IV y dehiscencia gastroduodenal fueron factores asociados a mayor mortalidad.
Palabras claves. Cáncer de estómago, factores de riesgo, gastrectomía, morbilidad, mortalidad.
Morbidity and Mortality after Subtotal versus Total Open Gastrectomy for Gastric Cancer with Curative Intent: Findings in a Historical Cohort from a Cancer Center
Summary
Introduction. Data on morbidity and mortality after subtotal or total gastrectomy are scarce in developing countries, especially considering the epidemiological shift in gastric cancer (decrease in distal and increase in proximal tumors).
Objective. To identify factors associated with morbidity and mortality in patients with gastric cancer undergoing curative-intent surgery at a cancer center in Ecuador. Materials and methods. Historical cohort study conducted at the National Oncology Institute “Dr. Juan Tanca Marengo” in Guayaquil (2019 – 2021). Only adenocarcinomas treated with curative intent were included. Outcomes were postoperative complications and mortality at 30, 90 days, and overall. Logistic regression was used to estimate factors associated with higher risk. Results. A total of 111 patients were included (87 subtotal, 24 total gastrectomy). At least one complication occurred in 15.4% (subtotal) and 17.9% (total). Thirty-day, 90-day, and overall mortality after subtotal gastrectomy were 1.1%, 2.3%, and 34.5%; after total gastrectomy, 0%, 4.2%, and 54.2%, respectively. Postoperative complications were significantly associated with Bormann III/IV tumors (OR 9.6; 95% CI 1.8 – 79.7; p = 0.0175) and longer hospital stay (OR 2.3; 95% CI 1.4 – 5.1; p <0.001). Mortality was associated with Bormann III/IV tumors (p = 0.0038) and gastro-duodenal leak (p = 0.0383). Conclusion. Ninety-day morbidity and mortality rates were lower than previously reported. Bormann III/IV tumors and postoperative gastro-duodenal leakage were associated with increased mortality.
Keywords. Stomach cancer, risk factors, gastrectomy, morbidity, mortality.
Abreviaturas
ASA: American Society of Anesthesiology.
CIE: Clasificación internacional de enfermedades.
DE: Desviación estándar.
ERGE: Enfermedad por reflujo gastroesofágico.
HR: Hazard ratio.
ILF: Irinotecan, leucovorina y 5-fluorouracilo.
IMC: Indice de masa corporal.
IMRT: Intensity-modulated radiotherapy.
ION: Instituto Oncológico Nacional.
MALT: Mucosa associated lymphoid tissue.
OR: Odds ratio.
RIC: Rango intercuartil.
RT-3Dc: Radioterapia tridimensional conformacional.
SOLCA: Sociedad de Lucha contra el Cáncer del Ecuador.
STROBE: STrengthening the Reporting of OBservational studies in Epidemiology.
UEES: Universidad Espíritu Santo.
XELOX: Capecitabina y oxaliplatino.
Introducción
El cáncer de estómago ocupa el quinto lugar en incidencia y el cuarto en mortalidad entre todos los tumores a nivel mundial.1 Representa el 5,6% del total de casos de cáncer diagnosticados por año, y el 7,7% de las muertes anuales. De acuerdo con la ubicación geográfica, la incidencia de cáncer de estómago es más alta en Asia Oriental, Europa Oriental y América del Sur, y es más baja en África y Norteamérica. En lo que respecta a Latinoamérica, las mayores tasas de incidencia por cáncer de estómago en hombres y mujeres se presentan en Guatemala, Honduras, Ecuador y Chile. Los países con las menores tasas son los Estados Unidos, Puerto Rico y Canadá. La supervivencia de cinco años del cáncer de estómago entre los hispanos es de aproximadamente 28%.1
El cáncer de estómago distal (antro/píloro) está asociado a la infección por H. pylori y constituye el tipo más frecuente de cáncer de estómago a nivel mundial.2 El cáncer de estómago proximal (cardias, fondo o cuerpo) está más asociado a la enfermedad por reflujo gastroesofágico (ERGE). Por dicha situación epidemiológica, al momento, la incidencia de cáncer de estómago está disminuyendo en países industrializados, al unísono de un paulatino incremento en los casos de cáncer proximal. No obstante, poco a poco se observa una situación semejante en países en vías de industrialización.3
Exceptuando el linfoma gástrico de tejido linfoide asociado a mucosa (mucosa associated lymphoid tissue, MALT)4 y los tumores mucinosos menores de 2 cm, en la gran mayoría de los casos, la gastrectomía constituye el único tratamiento curativo frente al cáncer de estómago. Dicha resección oncológica comprende tanto la gastrectomía subtotal (parcial) como la total. Tales procedimientos están indicados frente a una lesión distal, o que incluya una localización proximal, respectivamente.5
Una gastrectomía no es un procedimiento exento de morbilidad. La hemorragia digestiva, la formación de fístulas y la estenosis figuran entre las morbilidades posquirúrgicas reportadas con mayor frecuencia. La tasa de mortalidad a treinta días poscirugía es de aproximadamente el 1%. La morbimortalidad es mayor tras una gastrectomía total en comparación con la gastrectomía subtotal, independientemente de si se trata de una cirugía abierta o laparoscópica.6 Entre los factores asociados a mayor morbilidad figuran la edad avanzada, riesgo prequirúrgico III-IV, gastrectomía total y gastrectomía asociada a pancreatoesplenectomía. La edad avanzada, un menor índice de masa corporal y la hipoalbuminemia se asocian a mayor mortalidad.7
A nivel mundial, son cada vez más los casos de cáncer de estómago proximal requirentes de gastrectomía total. Además de ello, los reportes respecto de la tasa de mortalidad tras una gastrectomía subtotal y total tradicionalmente han sido descriptos a treinta días poscirugía o como sobrevida a largo plazo. Ambas definiciones pueden subestimar la verdadera mortalidad asociada con una resección oncológica, por lo que es preferible considerar la tasa de mortalidad a noventa días poscirugía como el desenlace oncológico a medir.8
Se han identificado diferentes factores asociados a la morbimortalidad posgastrectomía, tales como la edad avanzada, la presencia de comorbilidades, los niveles de hemoglobina y albúmina, y la realización de resecciones multiviscerales. Sin embargo, estos factores varían según los estudios, lo que puede atribuirse a diferencias metodológicas, como la falta de estratificación entre los tipos de gastrectomía (total vs. subtotal).7 Sin embargo, la razón de tales diferencias puede ir desde circunstancias epidemiológicas hasta la experiencia quirúrgica de cada centro.9
Se plantearon dos preguntas de investigación: ¿cuál es la morbilidad, mortalidad a treinta, noventa días y mortalidad global tras gastrectomía subtotal y total en un nosocomio de la localidad? Y: ¿cuáles son los factores asociados a dicha morbimortalidad?
Objetivos
El objetivo principal de este estudio fue identificar los factores potencialmente asociados a la morbilidad y mortalidad en pacientes con cáncer gástrico sometidos a cirugía con intención curativa.
Objetivos secundarios:
a) Determinar las tasas de morbilidad, mortalidad a treinta y noventa días y mortalidad global luego de la gastrectomía subtotal versus total con intención curativa por cáncer gástrico.
b) Identificar los factores asociados a morbimortalidad tras la gastrectomía subtotal y total realizada con intención curativa.
Materiales y métodos
Diseño del estudio
El presente es un estudio observacional, analítico, longitudinal, retrospectivo, del tipo cohorte histórica.10 Se llevó a cabo en pacientes con cáncer de estómago a quienes se les realizó gastrectomía subtotal o total con intención curativa en el Instituto Oncológico Nacional (ION) “Dr. Juan Tanca Marengo”, de la Sociedad de Lucha contra el Cáncer del Ecuador (SOLCA), un centro referente en la atención oncológica, ubicado en Guayaquil, Ecuador.
El período de reclutamiento de casos estuvo comprendido entre enero de 2019 y septiembre de 2021, con un seguimiento de los casos no menor a tres meses (extendiéndose el período de estudio hasta diciembre de 2021). Este trabajo comprendió dos cohortes de estudio: gastrectomía subtotal y total. Su diseño de adhirió a las recomendaciones respecto del “Fortalecimiento de la comunicación de estudios observacionales en Epidemiología” (STrengthening the Reporting of OBservational studies in Epidemiology, STROBE).11
Población y muestra
Se incluyeron los datos de pacientes adultos con diagnóstico histopatológico de adenocarcinoma gástrico a quienes se les realizó gastrectomía, independientemente de si recibieron o no atención oncológica integral en el mismo nosocomio anfitrión. Dado que el ION-SOLCA es principalmente un centro oncológico de referencia, se anticipa un reducido número de cirugías de urgencia. De forma semejante, en esa institución toda gastrectomía es abierta, motivo por el cual la selección de casos se limitó a dicho abordaje.
Se excluyeron los datos de los pacientes con: a) atenciones distintas a una cirugía digestiva propiamente (por ej.: gastrostomías); b) intervenciones sin intención curativa (gastrectomías paliativas o cirugías exploratorias “open-close”); c) reintervenciones; d) casos con linfoma gástrico (MALT o difuso de células grandes tipo B), tumores mucinosos o subepiteliales que hayan requerido gastrectomía, y e) pacientes con seguimiento clínico incompleto o datos clínicos insuficientes.
Procedimiento y técnica
Búsqueda estratégica de los casos. Se solicitó al Registro Hospitalario (Departamento de Bioestadística) del ION-SOLCA el listado de casos tipificados dentro de la categoría “neoplasia maligna de estómago», correspondiente a los códigos de la décima versión de la clasificación internacional de enfermedades (CIE-10) 16 y 16,0 – 16,9, y que hayan sido atendidos por Cirugía Digestiva (Departamento de Cirugía Oncológica). A partir de dicho listado, se realizó la selección de casos sobre la base de los criterios previamente establecidos.
Definición de las variables del estudio. Se recuperó información concerniente a: a) demografía: edad, género, cobertura sanitaria, presentación clínica inicial (hemorragia digestiva, oclusión o síndrome de dumping); b) diagnóstico oncológico: clasificación de Bormann, estadio clínico, sitio del tumor (distal en caso de corresponder a antro/píloro; proximal en caso de corresponder a cardias, fondo o cuerpo), y c) tratamiento oncoespecífico: gastrectomía (subtotal o total), histopatología (adenocarcinoma intestinal o difuso), quimioterapia (neoadyuvante y/o solamente adyuvante, esquema de quimioterapia) y radioterapia adyuvante (radioterapia tridimensional conformacional, RT-3Dc; o de intensidad modulada, IMRT-).
Definición de los desenlaces oncológicos. La morbilidad fue definida como la presencia de al menos algún evento adverso relacionado con la gastrectomía efectuada, durante los quince días posteriores a su realización. Se trató de una variable discreta polinomial mutuamente no excluyente. Se anticipó cuando menos los siguientes eventos adversos: absceso, dehiscencia de sutura esofagogástrica o gastro-duodenal, estenosis posquirúrgica, fístula, hemorragia digestiva, peritonitis y síndrome de Dumping. Adicionalmente, a la definición de morbilidad se agregó la estancia hospitalaria poscirugía. Se calcularon las tasas de mortalidad a los treinta días, a los noventa días y de forma global. La tasa de mortalidad global se definió como la proporción de pacientes que fallecieron durante el período del estudio, comprendido desde la fecha de la primera gastrectomía con intención curativa (enero de 2019) hasta los noventa días posteriores a la cirugía del último paciente incluido (diciembre de 2020). La sobrevida global se definió como el período comprendido entre la fecha de la gastrectomía y la última consulta, teleconsulta o fallecimiento del paciente.
Recuperación de la información. Toda la información concerniente a las variables y desenlaces oncológicos previamente descriptos fue ingresada en una hoja electrónica encriptada y en línea compatible con Microsoft Access. En caso de que algún paciente no haya continuado el seguimiento posquirúrgico en el ION-SOLCA, ya sea por decisión propia o por haber sido referido únicamente para la gastrectomía (recibiendo atención oncológica integral en otra institución), se realizó una teleconsulta para recuperar la información correspondiente. Finalmente, se consultó al Registro Hospitalario del ION-SOLCA y a la Dirección General de Registro Civil, Identificación y Cedulación del Estado ecuatoriano respecto de las fechas precisas de fallecimiento en los casos requeridos.
Análisis estadístico
Consideraciones técnicas. Un P-valor < .05 fue considerado como estadísticamente significativo. El análisis estadístico fue realizado en R v.4.0 (R Foundation for Statistical Computing; Viena, Austria).
Cálculo de la muestra. Considerando la tasa de mortalidad a treinta días posgastrectomía total reportada por Shannon y col., se estimó una muestra no menor a 91 casos, con un margen de error del 5% y un intervalo de confianza del 95%.
Estadística descriptiva. Las variables cualitativas fueron descriptas en media (desviación estándar, DE), o mediana (rango intercuartil, RIC), según correspondiese su distribución estadística (prueba de Kolmogórov-Smirnov). Las variables cualitativas fueron descritas en frecuencias (%). Se realizó un subanálisis según cada cohorte de estudio, y en función de la presencia de cuando menos un evento adverso (morbilidad) o fallecimiento durante el período de estudio (mortalidad).
Estadística analítica. Las variables del estudio y los desenlaces oncológicos entre cada cohorte de estudio y morbimortalidad fueron comparadas mediante las correspondientes pruebas de contraste de hipótesis: T de Student o U de Mann-Whitney en el caso de las variables cuantitativas con o sin distribución gaussiana, respectivamente; chi-cuadrado de Pearson o exacto de Fisher según corresponda a las frecuencias esperadas. La sobrevida global entre ambas cohortes de estudio fue ilustrada mediante una curva de Kaplan-Meier. Siempre que el número de eventos por subcohorte lo permitiera, la estimación de factores asociados a morbilidad (cuando menos un evento adverso) y mortalidad (fallecimiento durante el período de estudio) fue verificada mediante regresión logística (Odds Ratio, OR), regresión de Cox (Hazard Ratio, HR), o simplemente a través de la prueba de contraste de hipótesis respectiva.
Aspectos éticos
Este estudio contó con la aprobación del Comité de Ética de la comisión de titulación de la Facultad Posgrado de la Universidad Espíritu Santo (UEES), además del departamento de Docencia e Investigación del ION-SOLCA. Previo a la cirugía, todos los pacientes firmaron el respectivo consentimiento informado con fines asistenciales. En todo momento se precauteló la custodia de datos en apego al artículo 4 de la Ley Ecuatoriana de Derechos y Amparo del Paciente. La presente investigación respetó lo estipulado por el Código de Núremberg de 1947 y la Declaración de Helsinki de 1964 y sus posteriores enmiendas (última versión 2013).12
Resultados
Demografía y diagnóstico oncológico
Durante el período de reclutamiento, un total de 111 pacientes fueron incluidos. Todas las cirugías fueron abiertas. De estos, 20/111 (18%) requirieron intervención de urgencia. En 87 pacientes (78%) se realizó una gastrectomía subtotal y en 24 pacientes (22%) una gastrectomía total (Figura 1). La mediana de edad de la muestra fue de 68 (59 – 74,5) años, y 56/111 (50,5%) fueron de género femenino. En comparación con el grupo de gastrectomía subtotal, los pacientes en quienes se practicó gastrectomía total fueron significativamente más jóvenes (mediana de edad de 70 vs. 62 años, p = .004), con una presentación clínica inicial más severa (oclusión 21,8% vs. 79,2%, p < .001; dumping 29,9% vs. 87,5%, p < 0,001), e histopatología más agresiva (adenocarcinoma difuso 11,5% vs. 37,5%; p < 0,0054). (Tabla 1)
Figura 1. Flujograma STROBE de selección de casos
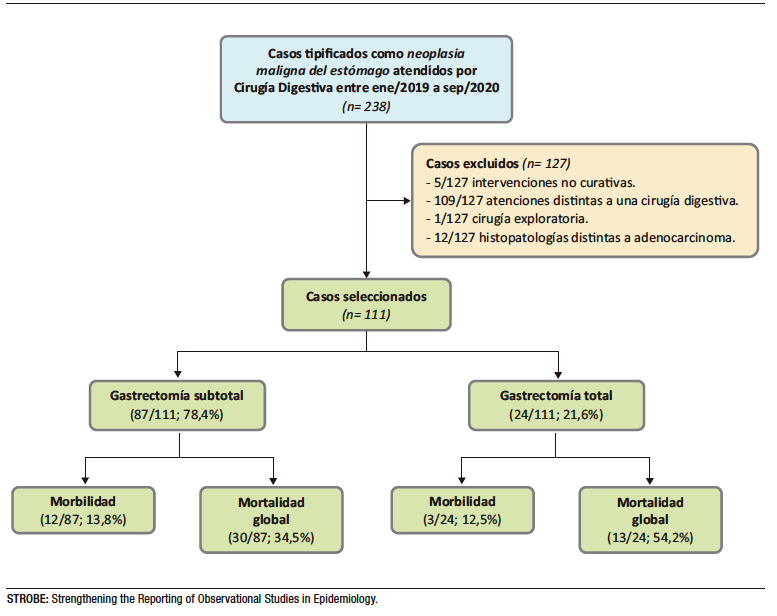
Tabla 1. Características de la población de estudio
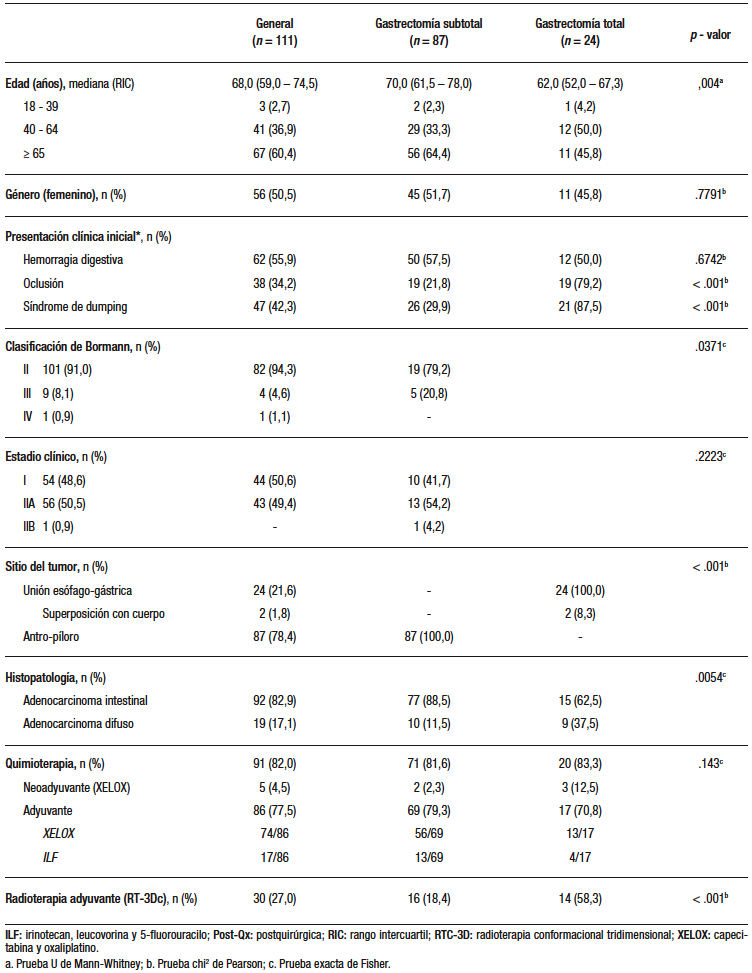
Tratamiento oncoespecífico
En 91/111 (82%) casos se indicó algún esquema de quimioterapia adyuvante, correspondiente al 81,6% de los casos posgastrectomía subtotal y 83,3% posgastrectomía total (p = .143). En 5/91 casos (4,5%) se administró también quimioterapia neoadyuvante; tres de ellos fueron posteriormente tratados con gastrectomía total. Todos los esquemas neoadyuvantes fueron del tipo XELOX (capecitabina y oxaliplatino) mientras que los esquemas adyuvantes fueron en su mayoría XELOX (74/86), pero también ILF (irinotecan, leucovorina y 5-fluorouracilo) en 17/86 casos. En 30/111 (27%) casos se indicó radioterapia adyuvante. Todas las irradiaciones fueron con técnica de RT-3Dc. Cabe recalcar que estos casos representaron el 18,4% de los casos posgastrectomía subtotal y el 58,3% posgastrectomía total
(p < .001). (Tabla 1)
Morbilidad
La estancia hospitalaria poscirugía fue más prolongada entre quienes fueron intervenidos mediante gastrectomía total (mediana 6 vs. 8 días; p < 0,452). En 15/111 (13,5%) casos se observó cuando menos un evento adverso asociado a la cirugía: 12/87 (15,4%; IC 95% 7,9 – 22,8) tras gastrectomía subtotal y 3/24 (17,9%; IC 95% 3,7 – 32,0) tras gastrectomía total. La hemorragia digestiva alta y el síndrome de Dumping fueron los eventos adversos más frecuentemente reportados, tanto en general (8/15 y 6/15, respectivamente) como entre los intervenidos mediante gastrectomía subtotal (5/12 en cada caso). Entre los intervenidos mediante gastrectomía total, el evento adverso más frecuente fue la hemorragia digestiva (3/3). La tasa de casos con eventos adversos en la cohorte de gastrectomía subtotal fue de 12/87 (13,8%) y de 3/24 (12,5%) en la de gastrectomía total, sin diferencias significativas (p = 1,000). El total de eventos adversos observados fue de 23 en la cohorte subtotal y de 7 en la total. No se observó una diferencia estadísticamente significativa en la ocurrencia de al menos un evento adverso según el tipo de gastrectomía.
Mortalidad
La mediana de seguimiento poscirugía de los casos estudiados fue de nueve meses. Ningún caso tuvo un seguimiento menor a tres meses. En general, la tasa de mortalidad a treinta, noventa días poscirugía, mortalidad global y sobrevida global fue de 1/111 (0,9%), 3/111 (2,7%), 43/111 (38,7%) y 9 (RIC 5,5 – 25,0) meses, respectivamente. En específico, la tasa de mortalidad a treinta, noventa días poscirugía, mortalidad global y sobrevida global entre los intervenidos mediante gastrectomía subtotal fue de 1/87 (1,1%; IC 95% 0,1 – 6,9), 2/87 (2,3%; IC 95% 0,1 – 8,6), 30/87 (34,5%; IC 95% 25,3 – 44,9) y 8 (5 – 25,5) meses; mientras que, mediante gastrectomía total, 0/24 (p = 1), 1/24 (4,2%; IC 95% 0,1 – 22,1; p = 0,5221), 13/24 (54,2%; IC 95% 35,1 – 72,0; p = 0,1296) y 9,5 (6 – 23,5, P = .2) meses, respectivamente. No existió diferencia estadísticamente significativa entre la mortalidad o sobrevida global, independientemente de su definición (HR 1,542; IC 95% 0,803 – 2,956; p = 2) (Figura 2). En la Figura 3 se detallan los eventos adversos entre los pacientes vivos vs. los fallecidos.
Figura 2. Curva de sobrevida ilustrando
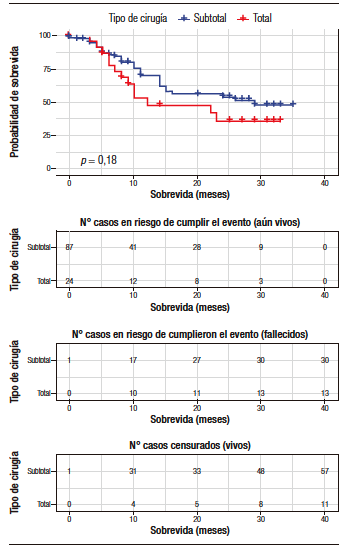
Figura 3. Número de casos vivos y fallecidos entre quienes presentaron algún evento adverso asociado a la cirugía (n= 15/111; 13,5%)
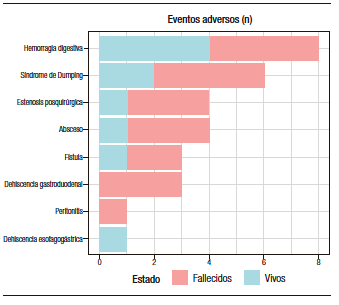
Factores asociados a morbimortalidad
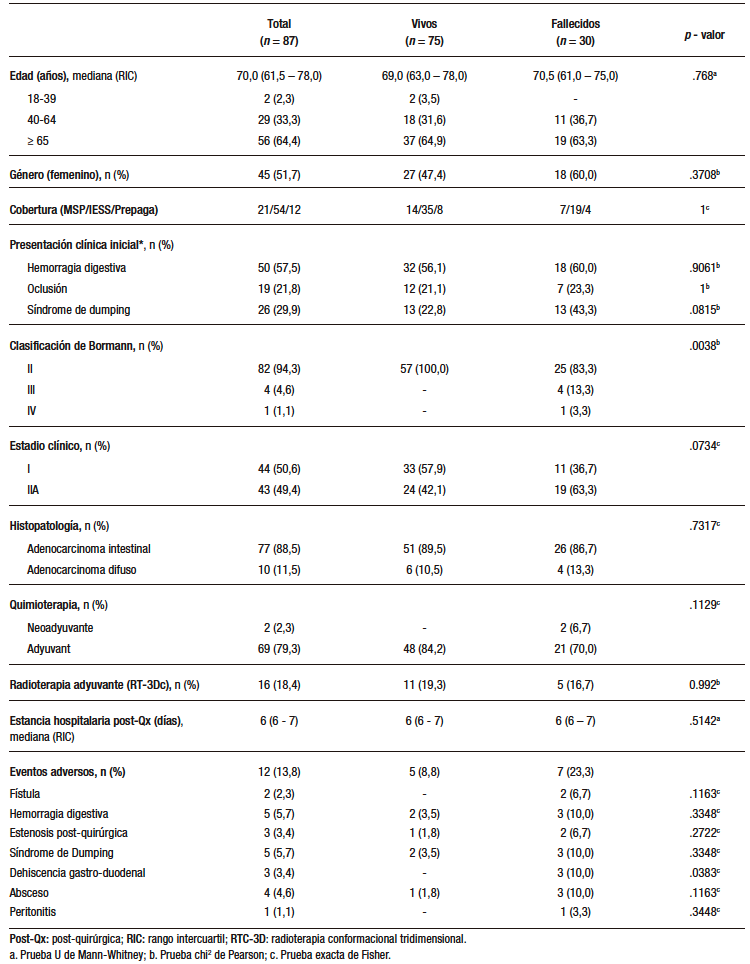
La presencia de cuando menos un evento adverso tras la gastrectomía subtotal se asoció significativamente con el antecedente de un Bormann III o IV (OR 9,639; IC 95% 1,845 – 79,688; p = 0,0175), y una mediana de estancia hospitalaria posoperatoria de 9 vs. 6 días (OR 2,332; IC 95% 1,442 – 5,076; p < .001). El fallecimiento (en cualquier momento posterior a la gastrectomía subtotal o total) también se asoció significativamente con una mayor frecuencia de casos Bormann III o IV (16,6% vs. 0%; p = .0038) y mayor frecuencia de casos con dehiscencia gastro-duodenal (10% vs. 0%; p = .0383). Asimismo, entre los casos fallecidos existió una frecuencia moderadamente superior entre el número de casos con síndrome de Dumping al debut (43,3% vs. 22,8%; p = .0815) o un estadio clínico IIA (63,3% vs. 42,1%; p = .0734). La Tabla 2 describe un subanálisis de factores asociados a morbilidad (eventos adversos) en pacientes con gastrectomía subtotal, y la Tabla 3, factores asociados a mortalidad en el mismo grupo de pacientes.
Tabla 2. Factores asociados a morbilidad (eventos adversos) posterior a gastrectomía subtotal
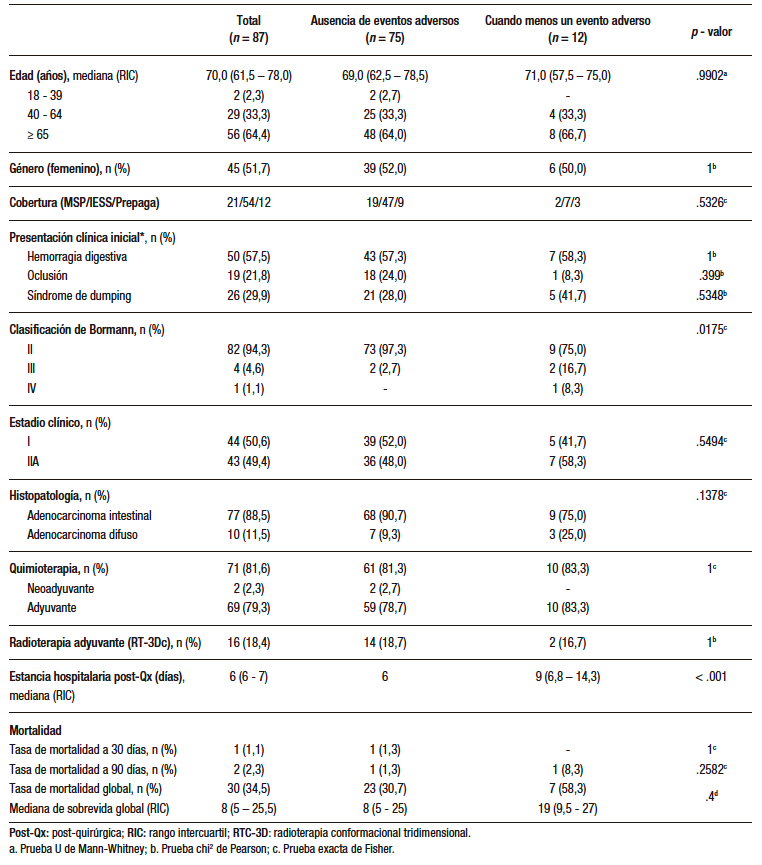
Tabla 3. Factores asociados a la mortalidad global en pacientes en quienes se realizó gastrectomía subtotal
Discusión
Los resultados de este estudio permiten aportar información local valiosa sobre los desenlaces clínicos tras una gastrectomía abierta con intención curativa en pacientes con cáncer gástrico. La tasa de morbilidad observada fue del 15,4% para la gastrectomía subtotal y del 17,9% para la gastrectomía total, con la hemorragia digestiva alta y el síndrome de Dumping como los eventos adversos más frecuentes en ambos grupos. Se identificaron como factores asociados a mayor morbilidad la presencia de tumores avanzados (Bormann tipo III o IV) y una estancia hospitalaria posoperatoria prolongada. En cuanto a la mortalidad, se reportaron tasas bajas a treinta y noventa días posoperatorios, tanto para la gastrectomía subtotal (1,1% y 2,3%, respectivamente) como para la total (0% y 4,2%, respectivamente). Sin embargo, la mortalidad global fue considerablemente elevada en ambos procedimientos, en especial tras la gastrectomía total (54,2% frente a 34,5%), lo cual podría estar relacionado con características tumorales y del huésped no evaluadas en profundidad en este análisis. Aunque el tamaño de la muestra limita la posibilidad de hacer las mismas inferencias que en estudios internacionales, se observa una mayor tasa de mortalidad entre los pacientes sometidos a gastrectomía total, lo cual coincide con lo reportado en la literatura.13 Un Bormann III o IV y la presencia de dehiscencia gastro-duodenal posoperatoria fueron factores asociados a una mayor mortalidad.
Al comparar nuestros resultados con los reportados en una cohorte de 1109 pacientes holandeses, se observan diferencias relevantes en cuanto a las tasas de morbilidad y mortalidad posoperatorias. En dicho estudio, los pacientes de 70 años o más presentaron una mayor frecuencia de complicaciones perioperatorias o posoperatorias (41,2%) en comparación con los menores de 70 años (32,5%), así como una tasa de mortalidad a treinta días más elevada (7,9% vs. 3,2%).23 En nuestra cohorte, si bien las tasas de morbilidad fueron más bajas (15,4% y 17,9% para gastrectomía subtotal y total, respectivamente), y la mortalidad a treinta días también fue inferior (1,1% y 0%, respectivamente), la mortalidad global fue considerablemente elevada, en particular tras una gastrectomía total (54,2%). Estas discrepancias podrían deberse a diferencias en la selección de pacientes, el acceso a tratamientos perioperatorios, como la quimioterapia neoadyuvante, o a las características propias del sistema de salud. Es importante destacar que, al igual que en el estudio holandés, nuestro análisis identificó factores clínicos y quirúrgicos específicos asociados a una mayor morbimortalidad, lo que refuerza la necesidad de estrategias individualizadas de manejo en contextos de recursos limitados.14
De forma similar, un estudio realizado en México en 691 pacientes sometidos a gastrectomía radical D2 identificó que la edad ≥ 70 años, un estado funcional según la clasificación de la sociedad americana de anestesiología (American Society of Anesthesiology, ASA) III-IV, la realización de gastrectomía total y la pancreatosplenectomía se asociaron con una mayor tasa de complicaciones posoperatorias. Además, la edad avanzada, un menor índice de masa corporal (IMC) y la hipoalbuminemia se identificaron como predictores de mortalidad tanto en la gastrectomía distal como total. Nuestros hallazgos coinciden parcialmente, ya que también observamos una mayor morbimortalidad en pacientes con enfermedad más avanzada (Bormann III-IV) y hospitalización prolongada, factores que pueden reflejar indirectamente un mayor deterioro funcional o nutricional. Si bien en nuestra cohorte no se evaluaron variables como el IMC o los niveles de albúmina, la elevada mortalidad global observada tras gastrectomía total (54,2%) resalta la importancia de considerar el estado nutricional y funcional preoperatorio como elementos clave para la estratificación del riesgo en poblaciones vulnerables.7
Aunque no fue un factor analizado en este trabajo, la experiencia clínica, representada a través del volumen de casos intervenidos, también es un factor asociado a morbimortalidad. En un estudio japonés que reunió a 71307 pacientes operados en 2051 instituciones, los cirujanos y hospitales de bajo volumen tenían pacientes significativamente mayores y con peor perfil de riesgo con diversas comorbilidades. La tasa de mortalidad operatoria disminuyó con el volumen del cirujano, 2,5% entre quienes operaban hasta dos gastrectomías totales por año y 0,6% entre quienes operaban más de 26 por año. La mortalidad operatoria fue del 3,1% entre los hospitales de bajo volumen de casos, 1,7% entre los intermedios y 1,2% entre los de alto volumen de casos. Después del ajuste de riesgo por cirujano, volumen hospitalario y características del paciente, el volumen hospitalario se asoció significativamente con la mortalidad operatoria (OR = 0,53; IC del 95%: 0,43 a 0,63).15
Al momento es muy escasa la literatura ecuatoriana respecto de los factores asociados con morbimortalidad tras una gastrectomía curativa por causas oncológicas, restringiéndose a trabajos de fines de grado. No obstante, se reportan resultados concordantes con la literatura internacional en cuanto a la morbimortalidad posquirúrgica en pacientes sometidos a cirugía con intención curativa.13 En la misma institución anfitriona de esta investigación, se han realizado varios estudios semejantes. En el 2013, un estudio de 260 casos (gastrectomía total 20,1%) reportó una mortalidad global del 16%, con una mediana de seguimiento de veinticuatro meses.16 Tras un período semejante, otro estudio realizado en el 2014 reportó una mortalidad global del 22% en una muestra de 85 casos (gastrectomía total 28%), reportándose como principales comorbilidades el hemoperitoneo y la estenosis posoperatoria, en dos casos distintos.17 Un reciente estudio concentrado en 17 pacientes con adenocarcinoma de la unión gastroesofágica, a quienes se les realizó gastrectomía total, estimó una morbilidad del 41,1% y una mortalidad global de 35,2%.18
Un estudio realizado en un hospital oncológico de Quito en el 2016 estimó en 128 individuos (gastrectomía total 14%) una mortalidad a cinco años del 42,1%.19 Un año más tarde, un estudio de esa misma institución en 129 pacientes (gastrectomía total 14%) reportó una mortalidad a treinta días y doce meses del 14% y 25%, respectivamente.20 Entre los eventos adversos asociados a la cirugía, se enlistan: infecciones 48%, hemorragia digestiva 19%, íleo 10%, y fístulas 4%. Un estudio que reunió a 277 pacientes (gastrectomía total 10,2%) atendidos en dos hospitales de Quito evaluó los resultados oncológicos tras linfadenectomía D1 (realizada en el 33,8%) vs. D2 (realizada en el 66,2%), estimando una mediana de sobrevida y tasa de sobrevida global de 26 vs. 20 meses y 63,8% vs. 57,6%.21 Llama la atención que los trabajos realizados en Quito muestran una frecuencia de gastrectomía total de aproximadamente el 10%, en comparación con las realizadas en Guayaquil, cuya frecuencia rodea el 20%.
Una de las principales fortalezas de este estudio es que aporta evidencia original sobre morbimortalidad posoperatoria tras gastrectomía subtotal y total en un centro oncológico de un país en vías de desarrollo, en un contexto en el que la información es escasa y las características epidemiológicas del cáncer gástrico están cambiando. Además, se identificaron factores clínicos y quirúrgicos específicos asociados a los desenlaces, lo que permite orientar estrategias de evaluación preoperatoria y seguimiento en poblaciones con recursos limitados.
Entre las principales limitaciones de este estudio se encuentran su diseño retrospectivo, que puede conllevar sesgos de selección e información, así como el tamaño reducido de la cohorte, especialmente en el grupo de gastrectomía total, lo que limita la potencia estadística para detectar asociaciones menos frecuentes. Asimismo, no se incluyeron variables preoperatorias relevantes como el estado nutricional (IMC, albúmina), comorbilidades específicas o el uso de quimioterapia neoadyuvante, que podrían haber influido en los desenlaces clínicos.
Conclusión
Este estudio aporta información valiosa sobre los desenlaces posoperatorios de la gastrectomía subtotal y total con intención curativa en pacientes con cáncer gástrico en un centro oncológico de Ecuador. Las tasas de morbimortalidad observadas fueron comparables o inferiores a las reportadas en otras series internacionales, a pesar de las limitaciones propias del contexto. La presencia de tumores Bormann tipo III/IV y la dehiscencia de la anastomosis gastroduodenal se asociaron significativamente con mayor riesgo de mortalidad, lo que subraya la importancia de una adecuada estratificación preoperatoria y del seguimiento estrecho en pacientes de alto riesgo. Futuros estudios prospectivos, con muestras más amplias y variables clínicas preoperatorias integradas, permitirán optimizar los resultados en este tipo de población.
Consentimiento para la publicación. Se obtuvo el consentimiento informado por escrito del paciente o su padre, tutor o familiar, para la publicación de los datos y/o imágenes clínicas en beneficio de la ciencia. La copia del formulario de consentimiento se encuentra disponible para los editores de esta revista.
Propiedad intelectual. Los autores declaran que los datos, las figuras y las tablas presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externa.
Conflicto de intereses. Los autores declaran no tener conflictos de intereses en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Chang-Hermida J, Miñán-Arana F, Carriel-Mendoza A G y col. Morbimortalidad posgastrectomía abierta subtotal versus total por cáncer de estómago, con intención curativa: hallazgos en una cohorte histórica de un centro oncológico. Acta Gastroenterol Latinoam. 2025;55(2):136-147. https://doi.org/10.52787/agl.v55i2.498
Referencias
- Ilic M, Ilic I. Epidemiology of stomach cancer. World J Gastroenterol. 2022;28:1187-203. https://doi.org/10.3748/WJG.V28.I12.1187
- Correa P. Human Gastric Carcinogenesis: A Multistep and Multifactorial Process- First American Cancer Society Award Lecture on Cancer Epidemiology and Prevention. Cancer Res. 1992;52:6735-40.
- Song H, Ekheden IG, Zheng Z, Ericsson J, Nyrén O, Ye W. Incidence of gastric cancer among patients with gastric precancerous lesions: observational cohort study in a low risk Western population n.d. https://doi.org/10.1136/bmj.h3867
- Mulalic E, Delibegovic S. An Aggressive Form of MALT Lymphoma of the Stomach with Pancreas Infiltration. Med Arch. 2016;70:235-7. https://doi.org/10.5455/medarh.2016.70.235-237
- Van Cutsem E, Sagaert X, Topal B, Haustermans K, Prenen H. Gastric cancer. The Lancet. 2016;388:2654-64. https://doi.org/10.1016/S0140-6736(16)30354-3
- Liu F, Huang C, Xu Z, Su X, Zhao G, Ye J, et al. Morbidity and Mortality of Laparoscopic vs Open Total Gastrectomy for Clinical Stage i Gastric Cancer: The CLASS02 Multicenter Randomized Clinical Trial. JAMA Oncol. 2020;6:1590–7. https://doi.org/10.1001/jamaoncol.2020.3152
- Paredes-Torres OR, García-Ruiz L, Luna-Abanto J, Meza-García K, Chávez-Passiuri I, Berrospi-Espinoza F, et al. Risk factors associated with postoperative morbidity and mortality in D2 radical gastrectomy for gastric cancer. Rev Gastroenterol Mex. 2021. https://doi.org/10.1016/j.rgmx.2020.11.004
- Shannon AB, Straker RJ, Fraker DL, Roses RE, Miura JT, Karakousis GC. Ninety-day mortality after total gastrectomy for gastric cancer. Surgery (United States). 2021;170:603-9. https://doi.org/10.1016/j.surg.2021.02.010
- Iwatsuki M, Yamamoto H, Miyata H, Kakeji Y, Yoshida K, Konno H, et al. Effect of hospital and surgeon volume on postoperative outcomes after distal gastrectomy for gastric cancer based on data from 145,523 Japanese patients collected from a nationwide web-based data entry system. Gastric Cancer. 2019;22:190-201. https://doi.org/10.1007/s10120-018-0883-1
- Hernández-Sampieri R. Metodología de la investigación. México D.F.: ECOE Ediciones. 2010.
- Von Elma E, Altmanb DG, Eggera M, Pocockd SJ, Gotzschee PC, Vandenbrouckef JP. Declaración de la Iniciativa STROBE (Strengthening the para la comunicación de estudios observacionales. Gac Sanit. 2008;22:144-50.
- Young M, Wagner A. Medical Ethics. StatPearls. 2021.
- Sędłak K, Bobrzyński Ł, Mlak R, Kołodziejczyk P, Pelc Z, Kobiałka S, et al. Proximal gastrectomy as an alternative to total gastrectomy in patients with advanced proximal gastric cancer: propensity score matching analysis of the 2-center study in European population. Journal of Gastrointestinal Surgery. 2025;29. https://doi.org/10.1016/J.GASSUR.2025.102091
- Nelen SD, Bosscha K, Lemmens VEPP, Hartgrink HH, Verhoeven RHA, de Wilt JHW. Morbidity and mortality according to age following gastrectomy for gastric cancer. British Journal of Surgery. 2018;105:1163-70. https://doi.org/10.1002/bjs.10836
- Iwatsuki M, Yamamoto H, Miyata H, Kakeji Y, Yoshida K, Konno H, et al. Association of surgeon and hospital volume with postoperative mortality after total gastrectomy for gastric cancer: data from 71,307 Japanese patients collected from a nationwide web-based data entry system. Gastric Cancer. 2021;24:526-34. https://doi.org/10.1007/s10120-020-01127-8
- Cabrera-García R. Correlación bidimensional lineal entre la sobrevida de pacientes con adenocarcinoma gástrico, intestinal y difuso, en ION SOLCA Juan Tanca Marengo 2005 – 2009. 2013.
- Véliz-Burgos E. Estudio de pacientes con cáncer gástrico y la sobrevida postquirúrgica en Hospital Oncológico SOLCA Dr. Juan Tanca Marengo 2009-2013 y una propuesta de manejo adyuvante. 2014.
- Ulloa-Ochoa P, Palomeque-Bueno J. Evaluación del tratamiento quirúrgico del adenocarcinoma en la unión gastroesofágica en SOLCA desde 1 enero 2011 – 30 abril 2018. 2018.
- Escaleras-Ordóñez Karen. Antecedente de tamaño tumoral al diagnóstico como predictor de sobrevida a los cinco años en pacientes con cáncer gástrico avanzado sometidos a gastrectomía en el Hospital Oncológico Solón Espinosa Ayala (SOLCA) Núcleo Quito. 2016.
- Baldeón-Alcívar A, Reyes-Cáceres J. Manejo quirúrgico del cáncer gástrico, en pacientes del Hospital ION SOLCA – Guayaquil 2014-2015. 2017.
- Parrales-Matute Diana; Calderón-Ruíz Paola. Sobrevida comparativa entre D1 vs D2, en adenocarcinoma gástrico entre los hospitales: Carlos Andrade Marín y Solca Quito; durante los años 2005-2010. 2017.
- Fujiya K, Kawamura T, Omae K, Makuuchi R, Irino T, Tokunaga M, et al. Impact of Malnutrition After Gastrectomy for Gastric Cancer on Long-Term Survival. Ann Surg Oncol. 2018;25:974-83. https://doi.org/10.1245/s10434-018-6342-8
Correspondencia: Miguel Puga -Tejada
Correo electrónico: mpuga@ieced.ec
Acta Gastroenterol Latinoam 2025;55(2):136-147
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE


