Nicolás Roccatagliata,1 Nebil Larrañaga,1 Germán Espil,1 Roberto Salgado (H),3 Jairo Hernández Pinzón,1 Christian Yepes Hernández,3 Jaime Cajamarca,2 Shigeru Kozima1
1Departamento de Diagnóstico por Imágenes.
2 Departamento de Anatomía Patológica.
3 Departamento de Cirugía.
CEMIC, Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2020;50(2):140-143
Recibido: 11/06/2017 / Aprobado: 02/06/2020 / Publicado en www.actagastro.org el 29/06/2020
Resumen
El tumor estromal gastrointestinal (GIST) es el tumor mesenquimal más frecuente en el tracto digestivo. Una de sus localizaciones más habituales es a nivel del intestino delgado (30%), y una de sus formas de presentación poco usuales es la obstrucción intestinal (10%). El propósito de este trabajo es la presentación de un caso de obstrucción intestinal secundario a un GIST y de la conducta adoptada.
Palabras claves. GIST, intestino delgado, obstrucción intestinal.
Distal ileum mass
Summary
GIST is the most common mesenchymal tumour in the digestive tract. One of the most frequent localization is at the small bowel (30%), and one of its unusual forms of presentation is as a bowel obstruction. The purpose of this article is to report a case of bowel obstruction secondary to a GIST and the adopted conduct.
Key words. GIST, small bowel, bowel obstruction.
Introducción
El la tomografía computada cumple un rol fundamental a la hora de evaluar y caracterizar la patología de íleon terminal, pudiendo orientar su etiología inflamatoria, infecciosa o neoplásica, y determinar la presencia de complicaciones. De ahí radica la importancia de una correcta y precoz interpretación de las imágenes, lo que permite establecer una adecuada planificación terapéutica.
Caso Clínico
Paciente masculino de 79 años con cambios en el ritmo evacuatorio, distensión y dolor abdominal de tres meses de evolución. Como antecedentes personales manifestaba hipertensión, hiperplasia prostática benigna y enfermedad bipolar.
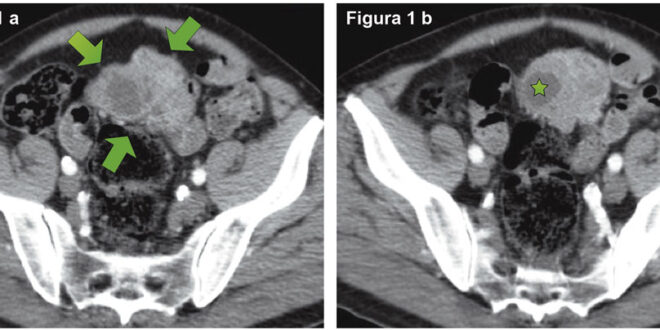
Se solicitó hemograma completo y placa simple de abdomen, que no mostraron hallazgos patológicos, por lo que se decidió realizar una tomografía computada de abdomen y pelvis con contraste oral y endovenoso. Esta evidenció a nivel del íleon terminal una masa heterogénea con áreas quísticas de aproximadamente 65 x 60 mm (Figura 1). Se derivó al servicio de oncología para establecimiento del plan terapéutico, y previo a la fecha de la cirugía programada el paciente presentó un cuadro agudo de obstrucción intestinal, evidenciando en la placa simple de abdomen una marcada distensión de asas de intestino delgado asociada a aislados niveles hidroaéreos (Figura 2), por lo que se decidió realizar laparotomía exploratoria.
Figura 1. A y B) Fase arterial; a nivel del íleon terminal se observa un engrosamiento parietal, de segmento corto, excéntrico, de aproximadamente 68 x 45 mm en el plano axial (flechas), con realce heterogéneo/parcheado tras la administración del contraste endovenoso, con áreas de aspecto quístico en su interior (estrella). No se evidencian otros hallazgos asociados (rarefacción de la grasa, adenomegalias, estratificación parietal).
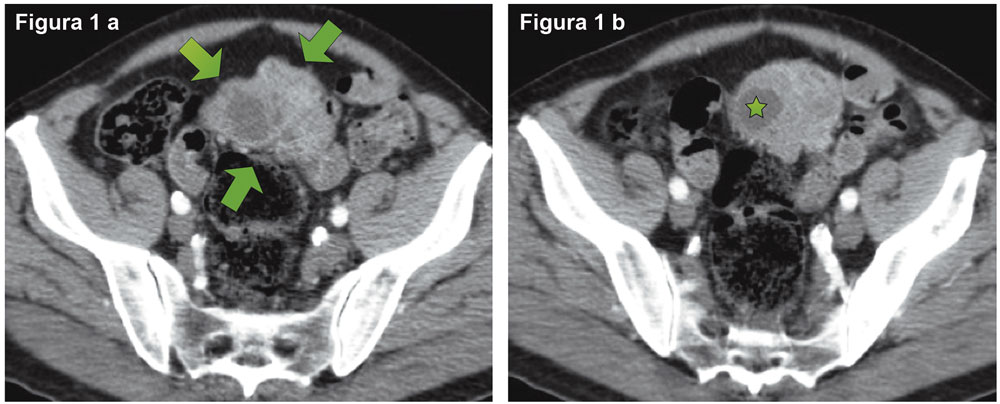
Figura 2. Radiografía simple de abdomen, frente, de pie. Se visualiza distensión de asas de intestino delgado, asociado a niveles hidroaéreos, a predominio de hipocondrio y flanco izquierdo.
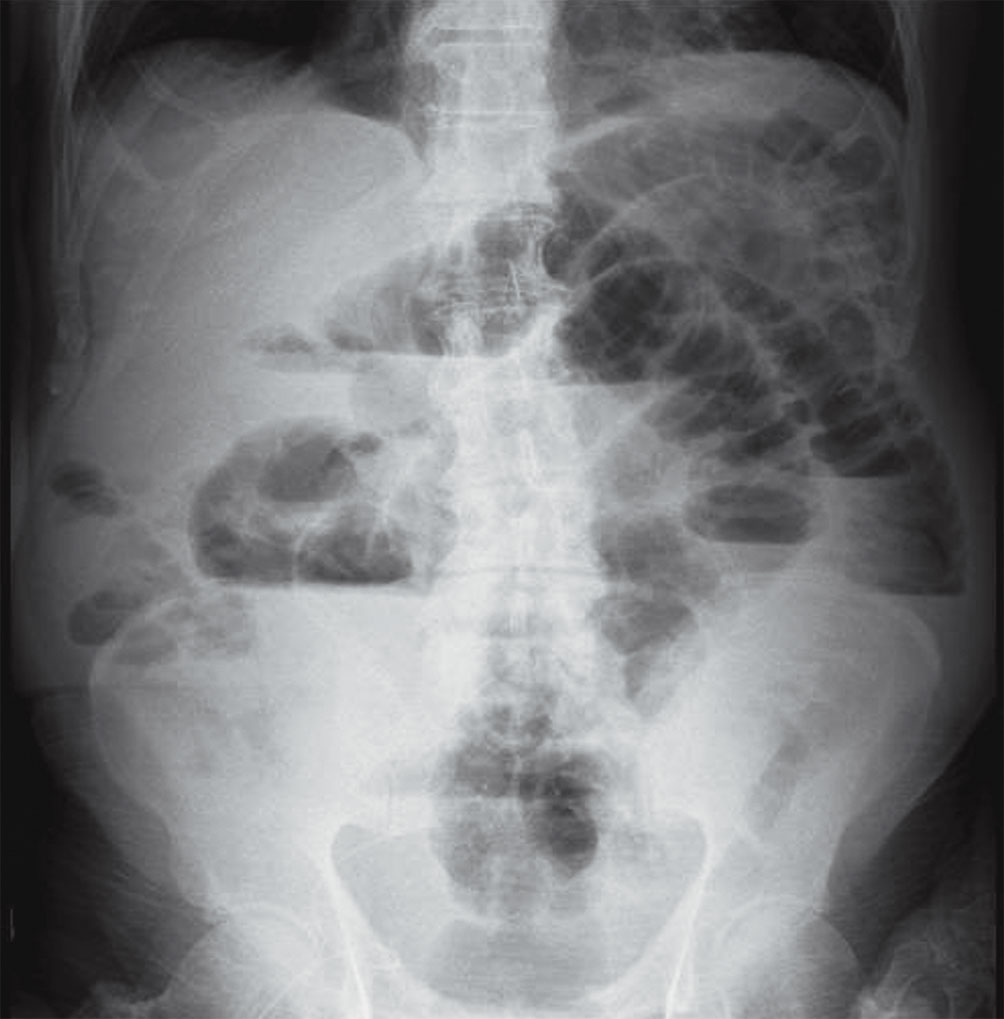
En la cirugía se evidenció a nivel de íleon terminal, a 30 cm de válvula ileocecal, una lesión abscedada y adherida al epiplón, por lo que se realizó enterectomía de 20 cm (Figura 3). La anatomía patológica de la pieza quirúrgica confirmó el diagnóstico de tumor del estroma gastrointestinal (Figura 4).
Figura 3. A y B) Pieza quirúrgica correspondiente a tumoración sólido quística (flechas), abscedada (estrella), que compromete la submucosa del íleon terminal. Obtenida mediante vía convencional (laparotomía).
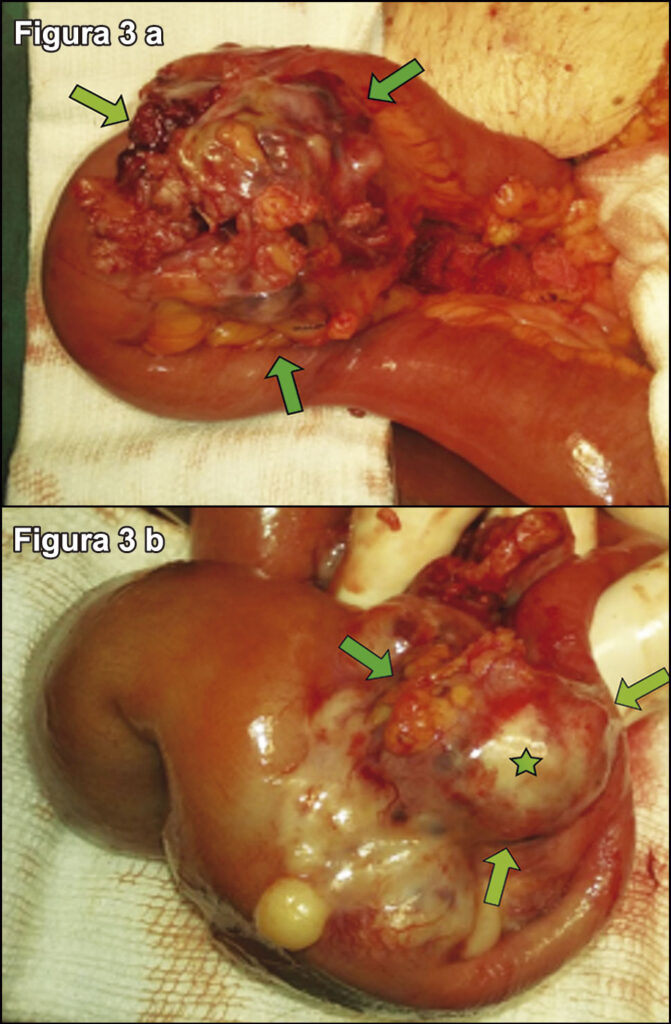
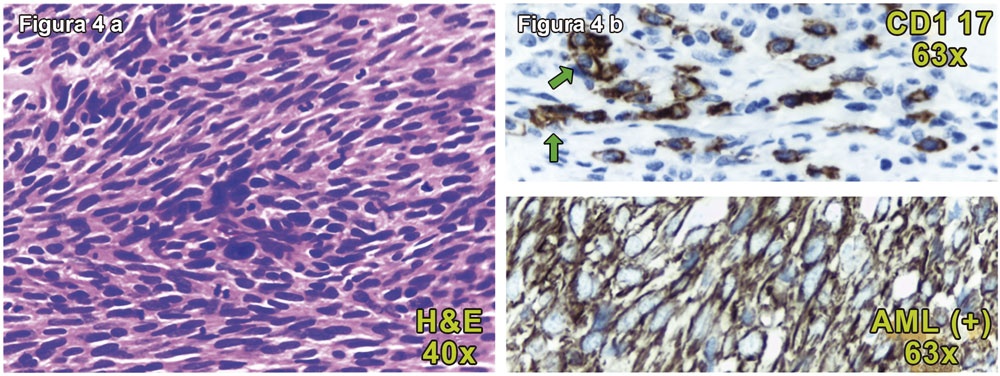
Figura 4. A) Proliferación fuso celular con núcleos elongados, hipercromáticos, se observan células con núcleos bizarros. B) Positividad para CD 117 y AML. Hallazgos compatibles con GIST.
Discusión
La aproximación diagnóstica de la patología en dicha topografía consiste en definir en primer término su extensión (segmento corto vs. segmento largo, afección única vs. multisegmentaria), y posteriormente buscar hallazgos asociados (imágenes ganglionares, rarefacción de la grasa adyacente, estratificación de la pared intestinal, realce de la lesión tras la administración de contraste endovenoso).
Teniendo esto en cuenta y considerando los hallazgos tomográficos (engrosamiento parietal único, de segmento corto, con espesor mayor a 20 mm, ausencia de rarefacción de la grasa adyacente y de estratificación de la pared intestinal), desde las imágenes se orientó el diagnóstico diferencial hacia etiologías neoplásicas (GIST, adenocarcinoma y linfoma) sobre etiologías infecciosas (tuberculosis, yersinia, campilobacter, salmonella) o inflamatorias (enfermedad de Crohn).1
De los diagnósticos diferenciales, el linfoma, por su frecuencia epidemiológica (tumor más frecuente en el intestino delgado)2 y debido a que es una lesión que puede ulcerarse, era una de las opciones diagnósticas más probables. Sin embargo, la afección intestinal del linfoma se caracteriza por presentarse como un engrosamiento parietal voluminoso y circunferencial que involucra un segmento relativamente largo del intestino, frecuentemente asociado a compromiso de cadenas ganglionares regionales, y es infrecuente que produzca obstrucción intestinal como complicación.
También era menos probable el diagnóstico de adenocarcinoma de intestino delgado, ya que este comúnmente afecta el duodeno y se asocia a enfermedad de Crohn, enfermedad celíaca y síndromes neoplásicos hereditarios como Peutz-Jeghers (antecedentes que no tenía nuestro paciente). Además, esta enfermedad se presenta como un engrosamiento anular, estenosante, de bordes irregulares, de un segmento corto y se asocia a leve rarefacción de la grasa adyacente (discordante con el engrosamiento parietal) con realce moderado en adquisiciones poscontraste endovenoso.1, 3
Los tumores del estroma gastrointestinal son las neoplasias no epiteliales más frecuentes del tracto gastrointestinal y derivan de precursores de las células intersticiales de Cajal presentes en el plexo mesentérico. Se ubican más frecuentemente a nivel del estómago (60-70%), del intestino delgado (30%), colorrectal (5%) y del esófago (< 2%).4 La edad promedio de presentación es entre los 40 y 70 años, sin diferencia en la incidencia entre géneros.5 La clínica suele ser inespecífica (dolor y distensión abdominal) y varía según su tamaño y localización; pueden presentarse sangrados o anemia, ictericia en caso de localización duodenal5 y raramente obstrucción intestinal (incidencia menor al 10%),6 como en el presente caso.
La tomografía computada es una herramienta de utilidad para su caracterización y la evaluación de su extensión local y a distancia. Los tumores pequeños se presentan como imágenes bien delimitadas, con densidad de partes blandas y realce homogéneo, ubicadas a nivel subseroso;7 los de mayor tamaño suelen ser heterogéneos, con realce periférico y asociarse a áreas de degeneración quística, necrosis y/o hemorragia,8 como fue el caso de nuestro paciente. Los GIST pueden además presentar ulceraciones o fístulas y por lo general no se asocian a compromiso ganglionar loco-regional o cambios mesentéricos adyacentes.1
Conclusión
Ante la presencia de patología en íleon terminal, la tomografía computada permite orientar su etiología inflamatoria, infecciosa o neoplásica, brindando información para la caracterización de las lesiones y la evaluación de posibles complicaciones. La correcta interpretación precoz de las imágenes cumple un rol fundamental para la evaluación integral del paciente y una adecuada planificación terapéutica.
Referencias
- Hoeffe Cl, Crema MD, Belkacem A, Azizi L, Lewin M, Arrivé L, et al. Multi–Detector Row CT: Spectrum of Diseases Involving the Ileocecal Area. RadioGraphics 2006; 26 (5): 1373-1390.
- Ghai S, Pattison J, Ghai S, O’Malley ME, Khalili K, Stephens M. Primary Gastrointestinal Lymphoma: Spectrum of Imaging Findings with Pathologic Correlation. RadioGraphics 2007; 27 (5): 1371-1388.
- McLaughlin PD, Maher MM. Primary Malignant Diseases of the Small Intestine. American Journal of Roentgenology 2013; 201: W9-W14. doi: 10.2214/AJR.12.8492
- Kim H, Lee JM, Kim KW, Park SH, Kim SH, Lee JY, et al. Gastrointestinal Stromal Tumors of the Stomach: CT Findings and Prediction of Malignancy. American Journal of Roentgenology 2004; 183: 893-898. doi: 10.2214/ajr.183.4.1830893
- Sandrasegaran K, Rajesh A, Rydberg J, Rushing DA, Akisik FM, Henley JD. Gastrointestinal stromal tumors: clinical, radiologic, and pathologic features. American Journal of Roentgenology 2005; 184 (3): 803-811.
- Miettinen M, Monihan JM, Sarlomo RM, Kovatich AJ, Carr NJ, Emory TS, et al. Gastrointestinal stromal tumors/smooth muscle tumors (GISTs) primary in the omentum and mesentery: clinicopathologic and immunohistochemical study of 26 cases. Am J Surg Pathol 1999; 23 (9): 1109-1118.
- King DM. The radiology of gastrointestinal stromal tumours (GIST). Cancer Imaging 2005; 5 (3): 150-156.
- Kang HC, Menias CO, Gaballah AH, Shroff S, Taggart MW, Garg N, et al. Beyond the GIST: Mesenchymal Tumors of the Stomach. RadioGraphics 2013; 33 (6): 1673-1690.
Correspondencia: Nicolás Roccatagliata
Correo electrónico: nrocca@gmail.com
Acta Gastroenterol Latinoam 2020;50(2):140-143
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE