José Carlos Sotelo,1, 2 Adrián Sambresqui,1 Rodrigo Ubeira,1 Guido Orbe,1 José Luis Fernández,1 Nicolás Ortiz,2 Guillermo Pfaffen,2 Franco Rizzo,3 Rojano Samer,3 Víctor Serafini,2 Luis Viola1
1Servicio de Gastroenterología, Hepatología y Endoscopía.
2Servicio de Cirugía. Sector de Cirugía Hepatobiliopancreática.
3Servicio de Imágenes, Sanatorio Güemes de Buenos Aires.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2019;49(4):367-374
Recibido: 28/05/2018 / Aprobado: 02/10/2019 / Publicado en www.actagastro.org el 17/12/2019
Resumen
El hematoma hepático posterior a una colangiopancreatografía retrógrada endoscópica (CPRE) es una rara complicación con pocos casos descriptos en la literatura. Presentamos el caso de una paciente de 47 años con antecedentes de colecistectomía laparoscópica, que ingresó por un cuadro de colestasis secundaria a litiasis coledociana, diagnosticada por colangiorresonancia magnética (CRM), por el que se realizó una CPRE con extracción de un lito con balón. La paciente reingresó 96 horas después del alta con dolor abdominal severo asociado a disnea clase funcional IV, encontrándose hemodinámicamente estable. En la tomografía computada se observó una colección hepática derecha de 135 x 75 mm, cuyo contenido impresionaba líquido. Se realizó un drenaje percutáneo, requirió un nuevo drenaje por una colección residual y una decorticación pleural por toracotomía debido a la afección de la cavidad pleural derecha, con buena evolución posterior y resolución del hematoma. El hematoma hepático post CPRE es una complicación rara pero que puede comprometer seriamente la vida del paciente. El manejo del mismo depende fundamentalmente de la clínica y el estado hemodinámico del paciente, optándose generalmente por el tratamiento conservador, pero pudiéndose llegar en algunas instancias graves a la necesidad de una intervención quirúrgica.
Palabras claves. Guía endoscópica, colangiopancreatografía retrógrada endoscópica, hematoma hepático subcapsular, complicación.
Hepatic hematoma post ERCP. Case report and literature review
Summary
Hepatic hematoma following retrograde endoscopic cholangiopancreatography (ERCP) is a rare complication with few cases described in the literature. We present the case of a 47-year-old woman with a history of laparoscopic cholecystectomy, admitted due to cholestasis secondary to a choledocolithiasis diagnosed by magnetic resonance cholangiography (CRM). Therefore, ERCP and lithiasis extraction with balloon were performed. The patient was readmitted 96 hours after discharge with severe abdominal pain associated with functional class IV dyspnea. She was hemodynamically stable. In the computed tomography (CT) a right hepatic collection of 135 x 75 mm, with liquid appearance content was observed. Percutaneous collection drainage was performed. Subsequently, she required a new percutaneous drainage to drain a residual collection and a pleural decortication by thoracotomy due to the affection of the right pleural cavity, with good evolution and resolution of the hematoma. The hepatic hematoma after ERCP is a rare complication but it can seriously compromise the patient. Its management depends mainly on the clinic and hemodynamic status. Generally, a conservative treatment is chosen but in some serious cases a surgical approach is required.
Key words. Endoscopic guide wire, endoscopic retrograde cholangiopancreatography, subcapsular hepatic hematoma, complication.
La colangiopancreatografía retrógrada endoscópica (CPRE) es un procedimiento terapéutico miniinvasivo utilizado para el abordaje de enfermedades biliopancreáticas, que no está exento de complicaciones. Las principales complicaciones descriptas son la pancreatitis aguda (3% a 10%), la colangitis (1,4%), la hemorragia (0,3% a 2%) y la perforación (0,08% a 0,6%).1 El hematoma hepático es una complicación rara y solo encontramos 32 casos descriptos en la literatura. Presentamos el caso de una paciente con un hematoma hepático post CPRE que fue manejada con drenajes percutáneos, pero que durante su evolución requirió una decorticación pleural derecha por afectación pleural por contigüidad. Además realizamos una revisión de los casos publicados en la literatura.
Caso clínico
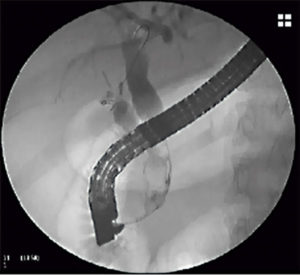
Se trata de una paciente de 47 años, con antecedente de colecistectomía laparoscópica dos años antes y posterior CPRE por litiasis residual, que ingresó por un cuadro de síndrome coledociano. Al ingreso presentaba ictericia cutáneo-mucosa asociada a dolor abdominal leve en la región epigástrica, sin signos clínicos de colangitis. Los datos de laboratorio arrojaron los siguientes resultados: hematocrito 42%, hemoglobina 14,1 g%, glóbulos blancos 7.100/mm3, bilirrubina total: 5,4 mg%, bilirrubina directa: 4,5 mg%, fosfatasa alcalina: 404 U/l, TGP: 223 U/l y TGO: 99 U/l. La colangiorresonancia magnética (CRM) mostró una dilatación de la vía biliar extrahepática con una imagen de defecto de señal en el colédoco distal, compatible con litiasis coledociana. Debido al hallazgo se decidió realizar una CPRE. En el procedimiento se identificó la papila con signos de papilotomía previa, se canuló la vía biliar con papilótomo y alambre guía. Con la colangiografía se evidenció una vía biliar extrahepática dilatada, de aproximadamente 13 mm, y una imagen negativa de 13 mm de diámetro en el colédoco distal. Debido a que la papila no presentaba mayor margen de corte, se decidió realizar una dilatación papilar con un balón tipo CRE de 10 mm. Posteriormente se logró la extracción del cálculo y de barro biliar con un balón extractor (Figura 1).
Figura 1. Imagen de CPRE: se visualiza la vía biliar extrahepática dilatada y un lito de gran tamaño en el colédoco distal.
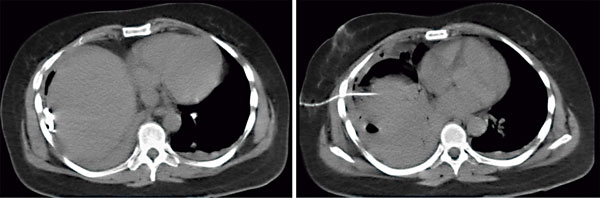
La paciente evolucionó con dolor abdominal leve en el epigastrio que mejoró con analgesia y amilasa post CPRE de 35 UI/l, por lo que se inició la alimentación y se le dio el alta 24 horas después del procedimiento. A las 96 horas reingresó por dolor abdominal severo a predominio del hemiabdomen superior, asociado a disnea clase funcional IV y dolor tipo puntada de costado. Negaba registros o equivalentes febriles y se encontraba hemodinámicamente estable. Laboratorio: hematocrito 39%, hemoglobina 12,7 g%, glóbulos blancos 18.100/mm3, amilasa 42 UI/l, lipasa 49,5 UI/l y hepatograma sin alteraciones. Se realizó una tomografía computada (TC) de abdomen y pelvis con contraste endovenoso, en la que se observó una colección hepática subfrénica derecha de 135 x 75 mm, con contenido particulado y burbujas aéreas, que elevaba la cúpula diafragmática e impresionaba de contenido hemático. Las vías biliares no estaban dilatadas (Figuras 2 y 3).
Figura 2 y 3. TC de abdomen con contraste endovenoso: se observa una colección hepática subfrénica derecha de 135 x 75 mm, con contenido particulado y burbujas aéreas, que eleva la cúpula diafragmática.
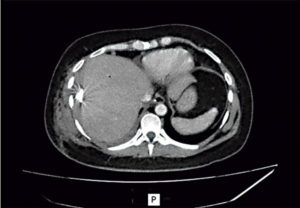
Con este hallazgo se decidió realizar el drenaje percutáneo de dicha colección bajo guía ecográfica, con la colocación de un catéter multipropósito de 12 Fr, lográndose evacuar 400 ml de líquido hematopurulento, cuyo cultivo fue positivo para Escherichia coli sensible. A las 24 horas, debido a que la paciente continuaba con sintomatología respiratoria, se realizó una nueva TC que evidenció una disminución marcada del componente líquido de la colección, persistencia de la imagen con contenido aéreo en contacto con la cúpula diafragmática y el agregado de un derrame pleural homolateral. Se decidió realizar el drenaje percutáneo guiado por tomografía de la colección residual subfrénica y la punción del derrame pleural, cuyo resultado fue interpretado como un empiema debido al examen físico-químico (aspecto turbio, ácido láctico 20 mg%, LDH 4.431 UI/l, glucosa 11 mg% y cultivo positivo para Escherichia coli sensible (Figuras 4 y 5). El empiema pleural fue manejado inicialmente con un tubo de avenamiento derecho, y posteriormente, dado que no se logró el drenaje completo y se observó un peel pleural, se realizó una decorticación por toracotomía con resolución completa de la patología pleural. La paciente evolucionó favorablemente con seguimiento ambulatorio. El hematoma se resolvió completamente y el drenaje se retiró a los 46 días (Figura 6).
Figura 4 y 5. TC de abdomen posterior al drenaje percutáneo de la colección: a la derecha se observa el drenaje colocado en primera instancia, visualizándose la evacuación clara del componente líquido de la colección. A la izquierda se observa el nuevo drenaje colocado para evacuar el líquido y el aire residual.
Figura 6. TC de abdomen con contraste, donde se evidencia la resolución total del hematoma.
Discusión
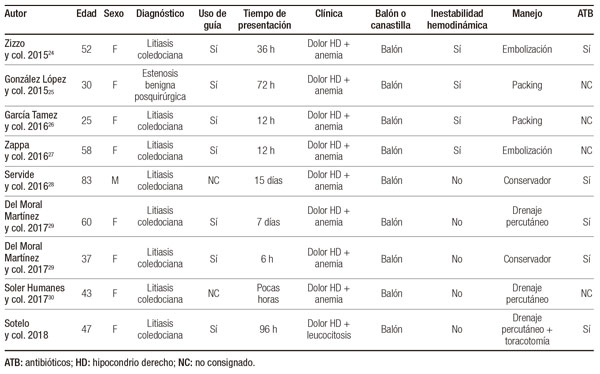
Dentro de las complicaciones de la CPRE, el hematoma hepático es raro y, desde el primer caso comunicado en el año 2000, solo hemos hallado 32 en nuestra revisión de la literatura. En la Tabla 1 resumimos los principales hallazgos de estas comunicaciones, comparándolos con los de nuestro caso.2-30
Con respecto a la fisiopatología, no está del todo clara pero se han planteados dos hipótesis. La primera estaría relacionada con el daño de los vasos intrahepáticos de pequeño calibre por el alambre guía metálico u otros accesorios durante el acceso a la vía biliar. Esta es la menos probable, debido a que los materiales utilizados han evolucionado, actualmente son más blandos y atraumáticos. Como segunda hipótesis se plantea que el sangrado se produciría debido a la tracción ejercida con el balón sobre los componentes del pedículo glissoniano, generando el daño de los vasos intrahepáticos. Esta parece ser la más probable e interesante, ya que tenerla en cuenta permitiría actuar previniéndola.2-29
El cuadro clínico del hematoma intrahepático es variable. Los síntomas más frecuentes son el dolor abdominal, presente en el 87% de los casos, la caída de la hemoglobina y el hematocrito, en el 54%, la fiebre en el 18% y la presencia de leucocitosis en el 9% de los casos reportados. Nuestra paciente se presentó estable hemodinámicamente. Sin embargo, es posible que en casos de sangrado agudo y severo esta complicación pueda manifestarse como shock hipovolémico, como sucedió en el 36% de los pacientes comunicados. El tiempo de presentación puede ir de unas horas a días después de la CPRE. En nuestro caso la consulta se realizó a las 96 horas posteriores. Cuando dividimos los rangos de presentación en aquellos que consultaron dentro de las 72 horas o luego de este intervalo de tiempo, vemos que la mayor parte consultó dentro de las 72 horas (73% vs. 27%), llegando hasta los 15 días posteriores en un solo caso.
El diagnóstico se realiza a través de métodos de imágenes como ecografía o TC con contraste. Esta última es especialmente útil para evaluar la extravasación de contraste, lo que indicaría sangrado activo y la necesidad de una conducta más agresiva frente al cuadro.27
El manejo de los pacientes depende fundamentalmente del estado clínico y hemodinámico. En el caso de un paciente estable hemodinámicamente y sin signos de infección se sugiere tratamiento conservador y profilaxis antibiótica. Hay múltiples casos que demuestran la efectividad de este abordaje, que fue el tratamiento realizado en el 42% de los pacientes.2, 3, 9-14, 17, 18, 28, 29 Por el contrario, en caso de sospecha de sobreinfección del hematoma, se opta por un abordaje más activo con drenaje percutáneo guiado por imágenes (TC o ecografía). Este abordaje, realizado en el 27% de los casos publicados, fue el que elegimos para nuestra paciente.2, 5, 8, 20-22, 29, 30 Si el paciente presenta inestabilidad hemodinámica y no responde a maniobras conservadoras y/o muestra sangrado activo en los estudios de imágenes se deberá valorar la necesidad de una embolización selectiva o superselectiva de los vasos intrahepáticos. Según la revisión, este tratamiento fue necesario en el 18% de los pacientes.4, 7, 9, 15, 27
El tratamiento quirúrgico es la última opción ante fallas de maniobras menos invasivas en un paciente inestable con deterioro del estado general, signos de irritación peritoneal y líquido libre en los estudios de imágenes. Tiene por objetivo evacuar el hematoma y realizar hemostasia de la región sangrante, pudiendo requerirse un packing en caso de hemorragia masiva. Además, en caso de afectación pleural por contigüidad y/o contaminación, como sucedió en nuestro caso, puede ser necesario el tratamiento quirúrgico de la cavidad pleural. En nuestra revisión encontramos que el abordaje quirúrgico fue necesario en el 21% de los pacientes, ya sea como tratamiento complementario posterior a maniobra menos invasiva o como tratamiento inicial (Tabla 1).6, 15, 16, 18, 23-26
Tabla 1. Hematoma hepático post CPRE: casos comunicados en la literatura.
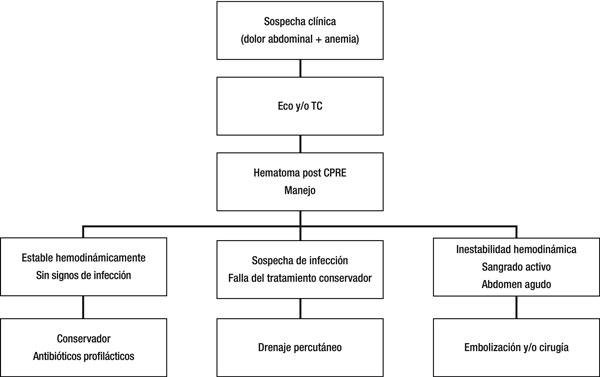
Por último, a manera de resumen mostramos un algoritmo de manejo de estos pacientes (Figura 7).
Figura 7. Algoritmo de manejo del hematoma hepático post CPRE.
Concluimos que el hematoma hepático post CPRE es una rara complicación del procedimiento, escasamente reportada y quizás subdiagnosticada debido a la variabilidad en su presentación. Dado que es una complicación que puede poner en peligro la vida del paciente, es importante la sospecha clínica ante el hallazgo de dolor abdominal súbito y caída del hematocrito. El manejo depende fundamentalmente de la clínica y el estado hemodinámico, optándose con mayor frecuencia por el tratamiento conservador, pero pudiendo requerir tratamientos más invasivos como el drenaje percutáneo del hematoma, la embolización en caso de sangrado activo o incluso la cirugía en pacientes severamente comprometidos.
Conflicto de interés. Los autores no declaran ningún conflicto de interés.
Sostén financiero. No hubo aportes que financiaran el estudio.
Referencias
- ASGE Standards of Practice Committee, Chandrasekhara V, Khashab MA, Muthusamy VR, Acosta RD, Agrawal D, Bruining DH, Eloubeidi MA, Fanelli RD, Faulx AL, Gurudu SR, Kothari S, Lightdale JR, Qumseya BJ, Shaukat A, Wang A, Wani SB, Yang J, DeWitt JM. Adverse events associated with ERCP. Gastrointest Endosc 2017; 85: 32-47.
- Ortega Deballon P, Fernández Lobato R, García Septiem J, Nieves Vázquez MA, Martínez Santos C, Moreno Azcoita M. Liver hematoma following endoscopic retrograde cholangiopancreatography (ERCP). Surg Endosc 2000; 14: 767-768.
- Horn TL, Peña LR. Subcapsular hepatic hematoma after ERCP: case report and review. Gastrointest Endosc 2004; 59: 594-596.
- Chi KD, Waxman I. Subcapsular hepatic hematoma after guide wire injury during endoscopic retrograde cholangiopancreatography: management and review. Endoscopy 2004; 36: 1019-1021.
- Ertuğrul I, Parlak E, Ibiş M, Altiparmak E, Saşmaz N, Sahin B. An unusual complication of endoscopic retrograde cholangiopancreatography. Dig Dis Sci 2006; 51: 1167-1168.
- Priego P, Rodríguez G, Mena A, Losa N, Aguilera A, Ramiro C, Lisa E, Conde S, Fresneda V. Subcapsular liver hematoma after ERCP. Rev Esp Enferm Dig 2007; 99: 53-54.
- Petit-Laurent F, Scalone O, Penigaud M, Barbeys J. Subcapsular hepatic hematoma after endoscopic retrograde cholangiopancreatography: case report and literature review. Gastroenterol Clin Biol 2007; 31: 750-752.
- Bhati CS, Inston N, Wigmore SJ. Subcapsular intrahepatic hematoma: an unusual complication of ERCP. Endoscopy 2007; 39: E150.
- Del Rosi M, Martínez Briceño Y, Louis Pérez C, Garassini Ch M. Hematoma intrahepático y subcapsular posterior a colangiopancreatografía retrógrada endoscópica (CPRE). Reporte de un caso y revisión. Gen 2007; 61: 210-211.
- McArthur KS, Mills PR. Subcapsular hepatic hematoma after ERCP. Gastrointest Endosc 2008; 67: 379-380.
- De La Serna-Higuera C, Fuentes Coronel A, Rodríguez Gómez SJ, Martín Arribas MI. Subcapsular hepatic hematoma secondary to the use of hydrophilic guidewires during endoscopic retrograde cholangiopancreatography. Gastroenterol Hepatol 2008; 31: 266-267.
- Cárdenas A, Crespo G, Balderramo D, Bordas JP, Sendino O, Llach J. Subcapsular liver hematoma after endoscopic retrograde cholangiopancreatography in a liver transplant recipient. Ann Hepatol 2008; 7: 386-388.
- Nari GA, Preciado Vargas J, Rosendo Ballesteros N. Una rara complicación de la CPRE: el hematoma subcapsular hepático. Cir Esp 2009; 85: 261-262.
- Revuelto Rey J, Gordillo Escobar E, Batalha P. Hematoma subcapsular hepático tras colangiopancreatografía retrógrada endoscópica. Med Intensiva 2010; 34: 224.
- Baudet J-S, Arguiñarena X, Redondo I, Tadeo E, Navazo L, Mendiz J, Montiel R. Subcapsular hepatic hematoma: an uncommon complication of endoscopic retrograde cholangiopancreatography. Gastroenterol Hepatol 2011; 34: 79-82.
- Pérez-Legaz J, Santos J, Ruiz-Tovar J, Moya-Forcén P, Armañanzas L, Gómez M, Oller I, Arroyo A, Calpena M. Subcapsular hepatic hematoma after ERCP (endoscopic retrograde cholangipancreatography). Rev Esp Enferm Dig 2011; 103: 550-551.
- Del Pozo D, Moral I, Poves E, Sanz C, Martín M. Subcapsular hepatic hematoma following ERCP: case report and review. Endoscopy 2011; 43: E164-165.
- Bartolo Rangel EF, Endoqui Anaya Y, Trejo Suárez J, Esperón Lorenzana I, Dávila Jolly H, Álvarez Olmos J, Montero López A, Ramos Xicoténcatl R. Hematoma hepático subcapsular roto y choque hipovolémico como una complicación inusual tras la realización de colangiopancreatografía retrógrada endoscópica. Reporte de un caso. Cir Gen 2012; 34: 217-220.
- Orellana F, Irarrázaval J, Galindo J, Balbontin P, Manríquez L, Plass R, Araya R, Ríos H, Sáenz R. Subcapsular hepatic hematoma post ERCP: a rare or an underdiagnosed complication? Endoscopy 2012; 44: E108-E109.
- Fei B-Y, Li C-H. Subcapsular hepatic haematoma after endoscopic retrograde cholangiopancreatography: an unusual case. World J Gastroenterol 2013; 19: 1502.
- Oliveira Ferreira A, Tato Marinho R, Velosa J. Infected hepatic hematoma 10 days after ERCP. Endoscopy 2013; 45: E402-403.
- Carrica SA, Belloni R, Baldoni F, Yantorno M, Correa G, Bologna A, Barbero R, Villaverde A, Chopita N. Intraparenchymal hepatic haematoma after endoscopic retrograde cholangiopancreotography overinfected by Citrobacter freundii and Klebsiella pneumoniae BLEE. Acta Gastroenterol Latinoam 2014; 44: 125-128.
- Klímová K, Padilla Suárez C, González Asanza C, Matilla Peña A, Cos Arregui E, Hernando Alonso A. Subcapsular hepatic hematoma after ERCP: a case report and revision of literature. Case Rep Clin Med 2014; 3: 161-166.
- Zizzo M, Lanaia A, Barbieri I, Zaghi C, Bonilauri S. Subcapsular hepatic hematoma after endoscopic retrograde cholangiopancreatography. Medicine (Baltimore) 2015; 94: e1041.
- González-López R, García-Cano E, Espinosa-González O, Cruz-Salgado Á, Montiel-Jarquin Á-J, Hernández-Zamora V. Tratamiento quirúrgico para hematoma subcapsular hepático posterior a colangiografía retrógrada endoscópica; caso inusual. Cir Cir 2015; 83: 506-509.
- García Tamez A, López Cossio JA, Hernández Hernández G, González Huezo MS, Rosales Solís AA, Corona Esquivel E. Subcapsular hepatic hematoma: an unusual, but potentially life-threating post-ERCP complication. Case report and literature review. Endoscopia 2016; 28: 75-80.
- Zappa MA, Aiolfi A, Antonini I, Musolino CD, Porta A. Subcapsular hepatic haematoma of the right lobe following endoscopic retrograde cholangiopancreatography: case report and literature review. World J Gastroenterol 2016; 22: 4411-4415.
- Servide MJ, Prieto M, Marquina T. Hepatic subcapsular hematoma: a rare late complication after ERCP. Rev Esp Enferm Dig 2016; 108: 234-235.
- Del Moral Martínez M, Delgado Maroto A, Cervilla Sáez de Tejada ME, Casado Caballero FJ, Salmerón Escobar FJ. Hepatic hematoma after ERCP: two new case reports. Rev Esp Enferm Dig 2017; 109: 470-473.
- Soler Humanes R, Suárez Muñoz MÁ, García García B. A post-endoscopic retrograde cholangiopancreatography subcapsular hepatic hematoma. Rev Esp Enferm Dig 2017; 109: 803.
Correspondencia: José Carlos Sotelo
Acuña de Figueroa 1240 (CP: AAX 1180). Servicio de Gastroenterología y Endoscopía, Sanatorio Güemes de Buenos Aires. Ciudad Autónoma de Buenos Aires, Argentina / Tel.: +54 (011) 495981200.
Correo electrónico: jose_sotelo2004@hotmail.com
Acta Gastroenterol Latinoam 2019;49(4):367-374
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE