Sofía Gamboa Miño ID· Gustavo Kohan ID· Rodrigo Vergara Sandoval ID· Josefina Dib
Hasan ID· Aldana Iaccarino ID· Frank Deroi Sánchez ID· Eduardo J. Houghton ID
Hospital Bernardino Rivadavia.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2025;55(2):114-123
Recibido: 13/04/2025 / Aceptado: 17/06/2025 / Publicado online: 30/06/2025 / https://doi.org/10.52787/agl.v55i2.482
Resumen
Introducción. El adenocarcinoma ductal de páncreas es una de las neoplasias malignas más letales, con una supervivencia a cinco años inferior al 10%. La mayoría de los pacientes se diagnostican en estadios avanzados, y se prevé un aumento en su incidencia y mortalidad en la próxima década. Objetivos. Estimar la supervivencia global de pacientes operados con diagnóstico de adenocarcinoma ductal de páncreas y analizar los factores clínico-patológicos asociados. Materiales y metodos. Estudio observacional, de cohorte retrospectiva y multicéntrico. Se incluyeron pacientes operados entre enero de 2019 y diciembre de 2024, con diagnóstico histológico de adenocarcinoma ductal de páncreas. Se establecieron factores en relación con la supervivencia global mediante análisis multivariado (regresión de Cox). Resultados. Fueron evaluados 122 pacientes. La media de edad fue de
66,6 años; el 53,3% eran mujeres. El 62,3% recibió quimioterapia posoperatoria. La supervivencia media global fue de 31,7 meses. La recidiva tumoral ocurrió en el 28,7%, y el 31,1% presentó complicaciones posoperatorias. El análisis multivariado mostró que la quimioterapia se asoció a una reducción significativa del riesgo de mortalidad (HR 0,09; IC95%: 0,04-0,21; p < 0,001). La recidiva (HR 2,5; IC95%: 1,25-5,03; p = 0,01) y el grado de diferenciación tumoral (HR 2,2; IC95%: 1,21-4,00; p = 0,01) se asociaron a mayor mortalidad. Conclusión. La cirugía combinada con quimioterapia adyuvante se asocia significativamente a una mayor supervivencia en pacientes con adenocarcinoma ductal de páncreas, mientras que una menor supervivencia se asocia a la presencia de recidiva y al grado de diferenciación tumoral.
Palabras claves. Adenocarcinoma, supervivencia, quimioterapia.
Prognostic Factors and Survival in Patients Undergoing Surgery for Pancreatic Ductal Adenocarcinoma: a MultiCenter Retrospective Analysis
Summary
Introduction. Pancreatic ductal adenocarcinoma (PDAC) is one of the most lethal malignancies, with a five-year survival rate of less than 10%. Most patients are diagnosed at advanced stages, and both incidence and mortality are expected to rise over the next decade. Objectives. To estimate overall survival in patients undergoing surgery for pancreatic ductal adenocarcinoma and to analyze associated clinicopathological factors. Materials and methods. A multicenter, retrospective cohort study was condcuted. Patients who underwent surgery between January 2019 and December 2024 with histologically confirmed pancreatic ductal adenocarcinoma were included. Factors associated with overall survival were identified through multivariate analysis using Cox proportional hazards regression. Results. A total of 122 patients were evaluated. The mean age was 66.6 years, and 53.3% were female. Postoperative chemotherapy was administered in 62.3% of cases. The median overall survival was 31.7 months. Tumor recurrence occurred in 28.7% of patients, and 31.1% experienced postoperative complications. Multivariate analysis revealed that adjuvant chemotherapy was significantly associated with reduced mortality risk (HR 0.09; 95% CI: 0.04-0.21; p < 0.001). Tumor recurrence (HR 2.5; 95% CI: 1.25-5.03; p = 0.01) and histological tumor differentiation (HR 2.2; 95% CI: 1.21-4.00; p = 0.01) were associated with increased mortality. Conclusion. Surgery combined with adjuvant chemotherapy is significantly associated with improved survival in patients with pancreatic ductal adenocarcinoma. Conversely, tumor recurrence and histological tumor differentiation are linked to decreased survival.
Keywords. Adenocarcinoma, survival, chemotherapy.
Introducción
El cáncer de páncreas constituye la tercera causa de muerte por cáncer en la población mundial. En las últimas décadas, su incidencia y mortalidad han mostrado una tendencia ascendente, particularmente en hombres (de 12,1% en 2000 a 12,7% en 2020), mientras que en mujeres se ha mantenido relativamente estable (de 9,3% a 9,6%).1 El adenocarcinoma ductal de páncreas (PDAC) representa la forma histológica más frecuente y letal de esta neoplasia. Entre el 80% y el 85% de los pacientes se diagnostican en estadios avanzados, y la tasa de supervivencia a cinco años es menor al 10%.2-4 Se estima que en los próximos años el PDAC será la segunda causa de muerte por cáncer en países desarrollados,3, 4 en parte debido al incremento de factores de riesgo como la obesidad, la diabetes y el tabaquismo.5
Desde el punto de vista quirúrgico, el PDAC no metastásico se clasifica como resecable, borderline o localmente avanzado, de acuerdo con el grado de compromiso vascular. A la clásica clasificación anatómica se suman en la actualidad criterios de resecabilidad biológica (valor de CA 19-9 < 500 U/ml) y estado funcional (basado en el performance status, siendo ECOG ≥ 2 una contraindicación relativa a la cirugía.6 En los casos resecables, el tratamiento estándar consiste en la resección quirúrgica, seguida de quimioterapia adyuvante. Para los tumores borderline o localmente avanzados, se recomienda el uso de quimioterapia neoadyuvante seguida de cirugía en pacientes respondedores.7-9
En cuanto a los esquemas de quimioterapia, los más utilizados incluyen FOLFIRINOX (5-fluorouracilo, leucovorina, irinotecán y oxaliplatino) y la combinación de gemcitabina con nab-paclitaxel, ambos recomendados en pacientes con buen estado funcional.10-13 En pacientes con limitaciones clínicas o edad avanzada, se suele emplear gemcitabina en monoterapia o capecitabina oral. Si bien FOLFIRINOX se asocia a mayor toxicidad, ha demostrado mejorar significativamente la supervivencia en comparación con la gemcitabina sola.14,15
A pesar de estos avances, la supervivencia global del PDAC continúa siendo baja. La alta heterogeneidad tumoral, la frecuente presentación en estadios avanzados y las desigualdades en el acceso al tratamiento multidisciplinario contribuyen a los pobres resultados observados en la práctica. En nuestro medio, muchos pacientes se enfrentan a demoras diagnósticas, barreras para acceder a la quimioterapia adyuvante y derivaciones tardías, lo cual impacta negativamente en su pronóstico.
Frente a esta realidad, el objetivo del presente estudio fue estimar la supervivencia global de pacientes adultos con diagnóstico de PDAC luego de la resección quirúrgica, y analizar los factores clínicos y patológicos asociados a la mortalidad.
Material y métodos
Diseño de estudio
Se realizó un estudio observacional, longitudinal, de cohorte retrospectivo, multicéntrico. Se estudió a todos los pacientes adultos que fueron operados en el período comprendido desde enero de 2019 hasta diciembre de 2024, con diagnóstico histológico de PDAC, a partir de espécimen quirúrgico. Se realizaron en total 426 cirugías pancreáticas de resección (duodenopancreatectomías o pancreatectomías izquierdas); solo 195 casos presentaron diagnóstico de PDAC, de los cuales se excluyeron 73 casos perdidos en el seguimiento, por lo que el total de pacientes analizados fue de 122.
Criterios de selección
Se incluyeron pacientes mayores de 18 años que, entre enero de 2019 y diciembre de 2024, presentaron en estudios tomográficos una lesión pancreática compatible con adenocarcinoma. Tras la resección quirúrgica y la confirmación histológica, se seleccionaron aquellos con diagnóstico definitivo de adenocarcinoma ductal de páncreas. No se consideraron aquellos casos en quienes se perdió el seguimiento ni los que presentaron historia clínica incompleta.
Procedimiento y técnica
Los pacientes fueron evaluados inicialmente mediante estudios por imágenes. La planificación quirúrgica se basó en la localización tumoral, la presencia o no de compromiso vascular y la extensión local de la enfermedad. Durante el procedimiento quirúrgico se realizaron los mismos pasos sistemáticamente. Tras la resección quirúrgica, el seguimiento se realizó con tomografía computada trifásica y determinación del marcador tumoral CA 19-9, cada tres meses durante los dos primeros años del posoperatorio, y luego semestralmente. En los casos en que estos estudios no fueron concluyentes, se indicó tomografía por emisión de positrones (PET/CT). Una vez confirmado el diagnóstico histológico de adenocarcinoma ductal de páncreas, los pacientes fueron derivados al servicio de oncología para iniciar el tratamiento quimioterápico. Finalmente, los casos seleccionados fueron incorporados a una base de datos electrónica para su análisis retrospectivo.
Las complicaciones posoperatorias requirieron distintos tipos de resolución: la fístula pancreática tipo A se controló con posterior retiro del drenaje; en la tipo B, se realizó drenaje percutáneo, y la tipo C requirió reoperación con abordaje convencional. Otras complicaciones posoperatorias que se trataron con reoperación y abordaje convencional fueron la hemorragia digestiva alta, el hemoperitoneo, la estenosis de gastroenteroanastomosis, la bilirragia y la trombosis portal. La colección posoperatoria se resolvió con drenaje percutáneo. Las fístulas biliar, mixta y quilosa fueron controladas con posterior retiro de los drenajes.
Desenlaces de estudio y recuperación de datos
Las variables dependientes fueron el fallecimiento y el tiempo de supervivencia global. Se dividió a los pacientes fallecidos según el momento del evento óbito en:
– Posoperatorio: hasta los treinta días de realizada la cirugía, durante la internación.
– Posexternación: luego de los treinta días de realizada la cirugía.
El tiempo de supervivencia global se definió como el tiempo transcurrido desde la cirugía hasta el evento muerte, medido en meses.
Se estudiaron las variables: edad (se expresó en años y se consideró la edad al momento del estudio), sexo (se otorgó sexo biológico consignado en la historia clínica, estableciéndose como femenino o masculino), localización del tumor (se clasificó según localización en el páncreas, cabeza, cuerpo o cola), grado de diferenciación tumoral (se clasificó en bien, moderado o pobremente diferenciado), y las variables dicotómicas: tratamiento con quimioterapia, presencia de complicaciones posoperatorias, presencia de metástasis ganglionar, compromiso vascular y perineural, y recidiva de la enfermedad (por marcadores e imágenes). Los datos fueron recuperados en hoja electrónica de excel.
Para clasificar las complicaciones correspondientes a fístula pancreática se utilizó el esquema de clasificación del Grupo Internacional de Estudio de Fístula Pancreática (ISGPF), agrupándolas en fístulas tipo A, B y C.16
Análisis estadístico
Estadística descriptiva. Las variables categóricas se expresaron como frecuencia y porcentaje, y las cuantitativas como media y desvío estándar (DE). La normalidad de las variables se evaluó con el test de Shapiro Wilks.
Estadística inferencial. Para la comparación de grupos se utilizó para variables cuantitativas el test de T de Student; para comparación de variables categóricas se utilizó el test de Chi cuadrado o el test Exacto de Fisher. Para la estimación de la supervivencia global se calculó el tiempo en meses transcurrido desde la realización de la cirugía oncológica y el fallecimiento (evento). Mediante curva de Kaplan-Meier se ilustró la supervivencia para los subgrupos planteados: indicación de quimioterapia adyuvante, complicaciones posoperatorias y presentación de recidiva. Los intervalos de confianza para la supervivencia se calcularon mediante el método de Greenwood. Los tiempos de supervivencia se compararon mediante el test de Mantel-Cox (Log-Rank). Se realizó análisis multivariado de Cox. El modelo convergió correctamente y el método para empates utilizado fue Breslow. Se estimaron los Hazard Ratio (HR) y sus intervalos de confianza.
Consideraciones técnicas. Se consideraron significativas aquellas pruebas con p < 0,05. Todos los análisis estadísticos fueron efectuados utilizando el programa estadístico SPSS versión 23 (SPSS Inc, Chicago, IL).
Nociones éticas
El estudio contó con la aprobación del Comité Institucional de Ética en Investigación. Se garantizó la confidencialidad de la identidad del paciente y de sus datos tantos personales como clínicos conforme a la Ley 25326 de Protección de Datos Personales (Ministerio de Justicia y Derechos Humanos, República Argentina). Este estudio se llevó a cabo en conformidad con el código de Núremberg de 1947 y la Declaración de Helsinki de 1964 y enmiendas posteriores (la última data del 2013).
Resultados
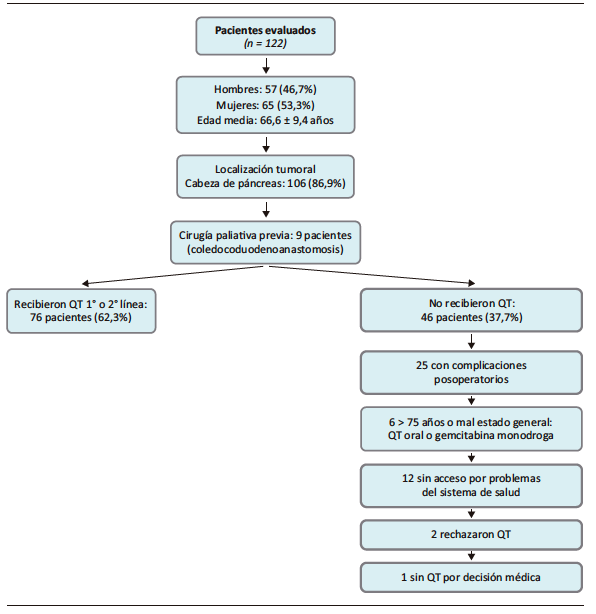
Se analizaron 122 casos. Correspondieron 57 a hombres (46,7%) y 65 a mujeres (53,3%), presentando una edad media de 66,6 años (DE ± 9.4). El sitio más frecuente de localización tumoral fue la cabeza del páncreas, presentándose en 106 casos (86,9%). Nueve pacientes (derivados de otros centros) tenían una cirugía paliativa previa (coledocoduodenoanastomosis) y fueron resecados por nuestro grupo. Recibieron tratamiento con quimioterapia de primera y segunda línea 76 pacientes (62,3%). Las causas que impidieron realizar tratamiento quimioterápico de primera o segunda línea a los 46 pacientes restantes fueron las siguientes: 25 presentaron complicaciones que demoraron la posibilidad de iniciar tratamiento; 6 tenían una edad superior a 75 años o un estado funcional que solo les permitió recibir quimioterapia vía oral (capecitabine) o gemcitabine monodroga; 12 no pudieron acceder al tratamiento debido a las dificultades del sistema público; 2 rechazaron la quimioterapia, y uno no recibió tratamiento por decisión del oncólogo tratante. (Ver flujograma a continuación).
El grado de diferenciación tumoral moderado fue el más prevalente, presentándose en 87 casos (71,3%) (Tabla 1).
Tabla 1. Características de la muestra de estudio
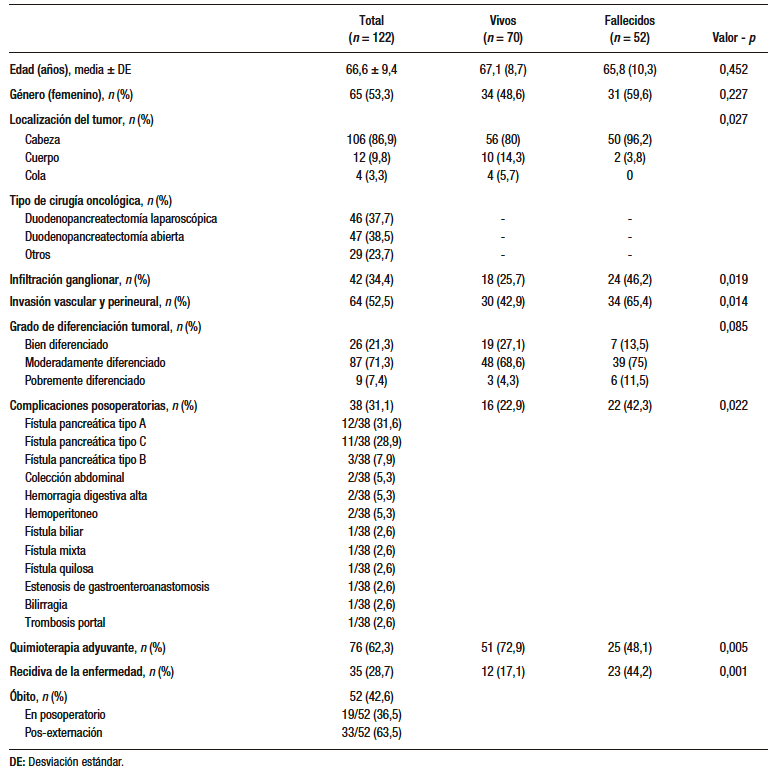
El 31,1% (38 casos, IC 95% = 23,6 – 39,8%) de los pacientes presentó complicaciones posoperatorias. La más frecuente fue la fístula pancreática (Tabla 1).
La supervivencia promedio fue de 31,7 meses (RIC: 24,3 – 47,6). El 28,7% (IC95% = 21,4-37,3%) de los pacientes presentaron recidiva de la enfermedad. Fallecieron 52 (42,62%, IC95%=34,2-51,5%) pacientes, de los cuales 19 (36,5%, IC95% = 28,4 – 50,1%) murieron durante los primeros treinta días posoperatorios, y
33 (63,5%, IC95% = 49,9 – 75,2%) luego de los treinta días (Tabla 1).
La cirugía realizada con mayor frecuencia fue la duodenopancreatectomía cefálica convencional, llevándose a cabo en 47 casos (38,5%, IC95% = 30,4 – 47,4%), seguida de la duodenopancreatectomía laparoscópica, en 46 casos (37,7%, IC95% = 29,6 – 46,6%)
(Tabla 1).
Se compararon las características clínicas entre pacientes fallecidos y no fallecidos. Se observó una diferencia significativa en cuanto a quimioterapia (p = 0,005), metástasis ganglionar (p = 0,019), invasión vascular/perineural (p = 0,014), complicaciones (p = 0,022) y recidiva de la enfermedad (p = 0,001). Aquellos pacientes que recibieron quimioterapia presentaron mayor supervivencia, mientras que los que tuvieron metástasis ganglionar y/o invasión vascular/perineural se asociaron a mayor mortalidad. También se observó mayor mortalidad en los pacientes que presentaron complicaciones y en aquellos que tuvieron recidiva de la enfermedad (Tabla 1).
El 51,4% de los pacientes no fallecidos correspondió a varones, mientras que el 48,6% fueron mujeres. En el caso de los pacientes fallecidos, el 40,4% correspondió a varones y el 59,6% a mujeres, evidenciándose un mayor porcentaje de supervivencia en hombres que en mujeres (p = 0,227).
De los pacientes vivos, el 72,9% recibió quimioterapia posoperatoria, mientras que en el caso de los fallecidos el 48,1% la recibió, observándose una diferencia significativa (p = 0,005) (Tabla 1).
Se observaron mayores complicaciones en los pacientes fallecidos, correspondiendo al 42,3%. Los pacientes vivos presentaron un 22,9% de complicaciones (p = 0,022).
El 44,2% de los pacientes fallecidos presentaron recidiva de la enfermedad antes del óbito, mientras que en el caso de los vivos se presentó recidiva en el 17,1%, observándose diferencia significativa (p = 0,001) (Tabla 1).
En el gráfico de Kaplan-Meier se observa que, transcurridos los meses, la tasa de supervivencia se redujo, alcanzando una probabilidad de supervivencia del 31% a los 66 meses de seguimiento.
El tiempo de supervivencia de aquellos pacientes que no recibieron quimioterapia fue de 9,3 meses (IC95% = 4 – 15%), a diferencia de en quienes sí recibieron quimioterapia, que fue de 40,1 meses (IC95% = 33,2 – 47%). El tiempo de supervivencia global fue de 31,7 meses (IC95% = 25,6 – 37,8%).
Los pacientes que recibieron quimioterapia posoperatoria presentaron una mayor tasa de supervivencia que aquellos que no la recibieron, observándose una probabilidad de supervivencia del 40% a los 66 meses de seguimiento, mientras que la probabilidad de supervivencia en pacientes que no hicieron tratamiento con quimioterapia fue del 23%, resultando estadísticamente significativo (p = 0,000) (Figura 1).
Figura 1. Supervivencia en meses de los pacientes con diagnóstico de adenocarcinoma ductal de páncreas según recibieron o no quimioterapia (A), presencia de complicaciones posoperatorias (B) y según recidiva o no de la enfermedad (C) (N=122)
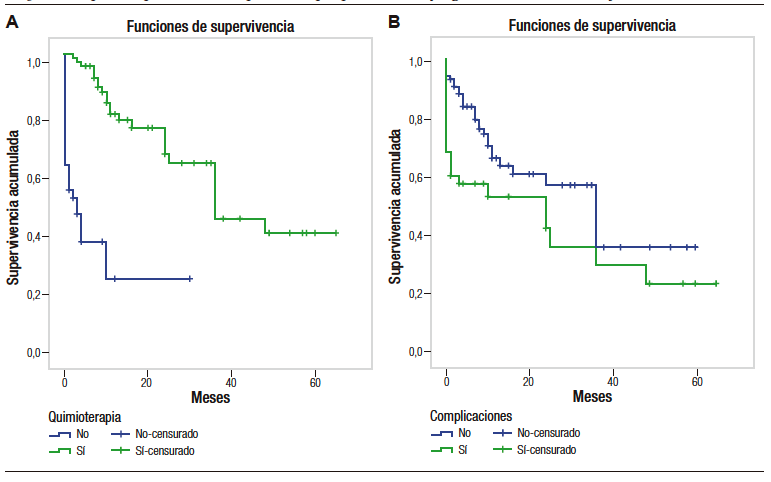
(Continuación) Figura 1. (C) (N=122)
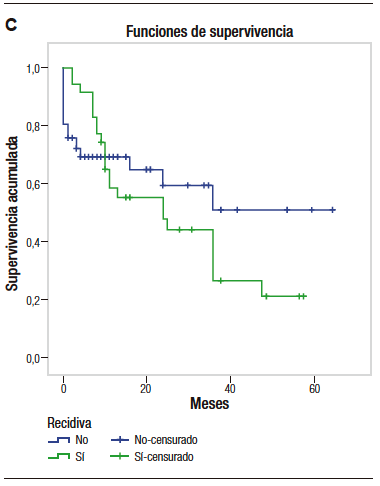
El tiempo promedio de supervivencia en aquellos pacientes que no presentaron complicaciones fue de 32,9 meses (IC95% = 26 – 40%), mientras que los pacientes que sí presentaron complicaciones tuvieron una supervivencia de 25,7 meses (IC95% = 16 – 35,5%). La probabilidad de supervivencia en pacientes que no presentaron complicaciones fue del 38%, siendo mayor que en aquellos que sí presentaron complicaciones, 22% (p = 0,031).
La supervivencia en aquellos pacientes que no presentaron recidiva de la enfermedad fue de 38,5 meses (IC95% = 30 – 47,1%), mientras que en los que sí tuvieron recidiva fue de 27,5 meses (IC95% = 20,3 – 34,6%). En aquellos pacientes sin recidiva de la enfermedad, la probabilidad de supervivencia a los 66 meses fue del 47%, mientras que en los pacientes con recidiva fue del 21% (p = 0,490).
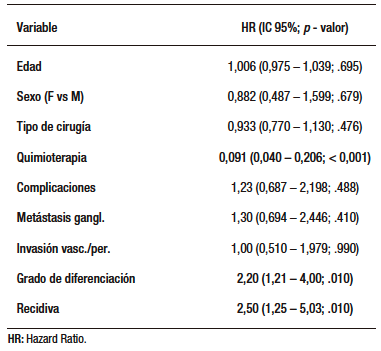
En el análisis multivariado, la quimioterapia fue el factor más protector. El HR de 0,09 indica una reducción de aproximadamente 91% en el riesgo de fallecer, ajustando por las demás variables. Recidiva de enfermedad y grado de diferenciación tumoral se asociaron con un mayor riesgo de muerte. Los factores como edad, sexo, tipo de cirugía, metástasis ganglionares, invasión vascular y complicaciones posoperatorias no mostraron significación estadística en este modelo multivariado, aunque podrían ser clínicamente relevantes en otros contextos (Tabla 2).
Tabla 2. Análisis multivariado del tiempo hasta el evento (regresión de COX), considerando el fallecimiento como el evento, y el período desde la cirugía oncológica como el tiempo
Discusión
El PDAC es una enfermedad en ascenso, responsable de más de 460.000 muertes anuales a nivel mundial. Históricamente, su tratamiento quirúrgico se ha asociado a una elevada morbimortalidad; sin embargo, los avances en la técnica quirúrgica, el manejo anestésico y el soporte posoperatorio han permitido mejorar significativamente estos resultados. La duodenopancreatectomía cefálica, tanto por vía abierta como mínimamente invasiva, presenta hoy en día una morbilidad aceptada cercana al 30% y una mortalidad posoperatoria a noventa días que oscila entre el 2% y el 6%.17 La mortalidad global de resecciones pancreáticas en nuestra serie fue del 4,46%.
No obstante, más allá de los progresos técnicos, el principal determinante de la supervivencia en pacientes con PDAC es el tratamiento oncológico sistémico. En nuestra serie, se evidenció una diferencia estadísticamente significativa en la supervivencia global entre los pacientes que recibieron quimioterapia y aquellos que no lo hicieron (40,1 meses vs. 9,3 meses). Este hallazgo coincide con múltiples publicaciones internacionales que destacan la importancia de la quimioterapia adyuvante como pilar terapéutico junto con la resección quirúrgica.15,18-21
Ahora bien, llama la atención que solo el 62,3% de los pacientes incluidos en nuestra cohorte hayan recibido quimioterapia posoperatoria. Esta proporción, aunque comparable a otras series locales, revela desafíos estructurales y clínicos. En nuestro análisis identificamos al menos cuatro causas principales que explican esta brecha terapéutica:
1- Complicaciones posoperatorias que dificultaron o impidieron el inicio oportuno del tratamiento adyuvante.
2- Edad avanzada y comorbilidades, que limitaron el acceso a esquemas convencionales, quedando algunos pacientes con gemcitabine monodroga o monoterapia oral (capecitabina).
3- Barreras en el sistema público de salud, con demoras administrativas, falta de disponibilidad de drogas o ausencia de interconsultas oncológicas.
4- Otras causas, como decisiones del paciente o del oncólogo tratante, en algunos casos sin indicación de quimioterapia aun con márgenes y ganglios negativos.
Estas dificultades ponen de relieve la necesidad de fortalecer los circuitos de atención multidisciplinaria, garantizar el acceso oportuno al tratamiento oncológico y considerar la centralización del manejo del cáncer de páncreas en centros de alto volumen.
En línea con estudios previos,22-25 también identificamos como factores pronósticos adversos la presencia de invasión perineural o vascular y la existencia de metástasis ganglionares. La recidiva tumoral, tanto local como sistémica, se asoció a una disminución significativa de la supervivencia, lo cual sugiere un posible comportamiento biológicamente agresivo de ciertas variantes del PDAC, independientemente del tratamiento realizado. Este hallazgo es coherente con los reportes de Daamen y colaboradores, quienes mostraron una tasa de recurrencia del 81% al año en pacientes operados de PDAC.26
En nuestro análisis multivariado, la quimioterapia posoperatoria resultó el factor más protector (HR 0,09; IC 95%: 0,040 – 0,206), mientras que la recidiva y el grado de diferenciación tumoral se asociaron a mayor riesgo de muerte. Estos datos refuerzan el valor de la quimioterapia como estrategia adyuvante y sugieren que la agresividad tumoral podría estar determinada por características biológicas aún no completamente caracterizadas.
En este sentido, el PDAC representa un desafío biológico por su alta heterogeneidad histológica, genética y microambiental. Variaciones en la celularidad tumoral, la densidad del estroma, la presencia de mutaciones específicas y la desregulación del microambiente inmunológico influyen en la respuesta al tratamiento. Actualmente, los esquemas quimioterápicos se aplican de manera uniforme, pero probablemente el futuro resida en el desarrollo de tratamientos personalizados, basados en perfiles moleculares y biomarcadores predictores de respuesta.
La implementación de terapias dirigidas, inmunoterapia o enfoques combinados adaptados al perfil individual del tumor podría revolucionar el tratamiento del PDAC en los próximos años. Mientras tanto, la indicación sistemática de quimioterapia adyuvante en pacientes operados, siempre que el estado clínico lo permita, sigue siendo una estrategia imprescindible.
Finalmente, es importante mencionar que nueve de los 195 pacientes inicialmente operados por PDAC en nuestra serie fueron derivados con cirugías paliativas previas, pese a ser técnicamente resecables. Este hallazgo resalta una brecha en la evaluación preoperatoria inicial y refuerza la necesidad de una centralización diagnóstica y terapéutica para garantizar una correcta estadificación, planificación quirúrgica y decisión terapéutica.
Este estudio presenta algunas limitaciones inherentes a su diseño. Se trata de un estudio retrospectivo, lo cual puede generar sesgos de selección e información. No se incluyeron variables moleculares o genéticas que pudieran aportar mayor comprensión sobre la biología tumoral. Hubo pérdida de seguimiento en una proporción de pacientes inicialmente incluidos. La heterogeneidad en el tratamiento quimioterápico (esquemas, tiempo de inicio, acceso) puede haber influido en los resultados. A pesar de estas limitaciones, consideramos que el presente trabajo aporta evidencia relevante sobre el comportamiento clínico del PDAC en nuestra población, reflejando una realidad muchas veces subrepresentada en la literatura internacional.
Conclusión
La quimioterapia adyuvante mejora significativamente la supervivencia en pacientes operados por PDAC. Los factores biológicos como la diferenciación tumoral y la recidiva impactan en el pronóstico, lo que justifica avanzar hacia un tratamiento más personalizado. Nuestros resultados, con un seguimiento a 66 meses, superan en supervivencia a series previas. Es necesario profundizar en estudios multicéntricos y prospectivos que permitan consolidar estrategias terapéuticas y reducir las inequidades en el acceso al tratamiento.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos, las figuras y las tablas presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Gamboa Miño S, Kohan G, Vergara Sandoval R y col. Factores pronósticos y supervivencia en pacientes operados de adenocarcinoma ductal de páncreas: análisis retrospectivo multicéntrico. Acta Gastroenterol Latinoam. 2025;55(2):114-123. https://doi.org/10.52787/agl.v55i2.482
Referencias
- Siegel RL, Miller KD, Wagle NS, Jemal A. Cancer statistics, 2023. CA Cancer J Clin. 2023;73(1):17-48.
- Rahib L, Smith BD, Aizenberg R, Rosenzweig AB, Fleshman JM, Matrisian LM. Projecting cancer incidence and deaths to 2030: the unexpected burden of thyroid, liver, and pancreas cancers in the United States. Cancer Res. 2014;74(11):2913-21.
- Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424.
- Rahib L, Wehner MR, Matrisian LM, Nead KT. Estimated projection of US cancer incidence and death to 2040. JAMA Netw Open. 2021;4(4):e214708.
- Yeo TP. Demographics, epidemiology, and inheritance of pancreatic ductal adenocarcinoma. Semin Oncol. 2015;42(1):8-18.
- Isaji S, Mizuno S, Windsor J, Bassi C, Del Castillo C, Hackert T, et al. International consensus on definition and criteria of borderline resectable pancreatic ductal adenocarcinoma 2017. Pancreatology. 2018;18(1):2-11.
- Van Dam J, Janssen Q, Besselink M, Homs M, Hjalmar C, Van Santvoort D, et al. Neoadjuvant therapy or upfront surgery for resectable and borderline resectable pancreatic cancer: A meta-analysis of randomized controlled trials. Eur J Cancer. 2022;160:140-9.
- O’Reilly D, Fou L, Hasler E, Hawkins J, O’Connell S, Pelone F, et al. Diagnosis and management of pancreatic cancer in adults: a summary of guidelines from the UK National Institute for Health and Care Excellence. Pancreatology. 2018;18(8):962-70.
- Boggi U, Kauffmann EF, Napoli N, et al. REDISCOVER guidelines for borderline-resectable and locally advanced pancreatic cancer: management algorithm, unanswered questions, and future perspectives. Updates Surg. 2024;76(1):1-15.
- Neoptolemos JP, Kleeff J, Michl P, Costello E, Greenhalf W, Palmer DH. Therapeutic developments in pancreatic cancer: Current and future perspectives. Nat Rev Gastroenterol Hepatol. 2018;15(6):333-48.
- Von Hoff DD, Ervin T, Arena FP, Chiorean EG, Infante J, Moore M, et al. Increased survival in pancreatic cancer with nab-Paclitaxel plus Gemcitabine. N Engl J Med. 2013;369
(18):1691-703. - Burris HA, Moore MJ, Andersen J, Green MR, Rothenberg ML, Modiano MR, et al. Improvements in survival and clinical benefit with gemcitabine as first-line therapy for patients with advanced pancreas cancer: A randomized trial. J Clin Oncol. 1997;15(6):2403-13.
- Oettle H, Post S, Neuhaus P, Gellert K, Langrehr J, Ridwelski K, et al. Adjuvant chemotherapy with gemcitabine vs. observation in patients undergoing curative-intent resection of pancreatic cancer: A randomized controlled trial. JAMA. 2007;297(3):267-77.
- Conroy T, Desseigne F, Ychou M, Bouché O, Guimbaud R, Bécouarn Y, et al. FOLFIRINOX versus Gemcitabine for metastatic pancreatic cancer. N Engl J Med. 2011;364(19):1817-25.
- Conroy T, Hammel P, Hebbar M, Ben Abdelghani M, Wei AC, Raoul JL, et al. FOLFIRINOX or Gemcitabine as adjuvant therapy for pancreatic cancer. N Engl J Med. 2018;379(25):2395-406.
- Pratt WB, Maithel SK, Vanounou T, Huang ZS, Callery MP, Vollmer CM. Clinical and economic validation of the international study group of pancreatic fistula (ISGPF) classification scheme. Ann Surg. 2007;245(3):443-51.
- Murimwa G, Karalis J, Meier J, et al. Factors associated with failure to operate and its impact on survival in early-stage pancreatic cancer. J Surg Oncol. 2023;128(4):540-8.
- Loss M, Konin A, Von Winkler N, et al. Completion pancreatectomy after pancreatoduodenectomy. Ann Surg. 2023;279(1):e87-93.
- Strobel O, Neoptolemos J, Jager D, Buchler M. Optimizing the outcomes of pancreatic cancer surgery. Nat Rev Clin Oncol. 2019;16(1):11-26.
- Okosaka T, Furuse J. Recent advances in chemotherapy for pancreatic cancer: evidence from Japan and recommendations in guidelines. J Gastroenterol. 2020;55(4):369-82.
- Javed A, Mahmud O, Fatimi A, et al. Predictors for long-term survival after resection of pancreatic ductal adenocarcinoma: a systematic review and meta-analysis. Ann Surg Oncol. 2024;31(2):123-34.
- Principe DR, Underwood PW, Korc M, Trevino JG, Munshi HG, Rana A. The current treatment paradigm for pancreatic ductal adenocarcinoma and barriers to therapeutic efficacy. Front Oncol. 2021;11:688377.
- Mahmud O, Javed A, Fatimi A, Habib A, Grewal M, He J, et al. ASO Author Reflections: The role of established prognostic factors in long term survival after resection of pancreatic ductal adenocarcinoma. Ann Surg Oncol. 2024;31(2):e101-3.
- Ferrone CR, Pieretti-Vanmarcke R, Bloom JP, Zheng H, Szymonifka J, Wargo JA, et al. Pancreatic ductal adenocarcinoma: Long-term survival does not equal cure. Surgery. 2012;152
(3 Suppl 1):S43-9. - Sancio JB, Campanati R, Do Prado Lima L, Rubiao F, De Freitas J, Correa de Melo F, et al. Preoperative prognostic factors in patients with ductal adenocarcinoma of the head of the pancreas. Rev Col Bras Cir. 2020;47:e20202513.
- Daamen L, Groot VP, Besselink MG, et al. Detection, treatment, and survival of pancreatic cancer recurrence in the Netherlands: A nationwide analysis. Ann Surg. 2022;275(5):769-75.
Correspondencia: Sofía Gamboa Miño
Correo electrónico: sofiagamboam@hotmail.com
Acta Gastroenterol Latinoam 2025;55(2):114-123
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE