Leandro Barbagelata ID
Hospital Italiano de Buenos Aires, Servicio de Cardiología.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2022;52(4):418-423
Recibido: 14/10/2022 / Aceptado: 08/12/2022 / Publicado online el 21/12/2022 / https://doi.org/10.52787/agl.v52i4.262
Resumen
La enfermedad arterial coronaria suele manifestarse con características típicas, producto de la oclusión parcial o total de la circulación en las arterias epicárdicas. Sin embargo, en un grupo específico de pacientes puede presentarse con síntomas no habituales. Es por esto que, al evaluar a un paciente con dolor torácico, es fundamental realizar una anamnesis exhaustiva para detallar las características de la presentación clínica así como una completa evaluación de los factores de riesgo y de los antecedentes cardiovasculares previos. De esta manera podrá evaluarse el pretest y la probabilidad clínica del paciente de presentar enfermedad arterial coronaria. Así mismo, con la ayuda de estudios complementarios, se llevará a cabo una evaluación que permita guiar futuras conductas diagnósticas y/o terapéuticas de acuerdo con el caso específico.
Palabras claves. Dolor torácico, enfermedad coronaria, síndrome coronario crónico.
Coronary Artery Disease and Chronic Chest Pain: Current Approach According to the Latest Guidelines
Summary
Coronary artery disease usually manifests with typical characteristics, resulting from partial or total occlusion of circulation in the epicardial arteries. However in a specific group of patients, may present with unusual symptoms. For this reason, when evaluating a patient with chest pain, it is essential to carry out an exhaustive anamnesis to detail the characteristics of the clinical presentation as well as a complete evaluation of risk factors and previous cardiovascular history. In this way, it will be possible to evaluate the pre-test and the clinical probability of the patient of developing coronary artery disease. In addition, with the help of complementary studies, an evaluation can be carried out to guide future diagnostic and/or therapeutic behaviors according to the specific case.
Keywords. Chest pain, coronary artery disease, chronic coronary syndrome.
Abreviaturas
EAC: Enfermedad arterial coronaria.
SCA: Síndrome coronario agudo.
SCC: Síndrome coronario crónico.
ECG: Electrocardiograma.
ETT: Ecocardiograma transtorácico.
CCG: Cinecoronariografía.
ATCC: Angiografía por tomografía computada coronaria.
FFR: Sigla en inglés de reserva fraccional de flujo.
Introducción
La enfermedad arterial coronaria (EAC) es un proceso patológico caracterizado por la acumulación de placa aterosclerótica en las arterias epicárdicas, que puede ocasionar una obstrucción parcial o total del flujo sanguíneo. Este proceso puede ser modificado realizando cambios en el estilo de vida, mediante fármacos y/o tratamientos invasivos, con el objetivo de estabilizar y, si es posible, producir una regresión de la enfermedad. Dicha patología puede presentar períodos largos y estables, pero también puede desestabilizarse de forma repentina, lo que sucede en la mayor parte de los casos a raíz de un evento aterotrombótico agudo causado por la erosión o ruptura de una placa vulnerable. Sin embargo, la EAC es un proceso crónico y progresivo que puede presentar períodos asintomáticos. Asimismo, la naturaleza dinámica de esta enfermedad genera distintas formas de presentación clínica, que pueden agruparse y ser categorizadas como síndromes coronarios agudos (SCA) o crónicos (SCC); en estos últimos, el escenario clínico más frecuente es el del paciente con síntomas anginosos estables y/o disnea.1
Abordaje del paciente con dolor torácico crónico y sospecha de EAC
El enfoque del manejo diagnóstico incluye cuatro pasos:
1. Caracterización de signos y síntomas
Es fundamental conocer las características del dolor torácico directamente de parte del paciente para una interpretación óptima. La historia clínica y el interrogatorio son las bases más importantes para considerar la presencia o ausencia de isquemia miocárdica, pero el origen de los síntomas cardíacos es complejo y su expresión es variable.
En cuanto a la presentación clínica, la angina de pecho crónica suele ser percibida como una molestia torácica retroesternal opresiva, que aumenta gradualmente en intensidad a lo largo de varios minutos y, por lo general, es precipitada por estrés físico o emocional. Los síntomas asociados, como dificultad para respirar, náuseas, presíncope o síncope son más frecuentes en los pacientes con diabetes, las mujeres y los ancianos. Una evaluación detallada de los factores de riesgo cardiovascular, el historial médico, los antecedentes familiares y los sociales deben complementar la evaluación de los síntomas de presentación.2, 3
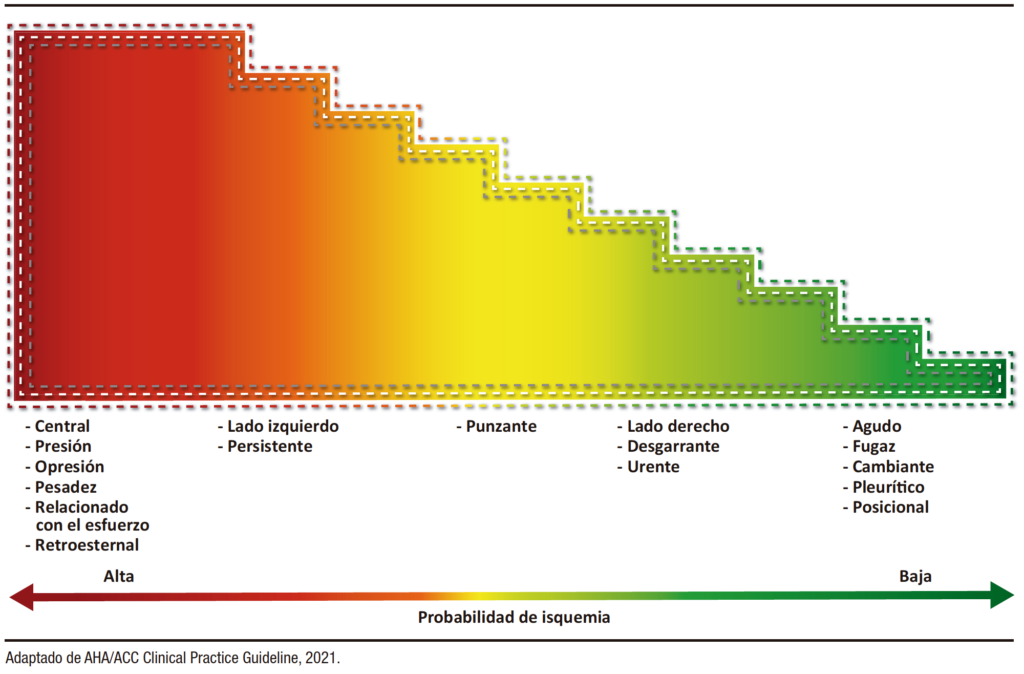
En la Tabla 1 se resumen los principales signos y síntomas que pueden identificarse en la evaluación de pacientes con dolor torácico según la Sociedad Argentina de Cardiología. En la Figura 1 se muestra el índice de sospecha de etiología coronaria en pacientes con dolor torácico.4, 5
Tabla 1. Los principales signos y síntomas en pacientes con dolor torácico
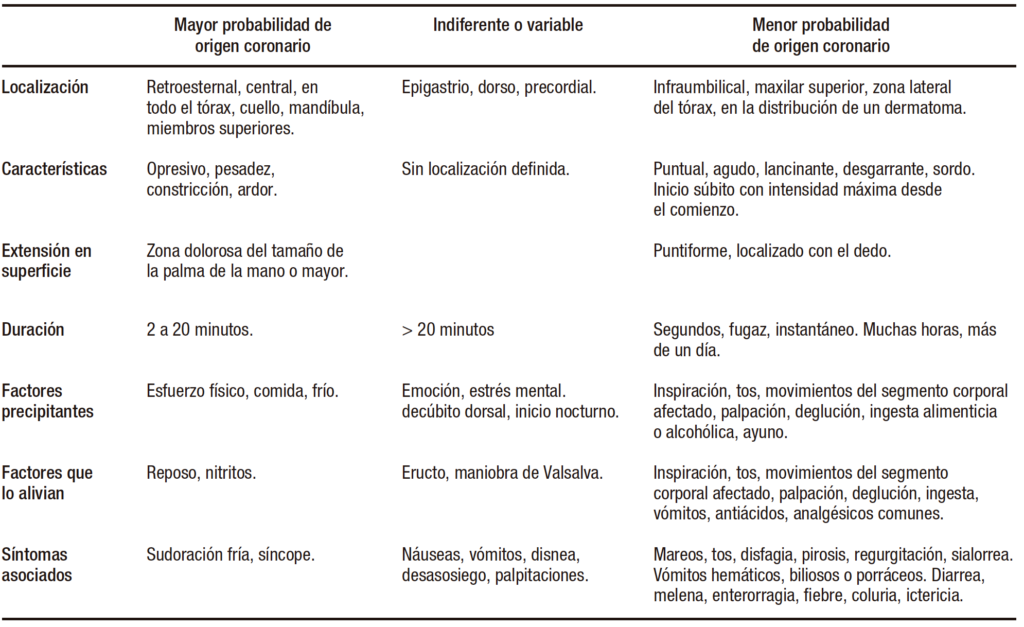
Figura 1. Índice de sospecha de etiología coronaria en pacientes con dolor torácico
2. Determinar las comorbilidades y otras posibles causas de dolor
Antes de considerar cualquier estudio, deben evaluarse el estado general de salud, las comorbilidades y la calidad de vida del paciente. Si es poco probable que la revascularización sea una opción, las pruebas adicionales pueden reducirse al mínimo y debe instituirse el tratamiento adecuado, que puede incluir una prueba con medicación antianginosa, incluso si no se ha confirmado el diagnóstico de EAC. Las imágenes funcionales no invasivas para detectar isquemia pueden ser una opción si es necesario verificar el diagnóstico. Si el dolor es claramente no anginoso, pueden estar indicadas otras pruebas diagnósticas para identificar alteraciones gastrointestinales, pulmonares o musculoesqueléticas que justifiquen el dolor.1
3. Estudios de primera línea
Las pruebas básicas en pacientes con sospecha de EAC y dolor torácico crónico incluyen un electrocardiograma (ECG) y ecocardiograma en reposo. Asimismo, los análisis de laboratorio son útiles para identificar factores de riesgo cardiovasculares y condiciones asociadas. La glucosa plasmática en ayunas y la hemoglobina glicosilada (HbA1c) deben medirse en todos los pacientes con sospecha de EAC. El conocimiento del metabolismo de la glucosa es importante debido a la asociación bien conocida entre la diabetes y los resultados cardiovasculares adversos, por lo cual esta población debe ser evaluada y tratada de acuerdo con guías específicas.6, 7 Adicionalmente, debe valorarse el perfil de lípidos en cualquier paciente con sospecha de EAC, para establecer el riesgo del paciente y determinar la necesidad de tratamiento.8 Otros parámetros que es imperativo evaluar son la tasa de filtrado glomerular, la urea y la creatinina, ya que es sabido que la enfermedad renal crónica aumenta la probabilidad de presentar EAC y repercute de forma negativa en su pronóstico.9
El ecocardiograma transtorácico (ETT) proporciona información valiosa sobre la anatomía y la función cardíacas, las cuales suelen estar preservadas en los SCC. Valores de fracción de eyección disminuida y/o alteraciones regionales de la contracción pueden aumentar la sospecha de daño miocárdico isquémico. De la misma manera, el ETT permite evaluar causas alternativas de dolor precordial y ayuda al diagnóstico de enfermedades cardíacas como valvulopatías, insuficiencia cardíaca congestiva y la mayoría de las miocardiopatías.10, 11
4. Evaluación pretest y selección apropiada de estudios
En pacientes en los cuales el diagnóstico de EAC es incierto, establecer un diagnóstico por medio de imágenes funcionales no invasivas para la detección de isquemia es razonable.1
En aquellos pacientes en los que la probabilidad clínica de presentar EAC es elevada, que tienen síntomas refractarios al tratamiento médico o que manifiestan dolor torácico atípico a una carga baja de ejercicio, podría realizarse directamente una cinecoronariografía (CCG) invasiva, sin realizar más pruebas diagnósticas. Posteriormente, la indicación de revascularización deberá ser guiada de acuerdo con la magnitud y el compromiso hemodinámico de las lesiones coronarias identificadas.12, 13
En el caso de que la EAC no pueda ser excluida por la presentación clínica, se recomienda realizar estudios no invasivos, a fin de establecer el diagnóstico y valorar el riesgo de eventos. Las guías actuales recomiendan el uso de imágenes funcionales no invasivas para la detección de isquemia (cámara gamma / ecoestrés) o de imágenes anatómicas como la angiografía por tomografía computada coronaria (ATCC) como prueba inicial para el diagnóstico de EAC en pacientes seleccionados.1
Las pruebas para el diagnóstico de EAC obstructiva están diseñadas para detectar isquemia miocárdica a través de cambios en el ECG, cambios en el movimiento de la pared por resonancia magnética nuclear cardíaca de estrés o ecocardiograma de estrés, o cambios de perfusión por tomografía computarizada por emisión de fotón único (SPECT). Estas se asocian con una alta precisión para la detección de estenosis coronarias significaltivas, en comparación con la prueba invasiva de medición de reserva fraccional de flujo (FFR).14
Como se mencionó anteriormente, la evaluación anatómica no invasiva mediante ATCC proporciona una alta precisión para la detección de estenosis coronarias obstructivas.
Sin embargo, las estenosis estimadas en 50% – 90% por inspección visual no siempre son funcionalmente significativas; es decir, no siempre inducen isquemia miocárdica. Por lo tanto, se recomienda realizar estudios funcionales invasivos o no invasivos para evaluar los hallazgos detectados en pruebas anatómicas, a menos que se detecte una estenosis de muy alto grado (> 90% de diámetro de estenosis) mediante una angiografía invasiva.12, 13 Asimismo, la ATCC es el estudio indicado en pacientes con un riesgo clínico bajo de EAC, sin diagnóstico previo de EAC y características asociadas con una probabilidad alta de buena calidad de imagen. Este método detecta la aterosclerosis coronaria subclínica, pero también puede descartar con precisión una EAC anatómica y funcionalmente significativa.14
En cuanto al ECG de esfuerzo, tiene un rendimiento diagnóstico inferior en comparación con las pruebas de diagnóstico por imágenes previamente mencionadas y un poder limitado para confirmar o descartar EAC obstructiva.13
Finalmente, la CCG es necesaria en pacientes con sospecha de EAC y pruebas no invasivas no concluyentes. Este estudio también puede estar indicado si la evaluación no invasiva sugiere un riesgo alto de eventos para determinadas opciones de revascularización.15 En pacientes con probabilidad clínica alta de EAC y síntomas crónicos que no responden a la terapia médica o con angina típica en un nivel bajo de ejercicio, la CCG temprana sin realizar una estratificación de riesgo no invasiva previa puede ser razonable para identificar lesiones potencialmente susceptibles de revascularización.
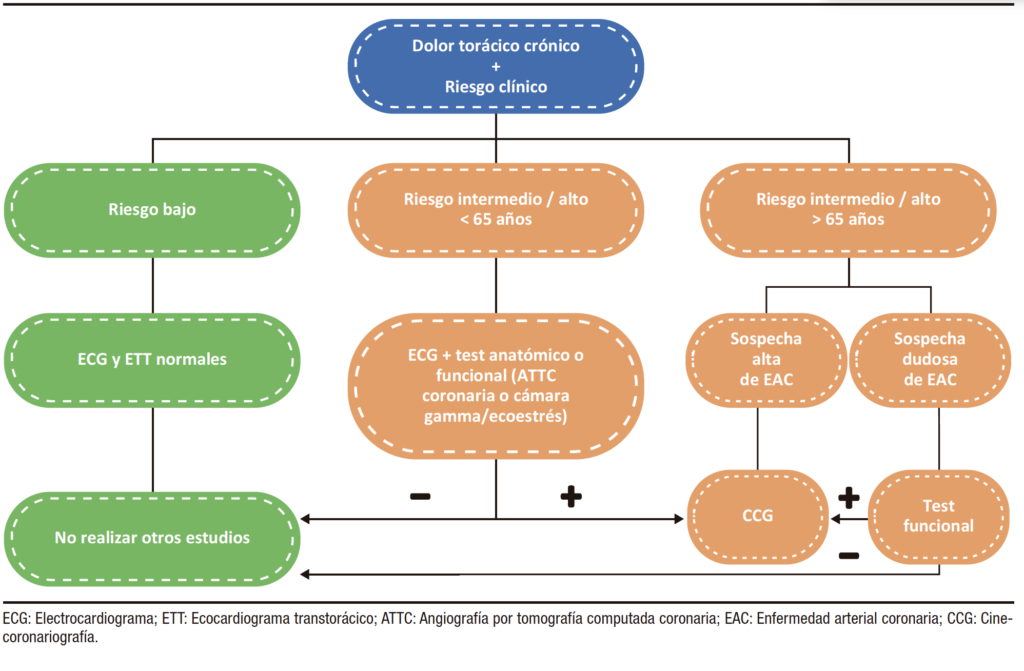
De igual modo, si está disponible, la evaluación funcional invasiva mediante FFR debe complementar la CCG, en especial en pacientes con estenosis coronarias del 50% – 90% o con enfermedades de múltiples vasos, debido a las frecuentes discrepancias entre la severidad angiográfica y hemodinámica de las estenosis coronarias.16-18 En la Figura 2 se resumen los principales métodos diagnósticos sobre la base del riesgo clínico de EAC de pacientes con dolor torácico crónico.
Figura 2. Métodos diagnósticos basados en el riesgo clínico de EAC de pacientes con dolor torácico crónico
Conclusión
La EAC tiene múltiples formas de presentación clínica y cada una de ellas reviste un riesgo particular.
Los pacientes con dolor torácico crónico representan un desafío diagnóstico, dada la amplia gama de posibles patologías (cardiovasculares y no cardiovasculares). Es por este motivo que resulta imprescindible evaluar las características de los síntomas referidos y analizar las comorbilidades y el riesgo pretest para EAC de forma individualizada. A partir de esto, los estudios diagnósticos de primera línea (como el ECG y el ETT) permiten realizar una aproximación diagnóstica, luego de la cual y sobre la base del riesgo clínico, deberá ser evaluado el requerimiento de estudios de mayor complejidad para poder guiar las estrategias terapéuticas correspondientes.
Propiedad intelectual. Los autores declaran que los datos, las figuras y la tabla presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2022 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Barbagelata L. Enfermedad coronaria y dolor torácico crónico: abordaje actual según las últimas guías. Acta Gastroenterol Latinoam. 2022;52(4):418-423. https://doi.org/10.52787/agl.v52i4.262
Referencias
- Knuuti J, Wijns W, Saraste A, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 202014;41(3):407-77. doi: 10.1093/eurheartj/ehz425
- Hsia RY, Hale Z, Tabas JA. A national study of the prevalence of lifethreatening diagnoses in patients with chest pain. JAMA Intern Med. 2016;176:1029-32.
- Fanaroff AC, Rymer JA, Goldstein SA, et al. Does this patient with chest pain have acute coronary syndrome?: the rational clinical examination systematicreview. JAMA. 2015;314:1955-65.
- Duronto E, Navarro Estrada JL, Benger J, et al. Consenso para el Manejo de Pacientes con Dolor Precordial. Rev Argent Cardiol. 2016;84:378-401. http://dx.doi.org/10.7775/rac.es.v84.i4.9074
- Gulati M, Levy PD, Mukherjee D, et al. 2021 AHA/ACC/ASE/CHEST/SAEM/SCCT/SCMR Guideline for the Evaluation and Diagnosis of Chest Pain: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 202130;144(22):e368-e454. doi: 10.1161/CIR.0000000000001029. Epub 2021 28 de octubre.
- 2019 ESC/EASD Guidelines on diabetes, pre-diabetes, and cardiovascular diseases. Eur Hear J. 2019: en prensa.
- Piepoli MF, Hoes AW, Agewall S, et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Eur Heart J. 2016;37:2315-2381.
- Catapano AL, Graham I, De Backer G, et al. 2016 ESC/EAS Guidelines for the management of dyslipidaemias. Eur Heart J. 2016;37:2999-3058.
- Di Angelantonio E, Chowdhury R, Sarwar N, et al. Chronic kidney disease and risk of major cardiovascular disease and nonvascular mortality: prospective population based cohort study. BMJ. 2010;341:c4986.
- Daly C, Norrie J, Murdoch DL, Ford I, Dargie HJ, Fox K; TIBET (Total Ischaemic Burden European Trial) study group. The value of routine non-invasive tests to predict clinical outcome in stable angina. Eur Heart J. 2003;24:532-540.
- Steeds RP, Garbi M, Cardim N, et al. Scientific Documents Committee. EACVI appropriateness criteria for the use of transthoracic echocardiography in adults: a report of literature and current practice review. Eur Heart J Cardiovasc Imaging. 2017;18:1191-1204.
- De Bruyne B, Pijls NH, Kalesan B, et al. FAME 2 Trial Investigators. Fractional flow reserve-guided PCI versus medical therapy in stable coronary disease. N Engl J Med. 2012;367:9911001.
- Tonino PA, De Bruyne B, Pijls NH, et al. FAME Study Investigators. Fractional flow reserve versus angiography for guiding percutaneous coronary intervention. N Engl J Med. 2009;360:213-224.
- Knuuti J, Ballo H, Juarez-Orozco LE, et al. The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J. 2018;39:3322-3330.
- Gueret P, Deux JF, Bonello L, et al. Diagnostic performance of computed tomography coronary angiography (from the prospective national multicenter multivendor EVASCAN study). Am J Cardiol. 2013;111:471-478.
- Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J. 2019;40:87165.
- Toth G, Hamilos M, Pyxaras S, et al. Evolving concepts of angiogram: fractional flow reserve discordances in 4000 coronary stenoses. Eur Heart J. 2014;35:2831-2838.
- Jeremias A, Maehara A, Genereux P, et al. Multicenter core laboratory comparison of the instantaneous wave-free ratio and resting Pd/Pa with fractional flow reserve: the RESOLVE study. J Am Coll Cardiol. 2014;63:1253-1261.
Correspondencia: Leandro Barbagelata
Correo electrónico: leandro.barbagelata@hiba.org.ar
Acta Gastroenterol Latinoam 2022;52(4):418-423
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE