Esteban H Campitelli,1, 2 María del V Sivanto2, 3
1Servicio de Gastroenterología del Hospital Aeronáutico Central.
2Centro Privado de Cirugía y Coloproctología.
3Instituto Argentino del Diagnóstico.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2018;48(4):296-301
Recibido: 18/02/2018 / Aprobado: 18/06/2018 / Publicado en www.actagastro.org el 17/12/2018
Resumen
El uso de opioides para el tratamiento del dolor crónico se ha incrementado. Uno de los efectos adversos más frecuentes es el estreñimiento crónico (EC). Algunos procinéticos pueden ser efectivos para su tratamiento. Objetivo. Evaluar la eficacia y la seguridad del prucalopride comparado con la combinación de lactulosa/bisacodilo en pacientes con EC inducido por opiodes. Material y métodos. Estudio prospectivo aleatorizado. Se incluyeron 50 pacientes en el grupo prucalopride y 50 en el grupo lactulosa/bisacodilo, tratados por cuatro semanas. Fueron evaluados con la escala visual de Bristol (EB) y con una encuesta de calidad de vida. Resultados. El grupo de prucalopride demostró ser seguro y eficaz, con diferencia estadísticamente significativa en el tratamiento del EC inducido por opioides, comparado con el grupo lactulosa/ bisacodilo (X2 = 4,058 y p < 0,05); no hubo diferencias significativas en la respuesta por edad y sexo en ambos grupos. Ningún paciente abandonó el tratamiento por efectos adversos. Conclusiones. Los resultados demostrarían que el prucalopride es seguro y eficaz en el tratamiento del EC secundario a opioides.
Palabras claves. Prucalopride, bisacodilo, opioides, estreñimiento crónico, agonista 5HT4.
Effectiveness of prucalopride in the chronic constipation induced by the use of opioids in an ambulatory population
Summary
The use of opioids for the treatment of chronic pain has increased. One of the most frequent adverse effects is chronic constipation (CC). Some prokinetics can be effective for its treatment. Objective. To evaluate the efficacy and safety of prucalopride compared to the combination of lactulose / bisacodyl in patients with CC induced by opioids. Material and methods. Prospective randomized study. Fifty patients were included in the prucalopride group and 50 in the lactulose / bisacodyl group treated for four weeks. They were evaluated with the Bristol visual scale (EB) and with a quality of life survey. Results. Prucalopride group proved to be safe and effective. It presented a statistically significant difference in the treatment of opioid-induced CC, compared with the lactulose / bisacodyl group. (X2 = 4.058 and p < 0.05); there were no significant differences in the response by age and sex in both groups. No patient abandoned the treatment due to adverse effects. Conclusions. The results would show that prucalopride is safe and effective in the treatment of CD secondary to opioids.
Key words. Prucalopride, bisacotyl, cronic constipation, 5HT4 agonist.
El uso de opioides en el tratamiento del dolor crónico se ha incrementado en los últimos años. El estreñimiento crónico (EC) es el efecto adverso más común y persistente.1 La estimulación de los receptores opioides μ determina el enlentecimiento de los movimientos colónicos y la disminución de las secreciones que conllevan a dicho estado.2, 3 El tratamiento habitual del estreñimiento, basado en las medidas higiénico dietéticas, el incremento de fibras y la actividad física resultan insuficientes para revertir el cuadro ocasionado por los opioides, razón por la cual se utilizan drogas laxantes, con errática respuesta.3 Drogas de uso frecuente como la lactulosa, el bisacodilo y el picosulfato de sodio son utilizadas por autoprescripción con pobres resultados. Ensayos controlados con lubiprostone, prucalopride, naloxegol han sido publicados para tal fin.4-6 Una serie de drogas que se focalizan en el PAMORA (peripherally acting μ-opioid receptor antagonist) están siendo evaluadas en la actualidad para revertir el estreñimiento en los pacientes tratados con opioides. Si bien el naloxegol ha sido de las primeras, hoy se evalúan el axelopran, avimopan y el nadelmedine, entre otros.7-14
El prucalopride es un procinético agonista altamente selectivo de los receptores 5HT4 con probado efecto en el tratamiento del EC, incluido el inducido por los opioides. La acción sobre los receptores 5HT4 desencadena movimientos propulsivos, de mezcla y liberación de agua a la luz del tubo digestivo, que no se ven influenciados por la acción de los analgésicos opioides, siendo la acción más efectiva cuanto mayor sea la densidad de receptores a nivel colónico. Si bien no ha sido aprobado para su uso por la FDA para este fin, los ensayos realizados en Europa lo muestran como efectivo.7 Por su mecanismo de acción, las drogas que actúan sobre el receptor μ no influyen significativamente en su respuesta, y su acción no condiciona el efecto opioide analgésico. Sin embargo, muchos de los antagonistas μ si lo hacen.15
Objetivo
Primario: evaluar la eficacia del prucalopride en comparación con la combinación de lactulosa/bisacodilo en el EC inducido por opioides. Secundario: evaluar la seguridad y tolerancia.
Material y métodos
Se realizó un estudio prospectivo, de intervención, aleatorizado, de comparación a muestras independientes y longitudinal, que comparó dos grupos durante un mes a dosis habituales de prucalopride 2 mg y bisacodilo 5 mg + lactulosa 15 ml. El protocolo fue aprobado por un Comité de Ética Independiente y los pacientes incluidos firmaron el consentimiento informado para participar del estudio. Los pacientes, junto con las medidas higiénico dietéticas, recibieron un tratamiento que no se alejó de las dosis publicadas en la bibliografía, razón por la cual el ensayo se consideró como clínico de fase IV (prucalopride 2 mg/día y bisacodilo 5 mg/lactulosa 15 ml/día). Se reclutaron pacientes durante siete meses, entre mayo y noviembre de 2017.
Criterios de inclusión
- Pacientes de ambos sexos, de 18 a 70 años.
- Dolor de origen no oncológico.
- Pacientes tratados con opioides por más de tres semanas, que hayan desarrollado estreñimiento definido claramente por la escala visual de Bristol.
- No ser estreñido previamente según criterio de Roma III.
- Firma del consentimiento informado.
Criterios de exclusión
- Pacientes polimedicados que pudiesen dificultar la evaluación de los resultados transcurridas las cuatro semanas.
- Sospecha de obstrucción mecánica del colon.
- Diabetes, anemia sintomática e insuficiencia cardíaca descompensada.
Criterios de eliminación
Cualquier desviación significativa del protocolo, en particular el no cumplimiento de los controles asignados o la aparición de criterios de exclusión no demostrados inicialmente.
Se incluyeron 50 pacientes en el grupo prucalopride (grupo I) y 50 en el grupo lactulosa/bisacodilo (grupo II). Se necesitaron 105 pacientes para obtener la población a estudiar, ya que tres del grupo II y dos del grupo I no quisieron ser parte del protocolo.
El primer paciente fue incluido en el grupo I, y si por negativa o razón oncológica del dolor no pudo ser incluido, el paciente inmediato posterior fue incluido en el grupo que no pudo ser ocupado, para no alterar la distribución en la elección de los pacientes según el grupo asignado. Las medidas higiénico-dietéticas se complementaron con un comprimido de 2 mg/día en el grupo I, y 30 ml de lactulosa más un comprimido de 5 mg de bisacodilo en el grupo II. Todos los pacientes recibieron siempre la dosis sugerida. El grupo I no utilizó dosis de 4 mg porque las diferencias terapéuticas no son significativas con el uso de 2 mg, y los efectos adversos aumentan considerablemente.10 Se evaluó a los pacientes semanalmente para observar la tolerancia y el cumplimiento del protocolo, pero el análisis estadístico de los resultados solo se realizó una vez finalizadas las cuatro semanas. Se empleó la escala de Bristol en la inclusión y los controles programados. Cabe destacar que los pacientes incluidos presentaron signos de estreñimiento como consecuencia del tratamiento con opioides. Se les pidió que se autoevaluaran en la escala, la que determinó su inclusión y fue la que refirieron al terminar las cuatro semanas.
La escala visual de Bristol es una herramienta de fácil comprensión para pacientes y médicos (Figura 1).14 La tolerancia al tratamiento y los efectos adversos fueron evaluados semanalmente. En los controles en los que los pacientes referían mucho malestar por falta de respuesta y perpetuación del EC, se realizó rescate con bisacodilo 5 mg según los protocolos publicados sobre el tema.16 Se consideró como buena adherencia al tratamiento haber tomado más del 60% de las dosis indicadas, habiendo sido evaluada a la semana tres, ya que la medicación provista debía traerse a cada consulta de control. En la semana tres se asentó el conteo de medicación, habiéndose elegido dicha semana por protocolo, y por haber superado el 50% del mismo. Todos los pacientes superaron dicho porcentual, en más del 80%.17
Figura 1. Escala visual de Bristol: evaluación de las características defecatorias.
Análisis estadístico
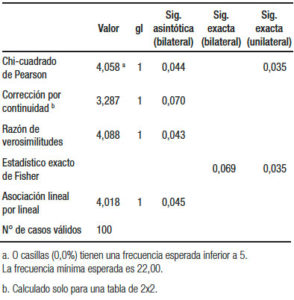
Los datos fueron analizados estadísticamente con el software SPSS 22.0, versión en español. Se consideró una p < 0,05 como estadísticamente significativa y el intervalo de confianza del 95% para las evaluaciones de regresión logística. Para la comparación de grupos se utilizaron Chi2 de Pearson, razón de verosimilitudes y el test exacto de Fisher. Para corroborar estos resultados se realizó una regresión logística utilizando el sexo como covariable.
Resultados
Los pacientes fueron ingresados, previa firma del consentimiento informado, entre mayo y noviembre de 2017. El protocolo fue aprobado por un Comité de Ética Independiente.
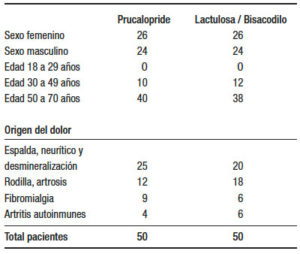
La distribución de la población y el origen de la indicación de los opioides se muestran en la Tabla 1. Más del 60% de los dolores dorsales eran de tipo neurítico por compresión, y los restantes por algún grado de colapso vertebral vinculado a razones postraumáticas o por disminución de la densidad mineral ósea. Los dolores de rodilla eran por artrosis.
Las drogas opioides más prevalentes que recibían para el tratamiento del dolor, sumadas a AINES y paraceta mol, fueron codeína 30 a 60 mg c/ 6 horas; tramadol 25 o 50 mg c/ 8 horas y oxicodona 10 mg c/ 12 horas.
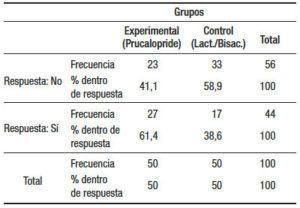
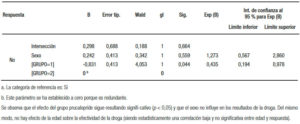
Todos los pacientes que fueron reclutados terminaron el estudio. La muestra estuvo conformada por 100 pacientes (47 hombres) con una edad mediana de 58 años (rango: 32-70); estos fueron asignados aleatoriamente a dos grupos: grupo I (n = 50 con prucalopride 2 mg/día) y grupo II (n = 50 con lactulosa 30 ml y bisacodilo 5 mg/ día); 3 y 11 sujetos de cada grupo, respectivamente requirieron un rescate con 5 mg de bisacodilo. Las respuestas a las drogas fueron evaluadas en forma posterior al rescate con bisacodilo en los casos en que este fue indicado. No se encontraron diferencias estadísticamente significativas (p > 0,05) en edad o sexo entre ambos grupos. Los pacientes incluidos en este protocolo fueron evaluados con la escala visual de Bristol para su inclusión, habiéndose observado un cambio significativo de la característica de sus heces. Todos los pacientes incluidos refirieron corresponder a los tipos 3, 4 y 5 previo a la ingesta de opioides, y haber cambiado el aspecto de sus heces al tipo 1 y 2. Se consideró positiva la respuesta de los pacientes que refirieron retornar al tipo 3 o superior. Cuanto mayor fue el tipo en la escala, mayor la distensión y el dolor abdominal, aunque la respuesta se haya considerado positiva (evaluar los distintos tipos en la Figura 1). El 61,4% de los pacientes tratados con prucalopride mostraron una respuesta positiva, mientras que en el grupo II la repuesta fue positiva en el 41,1%; diferencias estadísticamente significativas (X2 = 4,058 y p < 0,05). Por lo tanto, puede afirmarse que el prucalopride resulta más efectivo que los laxantes habituales para disminuir el estreñimiento en pacientes que consumen opiáceos por dolor crónico (Tablas 2 y 3). Estos resultados se ven reforzados por el hecho de que con los laxantes habituales un 22% requirió un rescate que tampoco resultó efectivo, y solo fue necesario en un 2% en el grupo prucalopride. Para corroborar y fortalecer estos resultados se realizó un test de regresión logística utilizando el sexo como covariable. Se observa que el efecto del grupo sigue resultando significativo (p < 0,05) y que el sexo no influye en los resultados producidos por efecto de la droga. Del mismo modo, no hay efecto de la edad sobre la efectividad del prucalopride (correlación baja y no significativa entre edad y respuesta) (Tabla 4).
Los efectos adversos fueron leves y no impidieron la continuación del protocolo, menos del 5% del grupo I refirió cefalea leve entre la primera y la tercera toma de prucalopride y cólicos predefecatorios cuando al comenzar el tratamiento. En el grupo II la distensión y los cólicos predominaron independientemente de los resultados obtenidos, en más de un 7%.
El prucalopride ha resultado más efectivo que los laxantes habituales en los pacientes que utilizan opiáceos para aliviar el EC inducido por opioides, sin existir diferencias de efectividad según edad o sexo. Del mismo modo, dadas las características del tipo de deposiciones, han generado menos distensión y dolor en el grupo prucalopride.
Tabla 1. Demografía y origen del dolor.
Tabla 2. Resultados de la prueba de Chi2 de la respuesta a la droga, según el grupo; p < 0,05 estadísticamente significativa para el grupo prucalopride.
Tabla 3. Pruebas del test de Pearson para dos grupos.
Tabla 4. Estimaciones de los parámetros del Grupo I prucal y el grupo II lact/bisac.
Discusión
Este es el primer estudio comparativo de la eficacia entre el prucalopride y los laxantes habituales (lactulosa y bisacodilo) en el tratamiento del EC producido por el uso de opiáceos para el tratamiento del dolor crónico de origen no oncológico realizado en la Argentina. El prucalopride es un agonista altamente selectivo de los receptores 5 HT 4 de la serotonina. La serotonina es un neurotransmisor ampliamente involucrado en la regulación de la motilidad, de la sensibilidad visceral y de la secreción intestinal.20 Los opioides, probadamente efectivos en el tratamiento del dolor crónico, al tener un efecto agonista sobre los receptores μ, generan un enlentecimiento de los movimientos y disminución de las secreciones, razón por la cual predisponen al estreñimiento crónico.13 Los agentes utilizados para revertir el efecto sobre el receptor μ, conocidos por su acción como PAMORA (peripherally acting μ-opioid receptor antagonist) tienen efecto para revertir el estreñimiento, pero conforme se eleva la dosis ejercen un efecto antagónico sobre el efecto analgésico del opioide en uso, haciendo necesario elevar las dosis, lo que genera un círculo vicioso.2, 10 Los resultados obtenidos muestran la eficacia del prucalopride respecto de los laxantes comúnmente usados, con una diferencia estadísticamente significativa: 61,4% vs. 41,1% (Chi2 X2 = 4,058 y p < 0,05).
Trabajos publicados sobre el tratamiento del EC vinculado a opiáceos consideran como efectivo un porcentaje mayor al 45% cuando se los comparan con placebo. De las drogas no antagonistas del receptor μ, se han evaluado el lubripostone, el linaclotide y otras están en fase II. Los resultados han sido aceptables solo para el lubiprostone, con valores estadísticos menos alentadores que para el prucalopride.13 Los nuevos procinéticos han dejado de presentar efecto tóxico cardiovascular, probablemente por su alta afinidad a los receptores 5HT4 digestivos. Los efectos adversos más comunes, tolerables y reversibles son la cefalea o el dolor retroocular, epigastralgia, náuseas y dolor intestinal, que suelen desaparecer con la segunda o tercera toma. Los efectos adversos referidos por los pacientes que realizaron este estudio fueron leves y tolerables, destacándose como los más importantes los cólicos como expresión de aceleración del tránsito y la distensión y tendencia a la diarrea en el grupo lactulosa/bisacodilo. Sería deseable la realización de un número mayor de trabajos para confirmar los resultados obtenidos.
Conclusiones
El prucalopride ha resultado ser seguro, eficaz y superior a los laxantes habituales en dosis de 2 mg/día durante un mes en el manejo del EC, uno de los efectos adversos más frecuentes producidos por el uso de opioides. Dicho efecto terapéutico no se ve influenciado por el sexo y la edad. Los efectos adversos han sido leves e infrecuentes, lo que motivó una alta adherencia al tratamiento.
Conflicto de intereses. Los autores declaran que no tienen conflicto de intereses.
Agradecimientos. Los autores agradecen a Nova Argentia S.A. el haber provisto el prucalopride, Prucal ® comprimidos de 2 mg como así también la lactulosa y el bisacodilo.
Referencias
- Bell TJ, Panchal SJ, Miaskowski C, Bolge SC, Milanova T, Williamson R. The prevalence, severity, and impact of opioid-induced bowel dysfunction: results of a US and European Patient Survey (PROBE 1). Pain Med 2009; 10: 35-42.
- Panchal SJ, Muller-Schwefe P, Wurzelmann JI. Opioid-induced bowel dysfunction: prevalence, pathophysiology and burden. Int J Clin Pract 2007; 61: 1181-1187.
- Camilleri M. Opioid-induced constipation: challenges and therapeutic opportunities. Am J Gastroenterol 2011; 106: 835-842.
- Pappagallo M. Incidence, prevalence, and management of opioid bowel dysfunction. Am J Surg 2001; 182: 11S-18S.
- Boudreau D, Von Korff M, Rutter CM, Saunders K, Ray GT, Sullivan MD, Campbell CI, Merrill JO, Silverberg MJ, Banta-Green C, Weisner C. Trends in long-term opioid therapy for chronic non-cancer pain. Pharmacoepidemiol Drug Saf 2009; 18: 1166-1175.
- Webster L, Chey W, Tack J, Lappalainen J, Diva U, Sostek M. Randomised clinical trial: the long-term safety and tolerability of naloxegol in patients with pain and opioid-induced constipation. Aliment Pharmacol Ther 2014; 40: 771-779.
- Sloots C, Rykx A, Cools M, Kerstens R, De Pauw, M. Efficacy and safety of prucalopride in patients with chronic noncancer pain suffering from opioid-induced constipation. Dig Dis Sci 2010; 55: 2912-2921.
- Coremans G, Kerstens R, De Pauw M, Stevens M. Prucalopride is effective in patients with severe chronic constipation in whom laxatives fail to provide adequate relief. Results of a double blind, placebo-controlled clinical trial. Digestion 2003; 67: 82-89.
- Sloots CE, Poen AC, Kerstens R, et al. Effects of prucalopride on colonic transit, anorectal function and bowel habits in patients with chronic constipation. Aliment Pharmacol Ther 2002; 16: 759-767.
- Adler HF, Atkinson AJ, Ivy AC. Effect of morphine and dilaudid on the ileum and of morphine, dilaudid and atropine on the colon of man. Arch Intern Med 1942; 69: 974-985.
- Quigley EM, Vandeplassche L, Kerstens R, Ausma J. Clinical trial: the efficacy, impact on quality of life, and safety and tolerability of prucalopride in severe chronic constipation-a 12-week, randomized, double-blind, placebo-controlled study. Aliment Pharmacol Ther 2009; 29: 315-328.
- Simpson K, Leyendecker P, Hopp M, Müller-Lissner S, Löwenstein O, De Andrés J, Troy Ferrarons J, Bosse B, Krain B, Nichols T, Kremers W, Reimer K. Fixed-ratio combination oxycodone/naloxone compared with oxycodone alone for the relief of opioid-induced constipation in moderate-to-severe noncancer pain. Curr Med Res Opin 2008; 24: 3503-3512.
- Nelson A, Camilleri M. Opioid-induced constipation: advances and clinical guidance. Ther Adv Chronic Dis 2016; 7: 121-134.
- Lewis S, Heaton K. Stool form scale as a useful guide to intestinal transit time. Scand J Gastroenterol 1997; 32: 920-924.
- Darren M, Brenner MD, William D, Chey MD. An evidence-based review of novel and emerging therapies for constipation in patients taking opioid analgesics. Am J Gastroenterol Suppl 2014; 2: 38-46.
- Manchikanti L, Abdi S, Atluri S et al. American Society of Interventional Pain Physicians (ASIPP) Guidelines for responsible opioid prescribing in chronic non-cancer pain: Part 2 – Guidance. Pain Physician 2012; 15: S67-S116.
- Karch FE, Lasagna L. Towards the operational identification of adverse drug reactions. Clin Pharmacol Ther 1977; 21: 247-254.
- Frank L, Kleinman L, Farup C et al. Psychometric validation of a constipation symptom assessment questionnaire. Scand J Gastroenterol 1999; 34: 870-877.
- Slappendel R1, Simpson K, Dubois D, Keininger DL. Validation of the PAC-SYM questionnaire for opioid-induced constipation in patients with chronic low back pain. Eur J Pain 2006; 10: 209-217.
- Camilleri M, Kerstens R, Rykx A et al. A placebo-controlled trial of prucalopride for severe chronic constipation. N Engl J Med 2008; 358: 2344-2354.
Correspondencia: Esteban H Campitelli
Av. Pedro Goyena 1776 Piso 4 Depto. F (CP: 1406). Ciudad Autónoma de Buenos Aires, Argentina
Tel.: 011 57715114
Correo electrónico: ehcampi@gmail.com
Acta Gastroenterol Latinoam 2018;48(3): 296-301
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE