David Solinas ID· Mauricio Ramírez ID· Alejandro Nieponice ID
Fundación Favaloro, Hospital Universitario.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2025;55(4):317-329
Recibido: 11/10/2025 / Aceptado: 09/12/2025 / Publicado online: 23/12/2025 / https://doi.org/10.52787/agl.v55i4.553
Resumen
La enfermedad por reflujo gastroesofágico representa una condición prevalente a nivel mundial con impacto significativo en la calidad de vida de los pacientes y una carga creciente para los sistemas de salud. En Argentina, se estima una prevalencia del 23% de síntomas típicos semanales, similar a lo reportado en otras regiones de Latinoamérica. Aunque la mayoría de los pacientes con esofagitis responden adecuadamente a los inhibidores de la bomba de protones, hasta un 30 a 40% de los casos puede mostrar una respuesta parcial o inadecuada, especialmente en aquellos con enfermedad no erosiva. En tal contexto, la cirugía es una alternativa válida y efectiva. Esta revisión tiene como objetivo analizar de manera actualizada y basada en evidencia, la evaluación funcional preoperatoria, las técnicas quirúrgicas, la selección de los pacientes y la relación entre la enfermedad por reflujo gastroesofágico y condiciones especiales como obesidad o enfermedades reumatológicas.
Palabras claves. Enfermedad por reflujo gastroesofágico, cirugía antirreflujo, funduplicatura, hernia hiatal, cirugía laparoscópica, cirugía robótica.
Surgical Procedures in Gastroesophageal Reflux Disease
Summary
Gastroesophageal reflux disease is a prevalent condition worldwide with a significant impact on patients’ quality of life and a growing burden on healthcare systems. In Argentina, the prevalence of typical weekly symptoms is estimated at 23%, which is similar to rates reported in other Latin American regions. Although most patients with esophagitis respond adequately to proton pump inhibitors, up to 30 – 40% of cases may show a partial or inadequate response, particularly among those with non-erosive disease. In such cases, surgery is a valid and effective alternative. The aim of this review is to provide an up-to-date, evidence-based analysis of preoperative functional evaluation, surgical techniques, patient selection, and the relationship between gastroesophageal reflux disease and special conditions such as obesity or rheumatological diseases.
Keywords. Gastroesophageal reflux disease, anti-reflux surgery, fundoplication, hiatal hernia, laparoscopic surgery, robotic surgical procedures.
Abreviaturas
ERGE: Enfermedad por reflujo gastroesofágico.
IBP: Inhibidores de la bomba de protones.
CAR: Cirugía antirreflujo.
ADS: Arcada dentaria superior.
pHz: Ph-impedanciometria.
MARE: Manometría esofágica de alta resolución.
EEI: Esfínter esofágico inferior.
SEGD: Seriada esófago-gastro-duodenal.
FLIP: Functional luminal imaging probe.
ID: Índice de distensibilidad.
UEG: Unidad esofagogástrica.
TIF: Trans-oral incisionless fundoplication.
RYGB: By pass gástrico en Y de roux.
Introducción
La enfermedad por reflujo gastroesofágico (ERGE) es una patología de alta prevalencia que afecta significativamente la calidad de vida y representa una carga creciente para los sistemas de salud. Se estima que entre el 10 y el 30% de la población mundial presenta síntomas compatibles. En Argentina se reporta una prevalencia del 23% de síntomas típicos semanales.1, 2
El tratamiento inicial se basa en la indicación de modificaciones en el estilo de vida y en el uso de inhibidores de la bomba de protones (IBP), que resultan eficaces en la mayoría de los casos. Sin embargo, entre 30 y 40% de los pacientes puede presentar una respuesta parcial o insatisfactoria.3
La cirugía antirreflujo (CAR) constituye una alternativa válida para pacientes seleccionados, permitiendo mejorar el control sintomático y reducir la necesidad de un tratamiento prolongado.
Esta revisión analiza los criterios diagnósticos, las herramientas funcionales, las opciones quirúrgicas disponibles y los escenarios clínicos especiales que inciden en el abordaje actual de la ERGE.
Fisiopatología de la enfermedad por reflujo gastroesofágico
La fisiopatología de la ERGE es multifactorial y se centra en la disrupción de los mecanismos que conforman la barrera antirreflujo y en la exposición esofágica anormal al contenido gástrico o gastroduodenal. Los mecanismos fisiopatológicos principales incluyen:4
Disfunción del esfínter esofágico inferior (EEI)
● Las relajaciones transitorias del EEI constituyen el principal mecanismo de reflujo en los sujetos sin hernia hiatal. Son eventos vagales no relacionados con la deglución, fisiológicos, pero con frecuencia y duración aumentadas en los pacientes con ERGE.4
● En un subgrupo se observa la hipotonía del EEI, con una presión basal < 10 mmHg, que favorece la ocurrencia de episodios de reflujo por incompetencia del cierre esofagogástrico.4
Hernia hiatal
● La hernia hiatal en cualquiera de sus formas (por deslizamiento, paraesofágica o mixta gigante), contribuye al desacoplamiento del EEI respecto del diafragma crural, eliminando el efecto esfinteriano sinérgico. Esta condición reduce la longitud intraabdominal del EEI y altera el ángulo de His, disminuyendo la eficacia de la barrera valvular.
Alteración del aclaramiento esofágico
● El aclaramiento mecánico mediante la peristalsis secundaria y el aclaramiento químico mediado por la secreción salival y el bicarbonato pueden estar comprometidos, especialmente en los pacientes con trastornos motores esofágicos o hiposalivación, ya que prolongan la exposición esofágica al reflujo.
Composición del reflujo
● Si bien el ácido clorhídrico es el principal agresor, puede estar presente la exposición combinada a bilis, pepsina y enzimas pancreáticas, especialmente en pacientes con cirugía gástrica previa o en el reflujo mixto. Estos componentes tienen un efecto citotóxico sinérgico sobre el epitelio esofágico.
Diagnóstico
La confirmación objetiva de ERGE según criterios fisiológicos establecidos, como los propuestos en el Consenso de Lyon para pH-impedanciometría, cápsula de pHmetria inalambrica, videoendoscopia digestiva alta y manometría de alta resolución, son fundamentales antes de indicar una intervención quirúrgica antirreflujo.5 Es imprescindible una evaluación integral para confirmar el diagnóstico, definir el fenotipo fisiopatológico, descartar diagnósticos diferenciales, orientar el tipo de tratamiento indicado y evaluar si el paciente es candidato a una intervención quirúrgica.
Evaluación clínica inicial
El consenso de Montreal6 centra su análisis en la anamnesis para detectar síntomas típicos y atípicos de reflujo. Esto es de particular relevancia, ya que identifica síntomas como pirosis y regurgitación, asociados a mejor respuesta al tratamiento. La respuesta a IBP constituye un criterio clínico útil, aunque no específico ni suficiente para la selección quirúrgica. La regurgitación es, particularmente, el síntoma que mejor se controla con la cirugía antirreflujo. A su vez, en un 30 – 40% de los pacientes, la respuesta a IBP puede ser parcial por persistencia de regurgitación no ácida o por una alteración en la sensorialidad (hipersensibilidad al reflujo). Este grupo de pacientes, junto con los que presentan síntomas atípicos como tos crónica, disfonía o asma, son los que deben evaluarse exhaustivamente para definir el mejor tratamiento.3, 6, 7
Videoendoscopia digestiva alta
La endoscopía debe ser realizada en todos los pacientes con síntomas de reflujo, ya que permite:8
● Diagnosticar hernia hiatal.
● Pesquisar el esófago de Barrett.
● Evaluar la presencia de esofagitis erosiva (clasificación de Los Ángeles).
● Evaluar anatomicamente la unión gastroesofágica
● Detectar la presencia o no de residuos de alimento en esófago/estómago a pesar del ayuno.
● Descartar anillos o estenosis como consecuencia del reflujo.
● Descartar tumores esofágicos y gástricos.
Sin embargo, hasta un 70% de los pacientes con ERGE puede presentar una endoscopía normal, por lo que es mandatorio una evaluación funcional complementaria.5
Manometría esofágica de alta resolución (MARE)
Su realización previa a cualquier tratamiento quirúrgico tiene gran importancia. No diagnostica ERGE, pero, a partir de la Clasificación de Chicago en su cuarta versión, evalúa y diagnostica9 la funcionalidad la unión gastroesofágica (presión basal del EEI, tipo de unión gastroesofágica, relajación, integral contráctil).
• Peristalsis del cuerpo esofágico.
• Diagnóstico de trastornos motores asociados o independientes del reflujo (acalasia, espasmo esofágico distal, esófago hipercontractil, entre otros).
● Longitud esofágica, lo cual es un dato clave de cara a una cirugía por ERGE, ya que puede modificar la técnica a utilizar.
Además, permite localizar con precisión el EEI para el posicionamiento adecuado de la sonda de pH-impedanciometría.10
Además de su rol diagnóstico y de planificación, algunos estudios han explorado el valor pronóstico de ciertos parámetros manométricos respecto al éxito de la cirugía antirreflujo.11
De forma preliminar, se ha sugerido que:
● Una longitud del EEI ≥ 4 cm podría asociarse a una mayor probabilidad de resolución de síntomas típicos tras la funduplicatura.11
● Una presión basal del EEI relativamente elevada (≈ ≥ 19 mmHg) se ha vinculado, en algunos trabajos, con la mejoría de los síntomas atípicos.11
No obstante, estos hallazgos provienen de series retrospectivas y requieren validación en cohortes más amplias antes de considerarse criterios definitivos. Su interpretación debe hacerse en conjunto con el resto de la evaluación funcional y anatómica del paciente.
Monitoreo ambulatorio de reflujo
La exposición acido-patológica es el patrón de oro evaluada por monitoreo ambulatorio de reflujo (pH-impedanciometria de 24hs o capsula de pHmetria inalambrica de 96hs). Según los criterios propuestos en el Consenso de Lyon,5, 12 este estudio permite valorar:
● Tiempo de exposición ácida total.
● Número de episodios de reflujo.
● Reflujo ácido y no ácido.
● Episodios de eructos, rumiación y eructos supra-gástricos.
● Asociación temporal entre síntomas y eventos de reflujo.
● Impedancia basal nocturna media.
Estos parámetros facilitan diferenciar los pacientes con ERGE objetivable de aquellos con condiciones asociadas a la hipersensibilidad o pirosis funcional.13, 14
En situaciones de hernias hiatales mixtas gigantes con disrupción anatómica severa, la indicación quirúrgica suele estar más vinculada al riesgo mecánico (volvulación, atascamiento) o a síntomas graves (disfagia, aspiraciones nocturnas) que a la documentación fisiopatológica de ERGE, por lo que el estudio puede no ser imprescindible.15
Valor pronóstico de la pH-impedanciometría de 24hs
Algunos estudios sugieren que determinados parámetros podrían asociarse con una mayor probabilidad de obtener un buen resultado tras la cirugía antirreflujo:16, 17
● Probabilidad de asociación sintomática (PAS) positivo (> 95 %), que refleja una relación temporal estrecha entre los episodios de reflujo y los síntomas.16, 17
● Exposición ácida aumentada, expresada por un tiempo con pH < 4 que supera los umbrales considerados patológicos (≈ 10 – 12% en 24 h) o un índice de DeMeester elevado. Ciertos trabajos han mostrado correlación con mejores desenlaces.16,17
● Síntomas típicos (pirosis, regurgitación) concomitantes con hallazgos objetivos de reflujo patológico parecen reforzar la predicción de beneficio quirúrgico.16, 17
Otros parámetros, como el número total de episodios de reflujo, la proporción de eventos proximales o el índice sintomático, no han demostrado una asociación consistente con la respuesta postoperatoria.16
En definitiva, la pH-impedanciometría de 24 h no solo aporta criterios diagnósticos, sino que también puede orientar la selección quirúrgica. No obstante, la magnitud de su valor predictivo sigue siendo objeto de debate, y los hallazgos deben interpretarse en conjunto con la clínica y la anatomía de cada paciente.
Los sistemas digitales portátiles o cápsulas inalámbricas (Bravo™) permiten cuantificar la exposición ácida mediante un registro prolongado de pH de hasta 96 horas. Aunque su disponibilidad en Latinoamérica aún es limitada, resultan especialmente útiles en pacientes con estudios de pH-impedanciometría de 24 horas con valores borderline o dentro de rangos fisiológicos, pero con síntomas compatibles con ERGE. El monitoreo extendido reduce la variabilidad día a día, mejora la tolerancia y aceptación por parte del paciente, y aumenta la sensibilidad diagnóstica.5, 12
Seriada esófago-gastro-duodenal
La seriada esófago-gastro-duodenal (SEGD) no constituye una herramienta diagnóstica de elección para confirmar la enfermedad por reflujo gastroesofágico, dado que no permite cuantificar la exposición ácida.
Sin embargo, puede resultar útil en la evaluación preoperatoria de inicio o en pacientes en los que estamos considerando una intervención para descartar patología estructural (estenosis, esófago corto, hernia hiatal), para definir la anatomía del hiato y del esófago distal, y evaluar el aclaramiento esofágico.18
En este contexto, la SEGD se emplea de forma complementaria a los estudios funcionales, aportando información morfológica que puede modificar la técnica a seleccionar.18
Planimetría por impedancia
En las guías AGA y Consenso de Dallas de 2025, se describe que la sonda de imagen de luz funcional (FLIP) constituye una herramienta diagnóstica valiosa en la práctica clínica, especialmente en el contexto de las intervenciones quirúrgicas del tracto digestivo superior, aunque es fundamental comprender que no debe emplearse para diagnosticar ERGE ni para determinar la necesidad de una intervención antirreflujo.19, 20
Los estudios sobre la función de barrera de la unión esofagogástrica en la ERGE no han logrado establecer un umbral discriminatorio claro para el índice de distensibilidad (ID) de la union esofago-gastrica (UEG) que permita diferenciar la ERGE sintomática de los controles.19, 20
A pesar de esta limitación diagnóstica y prequirúrgica para la ERGE, la planimetría tiene utilidad tanto en el intraoperatorio como en la evaluación posterior a la cirugía antirreflujo.
Utilidad Intraoperatoria
Durante la cirugía antirreflujo (CAR) y los procedimientos endoscópicos para el reflujo, la FLIP intraoperatoria es factible. El ID ha sido estudiado en un intento de prevenir la disfagia postoperatoria. Se reporta que un ID de la UEG inferior a 2 mm²/mm Hg después de la CAR se asocia con síntomas de disfagia y se nota que el cierre de los pilares del diafragma parece tener un impacto mayor en el ID que la propia funduplicatura.19
Se han propuesto rangos ideales de ID de la UEG para funduplicaturas específicas, como 2,6 – 3,7 mm²/mm Hg para Toupet y > 2,2 mm²/mm Hg para Nissen. Estos rangos tienen el potencial de guiar la toma de decisiones intraoperatorias, permitiendo ajustar la funduplicatura. No obstante, algunos estudios con FLIP intraoperatoria no han encontrado diferencias significativas en los seguimientos de hasta dos años.19
Utilidad Postoperatoria
La FLIP puede ser considerada en la evaluación de síntomas persistentes de obstrucción esofágica (como disfagia, regurgitación de tipo esofágico y/o dolor torácico relacionado con las comidas) después de una intervención antirreflujo. Es una herramienta crucial para investigar la disfagia post-funduplicatura, ya que puede evaluar la obstrucción de la UEG y dirigir el tratamiento mediante dilatación, con buenos resultados sintomáticos reportados. Además, puede identificar una peristalsis secundaria anormal en el 84% de los pacientes sintomáticos después de una CAR, la cual podría empeorar con una mayor duración post-CAR y/o resistencia al flujo de salida de la UEG.
En conclusión, aunque la FLIP no diagnostica directamente la ERGE, su valor reside en la caracterización detallada de la función esofágica y de la UEG antes, durante y después de las intervenciones del tracto digestivo superior, lo que la convierte en una herramienta para optimizar los resultados quirúrgicos y manejar eficazmente las complicaciones obstructivas.19
Tratamiento quirúrgico de la ERGE
La cirugía antirreflujo se considera indicada en los pacientes con diagnóstico confirmado por cualquiera de los puntos establecidos en Consenso de Lyon5 con:
● Respuesta parcial a IBP (regurgitación severa no controlada con IBP o síntomas persistentes) o intolerancia/contraindicación a estos fármacos.
● Complicaciones estructurales (Barrett, estenosis pépticas, etc.).
● Preferencia de evitar tratamiento médico.
En la literatura no existe una definición universalmente aceptada de «éxito» para la cirugía antirreflujo. Comúnmente, se consideran varios indicadores:
● Remisión sintomática sostenida sin necesidad de IBP.
● Mejoría objetiva de la exposición ácida por pH-impedanciometría de 24hs o VEDA que evidencie remisión de esofagitis sin IBP.
● Satisfacción del paciente, utilizada por su valor práctico: se reportan tasas entre el 80 – 96% post-funduplicatura laparoscópica en términos de mejoría de calidad de vida y disminución de síntomas (GERD-HRQL, Visick Score).21, 22
Tanto los parámetros subjetivos como los objetivos se deben interpretar en conjunto para evaluar el éxito real del procedimiento. Las distintas alternativas con sus ventajas y limitaciones se encuentra resumida en la Tabla 1.
Tabla 1. Opciones terapéuticas en ERGE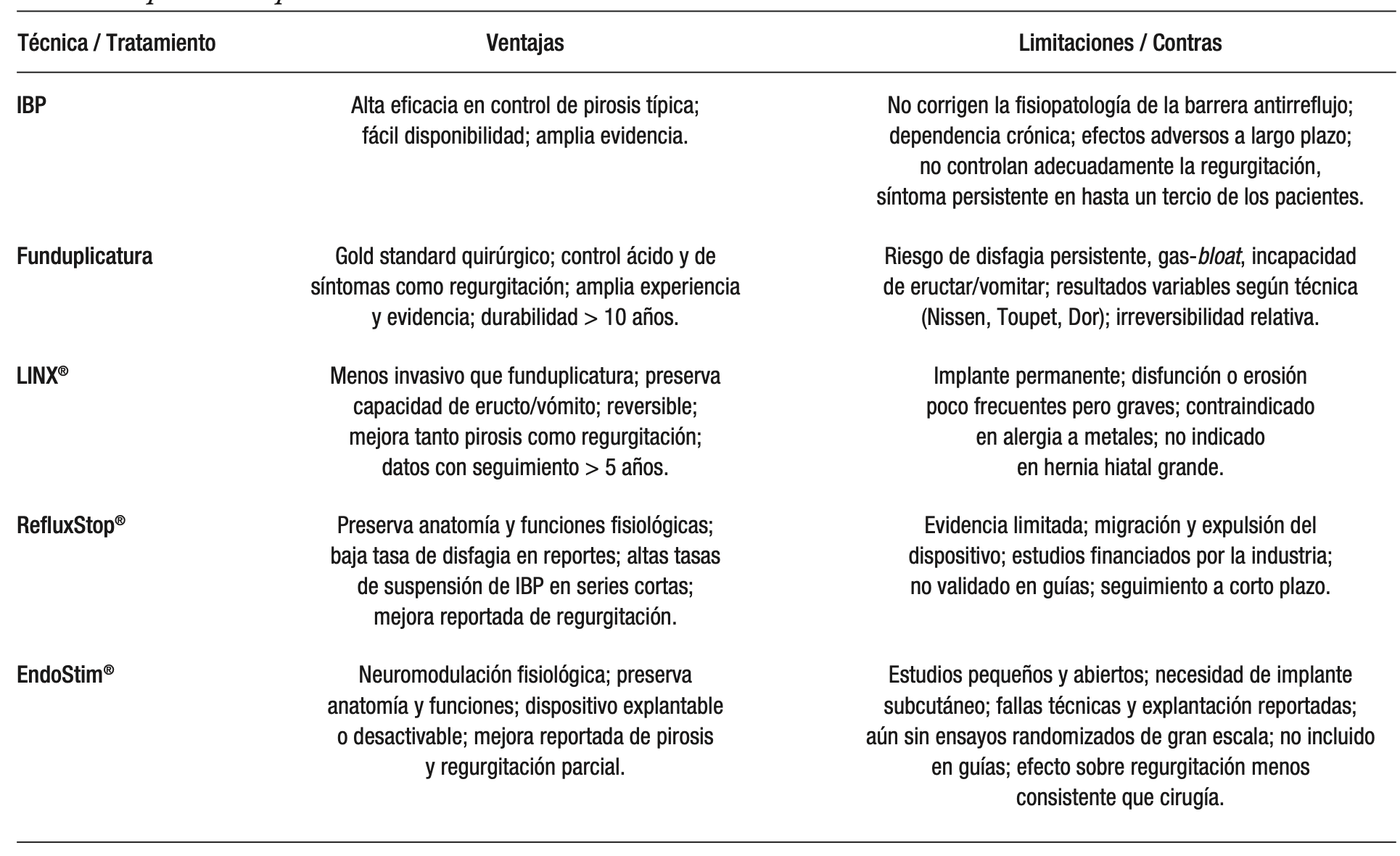
El estudio LOTUS, publicado en 2011, es un ensayo clínico aleatorizado y multicéntrico que abarca 11 países europeos en el que se investigó la eficacia a largo plazo de esomeprazol vs. funduplicatura. Los investigadores compararon las tasas de remisión y la prevalencia de síntomas entre los dos grupos durante un período de cinco años. Los hallazgos sugieren que ambas opciones son efectivas para mantener a los pacientes en remisión. Al analizar por síntoma señalaron que a 5 años la acidez y la regurgitación ácida están presentes con mayor frecuencia en el grupo con esomeprazol, y la disfagia/bloating en el grupo funduplicatura.23 Como dato importante, en este ensayo, si bien se enfatiza la estandarización de la técnica para obtener buenos resultados, no se especifica qué tipo de funduplicatura fue utilizada para el análisis. Como veremos más adelante, dentro de las funduplicaturas hay distintos efectos adversos reportados para cada una de ellas.
Funduplicaturas: Principios, técnicas y resultados
Las funduplicaturas consisten en envolver el fundus gástrico alrededor del esófago distal para aumentar la presión del esfínter esofágico inferior y restaurar la barrera antirreflujo (Figuras 1 a b c).
La elección de la técnica debe basarse en el conocimiento anatómico, funcional y en la evidencia clínica que respalde su eficacia y seguridad. La obesidad, la presencia de hernia hiatal y su tamaño, asociado a la longitud esofágica intraabdominal, son factores de riesgo bien conocidos para la recidiva de la hernia hiatal/ERGE en el corto a mediano plazo.
Las técnicas más empleadas incluyen:
● Funduplicatura de Nissen (360°): Técnica de envoltura total que ofrece un control sintomático exitoso. Puede asociarse a una mayor incidencia de disfagia postoperatoria (Figura 1)
● Funduplicatura de Toupet (270° posterior): Técnica de envoltura parcial que reporta éxito sintomático y de recidiva comparables a la funduplicatura de Nissen, con menor disfagia postoperatoria (Figura 2).
● Funduplicatura Collis-Nissen: Técnica aplicada fundamentalmente en el esófago corto para aumentar la longitud intraabdominal. Su uso es más debatido debido a la variabilidad en las indicaciones, la complejidad técnica y los resultados. Algunos estudios muestran un control sintomático comparable a la técnica de Nissen estándar, pero con mayor morbimortalidad. Su indicación debe ser estricta y reservada para casos específicos.
Figura 1. Funduplicatura de Nissen laparoscópica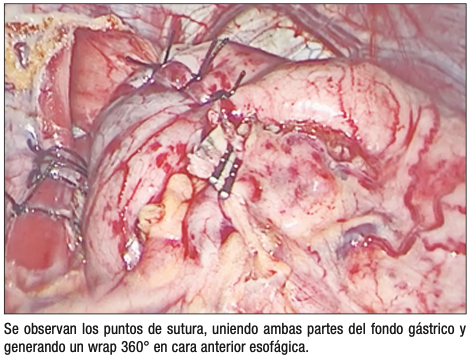
Figura 2. Funduplicatura de Toupet robótica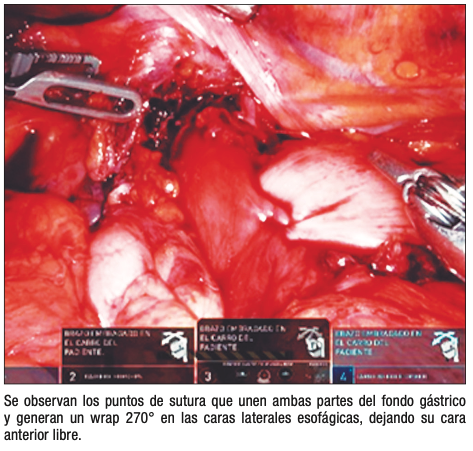
En conclusión, la cirugía antirreflujo laparoscópica presenta tasas de éxito sintomático en el 80 a 90% de los casos, una recurrencia clínica del 10 – 18% y recidivas que requiere reoperaciones en 3 a 7% de los pacientes,
si bien estos rangos se acotan a la baja en aquellos centros de alto volumen de pacientes y experiencia. La centralización quirúrgica es un factor clave para optimizar los resultados, minimizar las complicaciones y reducir las tasas de falla.23
La elección de la técnica quirúrgica debe personalizarse según el perfil funcional del paciente y sus características anatómicas, priorizando la eficacia y minimizando los efectos adversos como la disfagia. Hoy en día, los ensayos clínicos randomizados respaldan la funduplicatura tipo Toupet como primera línea de tratamiento quirúrgico, por presentar el mismo control de reflujo con menor morbilidad postoperatoria que la funduplicatura de Nissen (Tabla 2).
Tabla 2. Estudios randomizados Nissen vs Toupet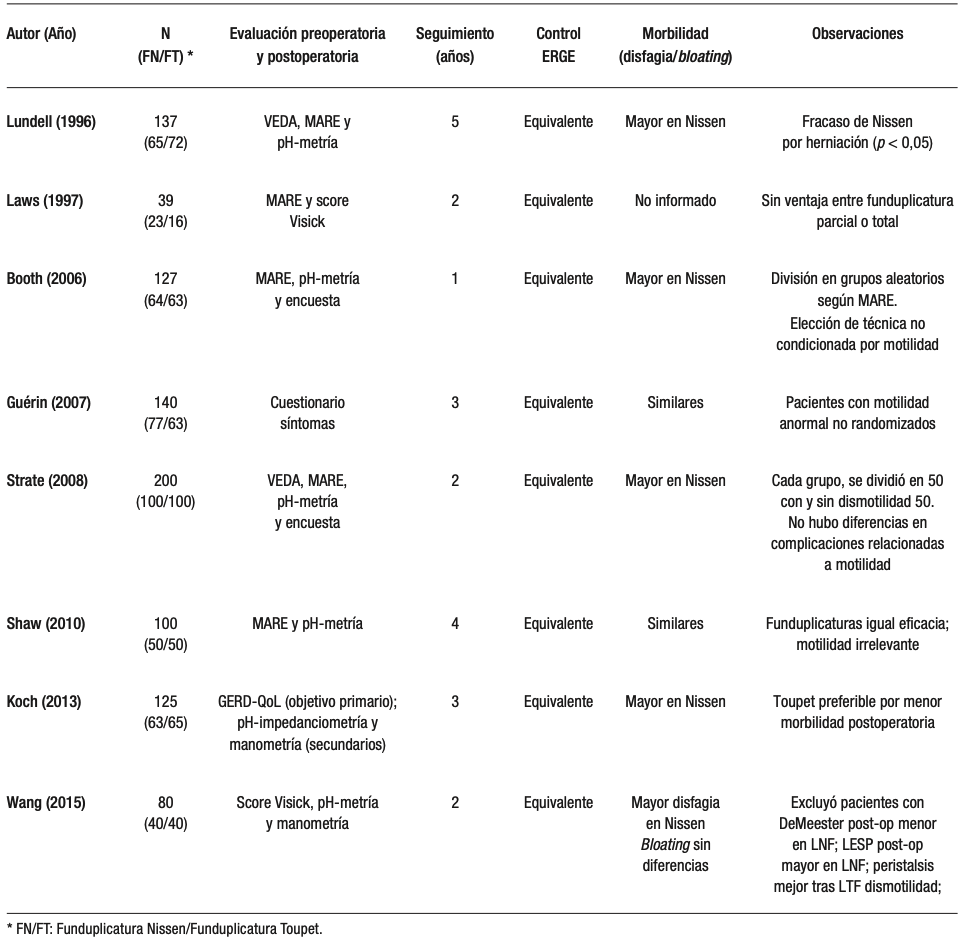
En 2016 Du et al., publicaron un metaanálisis englobando los estudios randomizados; los hallazgos sugieren que ambos procedimientos ofrecen un control igualmente bueno de la ERGE y una satisfacción similar del paciente. Aunque la funduplicatura de Nissen se asocia con un tiempo quirúrgico más corto (probablemente relacionada a la popularidad de esta técnica) y una mayor presión postoperatoria del esfínter esofágico inferior, también presenta una mayor incidencia inicial de disfagia, distensión por gases e incapacidad para eructar, principalmente en el primer año postoperatorio.24 Es propio mencionar que la estandarización de la técnica de funduplicatura presenta múltiples desafíos, inherentes a quién realiza la cirugía y la anatomía propia de cada paciente, por lo que se debe ser riguroso a la hora de analizar dichos reportes.
Dispositivo LINX® (Magnetic Sphincter Augmentation, MSA)
El LINX consiste en un anillo magnético de titanio implantado laparoscópicamente alrededor del EEI. La tensión magnética mantiene cerrado el EEI en reposo y permite su apertura durante la deglución o la eructación, preservando de manera fisiológica el tránsito esofagogástrico.25
Evidencia y resultados reportados:
●Eficacia clínica: múltiples series prospectivas y algunos registros multicéntricos han mostrado tasas de control sintomático de ERGE en torno al 80 – 90% a 5 años, con reducción significativa en la puntuación GERD-HRQL y en el uso de IBP; a su vez, estudios con pH-impedanciometría en el seguimiento demuestran una mejoría en la exposición ácida esofágica comparable con la funduplicatura.26, 27
●Seguridad y complicaciones: la principal limitación es la disfagia postoperatoria, que aparece hasta en el 40% en el corto plazo, pero suele resolverse en la mayoría de los casos con dilataciones o espontáneamente; menos del 5 al 7% requieren la explantación del dispositivo. La erosión, si bien es una complicación severa, se reporta en menos del 1,5% de las series disponibles.27
Actualmente no se dispone de estudios randomizados de alto volumen de pacientes que permitan comparar los resultados de LINX contra funduplicaturas. Los que se encuentran disponibles, lo comparan con la funduplicatura de Nissen, en donde se objetiva la superioridad del LINX en términos de bloating, capacidad de eructar y vomitar.2 Como se mencionó anteriormente, estos efectos ya eran superiores en la funduplicatura de Toupet, por lo que se necesitan cohortes randomizadas de estas dos técnicas y de mayor volumen para llegar a una conclusión categórica.
A su vez, en pacientes con hernias hiatales grandes, esófago corto o alteraciones de la motilidad, la disfagia preoperatoria a LINX impresiona ser mayor, es por esto que las guías internacionales, por ejemplo, SAGES 2021, reconocen el LINX como una alternativa válida en pacientes seleccionados con ERGE demostrada, refractaria a IBP y anatomía favorable, pero no lo recomiendan como sustituto universal de la funduplicatura.29
Reparación hiatal concomitante más funduplicatura transoral sin incisión (cTIF) en la enfermedad por reflujo gastroesofágico
El procedimiento combina la reparación crural convencional -con cierre posterior del hiato bajo visión laparoscópica- con una reconstrucción endoluminal de la válvula gastroesofágica mediante el dispositivo EsophyX®. Esta técnica permite una funduplicatura parcial interna de aproximadamente 270° y 3 cm de longitud, utilizando anclajes transmucosos y sin disección extensa del fundus.30
De esta forma, el cTIF intenta reproducir los principios de la funduplicatura parcial, con menor tensión mecánica y menor distorsión anatómica, preservando la capacidad de ventilar gas y deglutir de manera fisiológica.31
Resultados clínicos
La evidencia publicada específicamente sobre cTIF, aunque limitada, sugiere resultados prometedores. Chang et al. reportaron una serie de 60 pacientes con hernias hiatales promedio de 2,9 cm que recibieron reparación quirúrgica del hiato más TIF en la misma sesión. A los seis meses, los cuestionarios validados de síntomas de reflujo mostraron una mejora significativa, con puntuaciones de frecuencia y severidad que pasaron de 17,4 ‑16 a 4 ‑5, y una reducción drástica en la exposición ácida distal medida por pH a 1,28% postoperatorio. Ningún evento adverso grave fue documentado, y en la mayoría de los pacientes se logró discontinuar los IBP.31
Un análisis sistemático reciente que incluyó siete estudios observacionales con un total de 306 pacientes mostró que la tasa mediana de abandono de IBP tras cTIF fue del 73,8%, con mejoras significativas en los cuestionarios de calidad de vida. Las complicaciones fueron bajas (4,4%), con incidencias de disfagia y bloating de 5,3% y 6,9%, respectivamente, aunque se reconocen limitaciones importantes en los estudios, como su heterogeneidad y un seguimiento principalmente a corto y mediano plazo.32
El tratamiento cTIF ha demostrado factibilidad y eficacia incluso en pacientes con hernias paraesofágicas gigantes. Gergen et al. reportaron 12 casos con hernias de aproximadamente 5 cm, en los que se combinó reparación quirúrgica con TIF; todos los pacientes refirieron una resolución completa de los síntomas, en algunos casos con endoscopía y pruebas de pH confirmando la presencia de una válvula intacta y la ausencia de reflujo ácido a los seis meses. La morbilidad funcional fue mínima, con un solo paciente que requirió dilatación por disfagia y sin reportes de gas-bloat.33 Estudios adicionales en cohortes más grandes, de hasta 334 pacientes, corroboran estas tendencias, mostrando la reducción del uso de IBP, mejoría en los cuestionarios de síntomas y una baja necesidad de reintervención.34
La literatura específica sobre cTIF permite argumentar científicamente la opción de no realizar funduplicatura convencional en pacientes que ya se encuentran en quirófano con el hiato reparado. La combinación de reparación del hiato y TIF logra resultados sintomáticos comparables al control esperado con la funduplicatura, pero con menor incidencia de disfagia persistente y gas‑bloat. Además, el procedimiento respeta la anatomía del fundus y minimiza la manipulación de vasos cortos, reduciendo los riesgos intraoperatorios. La experiencia publicada indica que, si fuese necesario, la conversión a funduplicatura parcial o total sigue siendo factible, lo que permite una estrategia escalonada que prioriza inicialmente la preservación funcional.31,32
A pesar de estos resultados alentadores, la evidencia presenta limitaciones. La mayoría de los estudios tiene seguimiento corto-medio, la heterogeneidad de criterios de inclusión dificulta hacer extrapolaciones, y aún no existen ensayos aleatorizados comparativos a largo plazo frente a funduplicaturas clásicas. La selección adecuada del paciente y la experiencia del equipo quirúrgico son fundamentales, así como la documentación preoperatoria y la planificación intraoperatoria. En consecuencia, cTIF emerge como una alternativa prometedora para pacientes seleccionados, ofreciendo una opción menos invasiva desde el punto de vista funcional, con resultados sintomáticos significativos y baja morbilidad, aunque la funduplicatura convencional sigue siendo la intervención con evidencia más robusta a largo plazo.
RefluxStop®
El dispositivo Reflux Stop® consiste en un implante de polímero de silicona fijado en el fundus gástrico en forma previa a la reparación hiatal y la reconstrucción del ángulo de His (Figura 3), cuyo objetivo es restaurar la competencia antirreflujo mediante la prevención del desplazamiento del fundus y el esófago distal a través del hiato.35
A diferencia de la funduplicatura, no implica una compresión circunferencial del esófago, lo que teóricamente preserva funciones fisiológicas como eructar y vomitar, y reduce la incidencia de disfagia postoperatoria.
Estudios prospectivos europeos han reportado tasas de suspensión de IBP superiores al 90% a dos años, con mejoría significativa en los cuestionarios de calidad de vida. En pocas ocasiones fueron documentados eventos adversos graves, como migración aguda al tórax y eliminación del dispositivo por vía natural.36
Se debe mencionar que muchos de los estudios reportando tasas de éxitos superiores al 90% se encuentran financiados por la industria y la mayoría de las series reportadas presentan un tamaño muestral limitado y seguimiento a corto plazo, por lo que no se encuentra actualmente aceptado en las guías de práctica clínica. Por tales motivos es necesario contar con estudios randomizados de mayor tamaño muestral. Por el momento, debe considerarse como una tecnología emergente con evidencia insuficiente para reemplazar a las técnicas estándar.
Figura 3. Esquema de sistema Reflux Stop® in situ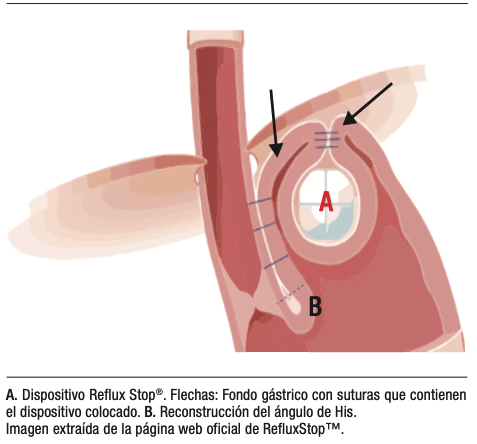
EndoStim®
El sistema EndoStim® es una terapia de neuromodulación que utiliza un generador implantable subcutáneo conectado a electrodos fijados en la musculatura del esfínter esofágico inferior (Figura 4). Su objetivo es incrementar la presión basal del esfínter mediante pulsos eléctricos intermitentes, manteniendo la relajación fisiológica. La técnica se realiza por vía laparoscópica, con posibilidad de reparación hiatal concomitante cuando es necesario.
A diferencia de la funduplicatura, no crea una barrera mecánica ni modifica de forma permanente la anatomía, lo que reduce la incidencia de síntomas obstructivos y permite, en caso de complicaciones, desactivar o retirar el dispositivo. Series prospectivas multicéntricas han mostrado una reducción significativa del tiempo de exposición ácida, mejoría de la calidad de vida y tasas de suspensión de IBP de 60 – 80% a 2 – 3 años de seguimiento.37, 38
Los efectos adversos incluyen infecciones del generador, fallas técnicas y necesidad de explantación en un número limitado de pacientes. No obstante, la mayoría de los estudios disponibles son abiertos, con bajo número de pacientes y seguimiento intermedio, frecuentemente con apoyo de la industria. Aún no están publicados ensayos randomizados de gran escala, y la técnica no figura en las guías clínicas internacionales como opción estándar. En la actualidad, EndoStim® debe considerarse una alternativa en investigación, con resultados iniciales alentadores en pacientes seleccionados, pero con evidencia insuficiente para recomendar su uso generalizado.
Figura 4. Dispositivo Endostim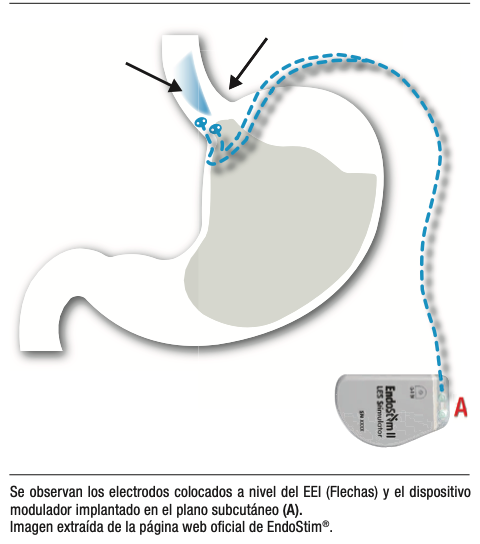
Manejo de la recidiva y condiciones especiales
La recidiva tras funduplicatura continúa siendo un desafío clínico-quirúrgico, cuya interpretación debe distinguir entre recurrencia clínica y verdadero fracaso quirúrgico. En pacientes no obesos, sin cirugías múltiples previas y con anatomía favorable, la re-funduplicatura laparoscópica constituye una opción válida, con buenos resultados sintomáticos y menor morbilidad que las alternativas derivativas.
ERGE y cirugía bariátrica
La obesidad es un factor de riesgo establecido para el desarrollo y la persistencia ERGE. El aumento de la presión intraabdominal, la disfunción del EEI y la presencia frecuente de hernia hiatal contribuyen a una mayor incidencia y gravedad del reflujo en esta población, que a su vez responde menos favorablemente al tratamiento médico.39, 40
La gastrectomía en manga, pese a su amplia difusión como técnica bariátrica, se asocia con una incidencia relevante de ERGE de novo o empeoramiento del reflujo preexistente.41 Los mecanismos incluyen el aumento de la presión intragástrica, la pérdida del ángulo de His y la alteración de la motilidad gástrica. Diversas series y metaanálisis reportan tasas de nuevo reflujo entre 20 y 40%, con progresión a esofagitis en un subgrupo significativo de pacientes.39, 41 Por ello, se recomienda cautela en la indicación de manga en pacientes con reflujo documentado y, en presencia de esofagitis severa o síntomas significativos, optar preferentemente por el bypass gástrico en Y de Roux (RYGB).39, 41, 42
Existen técnicas experimentales que combinan la manga gástrica con una funduplicatura parcial para mitigar el reflujo, pero la evidencia aún es preliminar y no se recomienda su uso fuera de ensayos clínicos controlados.
En contraste, en pacientes obesos, con múltiples fracasos previos o anatomía distorsionada, el RYGB ofrece una solución más robusta: controla de manera efectiva el reflujo, desvía el contenido biliar y reduce la acidez gástrica, a la vez que corrige factores anatómicos de riesgo.42 Su eficacia está bien documentada en la obesidad con ERGE refractaria y en contextos de fracaso repetido de funduplicatura, aunque a costa de mayor complejidad técnica y morbilidad.41 La derivación tipo Y de Roux está indicada principalmente en dos contextos:
1. Pacientes con reflujo sintomático a pesar del tratamiento médico con IMC mayor a 30 como indicación relativa y mayor a 35 como indicación absoluta
2. Pacientes con fracaso de funduplicatura previa en más de dos oportunidades y persistencia de síntomas a pesar del tratamiento con IBP o con evidencia
ERGE y condiciones especiales
La motilidad esofágica alterada y las enfermedades del tejido conectivo requieren un abordaje particularmente cuidadoso que es tratado en el Consenso de ICARUS publicado en 2019. En la esclerodermia y otras colagenopatías sistémicas, que presentan disfagia como síntoma intrínseco, motilidad esofágica inefectiva o aperistalsis esofágica que compromete el aclaramiento de reflujo, la funduplicatura es una opción que debe ser evaluada con rigurosidad por la posibilidad de disfagia severa llegando a un 70% de disfagia en algunas series.40
Asimismo, en pacientes con trastornos motores severos no asociados a colagenopatía, se aplica el mismo principio: no indicar rápidamente la funduplicatura y considerar terapias alternativas como el RYGB. La evidencia, aunque limitada, muestra que estos enfoques disminuyen la incidencia de disfagia postoperatoria con adecuado control del reflujo.39, 40
Conclusión
La enfermedad por reflujo gastroesofágico requiere un abordaje diagnóstico riguroso que permita seleccionar adecuadamente a los candidatos a cirugía. La valoración funcional preoperatoria aporta parámetros con valor pronóstico demostrado: una exposición ácida claramente patológica, un índice de DeMeester elevado, la presencia de síntomas típicos concordantes y una probabilidad de asociación sintomática positiva son predictores consistentes de buena respuesta quirúrgica. Asimismo, ciertos indicadores manométricos -como una longitud adecuada del EEI y presiones basales conservadas- pueden reforzar la expectativa de éxito, aunque requieren validación adicional.
En el ámbito intraoperatorio y postoperatorio, la planimetría de impedancia (FLIP) adquiere relevancia como herramienta para optimizar la calibración de la unión esofagogástrica y reducir la incidencia de disfagia, contribuyendo así a mejorar los resultados funcionales globales. Aunque no constituye un predictor prequirúrgico formal, su uso adecuado favorece la calidad y durabilidad del procedimiento.
La funduplicatura laparoscópica continúa siendo el estándar terapéutico más sólido, mientras que técnicas emergentes como LINX®, cTIF, RefluxStop® y EndoStim® ofrecen alternativas prometedoras en pacientes seleccionados, pero aún con evidencia limitada a largo plazo. La selección individualizada de la técnica -basada en el fenotipo fisiopatológico, anatomía hiatal, motilidad esofágica y comorbilidades como obesidad o colagenopatías- es esencial para optimizar resultados y minimizar complicaciones.
En conclusión, el manejo contemporáneo de la ERGE combina un diagnóstico objetivo, la integración de predictores de respuesta y una estrategia quirúrgica personalizada, permitiendo maximizar la eficacia terapéutica y asegurar resultados duraderos en el control del reflujo.
Propiedad intelectual. Los autores declaran que los datos, las tablas y las figuras presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: David Solinas D, Ramirez M y Nieponice A. Los procedimientos quirúrgicos para la enfermedad por reflujo gastroesofágico. Acta Gastroenterol Latinoam. 2025;55(4):317-329. https://doi.org/10.52787/agl.v55i4.533
Referencias
- Olmos JA, Pandolfino JE, Piskorz MM, et al. Latin American consensus on diagnosis of gastroesophageal reflux disease. Neurogastroenterol Motil. 2024;36(3):e14735. DOI:10.1111/nmo.14735
- Eusebi LH, Ratnakumaran R, Yuan Y, Solaymani-Dodaran M, Bazzoli F, Ford AC. Global prevalence of, and risk factors for, gastro-oesophageal reflux symptoms: A meta-analysis. Gut. 2018;67(3):430-40.
- El-Serag HB, Sweet S, Winchester CC, Dent J. Update on the epidemiology of gastro-oesophageal reflux disease: a systematic review. Gut. 2014;63(6):871-880.
- Tack J, Pandolfino JE. Pathophysiology of gastroesophageal reflux disease: new understanding in a new era. Neurogastroenterol Motil. 2018;30(1):e13246.
- Gyawali CP, Yadlapati R, Fass R, et al. Updates to the modern diagnosis of GERD: Lyon consensus 2.0. Gut. 2024;73(2):361-371. DOI:10.1136/gutjnl-2023-330616
- Vakil N, Van Zanten S V, Kahrilas P, Dent J, Jones R, Bianchi LK, et al. The Montreal definition and classification of gastroesophageal reflux disease: A global evidence-based consensus. Am J Gastroenterol. 2006;101(8):1900-20.
- Katz PO, Dunbar KB, Schnoll-Sussman FH, Greer KB, Yadlapati R, Spechler SJ. ACG Clinical Guideline for the Diagnosis and Management of Gastroesophageal Reflux Disease. Am J Gastroenterol. 2022;117(1):27-56.
- Nguyen NT, Thosani NC, Canto M, Lipham J, Abu Dayyeh B, Wilson E, Muthusamy V, Clarke J, Bell R, Janu P, Swanstrom L, Runge A, Kahrilas PJ. The American Foregut Society White Paper on the Endoscopic Classification of Esophagogastric Junction Integrity. Foregut. 2022;2(4):1-12. DOI:10.1177/26345161221126961
- Yadlapati R, Kahrilas PJ, Fox MR, Bredenoord AJ, Gyawali CP, Roman S, et al. Esophageal motility disorders on high-resolution manometry: Chicago classification version 4.0. Neurogastroenterol Motil. 2021;33(1):e14058. DOI: 10.1111/nmo.14058
- Gyawali CP, Rogers BD, Frazzoni M, Savarino E, Sifrim D, Yadlapati R, et al. The role of high-resolution manometry in the evaluation of esophageal symptoms and disorders. Neurogastroenterol Motil. 2019;31(12):e13649. https://pmc.ncbi.nlm.nih.gov/articles/PMC6771035/
- Park S, Lee JH, Kim M, Lee S, Lee H, Yang H, et al. Explo
ring objective factors to predict successful outcomes after laparoscopic Nissen fundoplication. Int J Surg. 2023;109:299-305. DOI:10.1097/JS9.0000000000000451 - Olmos JA, Pandolfino JE, Piskorz MM, Zamora N, Valdovinos Díaz MA, Remes Troche JM, et al. Latin American consensus on diagnosis of gastroesophageal reflux disease. Neurogastroenterol Motil. 2024;36(5):e14735. DOI:10.1111/nmo.14735
- Gabbard S, Vijayvargiya S. Functional heartburn: An underrecognized cause of PPI-refractory symptoms. Cleve Clin J Med. 2019;86(12):799-806. DOI: 10.3949/ccjm.86a.19006
- Yamasaki T, Sato H, Iwakiri K, et al. Reflux hypersensitivity: A new functional esophageal disorder. J Neurogastroenterol Motil. 2017;23(4):499-506. DOI: 10.5056/jnm17097
- Carrott PW, Hong J, Kuppusamy M, Koehler RP, Low DE. Clinical ramifications of giant paraesophageal hernias are underappreciated: making the case for routine surgical repair. Ann Thorac Surg. 2012;94(2):421-426.
- Desjardin M, Luc G, Collet D, Zerbib F. 24-hour pH-impedance monitoring on therapy to select patients with refractory reflux symptoms for antireflux surgery. A single center retrospective study. Neurogastroenterol Motil. 2016;28(1):146-152. DOI:10.1111/nmo.12715
- Francis DO, Goutte M, Slaughter JC, et al. Traditional reflux parameters and not impedance monitoring predict outcome after fundoplication in extraesophageal reflux. Laryngoscope. 2011;121(9):1902-1909. DOI:10.1002/lary.21897
- Canon CL, Levine MS, Bryn S, et al. Society of Abdominal Radiology consensus statement for barium esophagography in gastroesophageal reflux disease. AJR Am J Roentgenol. 2016;206(6):1093-1103. DOI:10.2214/AJR.15.15754
- Nguyen AD, Carlson DA, Patel A, Gyawali CP. AGA Clinical Practice Update on Incorporating Functional Lumen Imaging Probe Into Esophageal Clinical Practice: Expert Review. Gastroenterology. 2025;169:726-736.
- Carlson DA, Pandolfino JE, Yadlapati R, Vela MF, Spechler SJ, Schnoll-Sussman FH, et al. A Standardized Approach to Performing and Interpreting Functional Lumen Imaging Probe Panometry for Esophageal Motility Disorders: The Dallas Consensus. Gastroenterology. 2025;168(6):1114-1127.e5. DOI:10.1053/j.gastro.2025.01.234. PubMed PMID: 39914779.
- Velanovich V. The development of the GERD-HRQL symptom severity instrument. Dis Esophagus. 2007;20(2):130-134. DOI:10.1111/j.1442-2050.2007.00658.x
- Rijnhart-De Jong HG, Draaisma WA, Smout AJ, Broeders IA, Gooszen HG. The Visick score: a good measure for the overall effect of antireflux surgery?. Scand J Gastroenterol. 2008;43(7):787-793. DOI:10.1080/00365520801935467
- Galmiche JP, Hatlebakk J, Attwood S, et al. Laparoscopic antireflux surgery vs esomeprazole treatment for chronic GERD: the LOTUS randomized clinical trial. JAMA. 2011 May 18;305(19):1969-77. DOI: 10.1001/jama.2011.626
- Du X, Hu Z, Yan C, Zhang C, Wang Z, Wu J. A meta-analysis of long follow-up outcomes of laparoscopic Nissen (total) versus Toupet (270°) fundoplication for gastro-esophageal reflux disease based on randomized controlled trials in adults. BMC Gastroenterol. 2016;16(1):88. DOI:10.1186/s12876-016-0502-8
- Bonavina L, Saino G, Lipham JC, Demeester TR. LINX® Reflux Management System in chronic gastroesophageal reflux: a novel effective technology for restoring the natural barrier to reflux. Ther Adv Gastroenterol. 2013;6(4):261-8. DOI:10.1177/1756283X13486311
- Bell RCW, Lipham JC, Louie BE, et al. Magnetic sphincter augmentation superior to proton pump inhibitors for regurgitation in a 1-year randomized trial. Clin Gastroenterol Hepatol. 2020;18(8):1736-1743.e2.
- Alicuben ET, Bell RCW, Jobe BA, Buckley FP 3rd, Smith CD, Graybeal CJ, Lipham JC. Worldwide experience with erosion of the magnetic sphincter augmentation device. J Gastrointest Surg. 2018;22(9):1442-1447. DOI:10.1007/s11605-018-3775-0
- Aiolfi A, Asti E, Bernardi D, Bonitta G, Rausa E, Siboni S, Bonavina L. Early results of magnetic sphincter augmentation versus fundoplication for gastroesophageal reflux disease: systematic review and meta-analysis. Int J Surg. 2018;52:82-8. DOI:10.1016/j.ijsu.2018.02.034
- Telem D, et al. SAGES LINX® Safety and Effectiveness Analysis. SAGES TAVAC. 2021.
- Janu P, Shoughoury AB, Venkat K, Hurwich D, Galouzis T, Siatras J, et al. Hybrid TIF: Laparoscopic Hiatal Hernia Repair (HHR) Followed Immediately by Transoral Incisionless Fundoplication (TIF) Using the EsophyX Device – Efficacy and Safety in 99 Patients in a Community Setting. Abstract No. 865.
- Choi AY, Roccato MK, Samarasena JB, Kolb JM, Lee DP, Lee RH, Daly S, Hinojosa MW, Smith BR, Nguyen NT, Chang KJ. Novel Interdisciplinary Approach to GERD: Concomitant Laparoscopic Hiatal Hernia Repair with Transoral Incisionless Fundoplication. J Am Coll Surg. 2021 Mar;232(3):309-318. DOI:10.1016/j.jamcollsurg.2020.11.021. PMID:33346082.
- Jaber F, Ayyad M, Ayoub F, Elhusseiny T, Abdelrahman A, Hammoud S, et al. Concomitant hiatal hernia repair with transoral incisionless fundoplication for the treatment of refractory gastroesophageal reflux disease: a systematic review. Surg Endosc. 2024;38(10):5528‑5540. DOI:10.1007/s00464-024-11201-2
- Gergen AK, Wagh MS, Menard-Katcher P, Pratap A. Efficacy of Combined Hiatal Hernia Repair and Transoral Incisionless Fundoplication for Giant Paraoesophageal Hernias: Technique and Early Results. Surg Laparosc Endosc Percutan Tech. 2022 Jun;32(3):404-8.
- Faria I, Isik A, Salem A, Piazzi F, Salem YH. Concomitant Transoral Incisionless Fundoplication Outcomes and Efficacy for Gastroesophageal Reflux Disease: A Retrospective Analysis. Am J Gastroenterol. 2022 Oct;117(10S):e779. DOI: 10.14309/01.ajg.0000860936.27185.e8
- Forssell S, Bredenoord AJ. The RefluxStop™ device: safety and efficacy at 6 – 12 months. World J Surg. 2021;45(1):72-79
- Feka J, Saad M, Boyle N, Paireder M, Kristo I, Rieder E, Asari R, Schoppmann SF. Multicentric short term and safety study of ineffective esophageal motility patients treated with RefluxStop device. Sci Rep. 2024;14(1):15425. DOI:10.1038/s41598-024-65751-5
- Rodríguez L, Rodriguez P, Gómez B, Ayala JC, Oxenberg D, Perez-Castilla A, et al. Two-year results of intermittent electrical stimulation of the lower esophageal sphincter treatment of gastroesophageal reflux disease. Surgery. 2015 Mar;157
(3):556-67. - Hoppo T, Rodríguez L, Soffer E, Crowell MD, Jobe BA. Long-term results of electrical stimulation of the lower esophageal sphincter for treatment of proximal GERD. Surg Endosc. 2014 Dec;28(12):3293-3301
- Duke MC, Farrell TM. Surgery for Gastroesophageal Reflux Disease in the Morbidly Obese Patient. J Laparoendosc Adv Surg Tech. 2016;27(1). DOI:10.1089/lap.2016.29013.mcd
- Pauwels A, Boecxstaens V, Andrews CN, et al. How to select patients for antireflux surgery? The ICARUS guidelines (international consensus regarding preoperative examinations and clinical characteristics assessment to select adult patients for antireflux surgery). Gut. 2019;68(11):1928-1941. DOI: 10.1136/gutjnl-2019-318260
- Felsenreich DM, Kefurt R, Schermann M, Beckerhinn P, Kristo I, Krebs M, Prager G, Langer FB. Reflux, Sleeve Dilation, and Barrett’s Esophagus after Laparoscopic Sleeve Gastrectomy: Long-Term Follow-Up. Obes Surg. 2017. DOI:10.1007/s11695-017-2748-9
- Carroll R, Fontan F, Lehmann R, Smith J, Nau P. Laparoscopic Roux-en-Y gastric bypass for the management of hiatal hernia and failed fundoplication in patients with obesity. Ann Laparosc Endosc Surg. 2021;6:23. DOI:10.21037/ales-20-75
Correspondencia: Alejandro Nieponice
Correo electrónico: anieponi@ffavaloro.org
Acta Gastroenterol Latinoam 2025;55(4):317-329
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE



