Karla Rocío García-Zermeño1 ID· Jorge E. Aquino-Matus2 ID· Joanna Jiménez Pavón3 ID· José María Remes-Troche4 ID
1 Centro Integral de Gastroenterología y Motilidad Avanzada (CIGMA), Boca del Río, Veracruz, México.
2 Hospital Médica Sur, Unidad de Enfermedades Digestivas y Obesidad, Ciudad de México, México.
3 Departamento de Farmacogenética, Instituto Nacional de Psiquiatría Ramón de la Fuente Muñiz, Ciudad de México, México.
4 Laboratorio de Fisiología Digestiva y Motilidad Gastrointestinal. Instituto de Investigaciones Médico-Biológicas, Universidad Veracruzana, Veracruz, México.
Acta Gastroenterol Latinoam 2025;55(4):303-316
Recibido: 17/09/2025 / Aceptado: 03/11/2025 / Publicado online: 23/12/2025 / https://doi.org/10.52787/agl.v55i4.533
Resumen
Los neuromoduladores se han convertido en una herramienta fundamental dentro de la gastroenterología moderna, especialmente en los trastornos de la interacción cerebro-intestino. Originalmente desarrollados para el manejo de trastornos psiquiátricos, estos fármacos han demostrado capacidad para modular el dolor visceral, la hipersensibilidad intestinal y la motilidad digestiva, actuando a través de mecanismos centrales y periféricos. Entre los neuromoduladores más utilizados se encuentran los antidepresivos tricíclicos, efectivos en la reducción del dolor abdominal; los inhibidores selectivos de la recaptación de serotonina, útiles en pacientes con ansiedad o depresión como comorbilidades; y los inhibidores de la recaptación de serotonina-noradrenalina, empleados en cuadros de dolor visceral con características neuropáticas. Otros fármacos como los gabapentinoides, la mirtazapina, la buspirona y ciertos antipsicóticos también han mostrado beneficios en fenotipos específicos. La selección del fármaco depende del perfil clínico del paciente, de sus comorbilidades, su tolerancia y del riesgo de efectos adversos, especialmente en pacientes ancianos y polimedicados. El manejo de los neuromoduladores se caracteriza por el uso de dosis iniciales bajas con incrementos graduales y el seguimiento cercano del paciente. Además, se recomienda un abordaje multidisciplinario que integre intervenciones no farmacológicas como la terapia cognitivo-conductual, la hipnoterapia dirigida al intestino y programas de mindfulness. Esta combinación potencia la eficacia clínica, reduce el estigma y mejora la calidad de vida, consolidando a los neuromoduladores como parte esencial del tratamiento integral de los trastornos de la interacción cerebro-intestino.
Palabras claves. Neuromoduladores, trastornos de la interacción cerebro intestino, microbiota, antidepresivos, tricíclicos.
The Usefulness of Neuromodulators in Clinical Practice: The Gastroenterologist’s Viewpoint
Summary
Neuromodulators have become a fundamental tool in modern gastroenterology, particularly for disorders involving brain-gut interaction. Originally developed for the management of psychiatric disorders, these drugs have demonstrated the ability to modulate visceral pain, intestinal hypersensitivity, and gastrointestinal motility, acting through both central and peripheral mechanisms. The most widely used neuromodulators included tricyclic antidepressants, which are effective in reducing abdominal pain; selective serotonin reuptake inhibitors, which are useful for patients with comorbid anxiety or depression; and serotonin–norepinephrine reuptake inhibitors, which are used for visceral pain with neuropathic features. Other drugs, such as gabapentinoids, mirtazapine, buspirone, and certain antipsychotics, have also shown benefits in specific phenotypes. Drug selection depends on the patient´s clinical profile, comorbidities, tolerability, and risk of adverse effects, particularly for elderly and polymedicated patients. Neuromodulator management is characterized by the use of low initial doses with gradual increases and close patient monitoring. In addition, a multidisciplinary approach integrating non-pharmacological interventions such as cognitive-behavioral therapy, gut-directed hypnotherapy, and mindfulness-based programs, is recommended. This combination enhances clinical effectiveness, reduces stigma, and improves quality of life, consolidating neuromodulators as an essential part of the comprehensive treatment of disorders of brain-gut interaction.
Keywords. Neuromodulators, brain-gut interaction disorders, microbiota, antidepressants, tricyclics.
Introducción
En el contexto gastroenterológico, los neuromoduladores se definen como un grupo heterogéneo de fármacos con actividad psicotrópica primaria (antidepresiva, ansiolítica o antipsicótica) que han sido reapropiados para su uso en gastroenterología, debido a su capacidad para regular el procesamiento del dolor visceral, la sensibilidad y la motilidad gastrointestinales.1 Estos agentes incluyen principalmente a los antidepresivos tricíclicos (ATC), los inhibidores selectivos de la recaptación de serotonina (ISRS), los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), los antiepilépticos con propiedades neuromoduladoras, como los gabapentinoides, y, en casos seleccionados, algunos antipsicóticos.1, 2
El eje intestino-cerebro constituye una red compleja de comunicación bidireccional que integra señales neurales, endocrinas, inmunitarias y metabólicas entre el sistema nervioso central y el sistema nervioso entérico.3 Esta comunicación multimodal involucra vías vagales, simpáticas, el eje hipotálamo-hipófisis-adrenal, citocinas proinflamatorias y productos derivados de la microbiota intestinal, todos los cuales influyen de manera significativa en la función gastrointestinal, la percepción visceral y la respuesta inmunitaria local.3, 4
La relevancia clínica del eje intestino-cerebro radica en su papel central en la fisiopatología de múltiples trastornos gastrointestinales, tanto funcionales como orgánicos. Las alteraciones en esta comunicación bidireccional pueden resultar en hipersensibilidad visceral, dismotilidad, alteraciones en la permeabilidad de la barrera mucosa y activación de respuestas neuroinflamatorias que caracterizan a los trastornos de la interacción cerebro intestino (TICI).3, 4, 5 Además, este eje explica la alta prevalencia de comorbilidad psiquiátrica observada en pacientes con trastornos gastrointestinales, en quienes la ansiedad y la depresión no solo coexisten, sino que pueden exacerbar los síntomas digestivos a través de mecanismos neurobiológicos compartidos.
El presente artículo tiene como objetivo principal proporcionar una revisión integral de la utilidad clínica de los neuromoduladores en la práctica gastroenterológica contemporánea, desde la perspectiva específica del gastroenterólogo clínico. El alcance de esta revisión incluye la evaluación de la eficacia clínica de los diferentes grupos de neuromoduladores en las principales indicaciones gastroenterológicas, el análisis de los perfiles de seguridad y tolerabilidad, las consideraciones para la selección individualizada del tratamiento, y las estrategias de monitoreo y seguimiento. Asimismo, se abordará la perspectiva psiquiátrica reconociendo la importancia del manejo multidisciplinario en algunos pacientes.
La importancia del eje intestino-cerebro
El eje intestino-cerebro (EIC) es una red de comunicación bidireccional que integra el sistema nervioso central (SNC), el sistema nervioso entérico (SNE), el sistema neuroendocrino, el sistema inmune y la microbiota (Figura 1). El SNE es un sistema autónomo con entre 400 y 600 millones de neuronas. A diferencia de otros órganos periféricos, el tracto digestivo posee un entramado neuronal intrínseco capaz de coordinar sus funciones, incluso sin influencia directa del SNC. Estas neuronas se agrupan en dos plexos principales: el mientérico, encargado de la motilidad y el peristaltismo; y el submucoso, responsable de la regulación de la secreción, la absorción y la microcirculación. El SNE cumple funciones esenciales para la homeostasis gastrointestinal: regula la motilidad mediante patrones de contracción y relajación, controla la secreción y absorción de agua y electrolitos, ajusta el flujo sanguíneo local y participa en la integración neuroinmune y neuroendocrina, en estrecha interacción con mastocitos, linfocitos y células enteroendocrinas. Además, contiene circuitos reflejos completos que permiten respuestas autónomas a estímulos mecánicos y químicos, lo que explica cómo el intestino mantiene actividad coordinada incluso en ausencia de control central.6
Figura 1. Esquema del eje intestino-cerebro y sus principales mecanismos de comunicación
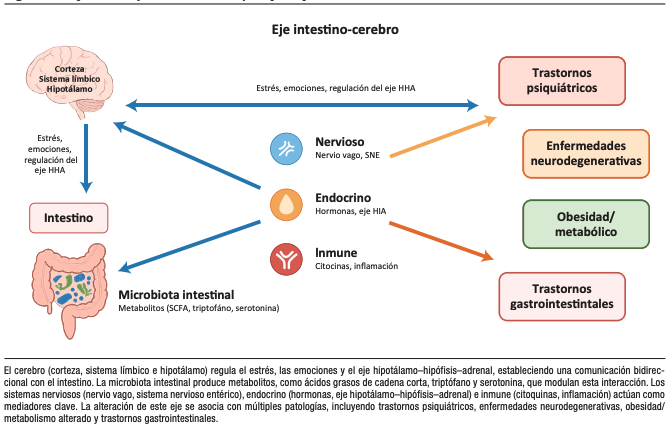
Una característica importante es la diversidad neuroquímica. Las neuronas entéricas utilizan neurotransmisores como acetilcolina, serotonina, óxido nítrico, polipéptido intestinal vasoactivo (VIP), ácido gamma-aminobutírico (GABA), entre otros, lo que explica por qué fármacos diseñados para el SNC pueden modular motilidad, sensibilidad y secreción a nivel digestivo. Esta base neurobiológica sustenta el uso de neuromoduladores como herramientas terapéuticas en los TICI.7
Por otra parte, la microbiota intestinal contribuye a la homeostasis del EIC. Sus metabolitos, como ácidos grasos de cadena corta, indoles, ácidos biliares secundarios, GABA y serotonina, actúan sobre células enteroendocrinas, neuronas entéricas y fibras vagales. Se ha demostrado, por ejemplo, que la ausencia de microbiota, como se observa en modelos axénicos, produce alteraciones en el desarrollo neurológico e inmune y aumenta la sensibilidad visceral a la distensión colónica. La colonización con microbiota específica puede revertir estas alteraciones y modular la ansiedad, confirmando el carácter bidireccional del EIC.8, 9 En humanos, múltiples estudios han mostrado que los pacientes con síndrome de intestino irritable (SII) presentan disbiosis, caracterizada por menor diversidad microbiana, reducción de géneros como Bifidobacterium y Lactobacillus e incremento de bacterias proinflamatorias. Estas alteraciones se asocian con activación mastocitaria y liberación de mediadores inflamatorios, contribuyendo a la hipersensibilidad visceral.10
Neurobiología compartida entre los trastornos de la interacción cerebro-intestino y los trastornos del ánimo
Como se mencionó previamente, la interconexión a lo largo del eje cerebro-intestino es una red bidireccional que integra los sistemas neuronales entérico y autonómico, el sistema neuroendocrino hipotálamo-hipófisis-adrenal (HPA) y la señalización inmune. Para fines prácticos podemos dividir los mecanismos neurobiológicos compartidos entre TICI y los trastornos del ánimo en cinco mecanismos fisiopatológicos:
a) Dismetabolismo de neurotransmisores (serotonina, GABA, noradrenalina, dopamina y glutamato).
La microbiota intestinal modula de forma directa e indirecta la síntesis, liberación y recaptación de neurotransmisores clave como serotonina, GABA y glutamato, lo que repercute en la motilidad intestinal, la sensibilidad visceral y el estado afectivo. Cerca del 95% de la serotonina corporal se produce en el intestino (células enterocromafines y neuronas entéricas), de modo que cualquier cambio en la biosíntesis periférica o en la disponibilidad de su precursor, el triptófano, tiene consecuencias centrales y viscerales: la derivación del triptófano hacia la vía de la quinurenina, favorecida por la presencia de inflamación y estrés crónico, se asocia con depresión, ansiedad e hipersensibilidad visceral.11, 12 Además, metabolitos microbianos como los ácidos grasos de cadena corta (AGCC) modulan la excitabilidad neuronal y la expresión de receptores, afectando circuitos de dolor y afecto.13, 14, 15
b) Disfunción del eje hipotálamo-hipófisis-adrenal y respuesta al estrés crónico.
La activación sostenida del eje HPA por estrés crónico incrementa la liberación sostenida de cortisol, reduce la concentración de factor neurotrófico derivado del cerebro (BDNF) y, por lo tanto, altera la plasticidad sináptica por lo que favorece los procesos neuronales que nos permiten percibir el estado interno del cuerpo (interocepción), facilitando la hipervigilancia somática y la hipersensibilidad visceral.13, 14 El estrés, además, induce disbiosis y aumenta la permeabilidad intestinal, retroalimentando la hiperactividad del eje HPA y amplificando la nocicepción visceral. Este marco mecanicista orienta al uso de neuromoduladores con efecto ansiolítico/antiestrés (ISRS/IRSN, buspirona), y a combinarlos con intervenciones mente‑intestino (psicoterapia focalizada en síntomas gastrointestinales, respiración diafragmática e higiene del sueño). Fármacos como trazodona o mirtazapina pueden ser útiles cuando el insomnio y la activación simpática perpetúan el círculo vicioso.
c) Inflamación sistémica y neuroinflamación.
La disbiosis y el aumento de la permeabilidad intestinal permiten el paso de señales microbianas (por ej., lipopolisacáridos) al torrente sanguíneo, activando respuestas inmunes que, a través de citoquinas y tráfico celular, impactan la permeabilidad de la barrera hematoencefálica, generando neuroinflamación con activación microglial.16, 17 Este eje inmune-cerebral contribuye a la aparición de síntomas neuropsiquiátricos como anhedonia, ansiedad, alteraciones cognitivas e hipersensibilidad visceral. El desequilibrio entre los linfocitos Th17 productores de interleucinas proinflamatorias IL-17, IL-22 e IL-23 y las células T reguladoras (Treg) parece desempeñar un papel relevante en la perpetuación de la inflamación sistémica de bajo grado.16, 17, 18 Hay evidencia sólida que respalda una relación bidireccional entre la inflamación de bajo grado y la depresión.19 Numerosos estudios han demostrado que un subconjunto de personas con trastorno depresivo mayor (TDM) presenta niveles elevados de marcadores inflamatorios periféricos, como la proteína C reactiva (PCR), la interleucina-6 (IL-6) y el factor de necrosis tumoral alfa (TNF-α).20, 21, 22, 23 Este estado inflamatorio no es universal en todos los pacientes que cursan con un TDM, sino un perfil sintomático específico. En particular, se asocia a la presencia de síntomas físicos y cognitivos (por ej., fatiga, problemas del sueño, pérdida de energía/astenia, anhedonia) más que a síntomas puramente emocionales (por ej., desesperanza, temor, tristeza).
La relación también es bidireccional: la propia depresión puede promover respuestas inflamatorias, generando un ciclo que se autoperpetúa, caracterizado por síntomas gastrointestinales y disbiosis que complican tanto la evolución de la enfermedad como el tratamiento.
d) Papel del nervio vago
El nervio vago constituye la principal autopista bidireccional entre intestino y cerebro, integrando señalización mecánica y quimiosensorial, así como la vía antiinflamatoria colinérgica.24 Modelos preclínicos muestran que la interrupción vagal atenúa la transferencia de fenotipos depresivos tras trasplante fecal, lo que subraya su papel en traducir señales microbianas e inmunes a cambios conductuales y viscerales.25 En clínica, el objetivo es aumentar el tono vagal mediante técnicas respiratorias, biofeedback y psicoterapia centrada en interocepción, y considerar, en casos seleccionados, neuromodulación no invasiva (por ej., estimulación transcutánea del vago) como adyuvante; la farmacoterapia neuromoduladora puede sinergizar con estas intervenciones al reducir la hiperreactividad central.
e) Ácidos grasos de cadena corta: acetato, propionato y butirato
Los AGCC, productos de la fermentación de fibra por la microbiota, ejercen efectos tróficos y epigenéticos en el sistema nervioso central, aumentando BDNF, reforzando la integridad de la barrera hematoencefálica y modulando la expresión de receptores y la excitabilidad neuronal. El butirato destaca por su capacidad de actuar como inhibidor de histona desacetilasas.18 Niveles reducidos de AGCC se han asociado con depresión e inflamación de bajo grado, ofreciendo un nexo plausible entre dieta, microbiota y síntomas afectivos y viscerales. En términos terapéuticos, esto respalda intervenciones dietéticas ricas en fibra y, de forma selectiva, el uso de probióticos/prebióticos como coadyuvantes. También ayuda a explicar por qué dosis bajas de ATC o IRSN pueden mejorar el dolor, al actuar sobre la modulación central de la sensibilidad.
Los TICI comparten tres mecanismos fisiopatológicos claves: la hipersensibilidad visceral, la dismotilidad, y las alteraciones a nivel del SNC/SNE. En la Figura 2, se representan todos los TICI de acuerdo con los criterios de Roma IV. Los estudios epidemiológicos más recientes muestran que más del 40% de la población mundial presenta al menos un diagnóstico de este espectro, con un impacto significativo en la calidad de vida y en los costos en salud. Es importante recordar que Roma IV marcó un giro conceptual al reconocer las alteraciones del EIC como origen de los síntomas digestivos.26 Actualmente están en desarrollo los criterios de Roma V que, sin duda, pondrán mayor énfasis sobre el EIC y los TICI.
Figura 2. Trastornos de la interacción cerebro-intestino de acuerdo con los criterios de Roma IV
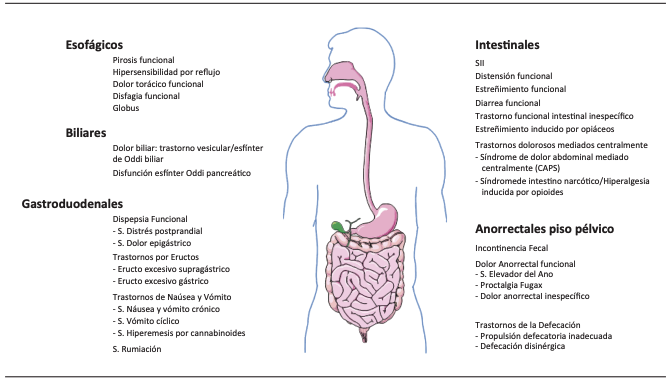
¿Por qué usar neuromoduladores en gastroenterología?
La justificación científica para el uso de neuromoduladores en gastroenterología se fundamenta en múltiples mecanismos de acción que abordan los componentes centrales y periféricos involucrados en la patogénesis de los TICI.2 A nivel central, estos fármacos modulan el procesamiento del dolor visceral a través de la modificación de neurotransmisores clave como serotonina, noradrenalina y GABA, alterando las vías descendentes de inhibición del dolor y reduciendo la hipervigilancia central característica de estos trastornos.1, 2
A nivel periférico, los neuromoduladores ejercen efectos directos sobre la motilidad gastrointestinal y los umbrales de percepción visceral. Los ATC, por ejemplo, pueden reducir la frecuencia de las contracciones intestinales y aumentar los umbrales de dolor visceral, mientras que los ISRS pueden normalizar patrones de motilidad alterados, a través de su acción sobre los receptores serotoninérgicos entéricos.2, 10 Adicionalmente, estos fármacos pueden influir en las respuestas neuroinmunes locales, modulando la liberación de citocinas proinflamatorias y la activación de mastocitos, procesos que contribuyen a la sensibilización visceral. La presencia frecuente de comorbilidad psiquiátrica en pacientes con TICI proporciona una justificación adicional para el uso de neuromoduladores, ya que un solo agente puede abordar simultáneamente los síntomas gastrointestinales y las manifestaciones psiquiátricas asociadas, mejorando la adherencia terapéutica y la calidad de vida global del paciente.8, 11
Neuromoduladores
Mecanismos de acción de los neuromoduladores
Los neuromoduladores ejercen sus efectos mediante mecanismos tanto centrales como periféricos (Tabla 1), actuando a través de diversas vías moleculares y celulares para regular la función y actuar sobre los mecanismos fisiopatológicos compartidos.
Tabla 1. Diferencias entre los mecanismos de acción de los neuromoduladores
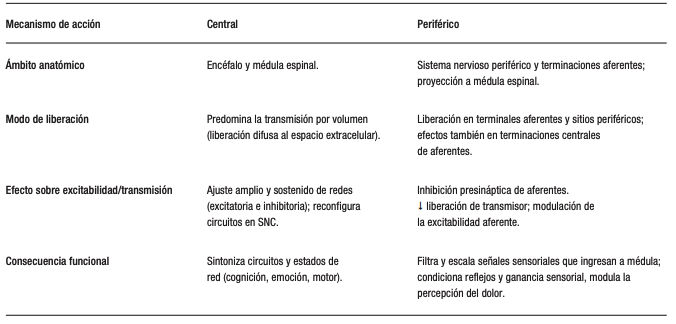
Mecanismos centrales: comprenden la modulación de la transmisión sináptica y de la excitabilidad neuronal en el encéfalo y la médula espinal, mediada principalmente por receptores acoplados a proteínas G (RCPG), que inician cascadas de señalización intracelular capaces de modificar la excitabilidad neuronal, la plasticidad sináptica y la liberación de neurotransmisores.
Mecanismos periféricos: incluyen la modulación de la excitabilidad de las fibras aferentes y de la transmisión sináptica en el sistema nervioso periférico y la médula espinal. Monoaminas como la serotonina, la dopamina y la noradrenalina pueden regular la neurotransmisión de las aferencias primarias modulando la inhibición presináptica, en particular mediante la despolarización aferente primaria, que reduce la liberación de transmisor desde las aferencias sensoriales. Este proceso está mediado por la activación de canales iónicos y receptores metabotrópicos, lo que conduce a una modulación global de la entrada sensorial a la médula espinal, modulando la percepción del dolor y requiriendo menores concentraciones para su activación.
Clasificación de acuerdo con su clase terapéutica
a) Antidepresivos tricíclicos (ATC)
Los ATC, como amitriptilina, nortriptilina o imipramina, son los neuromoduladores más estudiados en los TICI. Su acción combina la inhibición de la recaptación de serotonina y noradrenalina, potenciando las vías inhibitorias del dolor, y un efecto anticolinérgico periférico que retarda el tránsito intestinal, útil en síndrome de intestino irritable con diarrea (SII-D).1, 2 Un metaanálisis ha confirmado su eficacia sobre el dolor abdominal y los síntomas globales, con un número necesario a tratar (NNT) de cuatro.29 El ensayo ATLANTIS estableció a la amitriptilina como segunda línea de tratamiento en el SII refractario, con beneficios sostenidos a seis meses.30
b) Inhibidores selectivos de recaptación de serotonina (ISRS)
Los ISRS (sertralina, citalopram, escitalopram, paroxetina y fluoxetina) cumplen un rol distinto. Su efecto predominante es ansiolítico y antidepresivo, con un impacto indirecto en la percepción de los síntomas. Aceleran el tránsito intestinal, lo que los hace más útiles en síndrome de intestino irritable con estreñimiento (SII-E) y en pacientes con comorbilidad emocional. Aunque su efecto analgésico visceral es limitado en comparación con los ATC, mejoran el bienestar global y reducen la hipervigilancia y la catastrofización, factores claves en la percepción del paciente.1, 2
c) Inhibidores de recaptación de serotonina-noradrenalina (IRSN)
Los IRSN (duloxetina, venlafaxina) ejercen un bloqueo dual equilibrado. Aunque la evidencia en TICI es menor que con ATC, estudios preliminares y experiencia clínica muestran beneficios en dolor abdominal funcional (DAF) con comorbilidad ansioso-depresiva. La duloxetina, además, cuenta con amplio respaldo en dolor neuropático, lo que apoya su uso en fenotipos de dolor central.1, 2
d) Gabaérgicos
Los gabaérgicos o delta ligandos (gabapentina, pregabalina) disminuyen la excitabilidad neuronal al actuar sobre canales de calcio. Son eficaces en dolor neuropático, y en gastroenterología han mostrado resultados alentadores en dispepsia funcional (DF) y DAF al reducir la hiperalgesia visceral en pacientes refractarios a ATC o ISRS. Su uso se limita por mareo, somnolencia y la falta de ensayos clínicos de gran escala.1, 2
e) Otros neuromoduladores
Algunos fármacos específicos han mostrado utilidad en fenotipos particulares. Los agonistas 5-HT1A (buspirona, tandospirona) favorecen la relajación del fundus y la acomodación gástrica. La buspirona ha demostrado eficacia en el síndrome de distrés posprandial,30, 31, 32 mientras que la tandospirona ha mostrado resultados preliminares en DF y ansiedad asociada. Entre los tetracíclicos, la mirtazapina es útil en DF con saciedad precoz, náuseas, pérdida de peso y ansiedad, y la trazodona se ha utilizado en dolor torácico funcional con insomnio y ansiedad.33 Los antipsicóticos atípicos (levosulpirida, olanzapina, quetiapina) se emplean en contextos seleccionados: la levosulpirida como procinético en DF, y olanzapina o quetiapina como coadyuvantes en hipervigilancia o SMP.1,2, 30 Entre los anticonvulsivantes, el baclofeno (agonista GABA-B) reduce eructos supragástricos y rumiación. Otros fármacos, como topiramato y levetiracetam, se han estudiado en dolor visceral, síndrome del vómito cíclico y dolor torácico funcional, con resultados preliminares.1, 2
¿Cómo elegir el neuromodulador según el fenotipo y las comorbilidades?
La elección del neuromodulador en adultos con TICI debe fundamentarse en el fenotipo clínico predominante de acuerdo con la clasificación de ROMA IV, las comorbilidades tanto orgánicas como neuropsiquiátricas, los riesgos y las preferencias del paciente.2, 34
Los neuromoduladores tienen diversos efectos gastrointestinales sobre el dolor y la motilidad, así como efectos adversos e interacciones farmacológicas a considerarse en poblaciones de riesgo. Los ATC en dosis bajas y nocturnas son la primera línea en los pacientes con hipersensibilidad visceral; los ISRS son útiles en pacientes con ansiedad/depresión pero su efecto analgésico suele ser menor; los IRSN suelen prescribirse en pacientes con dolor neuropático y/o comorbilidad con fibromialgia, y la mirtazapina es la primera opción en cuadros asociados a insomnio, náuseas y pérdida de peso por hiporexia.1
En la Tabla 2 se resume la clasificación y los enfoques terapéuticos para los TICI en adultos, con énfasis en los neuromoduladores de primera línea y en los coadyuvantes.
Tabla 2. Clasificación y enfoques terapéuticos para los trastornos de la interacción cerebro-intestino en adultos

Asimismo, los neuromoduladores de acción central deben evitarse en algunos síntomas o síndromes de acuerdo con su perfil de efectos adversos. Los ISRS, IRSN, bupropión y topiramato deben evitarse en síndromes de náusea o vómito crónico. Los ATC y paroxetina pueden exacerbar el estreñimiento en pacientes con estreñimiento funcional o SII-E, y la mayoría de ISRS (excepto paroxetina) pueden empeorar la diarrea en pacientes con diarrea funcional o SII-D.31
En pacientes con hepatopatía crónica se suele evitar o ajustar la duloxetina, y en pacientes con enfermedad renal crónica se deben ajustar los delta-ligandos debido a un mayor riesgo de somnolencia. Los pacientes con sobrepeso u obesidad no son candidatos para mirtazapina, olanzapina o quetiapina, debido al incremento de peso clínicamente significativo.35
Interacciones farmacológicas
Las interacciones farmacológicas, especialmente en pacientes con polifarmacia, conllevan una baja tolerancia y el abandono del tratamiento, así como efectos adversos potencialmente letales, por lo que una prescripción responsable con un seguimiento estrecho del paciente mejora los desenlaces del tratamiento y la seguridad del paciente.
La interacción de los ATC con el citocromo CYP2D6 incrementa los niveles de fluoxetina, paroxetina y bupropión, con mayor riesgo de efectos anticolinérgicos y prolongación del intervalo QT. La interacción de los macrólidos, azoles y jugo de toronja con el citocromo CYP3A4 incrementa los niveles de buspirona. Combinar los ISRS/IRSN/TCA con triptanos, linezolid, inhibidores de monoamino-oxidasa (IMAO), tramadol o dextrometorfano puede precipitar el síndrome serotoninérgico. Los opioides y benzodiacepinas no se recomiendan en el manejo de los TICI, y los efectos sedativos pueden exacerbarse con los delta-ligandos.
El intervalo QT puede prolongarse con la combinación de escitalopram o citalopram con ATC, especialmente en mayores de 60 años, con alteraciones hidroelectrolíticas, hepatopatía crónica u otros fármacos que prolongan el intervalo QT (haloperidol, quetiapina, azitromicina, antihistamínicos, ondansetrón). Se recomienda tener un electrocardiograma basal antes de iniciar estos neuromoduladores.
Los ISRS incrementan el riesgo de hemorragia del tubo digestivo en pacientes que además consumen antiinflamatorios no esteroideos (AINEs) o aspirina. En un metaanálisis de once estudios que incluyó a 82605 pacientes, la tasa de sangrado fue mayor en el grupo de usuarios de ISRS/AINEs en comparación con ISRS (36,9% vs. 22,8%; RM 2,14, IC95% 1,52 – 3,02, p < 0,001). A su vez, se evidenció un mayor riesgo de sangrado en el grupo de usuarios ISRS/AINES en comparación con únicamente AINEs (40,9% vs. 34,2%; RM 1,49, IC 95% 1,20 – 1,84, p < 0,001).36 Dado el mayor riesgo de sangrado con el uso concomitante de AINEs e ISRS, se debe tener especial precaución al administrarlos en conjunto y valorar el uso de IBP o P-CAB como profilaxis, especialmente en pacientes con mayor riesgo de sangrado gastrointestinal.
Edad y perfil del paciente
En ancianos, para elegir un neuromodulador deben considerarse los riesgos propios del envejecimiento con respecto a la farmacocinética y la farmacodinámica, la vía de administración, las comorbilidades y la polifarmacia, para mejorar la tolerancia y reducir los efectos adversos.37 La estrategia de iniciar bajo y e ir lento (“start low, go slow”) cobra mayor relevancia en el paciente anciano, y se recomienda iniciar con la mitad o un cuarto de la dosis, con incrementos cada dos a cuatro semanas, con estrecha vigilancia de los efectos anticolinérgicos.1 En el caso de requerir ATC y de encontrarse disponibles en el mercado local, se prefiere nortriptilina o desipramina sobre amitriptilina.
En el análisis post hoc del estudio ATLANTIS que aleatorizó a pacientes con SII a amitriptilina contra placebo, se observó una diferencia cuantitativa en la efectividad en pacientes mayores de 50 años en el puntaje IBS-SSS (IBS Severity Scoring System) (DM – 46,5; IC 95% -74,2 a -18,8; p = 0,0010) y un alivio global subjetivo (RM 2,59; IC95% 1,47 a 4,55; p = 0,0010).38
La hiponatremia relacionada a ISRS/IRSN es más frecuente en ancianos y con el uso concomitante de diuréticos, por lo que se deben monitorizar los electrolitos séricos regularmente de acuerdo con la evolución clínica.
Manejo y seguimiento de la neuromodulación farmacológica
Inicio y ajuste de dosis
El principio de «iniciar bajo e ir lento» se aplica en todos los pacientes, para alcanzar una mayor tolerancia de los efectos adversos y un mayor apego al tratamiento.1, 34, 39
Los ATC se inician con dosis bajas nocturnas y se titulan cada 1 a 2 semanas de acuerdo con la respuesta y los efectos adversos (por ej., amitriptilina 12,5 mg por la noche, con incrementos de 6,25 a 12,5 mg cada 1 a 2 semanas hasta alcanzar 25 a 50 mg al día, incluso dividido en dos tomas).
Los ISRS suelen exacerbar los síntomas de ansiedad durante las primeras dos semanas, por lo que se recomienda indicarlos por la mañana (por ej., sertralina 25 mg por la mañana, con incrementos de 12,5 a
25 mg cada 1 a 2 semanas hasta alcanzar 50 a 100 mg por día). Por su parte, los IRSN en pacientes con dolor neuropático, comorbilidad afectiva relevante o fibromialgia también se prescriben por la mañana (por ej., duloxetina 30 mg por la mañana, con incremento hasta 60 mg en 1 a 2 semanas).
En pacientes con insomnio, náusea posprandial o pérdida ponderal importante, la mirtazapina (antidepresivo tetracíclico) o los antipsicóticos (olanzapina y quetiapina) suelen ser de utilidad (por ej., mirtazapina 7,5 mg por la noche, con incremento de 7,5 mg cada 1 a 2 semanas hasta alcanzar 15 a 30 mg cada noche). Por último, los delta-ligandos en pacientes con dolor neuropático suelen prescribirse por la noche debido a su efecto sedante (por ej., gabapentina 100 mg por la noche, con incrementos de 100 a 300 mg cada 1 a 2 semanas hasta alcanzar 300-600 mg hasta cada 8 horas).
Al suspender los ATC/ISRS/IRSN, se recomienda reducir gradualmente la dosis (por ej., 10%-25% cada 1 a 2 semanas) para minimizar los síntomas relacionados con el síndrome de descontinuación (mareo, insomnio, irritabilidad y parestesias).40
Tiempo hasta respuesta terapéutica
La analgesia visceral de los TCA se observa a las 2 a 4 semanas, con respuesta global a las 6 a 8 semanas, y la titulación flexible de acuerdo con respuesta clínica ha demostrado beneficios sostenidos. En el estudio ATLANTIS, que aleatorizó a 463 pacientes con SII a amitriptilina a dosis bajas (10 mg con titulación cada 3 semanas hasta 30 mg por día) o placebo por 6 meses, se observó una mayor reducción con amitriptilina en el IBS-SSS (-27,0; IC95% -46,9 a -7,109; p = 0,0079).30 Los ISRS/IRNS mejoran los síntomas afectivos incluso antes que la analgesia visceral entre 4 y 8 semanas, y se potencian con otras intervenciones no farmacológicas.
Monitoreo de efectos adversos
Antes de iniciar los neuromoduladores se recomienda realizar electrocardiograma en reposo si hay factores de riesgo para QT prolongado, investigar electrolitos en pacientes de riesgo (por ej., enfermedad renal crónica), presión arterial (por ej., IRNS) y pruebas hepáticas (por ej., duloxetina).
Una buena práctica clínica consiste en agendar una primera consulta en 2 a 4 semanas para evaluar tolerabilidad y ajustar el neuromodulador, seguido de una nueva consulta en 6 a 8 semanas para evaluar la respuesta clínica.1, 34, 39
Estrategias para mejorar la adherencia
La definición de los objetivos terapéuticos, la explicación de la latencia terapéutica y el plan de titulación reduce las expectativas irreales y mejoran el cumplimiento del tratamiento. Las revisiones de seguimiento cada 2 a 4 semanas para ajustar dosis y tratar los efectos adversos, y cada 6 a 8 semanas para evaluar la respuesta clínica suelen sostener la adherencia. Las habilidades de comunicación bidireccional entre el médico y el paciente mejoran la comprensión y lo involucran en el tratamiento, favoreciendo la adherencia.1 La comunicación médico-paciente efectiva y un plan escrito de manejo de efectos adversos y datos de alarma incrementan significativamente la adherencia.41
¿Qué hacer cuando los neuromoduladores no funcionan?
Modelo de atención interdisciplinaria
Para un adecuado abordaje interdisciplinario, antes de la referencia del paciente desde gastroenterología a un especialista en salud mental, se le debe explicar el modelo cerebro‑intestino de modo accesible, subrayando que las intervenciones psicológicas actúan sobre circuitos fisiológicos del dolor y de la interocepción y no constituyen una “psiquiatrización” del cuadro.
La validación del sufrimiento, la psicoeducación sobre la interocepción y la coordinación entre gastroenterología y salud mental son pilares para reducir el uso ineficiente de servicios y mejorar resultados. La explicación al paciente debe enfatizar que los neuromoduladores no “psiquiatrizan” su caso ni “tapan” los síntomas, sino que reequilibran circuitos que conectan el intestino y el cerebro, responsables de la sensibilidad, el dolor y la interocepción. Esa psicoeducación reduce el estigma, mejora la adherencia e incrementa la probabilidad de éxito terapéutico.
La referencia a un psiquiatra se deberá contemplar en casos en los que se detecte comorbilidad con trastornos del afecto o ansiedad –en especial de gravedad moderada a severa–, ante la sospecha de otros trastornos psiquiátricos –como trastornos de la conducta alimentaria o trastorno obsesivo compulsivo–, y en caso de necesitar combinar neuromoduladores de acción periférica con otros de acción central.
La comunicación clínica empática, las metas compartidas y la coordinación entre gastroenterología, psicología y psiquiatría son determinantes del éxito sobre los TICI y sus comorbilidades.
Criterios para derivación a psiquiatría
Se recomienda manejar en conjunto con psiquiatría cuando exista:1–3
• Depresión moderada–severa, riesgo suicida, trastorno de pánico grave o trastorno de estrés postraumático.
• Sospecha de trastorno bipolar o historia personal/familiar de viraje maníaco/hipomaníaco.
• Psicosis, ideación suicida activa o uso problemático de sustancias.
• Refractariedad tras tratamientos adecuados (dosis/tiempo) o polifarmacia compleja.
• Eventos adversos significativos (prolongación marcada del intervalo QT, síndrome serotoninérgico) o comorbilidad psiquiátrica que requiera optimización farmacológica específica.
Intervenciones no farmacológicas basadas en psicoterapia
La terapia cognitiva‑conductual (TCC), la hipnoterapia dirigida al intestino y los programas basados en atención plena (mindfulness) constituyen intervenciones no farmacológicas de primera línea dentro del abordaje integral de los TICI y de la comorbilidad afectiva y ansiosa que los acompaña.42, 43 Estas terapias no invalidan el origen corporal del malestar; por el contrario, lo contextualizan en redes cerebro-viscerales susceptibles de ser moduladas con técnicas psicológicas estructuradas que muestran beneficios clínicos sostenidos.44
La TCC se orienta a identificar y modificar patrones de pensamiento y conductas que perpetúan el ciclo síntoma‑ansiedad‑evitación.45 En pacientes con SII, dispepsia funcional y otros TICI, la TCC aborda creencias de catastrofización, hipervigilancia interoceptiva y conductas de seguridad (restricciones dietéticas extremas, evitación de actividades, uso excesivo de servicios), al tiempo que entrena habilidades de afrontamiento, exposición interoceptiva y normalización del ritmo de vida.44, 45 Típicamente se plantea en un formato breve con metas explícitas, tareas entre sesiones y monitorización de síntomas; los programas presenciales estándar abarcan entre diez y dieciséis sesiones, aunque existen versiones de “mínimo contacto” por teléfono, internet o aplicaciones móviles que preservan una parte relevante del efecto terapéutico.42, 46 En la práctica gastroenterológica, la TCC reduce la intensidad y la interferencia de dolor abdominal, distensión y alteraciones del hábito intestinal, mejora la calidad de vida y atenúa la comorbilidad ansioso‑depresiva, con ganancias que suelen mantenerse a mediano plazo cuando se sostienen las habilidades aprendidas.43, 46
La hipnoterapia dirigida al intestino utiliza un estado de atención focalizada y receptividad incrementada para introducir sugerencias terapéuticas que reencuadran la relación del paciente con las sensaciones viscerales y con el estrés.47 Los protocolos contemporáneos combinan inducciones breves, metáforas viscerales y sugerencias poshipnóticas orientadas a disminuir la hipersensibilidad, recuperar la sensación de control y modular el impacto del estrés sobre el eje intestino‑cerebro.47, 48 Habitualmente se programa una serie de siete a doce sesiones con frecuencia semanal, con práctica domiciliaria mediante audios, ajustando la frecuencia según la gravedad clínica. Aunque la evidencia más robusta proviene del SII, la utilidad se ha extendido a otras entidades funcionales. En la experiencia clínica, la hipnoterapia ofrece mejoras duraderas en el dolor, la urgencia, la distensión y el bienestar, y resulta especialmente valiosa en personas con marcada hipervigilancia somática o respuestas de ansiedad condicionadas a contextos digestivos.49
Los programas de mindfulness no buscan eliminar el síntoma, sino cambiar la relación con él.50 Mediante entrenamiento sistemático en atención al presente, conciencia corporal sin juicio y regulación emocional, el paciente aprende a observar sus sensaciones intestinales, pensamientos y emociones con menor reactividad.50 Este cambio reduce el sufrimiento asociado al síntoma, atenúa la rumiación y mejora el manejo del estrés, con efectos indirectos sobre la hipersensibilidad visceral y la variabilidad de la motilidad.46, 50 Intervenciones estructuradas, desde formatos breves hasta programas estandarizados de varias semanas han mostrado efectos clínicamente significativos en reducción de distrés, mejoría de síntomas gastrointestinales y descenso de la ansiedad específica relacionada con la digestión, además de favorecer la adherencia a hábitos saludables.50
La elección entre TCC, hipnoterapia o mindfulness puede guiarse por el fenotipo predominante: patrones de catastrofización, evitación y conductas de seguridad orientan hacia la TCC; en casos de hipervigilancia visceral intensa con ansiedad condicionada o pobre sensación de control se favorece la hipnoterapia; el estrés crónico, la reactividad emocional elevada y la necesidad de habilidades transdiagnósticas de regulación inclinan hacia mindfulness.
Conclusión
Los neuromoduladores han emergido como una herramienta terapéutica fundamental en el arsenal del gastroenterólogo moderno para el manejo de los TICI. La evidencia científica acumulada durante las últimas décadas demuestra inequívocamente que estos fármacos, originalmente desarrollados para el tratamiento de trastornos psiquiátricos, poseen propiedades únicas que los convierten en agentes altamente efectivos para modular el procesamiento del dolor visceral, la sensibilidad intestinal y la motilidad gastrointestinal a través de mecanismos centrales y periféricos específicos. La comprensión profunda del eje intestino-cerebro como una red compleja de comunicación bidireccional ha proporcionado el marco conceptual necesario para justificar científicamente el uso de ATC, ISRS, IRSN, y gabapentinoides en condiciones como el SII, la dispepsia funcional y otros trastornos funcionales digestivos. Su implementación exitosa requiere de una selección cuidadosa basada en las características individuales del paciente, un conocimiento detallado de sus perfiles farmacológicos y de seguridad, y la adopción de estrategias de dosificación graduales con monitoreo clínico apropiado. La integración de intervenciones no farmacológicas como la terapia cognitivo-conductual, la hipnoterapia dirigida al intestino y los programas de mindfulness, junto con un enfoque multidisciplinario que incluya la colaboración con psiquiatría cuando se necesite, optimiza los resultados terapéuticos y mejora significativamente la calidad de vida de los pacientes. A medida que avanza la investigación en neurobiología del dolor visceral, farmacogenómica y medicina personalizada, es probable que el papel de los neuromoduladores en gastroenterología continúe evolucionando hacia enfoques más precisos y efectivos, consolidándose su posición como componentes esenciales del tratamiento integral de los TICI en la práctica clínica contemporánea.
Propiedad intelectual. Los autores declaran que los datos, las tablas y las figuras presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: García-Zermeño K R, Aquino-Matus J E y Jiménez Pavón J y col. Utilidad de los neuromoduladores en la práctica clínica: visión del gastroenterólogo. Acta Gastroenterol Latinoam. 2025;55(4):303-316. https://doi.org/10.52787/agl.v55i4.533
Referencias
- Gómez-Escudero O, Coss-Adame E, Rao SS, et al. Clinical practice recommendations on the use of neuromodulators in gastroenterology: AMG-AMNM expert joint review. Rev Gastroenterol Mex. 2025;90(1):45-58.
- Drossman DA, Tack J, Ford AC, et al. Neuromodulators for functional gastrointestinal disorders (disorders of gut-brain interaction): a Rome Foundation Working Team report. Gastroenterology. 2018;154(4):1140-71.e1.
- Mogilevski T. The bi-directional role of the gut-brain axis in inflammatory and other gastrointestinal diseases. Curr Opin Gastroenterol. 2021;37(6):565-71.
- Aljeradat B, Kaddoumi A, Qinna NA, et al. Neuromodulation and the Gut-Brain Axis: Therapeutic Mechanisms and Implications for Gastrointestinal and Neurological Disorders. Pathophysiology. 2024;31(2):234-51.
- Camilleri M. Peripheral mechanisms in irritable bowel syndrome. N Engl J Med. 2012;367(17):1626-35.
- Fleming MA 2nd, Ehsan L, Moore SR, Levin DE. The enteric nervous system and its emerging role as a therapeutic target. Gastroenterol Res Pract. 2020;2020:8024171.
- Chanpong A, Borrelli O, Thapar N. Recent advances in understanding the roles of the enteric nervous system. Fac Rev. 2022;11:7.
- Carabotti M, Scirocco A, Maselli MA, Severi C. The gut-brain axis: interactions between enteric microbiota, central and enteric nervous systems. Ann Gastroenterol. 2015;28(2):203-9.
- O’Riordan KJ, Moloney GM, Keane L, Clarke G, Cryan JF. The gut microbiota–immune–brain axis: therapeutic implications. Cell Rep Med. 2025;6(3):101982.
- Almonajjed MB, Wardeh M, Atlagh A, Ismaiel A, Popa SL, Rusu F, Dumitrascu DL. Impact of microbiota on irritable bowel syndrome pathogenesis and management: a narrative review. Medicina (Kaunas). 2025;61(1):109.
- Chang L, Wei Y, Hashimoto K. Brain-gut-microbiota axis in depression: A historical overview and future directions. Brain Res Bull. 2022;182:44-56. https://doi.org/10.1016/j.brainresbull.2022.02.004
- Liu L, Wang H, Chen X, Zhang Y, Zhang H, Xie P. Gut microbiota and its metabolites in depression: from pathogenesis to treatment. eBioMedicine. 2023;90:104527. https://doi.org/10.1016/j.ebiom.2023.104527
- Li Z, Bi T. Causal effects of gut microbiota, metabolites, immune cells, liposomes, and inflammatory proteins on anorexia nervosa: A mediation joint multi-omics Mendelian randomization analysis. J Affect Disord. 2025;368:343-58. https://doi.org/10.1016/j.jad.2024.09.115
- Deng Y, Zhou M, Wang J, Yao J, Yu J, Liu W, Wu L, Wang J, Gao R. Involvement of the microbiota-gut-brain axis in chronic restraint stress: disturbances of the kynurenine metabolic pathway in both the gut and brain. Gut Microbes. 2021;13(1):1869501. https://doi.org/10.1080/19490976.2020.1869501
- Gawlik-Kotelnicka O, Burzyński J, Rogalski J, Skowrońska A, Strzelecki D. Probiotics may be useful for drug-induced liver dysfunction in patients with depression – A secondary analysis of a randomized clinical trial. Clin Nutr ESPEN. 2024;63:604-14. https://doi.org/10.1016/j.clnesp.2024.07.1024
- Xie Y, Zhu H, Yuan Y, Guan X, Xie Q, Dong Z. Baseline gut microbiota profiles affect treatment response in patients with depression. Front Microbiol. 2024;15:1429116. https://doi.org/10.3389/fmicb.2024.1429116
- Gruenbaum BF, Merchant KS, Zlotnik A, Boyko M. Gut Microbiome Modulation of Glutamate Dynamics: Implications for Brain Health and Neurotoxicity. Nutrients. 2024;16:4405. https://doi.org/10.3390/nu16244405
- Cheng J, Hu H, Ju Y, Liu J, Wang M, Liu B, Zhang Y. Gut microbiota-derived short-chain fatty acids and depression: deep insight into biological mechanisms and potential applications. Gen Psychiatry. 2024;37:e101374. https://doi.org/10.1136/gpsych-
2023-101374 - Kukucka O, Ferencova N, Visnovcova Z, Ondrejka I, Hrtanek I, Kovacova V, Macejova A, Mlyncekova Z, Tonhajzerova I. Mechanisms Involved in the Link between Depression, Antidepressant Treatment, and Associated Weight Change. Int J Mol Sci. 2024;25(8):4511. https://pubmed.ncbi.nlm.nih.gov/38674096/
- Nikolova VL, Smith MRB, Hall LJ, Cleare AJ, Stone JM, Young AH. Perturbations in gut microbiota composition in psychiatric disorders: a review and Meta-analysis. JAMA Psychiatry. 2021;78(12):1343-54.: https://doi.org/10.1001/jamapsychiatry.2021.2573
- Borgiani G, Possidente C, Fabbri C, Oliva V, Bloemendaal M, Arias Vasquez A, Dinan TG, Vieta E, Menchetti M, De Ronchi D, Serretti A, Fanelli G. The bidirectional interaction between antidepressants and the gut microbiota: are there implications for treatment response? Int Clin Psychopharmacol. 2024;40(1):3-26. https://doi.org/10.1097/YIC.0000000000000533
- Miller AH. Advancing an inflammatory subtype of major depression. Am J Psychiatry. 2025;182(6):516-24. https://pubmed.ncbi.nlm.nih.gov/40329642/
- Frank P, Jokela M, Batty GD, et al. Association between systemic inflammation and individual symptoms of depression: a pooled analysis of 15 population-based cohort studies. Am J Psychiatry. 2021;178(12):1107-18. https://pubmed.ncbi.nlm.nih.gov/34645276/
- Özçete ÖD, Banerjee A, Kaeser PS. Mechanisms of neuromodulatory volume transmission. Mol Psychiatry. 2024;29(11):3680-93. https://pubmed.ncbi.nlm.nih.gov/38789677/
- Merighi A, Salio C, Ferrini F, Lossi L. Neuromodulatory function of neuropeptides in the normal CNS. J Chem Neuroanat. 2011;42(4):276-87. https://pubmed.ncbi.nlm.nih.gov/
21385606/ - Mearin F, Lacy BE, Chang L, Chey WD, Lembo AJ, Simren M, Spiller R. Bowel Disorders. Gastroenterology. 2016:S00
16-5085(16)00222-5. https://pubmed.ncbi.nlm.nih.gov/27
144627/ - Lacy BE, Pimentel M, Brennan T, et al. ACG Clinical Guideline: Management of Irritable Bowel Syndrome. Am J Gastroenterol. 2021;116(1):17-44.
- Luo Y, Keefer L. The Clinical value of brain-gut behavioral therapies for functional esophageal disorders and symptoms. Neurogastroenterol Motil. 2022;34(8):e14373.
- Ford AC, Lacy BE, Harris LA, et al. Effect of antidepressants and psychological therapies in irritable bowel syndrome: an updated systematic review and meta-analysis. Am J Gastroenterol. 2019;114(1):21-39.
- Ford AC, Wright-Hughes A, Alderson SL, et al. Amitriptyline at low-dose and titrated for irritable bowel syndrome as second-line treatment in primary care (ATLANTIS): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2023;402(10414):1773-85.
- Sobin WH, Heinrich TW, Drossman DA. Central neuromodulators for treating EIC functional GI disorders: a primer. Am J Gastroenterol. 2017;112(5):693-702.
- Tack J, Janssen P, Masaoka T, Farré R, Van Oudenhove L. Efficacy of buspirone, a fundus-relaxing drug, in patients with functional dyspepsia. Clin Gastroenterol Hepatol. 2012;10(11):1239-45.
- Tack J, Ly HG, Carbone F, et al. Efficacy of mirtazapine in patients with functional dyspepsia and weight loss. Clin Gastroenterol Hepatol. 2016;14(3):385-392.e4.
- Keefer L, Ko CW, Ford AC. AGA Clinical Practice Update on Management of Chronic Gastrointestinal Pain in Disorders of Gut–Brain Interaction: Expert Review. Clinical Gastroenterology and Hepatology. 2021;19:2481-2488.e1. https://doi.org/10.1016/j.cgh.2021.07.006
- Osborn DPJ, Petersen I, Beckley N, Walters K, Nazareth I, Hayes J. Weight change over two years in people prescribed olanzapine, quetiapine and risperidone in UK primary care: Cohort study in THIN, a UK primary care database. J Psychopharmacol. 2018;32:1098-103. https://doi.org/10.1177/0269881118780011
- Haghbin H, Zakirkhodjaev N, Husain FF, Lee-Smith W, Aziz M. Risk of Gastrointestinal Bleeding with Concurrent Use of NSAID and SSRI: A Systematic Review and Network Meta-Analysis. Dig Dis Sci. 2023;68:1975-82. https://doi.org/10.1007/s10620-022-07788-y
- Hanna-Jairala I, Drossman DA. Central Neuromodulators in Irritable Bowel Syndrome: Why, How, and When. American Journal of Gastroenterology. 2024;119:1272-84. https://doi.org/
10.14309/ajg.0000000000002800 - Wright-Hughes A, Ow PL, Alderson SL, Ridd MJ, Foy R, Bishop FL, et al. Predictors of response to low-dose amitriptyline for irritable bowel syndrome and efficacy and tolerability according to subtype: post hoc analyses from the ATLANTIS trial. Gut. 2025;74:728-39. https://doi.org/10.1136/GUTJNL-
2024-334490 - Stanculete MF, Dumitrascu DL, Drossman DA. Neuromodulators in the Brain-Gut Axis: their Role in the Therapy of the Irritable Bowel Syndrome. Journal of Gastrointestinal and Liver Diseases. 2021;30:517-25. https://doi.org/10.15403/jgld-4090
- Fornaro M, Cattaneo CI, De Berardis D, Ressico F V., Martinotti G, Vieta E. Antidepressant discontinuation syndrome: A state-of-the-art clinical review. European Neuropsychopharmacology. 2023;66:1-10. https://doi.org/10.1016/j.euroneuro.2022.10.005
- Haskard Zolnierek KB, Dimatteo MR. Physician communication and patient adherence to treatment: A meta-analysis. Med Care. 2009;47:826-34. https://doi.org/10.1097/MLR.0b013e
31819a5acc - Palsson OS, Ballou S. Hypnosis and Cognitive Behavioral Therapies for the Management of Gastrointestinal Disorders. Curr Gastroenterol Rep. 2020;22(7):31.
- Adler EC, Levine EH , Ibarra AN , Boparai ES, Hung YY, McCrary QD, et al. Hipnoterapia dirigida al intestino para el síndrome del intestino irritable: una revisión sistemática y un metaanálisis. Neurogastroenterol Motil. 2025;37(7):e70037. DOI:10.1111/nmo.7003
- Roger AH, Gudleski GD, Quigley BM, Zvolensky MJ, Lackner JM. Catastrofización del dolor y resultados clínicos en pacientes que reciben una nueva terapia cognitivo-conductual para el síndrome del intestino irritable: un enfoque terapéutico experimental. Behav Ther. 2023;54(4):623-36. DOI:10.1016/j.beth.2023.01.004
- Radu M, Moldovan R, Pintea S, Băban A, Dumitrașcu DL. Predictores de resultados en intervenciones cognitivas y conductuales para el síndrome del intestino irritable. Un metaanálisis. J Gastrointest Liver Dis. 2018;27(3):257-63. DOI:10.15403/ jgld.2014.1121.273.b
- Wallén H, Lindfors P, Andersson E, Hedman-Lagerlöf E, Hesser H. Retorno de la inversión en terapia de exposición por internet para el síndrome del intestino irritable: un ensayo controlado aleatorizado. BMC Gastroenterol. 2021;21(1):289. DOI:10.1186/s12876-021-01867
- Hasan SS, Pearson JS, Morris J, Whorwell PJ. Hipnoterapia por Skype para el síndrome del intestino irritable: efectividad y comparación con el tratamiento presencial. Int J Clin Exp Hypn. 2019;67(1):69-80. DOI:10.1080/00207144.2019.1553766
- Császár-Nagy N, Bókkon I. Hipnoterapia y SII: ¿memoria de estrés implícita a largo plazo en el ENS ? Heliyón. 2023;9(1): e12751. DOI:10.1016/j.heliyon.2022.e1275
- Lee HH, Choi YY, Choi MG. La eficacia de la hipnoterapia en el tratamiento del síndrome del intestino irritable: una revisión sistemática y metaanálisis. J Neurogastroenterol Motil. 30 de abril de 2014;20(2):152-62. DOI:10.5056/jnm.2014.20.2.152. PMID: 24840368; PMCID: PMC4015203.
- Baboș CI, Leucuța DC, Dumitrașcu DL. Meditación y síndrome del intestino irritable: una revisión sistemática y un metaanálisis. J Clin Med. 2022;11(21):6516. DOI:10.3390/jcm11216516
Correspondencia: José María Remes-Troche
Correo electrónico: jose.remes.troche@gmail.com
Acta Gastroenterol Latinoam 2025;55(4):303-316
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE



