Alejandro Marcelo Suárez ID· Matías Dan Federici ID· Andrés Esteban Rocca ID
Unidad de Endoscopía Digestiva, Hospital de Gastroenterología Dr. Carlos Bonorino Udaondo.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2023;53(3):291-300
Recibido: 01/06/2023 / Aceptado: 03/09/2023 / Publicado online el 29/09/2023 /
https://orcid.org/10.52787/agl.v53i3.327
Resumen
Introducción. Los métodos endoscópicos convencionales demostraron tener una pobre eficacia hemostática en el tratamiento de los tumores esofagogastroduodenales sangrantes. Trabajos recientes han sugerido, por el contrario, un elevado éxito terapéutico con el uso de TC-325 (Hemospray®, Cook Medical, Winston-Salem, NC) en este subgrupo de pacientes. Su fácil aplicación y la posibilidad de hacerlo en extensas superficies permiten posicionarlo como un tratamiento prometedor para esta indicación, dada la naturaleza difusa del sangrado en este tipo de lesiones. Objetivos. Nuestro objetivo primario fue evaluar el rol hemostático inmediato y a las 72 horas del tratamiento con TC-325 en los pacientes con hemorragia digestiva alta de origen tumoral que ingresaron a nuestra institución. Nos propusimos como objetivo secundario analizar su tasa de resangrado al mes y las complicaciones. Materiales y métodos. Análisis retrospectivo, observacional y longitudinal, realizado entre marzo de 2018 y mayo de 2022, sobre la base de los registros electrónicos de la Unidad de Endoscopía Digestiva del Hospital de Gastroenterología Dr. Carlos Bonorino Udaondo, las historias clínicas de internación y los registros de seguimiento ambulatorio del servicio de Oncología. Se incluyó a todos los pacientes con tumores digestivos altos con sangrado activo comprobado durante videoendoscopía digestiva alta (VEDA), con datos disponibles al menos para analizar nuestro objetivo primario. Se recolectaron sus variables clínicas, demográficas y endoscópicas, así como datos de laboratorio, localización tumoral y severidad del sangrado. Resultados. Un total de 21 pacientes, 81% hombres, y con una edad media de 65 años fueron incluidos. El síntoma de presentación más frecuente fue melena (81%), siendo la localización gástrica la más frecuente (71,4%) y el adenocarcinoma de tipo intestinal el tipo histológico más común. La hemostasia inmediata se logró en 19/21 pacientes (91%) tratados con TC-325. El 100% de los 18 enfermos que sobrevivieron a las 72 horas se mantuvieron libres de resangrado al finalizar dicho período. Asimismo, de los 16 pacientes vivos a los 30 días, solo 4 (25%) resangraron, lo cual permitió la aplicación de tratamientos hemostáticos definitivos en mejores condiciones clínicas en 10 de ellos (3 enfermos fueron operados y otros 7 recibieron radio y/o quimioterapia). El tratamiento con Hemospray fue muy seguro, sin ninguna complicación inmediata o diferida. No obstante, por tratarse de pacientes con tumores localmente avanzados o neoplasias diseminadas, su pronóstico fue desfavorable, con una mortalidad a 1 y 6 meses del 24% y 66% respectivamente. Conclusión. El tratamiento de las hemorragias digestivas altas tumorales con TC-325 es muy efectivo y seguro. Su alta tasa de hemostasia inmediata y precoz sugiere un prometedor papel como terapia puente, permitiendo la aplicación posterior de tratamientos hemostáticos más definitivos. La mortalidad a mediano plazo permanece igualmente elevada, dado el estadio tumoral en general avanzado.
Palabras claves. Hemorragia digestiva alta tumoral, hemostasia endoscópica, TC-325 (Hemospray®).
Hemostatic Role of TC-325 in Tumor-Related Upper Gastrointestinal Bleeding: Experience in a Tertiary Care Centre
Summary
Introduction. Conventional endoscopic methods have shown poor hemostatic efficacy in the treatment of bleeding esophagogastroduodenal tumors. Recent studies have suggested, on the contrary, a high therapeutic success with the use of TC-325 (Hemospray®, Cook Medical, Winston-Salem, NC) in this subgroup of patients. Its easy application and its ability to cover a large surface area appear to position it as a promising treatment for this indication, given the diffuse nature of bleeding in this type of lesions. Objectives. Our primary aim was to evaluate the immediate and 72-hour hemostatic role of TC-325 in patients with upper gastrointestinal bleeding of tumor origin admitted to our institution. Our secondary objective was to analyze their rebleeding rate at one month and complications. Materials and Methods. Retrospective, observational and longitudinal analysis, conducted between March 2018 and May 2022, based on the electronic records of the Digestive Endoscopy Unit of the Hospital de Gastroenterología Dr. Carlos Bonorino Udaondo, inpatient medical records and outpatient follow-up records of the Oncology service. We included all patients with upper gastrointestinal tumors with active bleeding verified during upper digestive video endoscopy (UDVE), with data available at least to analyze our primary objective. Clinical, demographic and endoscopic variables were collected, as well as laboratory data, tumor location and bleeding severity. Results. A total of 21 patients, 81% men, with a mean age of
65 years were included. The most frequent presenting symptom was melena (81%), with gastric location being the most frequent (71.4%), and intestinal adenocarcinoma being the most common histological type. Immediate hemostasis was achieved in 19/21 patients (91%) treated with TC-325. Of the 18 patients who survived to 72 hours, 100% remained free of rebleeding at the end of this period. Furthermore, of the 16 patients alive at 30 days, only 4 (25%) rebleed, which allowed the application of definitive hemostatic treatments in better clinical conditions in 10 of them (3 patients underwent surgery and 7 others received radio and/or chemotherapy). Hemospray treatment was very safe, with no immediate or delayed complications. However, as these patients had locally advanced tumors or disseminated neoplasms, their prognosis was unfavorable, with mortality at 1 and 6 months of 24%
and 66% respectively. Conclusion. Treatment of tumoral upper gastrointestinal bleeding with TC-325 is very effective and safe. Its high rate of immediate and early hemostasis suggests a promising role as a bridging therapy, allowing the subsequent application of more definitive hemostatic treatments. Medium-term mortality remains equally high, given the generally advanced tumor stage.
Keywords. Tumor upper gastrointestinal bleeding, endoscopic hemostasis, TC-325 (Hemospray®).
Abreviaturas
TC-325: Hemospray®, Cook Medical, Winston-Salem, NC.
VEDA: Videoendoscopía digestiva alta.
HDA: Hemorragia digestiva alta
G.B.: Score de Glasgow-Blatchford.
HC: Historia clínica.
TBQ: Tabaquismo.
HTA: Hipertensión arterial.
DBT: Diabetes mellitus.
PAS: Presión arterial sistólica.
TNE: Tumor neuroendocrino.
EPOC: Enfermedad pulmonar obstructiva crónica.
IAM: Infarto agudo de miocardio.
CABA: Ciudad Autónoma de Buenos Aires.
Introducción
Los tumores esofagogastroduodenales son responsables de hasta el 5% de las hemorragias digestivas altas.1,2 Su fisiopatología secundaria al daño vascular difuso por invasión tumoral directa genera un sangrado en extensas superficies, que lo hacen poco apto para su tratamiento con los métodos endoscópicos convencionales.3 Tanto la inyección como las terapias térmicas y/o mecánicas han demostrado, en serie de casos y estudios de cohorte, tener una pobre hemostasia inmediata de apenas el 40%, y una alta tasa de resangrado de alrededor del 56% a los 30 días.3,4 TC-325 (Hemospray®, Cook Medical, Winston-Salem, NC) es una tecnología hemostática emergente recientemente introducida en el tratamiento de la hemorragia digestiva alta. Está compuesto por un polvo inorgánico biológicamente inerte no absorbible, que al entrar en contacto con la sangre se vuelve coherente y adhesivo, formando una barrera mecánica que detiene el sangrado. Esta última también actúa concentrando plaquetas y factores de coagulación, favoreciendo así aún más la hemostasia. Su fácil aplicación endoscópica a través de un catéter, sobre extensas superficies y sin entrar en contacto con el tejido tumoral, lo convierten en un medio atractivo para tratar estas complejas hemorragias. Recientes trabajos demuestran su alta eficacia en este subgrupo de enfermos, con tasas de hemostasia inmediata post endoscopía y a las 72 horas del 90% al 97% y del 75% al 96% respectivamente.1-6 Aunque eliminado luego de transcurridas 24 a 48 horas, esta alta eficacia inicial permitiría detener el sangrado y estabilizar hemodinámicamente a estos pacientes, permitiendo, a posteriori, la aplicación de tratamientos hemostáticos más definitivos (embolización vascular, radioterapia o cirugía) en mejores condiciones clínicas.4,7,8 Sobre esta hipótesis, realizamos el presente trabajo, cuyo objetivo primario fue evaluar el rol hemostático inmediato y a las 72 horas de aplicado del Hemospray®, en el tratamiento de los pacientes con hemorragia digestiva alta de origen tumoral que ingresaron a nuestra institución. Asimismo, nuestros objetivos secundarios fueron analizar su tasa de complicaciones y resangrado al mes”.
Materiales y métodos
Diseño del estudio: Análisis retrospectivo, observacional y longitudinal sobre la base de los registros electrónicos de la Unidad de Endoscopía Digestiva del Hospital Bonorino Udaondo, de la historia clínica de internación y de los registros de seguimiento ambulatorio del servicio de Oncología.
Se incluyó a todos los pacientes con tumores esofagogastroduodenales sangrantes que, entre marzo de 2018 y mayo de 2022, hubieran recibido tratamiento hemostático con TC-325, ya sea como monoterapia o combinado con otros tratamientos endoscópicos convencionales (inyección, métodos térmicos o mecánicos) y que cumplieran los siguientes requisitos: 1) pacientes con hemorragia digestiva alta (HDA) secundaria a tumores digestivos objetivada por videoendoscopía digestiva alta (VEDA), 2) edad > 18 años, 3) descripción explícita en el informe endoscópico de la hemostasia inmediata exitosa o fallida postratamiento con Hemospray®, y 4) seguimiento pos-VEDA terapéutica de al menos 72 horas, e ideal, aunque no necesariamente, de hasta 30 días para evaluar un eventual resangrado.
Se definió hemostasia inmediata a la completa detención del sangrado inmediatamente luego del tratamiento, indicado así y en forma explícita en el correspondiente reporte endoscópico. Se definió como resangrado a la aparición de melena y/o hematemesis y/o hematoquezia asociada a inestabilidad hemodinámica en paciente previamente compensado, o caída de la concentración de
Hb ≥ 2 gr/litro en 24 horas, con confirmación endoscópica en nueva endoscopía. Por el contrario, fueron excluidos todos los enfermos a los que se les realizó tratamiento con TC-325 y en los cuales se encontró causa de sangrado benigna, como así también todos aquellos con falta de datos en la historia clínica y/o seguimiento menor a 72 horas postratamiento que impidieran evaluar el objetivo primario del presente estudio.
Se consideró como complicación solo a aquellas severas y que alteraran el manejo del paciente: embolización sistémica, perforación u obstrucción intestinal, endoscopio retenido en el cardias por adherencia con el polvo hemostático, potenciales reacciones alérgicas. La oclusión temporaria del canal del endoscopio o del catéter aplicador durante el procedimiento, en cambio, no fueron considerados.
Se analizaron los siguientes datos clínicos y/o demográficos: a. edad; b. sexo; c. síntoma de presentación (hematemesis, melena, hematoquecia); d. frecuencia cardíaca; e. presión arterial; f. laboratorio al ingreso (hemograma, plaquetas, urea, coagulograma); g. longitud de estadía hospitalaria; h. aplicación posterior o no de otras terapéuticas hemostáticas definitivas como radioterapia, embolización o cirugía.
Se incluyó información endoscópica sobre los siguientes hallazgos: 1. localización tumoral; 2. tipo de sangrado (pulsátil en jet, babeo hemático, vaso visible, coágulo adherido); 3. tratamiento hemostático con TC-325 como monoterapia o combinado con otras terapias endoscópicas; 4. descripción de hemostasia inmediata exitosa o fallida postratamiento.
Asimismo, en todos los pacientes en los que fue posible se calcularon los scores de Glasgow-Blatchford (G.B.) y Rockall, dada su importancia pronóstica y como indicadores de la gravedad de la hemorragia. El primero incluye datos clínicos, de laboratorio y comorbilidades asociadas, siendo utilizado como indicador de la necesidad de intervenciones terapéuticas para detener el sangrado. El otro incorpora la edad del paciente, datos clínicos y endoscópicos, que permiten predecir su mortalidad. Fueron considerados como pacientes de alto riesgo aquellos con un score de G.B. y de Rockall ≥ 7 puntos y ≥ 5 puntos respectivamente).9,10
La recolección de datos fue realizada por M.F. y A.M.S., médicos de guardia y staff respectivamente de la Unidad de Endoscopía del Hospital de Gastroenterología C. Bonorino Udaondo, los cuales no presentaban ningún conflicto de interés para la realización del presente trabajo.
Las endoscopías fueron realizadas por médicos de guardia y/o staff de nuestra Unidad, utilizándose videogastroscopios Sonoscape HD-500 y Aohua AQL-100.
El uso de TC-325 así como el número de disparos realizados estuvieron a criterio de los endoscopistas tratantes, todos con adecuado entrenamiento previo en la utilización de este nuevo método hemostático. En todos los casos se usó el TC-325 (Hemospray, Cook Medical, Winston-Salen, North Carolina, EE. UU.) con una dosis máxima de hasta 20g por sesión.
El presente estudio fue realizado respetando los requisitos éticos, legales y jurídicos establecidos en las normas bioéticas nacionales (Ley sobre Protección de Derechos de Sujetos en Investigaciones en Salud CABA) e internacionales (Núrenberg, Helsinki, derechos humanos).
Por las características del estudio no se tomaron consentimientos informados para la evaluación de los datos de las HC, pero todos los pacientes firmaron el consentimiento para la realización de la endoscopía. Solo los médicos participantes del estudio tuvieron acceso a los datos personales de los pacientes, los cuales fueron analizados respetando siempre su confidencialidad.
Análisis estadístico
Se utilizó el programa Microsoft Excel como gestor de la base de datos, empleándose el programa Calculate de QxMD para dispositivos móviles, a fin de calcular el puntaje de los scores G.B. y Rockall. Las variables categóricas se informaron como frecuencias y porcentajes, mientras que las variables continuas se informaron como media +/- desvío estándar (+/- DE) y/o mediana y rango intercuartílico como medida de dispersión, según distribución.
Resultados
El análisis de los registros electrónicos de nuestra unidad entre marzo de 2018 y mayo 2022 reveló un total de 37 pacientes en los que el TC-325 fue utilizado como método hemostático endoscópico durante una hemorragia digestiva alta. Cinco de ellos fueron excluidos por la etiología benigna de su sangrado, mientras que en otros 11 la falta de datos, información y/o seguimiento menor a 72 horas impidió su inclusión. De esta manera, un total de 21 pacientes quedaron seleccionados para nuestro análisis.
Del total de 21 pacientes, el 81% eran hombres y con una edad media de 65 +/- 12,3 años. Asimismo, la mayoría (81%) presentaban una o más comorbilidades asociadas, con un promedio de dos comorbilidades por paciente, siendo las más prevalentes TBQ (47,6%), HTA (33,3%) y diabetes mellitus tipo 2 (DBT tipo 2)(23,8%). La frecuencia cardíaca (FC) y la presión arterial sistólica (PAS) promedio al ingreso hospitalario fueron de 91+/- 12/min y 104 +/- 7mmHg, con un score de G.B. y Rockall promedio de 11,8 +/- 1,5 y 7,9 +/- 1,2 puntos respectivamente, por lo que fueron considerados como pacientes de alto riesgo. El síntoma de presentación más frecuente fue melena, en 15 pacientes (70%); hematemesis, solo en otros 2 (9%), mientras que en los 4 pacientes restantes el sangrado tumoral fue un hallazgo inesperado de endoscopías programadas para estudio de anemia y/o síntomas digestivos. El patrón de sangrado endoscópico fue en babeo hemático en 15/21 pacientes (71%), y en los 6 restantes como grandes coágulos inicialmente adheridos a la superficie tumoral que, al removerse durante la endoscopía, comenzaron también con sangrado activo en napa. La localización tumoral gástrica fue la más frecuente (15/21, 71,4%), y el adenocarcinoma de tipo intestinal fue el tipo histológico más común (15/19, 78,8%). Los datos clínicos y demográficos, localización e histología tumoral son presentados en las Tablas 1 y 2.
Tabla 1. Datos clínicos y demográficos. Localización e histología tumoral
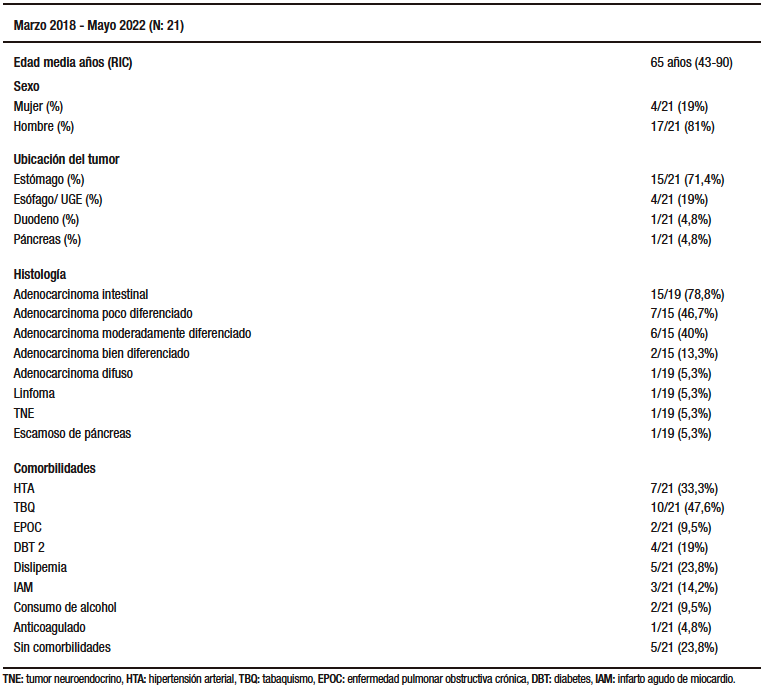
Tabla 2. Datos clínicos y demográficos. Localización e histología tumorales
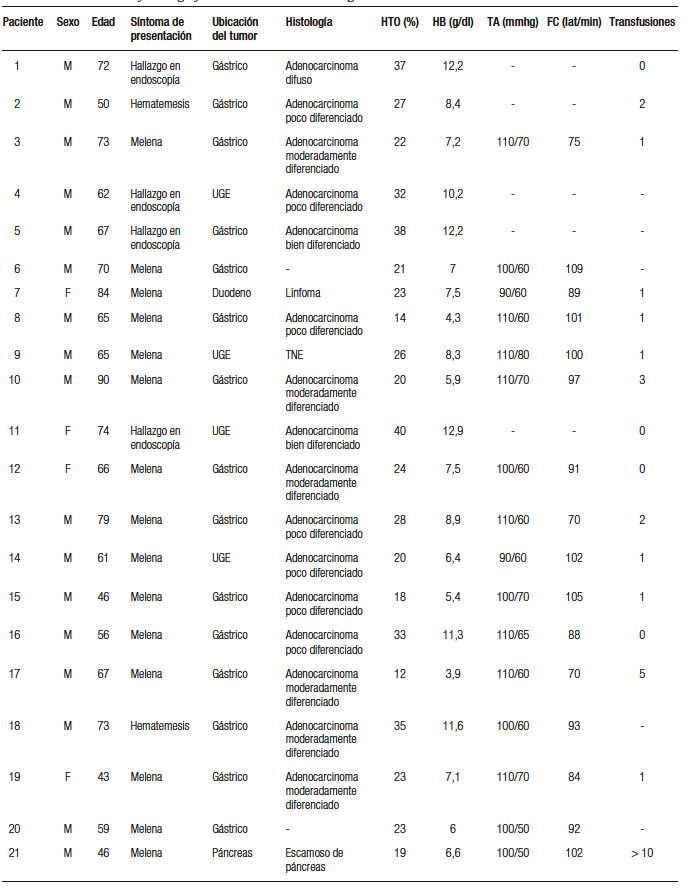
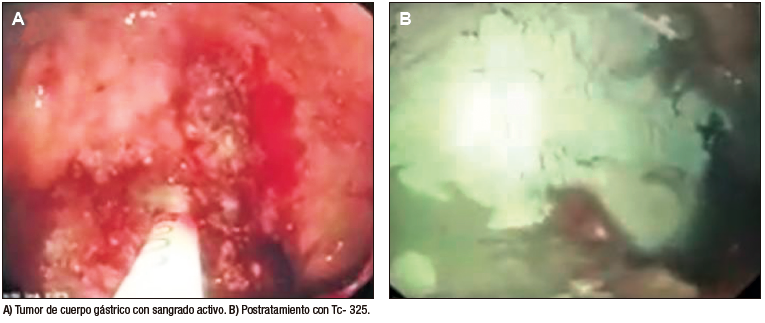
El TC-325 fue utilizado como monoterapia en 17 pacientes (81%) y como terapia combinada con inyección de adrenalina 1/10000 en los 4 restantes. La hemostasia inmediata fue lograda en 19 de 21 pacientes (91%) tratados con TC-325 (Figura 1). Los dos pacientes con sangrado persistente tenían un adenocarcinoma gástrico y pancreático con infiltración gástrica, ambos en estadios avanzados, con anemia severa y altos requerimientos transfusionales. La hemorragia persistió pese a nuevos tratamientos con TC-325, por lo que fueron derivados para realizar radioterapia hemostática, ya fuera sola o asociada a quimioterapia. Todos los pacientes con hemostasia inicial exitosa se mantuvieron libres de recurrencia hemorrágica a las 72 horas, y solo uno de ellos falleció durante dicho período por progresión de su enfermedad y sin evidencia de resangrado. Asimismo, solo 4 de 16 enfermos vivos a los 30 días (25%) resangraron en ese lapso (2 pacientes más fallecieron antes del mes, también por progresión de su neoplasia y sin evidencia de recurrencia hemorrágica). Aun así, en 2 de esos 4 enfermos el resangrado fue incluso relativamente tardío, más allá de la semana de aplicación del TC-325, lo que permitió en ellos, como en el resto, su estabilización y la posterior aplicación de una terapia hemostática definitiva. De esta manera, 3 pacientes fueron operados (gastrectomía total o subtotal), 7 recibieron radioterapia y/o quimioterapia, y en los 8 restantes el tratamiento paliativo fue la elección, dado el estadio avanzado de la neoplasia, el mal estado general y/o la falta de respuesta a tratamientos oncológicos previos. El tratamiento con TC-325 fue muy seguro, sin ninguna complicación inmediata o diferida que pudiera ser atribuida a su uso. No obstante, por tratarse de pacientes con tumores localmente avanzados o neoplasias diseminadas, su pronóstico fue desfavorable, con una mortalidad a 1 y 6 meses del 24% y del 66% respectivamente (este último dato solo disponible en 18 pacientes, dada la pérdida de seguimiento en los 3 restantes). La mayoría de nuestros enfermos fallecieron por progresión neoplásica, estando libres de recurrencia hemorrágica al momento del óbito. Solo 1 de nuestros 21 pacientes falleció a los 30 días como consecuencia directa de un resangrado incontrolable, siendo así la mortalidad por recurrencia hemorrágica de apenas el 4,76% durante dicho período (Tabla 3).
Figura 1. Diagrama de flujo de los participantes
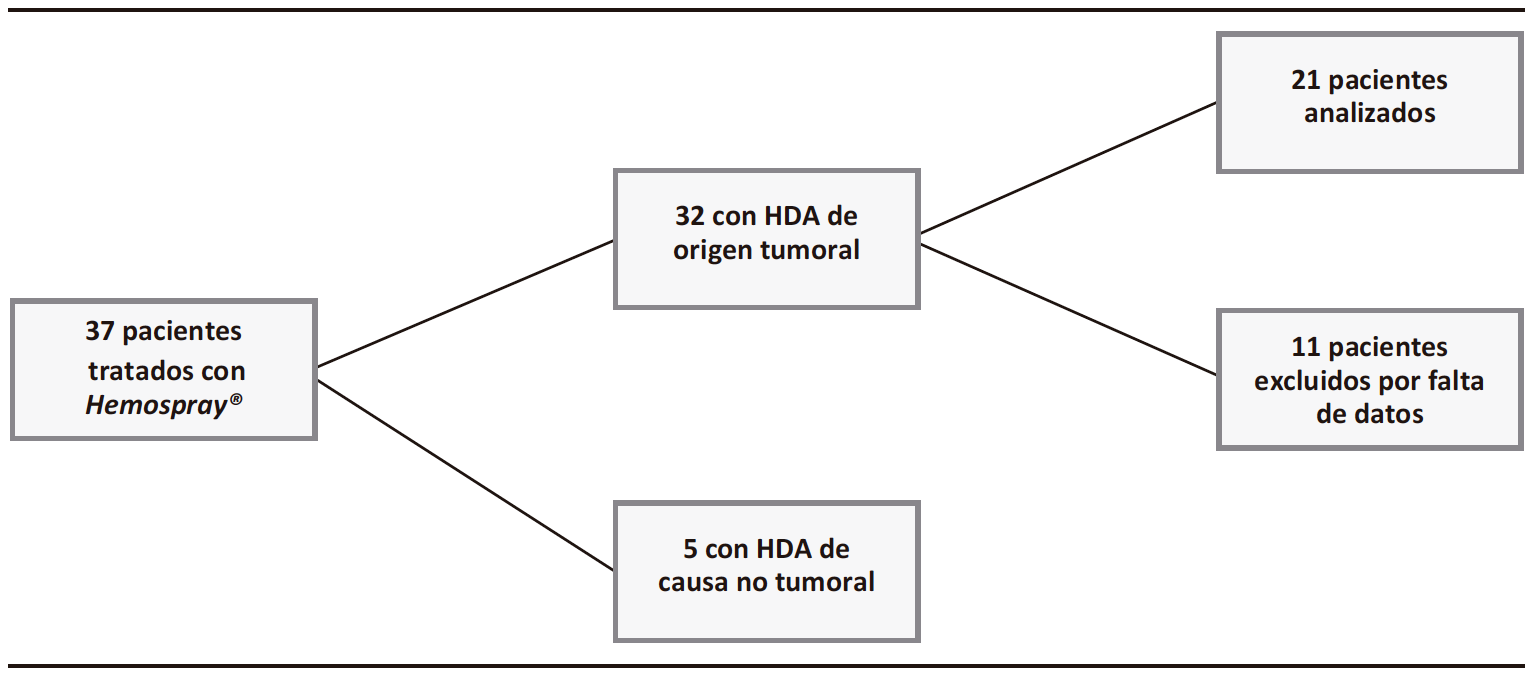
Tabla 3. Resultados pacientes tratados con TC-325

Discusión
La hemorragia digestiva alta secundaria a tumores gastrointestinales representa una situación clínica desafiante. Las técnicas de hemostasia endoscópica convencionales suelen fracasar debido a la naturaleza difusa del sangrado, la angiogénesis patológica del tejido tumoral y su intensa friabilidad exacerbada con su manipulación. El TC-325, dado su fácil administración en superficie extensas y aun en aquellas de difícil accesibilidad, ha sido sugerido en numerosos trabajos como un método hemostático óptimo para el tratamiento de este tipo de lesiones.1-8,11 Nuestro estudio mostró una hemostasia inmediata en el 91% de los pacientes tratados, y del 100% a las 72 horas en aquellos enfermos con hemostasia inicial exitosa y sobrevivientes al final de dicho período. Asimismo, nuestra tasa de resangrado del 25% a los 30 días es comparativamente menor a las tasas de sangrado recurrente del 29% al 86% reportadas con los tratamientos de sostén y/o técnicas endoscópicas convencionales.12-20 Nuestros resultados favorables se mantuvieron independientemente de la utilización de TC-325 como monoterapia o combinada con otras técnicas endoscópicas, o de la localización del tumor (gástrico, duodenal o de la unión gastroesofágica). La barrera mecánica formada por la cohesión del polvo hemostático al entrar en contacto con la sangre es la probable explicación de la detención del sangrado y de nuestras altas tasas de hemostasia inmediata y precoz. No obstante, el tiempo de residencia del TC-325 aplicado sobre la superficie tumoral es de alrededor de 24 horas,21 luego del cual se desprende y es eliminado, perdiendo entonces su efecto hemostático local ya descripto. Por tal motivo, sus efectos más duraderos, en particular nuestra baja tasa de resangrado al mes, son, en cambio, más difíciles de explicar. Es probable que sus efectos secundarios, estimulando la cascada de coagulación y agregación plaquetaria en el sitio de aplicación,22 sean más prolongados y favorezcan una hemostasia más duradera. También es probable que esta detención del sangrado, aunque temporaria, permita estabilizar al enfermo y ponerlo en condiciones para la aplicación de tratamientos hemostáticos más definitivos (radioquimioterapia, embolización y/o cirugía), explicándose así este efecto hemostático más prolongado. Todo es puramente especulativo y nuestro escaso número de pacientes nos impide obtener una conclusión definitiva al respecto.
Nuestros resultados coinciden, en general, con los de numerosos estudios realizados con TC-325 en similar grupo de enfermos.1-8,11 Hasta la fecha, el trabajo multicéntrico francés de Hussein y colaboradores2 es el más grande, habiendo reunido un total de 105 pacientes con sangrado digestivo tumoral esofagogastroduodenal. Su tasa de hemostasia inmediata del 97,7% y la de resangrado del 27,7% a los 30 días son parecidas a las encontradas en nuestro trabajo. Asimismo, solo existen actualmente dos estudios controlados y aleatorizados que comparan este tratamiento versus el manejo conservador en este grupo de enfermos. Uno de ellos,5 un ensayo piloto, controlado y aleatorizado de 20 pacientes, mostró una tasa de hemostasia inmediata del 90% en la cohorte TC-325 versus 40% en el grupo de atención estándar, lo que sugiere que este nuevo polvo hemostático es una prometedora modalidad terapéutica. El otro estudio, con un total de 59 enfermos incluidos, no pudo, por el contrario, demostrar ninguna diferencia significativa en las tasas de resangrado y/o mortalidad a 30 días entre ambos grupos.6 Futuros trabajos comparativos con mayor seguimiento y número de pacientes serán necesarios antes de confirmar estos resultados y recomendar su uso. No obstante, no impresiona que el mejor manejo de estas hemorragias tumorales disminuya su mortalidad. A pesar de la terapéutica, esta última permanece elevada debido a la patología de base (cáncer avanzado), el estadio avanzado de estas neoplasias y su casi inevitable progresión a mediano plazo.1-8,11 Esto explica la elevada mortalidad a los 6 meses, del 66% de nuestros pacientes, similar a las reportadas en otros estudios, en los cuales la mayoría de los enfermos habían fallecido al finalizar dicho período.5 Finalmente, es de destacar la ausencia de complicaciones asociadas con el uso de TC-325, tanto en nuestro estudio como en el resto de los trabajos previamente citados. Casi ningún efecto adverso mayor ha sido descripto hasta la fecha, convirtiéndolo de esta manera en un tratamiento muy seguro. Recientemente, un caso de endoscopio retenido por el Hemospray®ha sido descripto en un paciente con un tumor cardial con sangrado activo.22 La ubicación de la lesión obligó a realizar la terapéutica con el endoscopio en retroflexión, por lo que la cubierta del instrumental fue también inevitablemente rociada con el polvo hemostático. Esto impidió el retiro del endoscopio al finalizar el tratamiento, requiriendo intubación del paciente y ARM por 48 horas antes de poder retirar el instrumental sin inconvenientes. Nosotros no hemos tenido esta complicación, pero nuestra escasa cantidad de tumores cardiales nos impide nuevamente extraer mayores conclusiones.
Las principales limitaciones de nuestro estudio son su carácter retrospectivo y el escaso número de pacientes incluidos. Un sesgo en la recolección de datos es posible, dada la frecuente falta de información en algunas historias clínicas examinadas, con pacientes cuyo seguimiento se perdió y/o no hay indicación de su causa directa de muerte. Es de esperar que la implementación de la historia clínica electrónica, próxima a realizarse en nuestro hospital, mejore en el futuro este inconveniente. No obstante, creemos que nuestro estudio tiene el valor de mostrar las dificultades y los resultados reales de la atención y el tratamiento de estos complejos enfermos en un hospital público de referencia de la Ciudad Autónoma de Buenos Aires. Finalmente, en el contexto actual de recursos limitados y necesaria asignación racional de los mismos, una mayor experiencia como así también estudios de costo/efectividad serán necesarios antes de establecer el verdadero rol terapéutico en nuestro medio de este novedoso método hemostático.
Conclusión
Nuestros datos muestran que el TC-325 tiene un prometedor papel potencial como monoterapia de primera línea en el tratamiento endoscópico de las hemorragias digestivas altas de origen maligno. La alta tasa de hemostasia inmediata y precoz, así como su baja frecuencia de resangrado, sugieren su utilidad como puente hacia una terapia hemostática más definitiva. Se requieren más ensayos controlados y aleatorizados para confirmar estos resultados.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad Intelectual. Los autores declaran que los datos, las tablas y las figuras presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2023 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Federici M, Suárez A M. Rol hemostático del TC-325 en la hemorragia digestiva alta tumoral: experiencia en un centro de tercer nivel. Acta Gastroenterol Latinoam. 2023;53(3):291-300. https://doi.org.10.52787/agl.v53i3.327
Referencias
- Arena M, Masci E, Eusebi LH, Iabichino G.,et al. Hemospray for the treatment of acute bleeding due to upper gastrointestinal tumours. Digestive and Liver Disease. 2017,49:514-7.
- Hussein M, Alzoubaidi D, O´Donnell M, De La Serna A, et al. Hemostatic powder TC-325 treatment of malignancy-related upper gastrointestinal bleeds: International registry outcomes. Journal of Gastroenterology and Hepatology. 2021,36:3027-32.
- Pittayanon R, Rerknimitr R, Barkum A. Prognostic factors affecting outcomes in patients with malignant GI bleeding treated with a novel endoscopically delivered hemostatic powder. Gastrointest. Endosc. 2018,87:994-1002.
- Meng ZW, Marr KJ, Mohamed R, James PD. Long-Term effectiveness, safety and mortality associated with the use of TC-325 for malignant-related upper gastrointestinal bleeds: A multicenter retrospective study. Journal of Canadian Association of Gastroenterology. 2019,2(2):91-7.
- Chen YI, Wyse J, Lu Y, Martel M, Barkun A. TC-325 hemostatic powder versus current standard of care in managing malignant GI bleeding: a pilot randomized clinical trial. Gastrointest. Endosc. 2020,91:321-8.
- Costa Martins B, Abnader Machado A, Corsato Scomparin R, Andrade Paulo G, Safatle-Ribeiro A, et al. TC-325 hemostatic powder in the management of upper gastrointestinal malignant bleeding: a randomized controlled trial. Endosc Int Open. 2022;10:E1350-E1357.
- Pittayano R, Prueksapanich P, Rerknimitr R. The efficacy of Hemospray in patients with upper gastrointestinal bleeding from tumor. Endoscopy International Open. 2016;04:E933-E936.
- Chen YI, Barkun A, Soulellis C, Mayrand S, Ghali P. Use of the endoscopically applied hemostatic powder TC-325 in cancer-related upper GI hemorrhage: preliminary experience. Gastrointest. Endosc. 2012,75(6):1278-81.
- Stanley AJ, Laine L, Dalton HR, Ngu JH, Schultz M, et al. Comparison of risk score systems for patients presenting with upper gastrointestinal bleeding: international multicenter prospective study. BMJ. 2017;356: i6453.
- Wang CH-Y, Qin J, Wang J, Sun CH-Y, Cao T, Zhu D-D.Rockall score in predicting outcomes of elderly patients with acute upper gastrointestinal bleeding. World J Gastroenterol. 2013;
19(22):3466-72. - Leblanc S, Vienne A, Dhooge M, Coriat R, Chaussade S, Prat F. Early experience with a novel hemostatic powder used to treat upper GI bleeding related to malignancies or after therapeutic interventions. Gastrointest. Endosc. 2013,78(1):169-75.
- Haddara S, Jacques J, Lecleire S, Branche J, et al. A novel hemostatic powder for upper gastrointestinal bleeding: a multicenter study (the “GRAPHE” registry). Endoscopy. 2016;48(12):
1084-95. - Song IJ, Kim HJ, Lee JA, et al. Clinical outcomes of endoscopic hemostasis for bleeding in patients with unresectable advanced gastric cancer. J Gastric Cancer. 2017;17:374-83.
- Loftus EV, Alexander GL, Ahlquist DA, et al. Endoscopic treatment of major bleeding from advanced gastroduodenal malignant lesions. Mayo Clin Proc.1994;69:736-40.
- Savides TJ, Jensen DM, Cohen J, et al. Severe upper gastrointestinal tumor bleeding: endoscopic findings, treatment, and outcome. Endoscopy. 1996;28:244-8.
- Sheibani S, Kim JJ, Chen B, et al. Natural history of acute upper GI bleeding due to tumours: short-term success and long-term recurrence with or without endoscopic therapy. Aliment Pharmacol Ther. 2013;38:144-50.
- Chang YT, Wang HP, Huang SP, et al. Clinical application of argon plasma coagulation in endoscopic hemostasis for non-ulcer non-variceal gastrointestinal bleeding: a pilot study in Taiwan. Hepatogastroenterology. 2002;49:441-3.
- Martins BC, Wodak S, Gusmon CC, et al. Argon plasma coagulation for the endoscopic treatment of gastrointestinal tumor bleeding: a retrospective comparison with a non-treated historical cohort. United Eur Gastroenterol J. 2016;4:49-54.
- Akhtar K, Byrne JP, Bancewicz J, et al. Argon beam plasma coagulation in the management of cancers of the esophagus and stomach. Surg Endosc. 2000;14:1127-30.
- Chen YI, Barkun AN. Hemostatic powders in gastrointestinal bleeding: a systematic review. Gastrointest Endosc Clin North Am. 2015;25:535-52.
- Thosani N, Rao B, Ghouri Y, et al. Role of argon plasma coagulation in management of bleeding GI tumors: evaluating outcomes and survival. Turk J Gastroenterol. 2014;25(Suppl 1):38-42.
- Raymond Shi Liang Yii, Kee Huat Chuah, Keat Seong Poh, Peng Choong Lau et al. Retained Endoscope: An Unexpected but Serious Complication of Hemospray. Digestive Diseases and Sciences. 2022;67:344-7.
- Karna R, Deliwala S, Ramgopal B, Mohan BP, Kassab L, et al. Efficacy of topical hemostatic agents in malignancy-related GI bleeding: a systematic review and meta-analysis. Gastrointest Endosc. 2023;97:202-8.
- Paoluzi OA, Cardamonea C, Aucello A, Neri B, Grassoa E, Giannellia M, Di Iorio L, et al. Efficacy of hemostatic powders as monotherapy or rescue therapy in gastrointestinal bleeding related to neoplastic or non-neoplastic lesions. Scand J of Gastroenterol. 2021;56(12):1506-13.
Correspondencia: Alejandro Marcelo Suárez
Correo electrónico: alemarsuarez60@gmail.com
Acta Gastroenterol Latinoam 2023;53(3):291-300
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE