Claudio Murillo Matamoros, Marta Muñiz Muñoz, Miguel Suárez Matías, Pablo Olcina Domínguez, Laura Valiente González, María del Moral Martínez, Teresa de Jesús Martínez Pérez, Raquel Martínez Fernández, Carmen Julia Gómez Ruiz, Miriam Viñuelas Chicano, Julia Morillas Ariño, Jesús García Cano Lizcano, José Ignacio Pérez García
Servicio de Aparato Digestivo, Hospital Virgen de la Luz. Cuenca, España.
Acta Gastroenterol Latinoam 2020;50(2):173-176
Recibido: 17/11/2018 / Aprobado: 23/04/2019 / Publicado en www.actagastro.org el 29/06/2020
Resumen
La pancreatitis del surco es un tipo muy infrecuente de pancreatitis crónica de etiología incierta, que ocurre en el surco pancreatoduodenal. A pesar de los grandes avances en las técnicas de imagen, realizar un diagnóstico definitivo es dificultoso por la compleja anatomía de esta área. Por este motivo, el tratamiento quirúrgico es requerido con frecuencia debido a la imposibilidad de excluir malignidad. Presentamos el caso de un paciente con antecedente de pancreatitis crónica que ingresa por clínica de obstrucción duodenal. El diagnóstico fue difícil, sobre todo por la necesidad de excluir procesos neoplásicos de la encrucijada duodenopancreática. La ecoendoscopía resultó fundamental para establecer un diagnóstico definitivo, permitiendo la realización de PAAF y la correcta valoración de la pared duodenal.
Palabras claves. Pancreatitis crónica, estenosis duodenal, ecoendoscopía.
Groove pancreatitis: a diagnostic and therapeutic challenge
Summary
Groove pancreatitis is a very uncommon type of chronic pancreatitis of uncertain etiology that occurs in the pancreatoduodenal groove. Despite the great advances in imaging techniques, making a definitive diagnosis is difficult because of the complex anatomy of this area. Therefore, surgical treatment is often required due to the impossibility of excluding malignancy. We present the case of a patient with a history of chronic pancreatitis admitted due to duodenal obstruction. The diagnosis was difficult, especially for the need to exclude the neoplasms of the duodenal-pancreatic area. Endoscopic ultrasound was essential to establish a definitive diagnosis, allowing FNAP and correct assessment of the duodenal wall.
Key words. Chronic pancreatitis, duodenal stenosis, endosonography.
Abreviaturas
PAAF: Punción aspiración con aguja fina.
CEA: Antígeno carcinoembrionario.
CA 19-9: Antígeno carbohidrato 19-9.
TAC: Tomografía axial computarizada.
RMN: Resonancia magnética nuclear.
DPC: Duodenopancreatectomía cefálica.
Introducción
La pancreatitis crónica del surco pancreatoduodenal es un tipo de pancreatitis crónica segmentaria caracterizada por cicatrización fibrótica del surco, un área comprendida entre la cabeza del páncreas (medialmente), la segunda porción duodenal (lateralmente), la región antral (anterior) y la tercera porción duodenal (posterior).1 Su fisiopatología parece poco clara, aunque se cree que el consumo de alcohol y la presencia de tejido pancreático ectópico en la región duodenal pueden jugar un papel en su desarrollo.2 La incidencia reportada varía entre un 2,7% y 24,5% de casos de pancreatoduodenectomías realizadas por pancreatitis crónica.3, 4 Puede simular un carcinoma pancreático,5, 6 coexistir con él, o incluso enmascararlo.7
Se presenta un caso clínico de un paciente con pancreatitis del surco en el que la ecoendoscopía resultó de gran utilidad para establecer el diagnóstico definitivo y como guía terapéutica. Debe tenerse en cuenta como parte del diagnóstico diferencial en pacientes con antecedente de pancreatitis crónica con masas pancreáticas o estenosis duodenales que presentan clínica de obstrucción duodenal.
Caso clínico
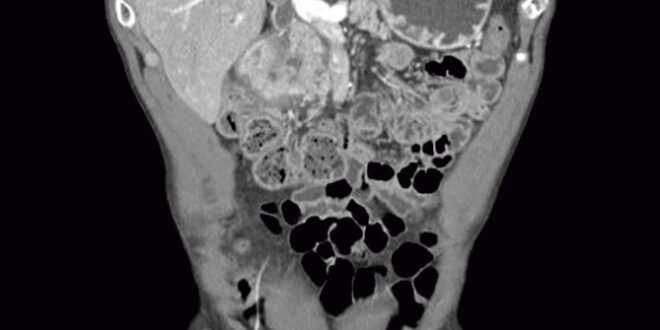
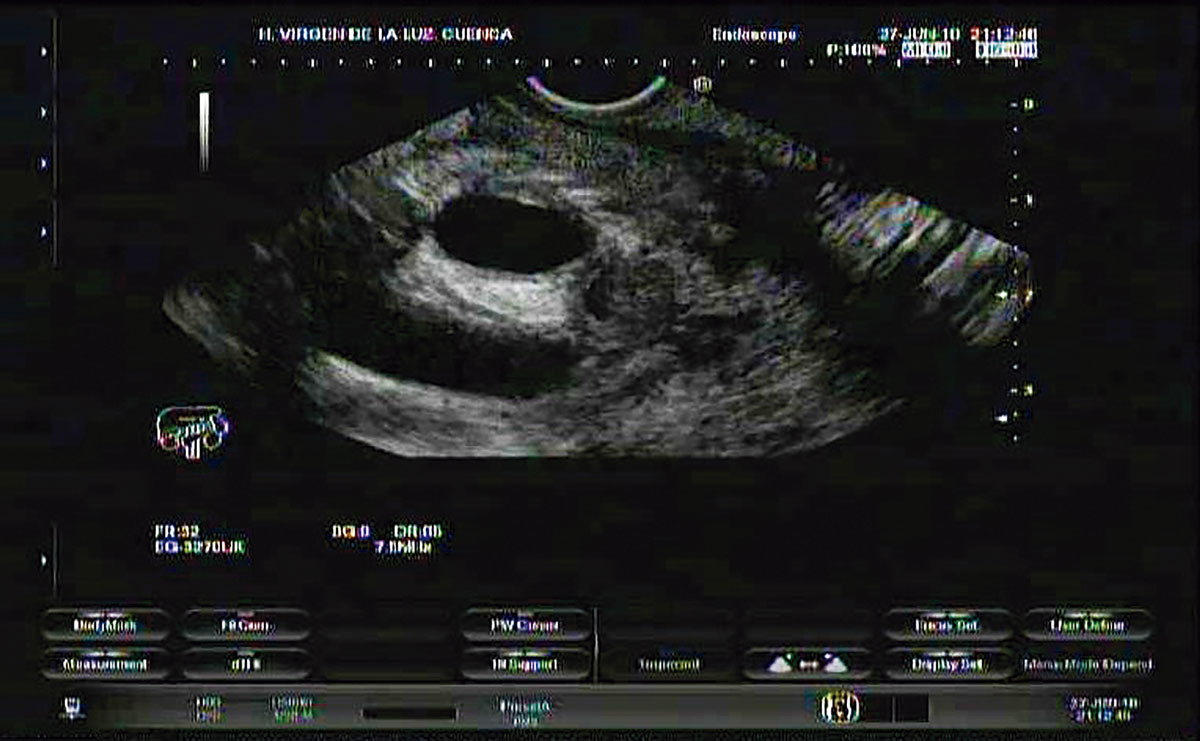
Varón de 45 años de edad que acude al servicio de urgencias por náuseas y vómitos biliosos incoercibles, de varias horas de evolución, que le impiden la ingesta oral, asociado a dolor en hemiabdomen superior y pérdida de peso no cuantificada. El paciente tiene historia de abuso de alcohol desde hace 16 años, y fue diagnosticado de pancreatitis crónica de etiología alcohólica hace 14 meses. Al examen físico destacaba presentar palidez mucocutánea y signos de desnutrición. Analíticamente presentaba patrón de colestasis, discreta elevación de amilasa y leve elevación de los marcadores tumorales CEA y CA-19.9 (solicitados por antecedente de carcinoma gástrico precoz resecado endoscópicamente). Dados sus antecedentes se realiza un TAC abdominal (Figura 1) que muestra dilatación de la vía biliar intrahepática y extrahepática así como engrosamiento del píloro, primera y segunda porción duodenal con realce submucoso y alguna colección parietal, sugestivo de pancreatitis crónica del surco pancreatoduodenal. Se realiza una gastroscopía (Figuras 2 y 3) en la que se visualiza una mucosa irregular a nivel de bulbo y de primera rodilla duodenal con importante engrosamiento de pliegues con mucosa edematosa, friable y erosionada que estenosa parcialmente la luz permitiendo el paso del endoscopio, pero sin distender a la insuflación; a nivel de segunda rodilla duodenal, la mucosa es de aspecto normal. Se toman biopsias de primera rodilla duodenal, que son negativas para malignidad. Se decide completar el estudio mediante ecoendoscopía (Figura 4), que muestra una masa en cabeza de páncreas que provoca atrapamiento de la vía biliar (Figura 5), y segunda porción duodenal con engrosamiento evidente de la capa mucosa, siendo la muscular propia normal. Se realiza PAAF, la cual fue negativa para células malignas, mostrando una inflamación crónica inespecífica.
Figura 1. TAC abdominal: puede observarse dilatación de la vía biliar intrahepática y extrahepática así como engrosamiento del píloro, primera y segunda porción duodenal con realce submucoso y alguna colección parietal, sugestivo de pancreatitis crónica del surco pancreatoduodenal.

Figura 2. Gastroscopia: se visualiza una mucosa irregular a nivel de bulbo y de primera rodilla duodenal con importante engrosamiento de pliegues con mucosa edematosa que estenosa parcialmente la luz permitiendo el paso del endoscopio, pero sin distender a la insuflación.
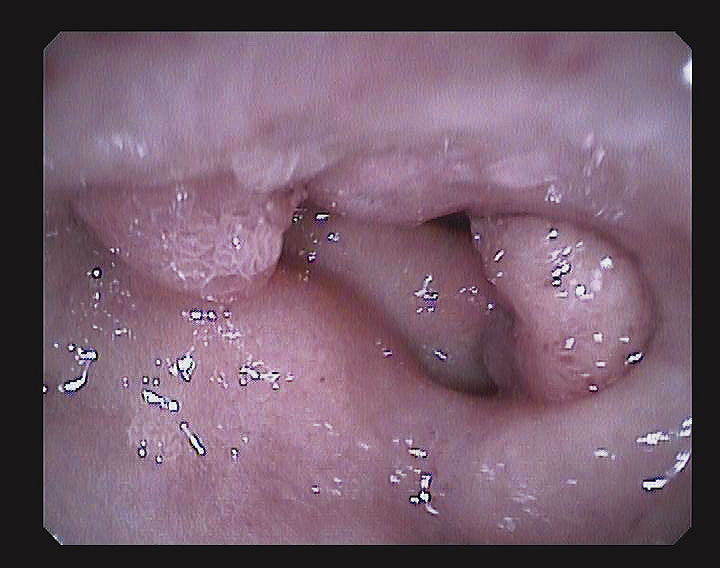
Figura 3. Gastroscopia: a nivel de segunda rodilla duodenal, la mucosa es de aspecto normal.

Figura 4 y 5. Ecoendoscopía: masa en cabeza de páncreas que provoca atrapamiento de la vía biliar.

Con el diagnóstico de pancreatitis del surco, se presenta el caso en sesión multidisciplinar y se decide intervención quirúrgica. Se visualiza induración de todo el páncreas, y masa inflamatoria en cabeza pancreática. Se toman muestras del quiste en cabeza pancreática para citología. Se realiza gastroyeyunostomía de tipo Braun en cara posterior, con anastomosis yeyunoyeyunal a pie de asa, que cursa sin complicaciones inmediatas. En la citología del quiste de cabeza pancreática se visualizan células mesoteliales reactivas, macrófagos y células epiteliales sin atipias.
En el momento actual el paciente presenta buen estado general, ha ganado peso y no ha vuelto a presentar crisis de dolor abdominal ni vómitos.
Discusión
El diagnóstico diferencial de la pancreatitis del surco incluye tras grandes categorías: las lesiones inflamatorias, las neoplasias y las anomalías congénitas. Puede cursar de forma asintomática o producir dolor abdominal, pancreatitis agudas de repetición, pérdida de peso, náuseas y vómitos, en relación con cambios inflamatorios, la fibrosis local y la estenosis duodenal.8 Más raramente, se ha descrito ictericia como consecuencia de la compresión de la vía biliar.9
Las pruebas de imagen como la ecografía, TAC o RMN pueden orientarnos al diagnóstico, observando un engrosamiento de la pared duodenal, así como lesiones quísticas intraparietales. En algunos casos podremos observar cambios compatibles con pancreatitis crónica, dilatación de colédoco o conducto pancreático principal o dilatación gástrica secundaria a la estenosis duodenal producida por los quistes.10
La endoscopía digestiva alta puede mostrar una estenosis duodenal, con cierto edema y eritema mucoso, siendo las biopsias inespecíficas.11
La ecoendoscopía constituye la técnica más útil en el diagnóstico, ya que nos va a permitir valorar la pared duodenal, el parénquima pancreático y obtener estudio histológico.12 En un estudio que evaluó el rendimiento de PAAF por ecoendoscopía en pacientes con masas pancreáticas, la sensibilidad y especificidad fueron del 94,7% y 100%, respectivamente.13
El tratamiento sigue siendo controvertido. La duodenopancreatectomía cefálica (DPC) representa el procedimiento clásicamente utilizado. Las derivaciones como la gastroenteroanastomosis o la quistoyeyunostomía también han sido descritas.14 Una cirugía más conservadora, como la resección segmentaria duodenal, puede ser de elección en algunos casos, como el de nuestro paciente.15
Conclusión
La pancreatitis crónica del surco pancreatoduodenal probablemente se trate de una entidad más frecuente de lo que se ha referido en la bibliografía, y cuyo diagnóstico precisa un alto índice de sospecha. La ecoendoscopía permite en estos casos hacer el diagnóstico diferencial con otras lesiones quísticas extradigestivas y guiar el tratamiento más apropiado para el paciente.
Sostén financiero. No se han recibido becas ni aportes económicos para la realización de la publicación.
Referencias
- Yu J, Fulcher AS, Turner MA, Halvorsen RA. Normal Anatomy and Disease Processes of the Pancreatoduodenal Groove: imaging Features. American Journal of Roentgenology 2004; 183: 839-846.
- Casetti L, Bassi C, Salvia R, Butturini G, Graziani R, Falconi M, Frulloni L, Crippa S, Zamboni G, Pedrezoli P. ‘‘Paraduodenal’’ pancreatitis: results of surgery on 58 consecutives patients from a single institution. World J Surg 2009; 33: 2664-2669.
- Stolte M, Weiss W, Volkholz H, Rosch W. A special form of segmental pancreatitis: “groove pancreatitis” Hepatogastroenterology 1982; 29: 198-208.
- Yamaguchi K, Tanaka M. Groove pancreatitis masquerading as pancreatic carcinoma. Am J Surg 1992; 163: 312-316.
- Levenick JM, Gordon SR, Sutton JE, Suriawinata A, Gardner TB. A comprehensive, case based review of groove pancreatitis. Pancreas 2009; 38: 169-175.
- Manzelli A, Petrou A, Lazzaro A, Brennan N, Soonawalla Z, Friend P. Groove pancreatitis. A mini series report and review of literature. Journal of The Pancreas 2011; 12: 230-233.
- Malde DJ, Oliveira-Cunha M, Smith AM. Pancreatic carcinoma masquerading as groove pancreatitis: Case report and review of the literature. Journal of The Pancreas 2011; 12: 598-602.
- Repiso A, Gómez-Rodríguez R, García-Vela A, Martínez-Chacón J, González de Frutos C, Pérez-Grueso MJ, Carrobles JM. Cystic dystrophy of the duodenal wall. An underdiagnosed complication in aberrant pancreas. Gastroenterol Hepatol 2006; 29: 345-348.
- Rebours V, Lévy P, Vullierme MP, Couvelard A, O’Toole D, Aubert A, Palazzo L, Sauvanet A, Hammel P, Maire F, Ponsot P, Ruszniewski P. Clinical and morphological features of duodenal cystic dystrophy in heterotopic pancreas. Am J Gastroenterol 2007; 102: 871-879.
- Fléjou JF, Potet F, Molas G, Bernades P, Amouyal P, Fékété F. Cystic dystrophy of the gastric and duodenal wall developing in heterotopic pancreas: an unrecognised entity. Gut 1993; 34: 343-347.
- Jacobson BC, Crawford JM, Farraye FA. GI Tract Endoscopic and Tissue Processing Techniques and Normal Histology. Surgical Pathology of the GI Tract, Liver, Biliary Tract, and Pancreas 2009: 3-30.
- Argüello L, Pellisé M, Miquel R. Utilidad de la ultrasonografía endoscópica en la evaluación de los tumores submucosos y compresiones extrínsecas del tubo digestivo. Gastroenterol Hepatol 2002; 25: 13-18.
- Eloubeidi MA, Jhala D, Chhieng DC, Chen VK, Eltoum I, Vickers S. Yield of endoscopic ultrasound-guided fine-needle aspiration biopsy in patients with suspected pancreatic carcinoma: emphasis on atypical, suspicious, and false-negative aspirates. Cancer 2003; 99: 285-229.
- Bauer P, Smadja M, Lechaux JP. Dystrophie kystique sur pancreas aberrant traitée par gastro-entérostomie. Presse Med 1993; 22: 964-965.
- Marmorale A, Tercier S, Peroux JL, Monticelli I, McNamara M, Huguet CM, Huguet C. Cystic dystrophy in heterotopic pancreas of the second part of the duodenum. One case of conservative surgical procedure. Ann Chir 2003; 128: 180-184.
Correspondencia: Claudio Murillo Matamoros
Hospital Virgen de la Luz. 16002, Cuenca, España
Tel.: +34 969-179-928
Correo electrónico: muri11@hotmail.com
Acta Gastroenterol Latinoam 2020;50(2):173-176
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE