Ana L. Ordoñez-Vázquez1 ID· Abigail Fuentes-Montalvo2 ID· Enrique Coss-Adame2 ID
1 Departamento de Gastroenterología del IMSS Hospital General de Zona No. 33, Bahía de Banderas, San Clemente de Lima, Nayarit, Tepic.
2 Laboratorio de Motilidad Gastrointestinal del Instituto de Ciencias Médicas y Nutrición Salvador Zubirán, CDMX, CDMX.
Acta Gastroenterol Latinoam 2025;55(2): 88-102
Recibido: 23/05/2025 / Aceptado: 10/06/2025 / Publicado online: 30/06/2025 / https://doi.org/10.52787/agl.v55i2.495
Resumen
La malabsorción de lactosa y la intolerancia a la lactosa son condiciones frecuentes, clínicamente distintas. La malabsorción de lactosa se refiere al paso de este carbohidrato no digerido al colon, debido a deficiencia de lactasa, mientras que la intolerancia implica la aparición de síntomas gastrointestinales tras su ingesta, en presencia de malabsorción. La alactasia es una forma congénita rara de ausencia total de actividad de la lactasa. La hipolactasia primaria es una reducción fisiológica y genética de la lactasa en la edad adulta. La prevalencia global de malabsorción alcanza hasta dos tercios de la población, con cifras elevadas en América Latina y México. El diagnóstico puede realizarse mediante pruebas no invasivas, como la prueba de aliento con lactosa, pruebas genéticas, test de gaxilosa y prueba de tolerancia a la lactosa; o bien mediante métodos invasivos como la medición enzimática en biopsias duodenales. El tratamiento debe centrarse en controlar los síntomas sin comprometer el estado nutricional, mediante dietas bajas en lactosa, suplementos de lactasa exógena y el uso de probióticos o prebióticos. Es fundamental evitar restricciones innecesarias que puedan llevar a deficiencias nutricionales o a trastornos alimentarios, como el de restricción o evitación de la ingesta de alimentos. Un enfoque diagnóstico y terapéutico individualizado mejora la calidad de vida y el manejo clínico de estos pacientes.
Palabras claves. Lactosa, lactasa, intolerancia, malabsorción, hipolactasia.
Lactose Malabsorption and Intolerance
Summary
Lactose malabsorption and lactose intolerance are common yet clinically distinct conditions. Lactose malabsorption refers to the passage of undigested lactose into the colon due to lactase deficiency, whereas lactose intolerance involves the onset of gastrointestinal symptoms following lactose ingestion in the presence of malabsorption. Alactasia is a rare congenital disorder characterized by complete absence of lactase activity. Primary hypolactasia is a physiological and genetically determined decline in lactase activity occurring in adulthood. Globally, the prevalence of lactose malabsorption affects up to two-thirds of the population, with particularly high rates in Latin America and Mexico. Diagnosis can be established through non-invasive methods such as the hydrogen breath test, genetic testing, the gaxilose test, and lactose tolerance testing, or through invasive procedures like enzymatic activity measurement in duodenal biopsies. Management should aim to control symptoms without compromising nutritional status and may include low-lactose diets, oral lactase enzyme supplementation, and the use of probiotics or prebiotics. Avoiding unnecessary dietary restrictions is essential to prevent nutritional deficiencies or the development of avoidant/restrictive food intake disorder. An individualized diagnostic and therapeutic approach improves both clinical outcomes and quality of life in affected patients.
Keywords. Lactose, lactase, intolerance, malabsorption, hypolactasia.
Abreviaturas
FODMAPs: Oligosacáridos, disacáridos, monosacáridos y polioles fermentables, por sus siglas en inglés.
IL: Intolerancia a la lactosa.
DPL: Deficiencia primaria de lactasa.
MA: Malabsorción de lactosa.
HAE: Prueba de medición de hidrógeno en aire espirado.
ARFID: Trastorno por evitación o restricción de la ingesta alimentaria, por su sigla en inglés.
H2: Hidrógeno.
CO2: Dióxido de carbono.
CH4: Metano.
AGCC: Ácidos grasos de cadena corta.
PLP: Persistencia de la lactasa primaria.
SII: Síndrome de intestino irritable.
SIBO: sobrecrecimiento bacteriano de intestino delgado, por sus siglas en inglés.
TICI: Trastornos de la interacción cerebro-intestino.
NPL: No persistencia de lactasa.
O2: Oxígeno.
N2: Nitrógeno.
H2S: Sulfuro de hidrógeno.
NH3: Amoníaco.
Ppm: Partes por millón.
GOS: Galactooligosacáridos.
UFC: Unidades formadoras de colonias.
S-NIAS: Prueba de detección de nueve ítems del trastorno por evitación o restricción de la ingesta alimentaria, por su sigla en inglés.
Introducción
Se estima que el 70% de los adultos que experimentan dolor y distensión abdominal, meteorismo y/o diarrea refieren como desencadenante o factor exacerbante el consumo de alimentos como los lácteos y/o ciertos carbohidratos. De esta población, el 89% ya ha realizado restricciones dietéticas antes de acudir a una valoración médica, principalmente mediante una dieta sin lactosa o baja en oligosacáridos, disacáridos, monosacáridos y polioles fermentables (FODMAPs), sin considerar que el consumo de lácteos puede ofrecer beneficios para la salud y la microbiota en cualquier etapa de la vida.1 Por lo tanto, la restricción injustificada de lácteos podría tener consecuencias negativas en la calidad de vida y en el estado nutricional de los pacientes. A pesar de que la primera descripción de casos de intolerancia a la lactosa (IL) data del año 400 a. C, la entidad clínica comenzó a reconocerse en los últimos cincuenta años.2 La prevalencia aproximada de la IL es del 57% a nivel global, del 50% en Sudamérica, y del 53% en la población mexicano-estadounidense.3 En México, la causa más común es la deficiencia primaria de lactasa (DPL), que se estima que ocurre en el 30% de los mexicanos adultos.4 El síndrome clínico más común de malabsorción de carbohidratos es el relacionado con la lactosa. Sus características clínicas son inespecíficas, se asemejan y/o pueden superponerse con otros trastornos funcionales digestivos y/o enteropatías, e incluyen meteorismo, distensión abdominal y diarrea osmótica.5 La malabsorción de lactosa (MA) y la IL son dos entidades clínicas distintas que con frecuencia se confunden, son pobremente abordadas por el inusual uso de métodos diagnósticos como la prueba de medición de Hidrógeno en aire espirado (HAE) o prueba de aliento con lactosa y, por ello, están sobre diagnosticadas. Otro factor, otro factor que dificulta el abordaje diagnóstico es la falta de un método estándar de oro, la disponibilidad limitada de los métodos actuales en la mayoría de los centros de atención clínica y el costo de estos. En pacientes en quienes se confirma la presencia de MA e IL, el manejo debe ser multidisciplinario y el pilar del tratamiento debe ser la modificación dietética que promueva la resolución de los síntomas, sin incrementar el riesgo de desnutrición ni el desarrollo del trastorno por evitación o restricción de la ingesta alimentaria (ARFID, por su sigla en inglés).
El objetivo de esta revisión narrativa es actualizar la evidencia más reciente relacionada con la MA e IL en la población adulta. No se abordarán los errores congénitos del metabolismo de la lactosa, como la deficiencia congénita de lactasa (alactasia), la cual tiene un patrón de herencia autosómico recesivo y es grave, ni la entidad conocida como alergia a la proteína de la leche de vaca.
Conceptos fisiopatológicos
● ¿Qué es la lactosa y dónde podemos encontrarla?
La lactosa, también conocida como β-galactosil-1,4-glucosa, es un disacárido y constituye el principal carbohidrato presente en la leche y sus derivados. La leche es un alimento producido exclusivamente por especies de mamíferos, incluidos los humanos, con excepción de los leones marinos y las morsas. La lactosa es relevante en la nutrición humana ya que, en la etapa neonatal y la infancia, la leche materna constituye la principal fuente de nutrientes, proporcionando glucosa y aminoácidos. Sin embargo, en la vida adulta, su consumo tiende a disminuir progresivamente, sin que esto comprometa el aporte de macro y micronutrientes, al formar parte de una dieta variada y equilibrada. La leche humana es la que tiene el aporte más elevado de lactosa (7,5 g/100 mL vs. 5 g/100 mL en leche de vaca y otros mamíferos).6 La cantidad de lactosa en los alimentos lácteos es proporcionalmente inversa al grado de fermentación (a mayor fermentación, mayor producción de ácido láctico y menor contenido de lactosa), como se observa en la Figura 1.
Además, pueden encontrarse cantidades pequeñas de lactosa en alimentos no lácteos como carnes, pan, salsas, postres, aceites y grasas, así como en medicamentos (como excipientes o principios activos), conservantes y aditivos.
Figura 1. Contenido de lactosa en distintos tipos de lácteos y derivados
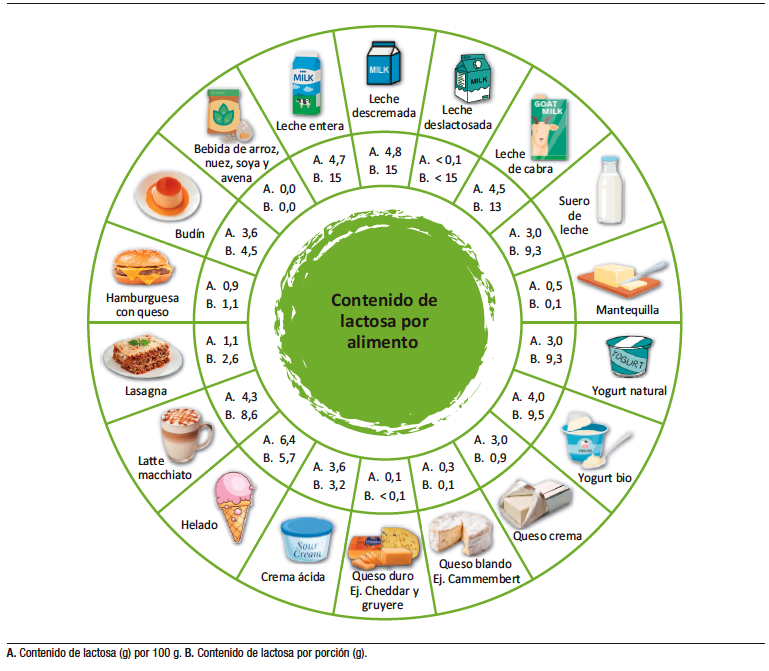
● ¿Cómo se lleva a cabo la digestión y absorción de la lactosa?
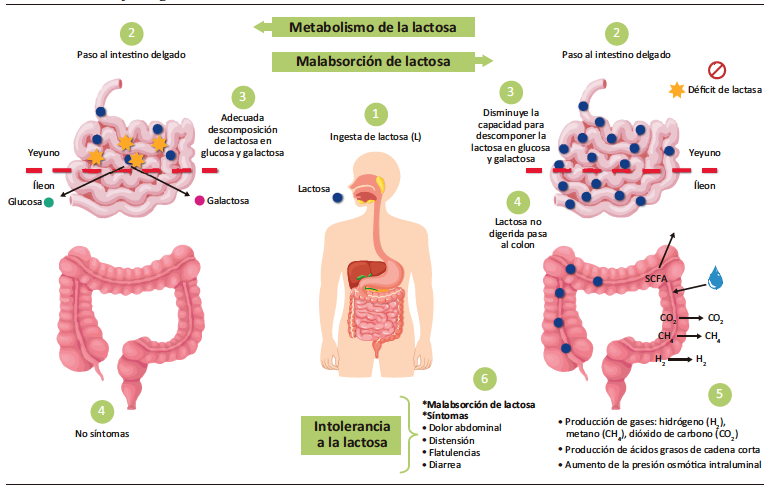
La lactasa es una enzima perteneciente a la familia de las β-galactosidasas, que cataliza la hidrólisis de la lactosa en D-glucosa y D-galactosa. Se localiza en el borde en cepillo de los enterocitos maduros, con máxima expresión en el yeyuno medio.6 Es la última disacaridasa del intestino delgado en desarrollarse durante la vida intrauterina. En recién nacidos prematuros (26-34 semanas de gestación), su actividad alcanza aproximadamente el 30% de su capacidad funcional, mientras que en recién nacidos a término se encuentra en su punto máximo. Posteriormente, durante las primeras dos décadas de vida, su actividad disminuye de forma progresiva,7 lo que sugiere que la hipolactasia primaria o deficiencia primaria de lactasa es un evento programado y normal en el desarrollo de la vida adulta. Durante la digestión, la lactasa escinde la molécula de lactosa mediante su actividad α-glucosidasa, y los monosacáridos resultantes son transportados activamente hacia los enterocitos por el transportador sodio/glucosa SGLT1. En condiciones de alta concentración de lactosa, interviene un segundo transportador: GLUT2. Desde los enterocitos, la glucosa se desplaza hacia los capilares por difusión facilitada. En presencia de MA, la lactosa no digerida entra en contacto con el microbiota intestinal. Su fermentación bacteriana incrementa la producción de hidrógeno (H2), dióxido de carbono (CO2), metano (CH4) y ácidos grasos de cadena corta (AGCC). La lactosa no digerida genera un aumento en la osmolaridad, provocando el desplazamiento de agua hacia la luz intestinal. Además, la fermentación en el colon incrementa la carga osmótica. En resumen, se produce dolor abdominal, distensión y diarrea osmótica, si la carga de lactosa excede la capacidad fermentativa de la microbiota colónica o si la producción de AGCC supera la capacidad de reabsorción del colon.8 En la Figura 2 se ilustran los principales mecanismos fisiopatológicos relacionados con la MA y la IL.
Figura 2. Eventos fisiológicos durante el metabolismo de la lactosa, malabsorción e intolerancia a la lactosa
● ¿Cuáles son los beneficios de consumir lácteos?
Los lácteos son una fuente importante de proteínas, calcio, magnesio, potasio, selenio, zinc, vitamina A, vitamina B12, vitamina D, riboflavina, ácido pantoténico y leucina. Estos micronutrientes contribuyen al proceso anabólico de formación de masa muscular, al aporte adecuado de calcio y vitamina D, y a la prevención de fracturas por fragilidad en adultos mayores. Evidencia reciente ha demostrado efectos positivos del consumo de lactosa sobre el estado general de salud en la población adulta. Además, un metaanálisis reciente de estudios prospectivos identificó que el consumo total de lácteos se asocia con un riesgo modestamente menor de hipertensión, enfermedad coronaria y accidente cerebrovascular.9 En pacientes con MA e IL, la lactosa podría ejercer una actividad prebiótica al promover el crecimiento de bacterias comensales como Bifidobacterias y Lactobacillus y la reducción de especies como Bacteroides y Clostridia, contribuyendo al equilibrio de la microbiota colónica y a la diferenciación de los colonocitos.10, 11
● Genética molecular de la malabsorción e intolerancia a la lactosa
La lactasa está codificada por el gen MCM6, localizado en el brazo largo del cromosoma 2 (región 2q21), y su expresión está regulada por una región promotora. En estudios genéticos de pacientes con MA, se han identificado dos formas de deficiencia de lactasa: a) la deficiencia congénita, que es un error del metabolismo con manifestaciones graves desde la etapa neonatal y b) la hipolactasia primaria o DPL, que es un fenómeno fisiológico del desarrollo humano asociado con la regulación negativa de la expresión de lactasa, relacionado con los genotipos C/C-13910 y G/G-13915. Sin embargo, como resultado de mutaciones de ganancia de función ocurridas a lo largo de la evolución humana, existe una proporción de la población que presenta un genotipo de persistencia de lactasa primaria (PLP), asociado con una alta actividad de lactasa durante toda la vida y con un fenotipo de tolerancia a grandes cantidades de lactosa en la dieta. Esta variante se observa predominantemente en poblaciones europeas, africanas, de Oriente Medio y del sur de Asia. Los genotipos correspondientes incluyen el alelo mutante C/T-13910 y T/T-13910.12 Adicionalmente a los genotipos previamente descritos, se han identificado otros polimorfismos en la región promotora del gen de la lactasa cuya prevalencia varía según la región geográfica. También se han descrito procesos epigenéticos relacionados con la metilación del ADN dependientes de la edad, que influyen en la expresión clínica del fenotipo.13, 14
● Panorama epidemiológico de la malabsorción e intolerancia a la lactosa
La prevalencia e incidencia globales de MA e IL pueden estar subestimadas o sobrestimadas debido a la ausencia de un estándar de oro diagnóstico. Se estima que la MA afecta aproximadamente a dos tercios de la población mundial, con una amplia variación geográfica: desde el 28% en Europa hasta el 70% en Oriente Medio. En general, la frecuencia aumenta con la edad, en relación con los cambios fisiológicos previamente descritos en la actividad de la lactasa.10 Un estudio de 2021 reportó una prevalencia de IL del 66% (57-75%) en la población general, 54% (37-70%) en consumidores de lácteos (> 15 g de lactosa al día) y 73% (61-84%) en no consumidores. Notablemente, la IL fue más frecuente entre los no consumidores de lácteos (PR 1,36; IC95%: 0,99 – 1,89) y en personas con síndrome de intestino irritable (SII).15,16 Nybacka y cols. identificaron una asociación entre la presencia de SII y la evitación del consumo de lactosa (OR 5,0; p < 0,001), relacionada con la presencia de dolor abdominal, preocupación y ansiedad.16 Estudios previos han mostrado que la ingesta media de proteínas, calcio, vitaminas D y B12 en adultos que no consumen lácteos es menor que en aquellos que los consumen. Esto sugiere un posible impacto negativo de estrategias terapéuticas no justificadas para el manejo de la IL, las cuales podrían limitar la inclusión de alimentos ricos en nutrientes en la dieta de adultos mayores.16 Finalmente, la IL se asocia con una percepción negativa de la calidad de vida. En un estudio que incluyó a 580 pacientes a quienes se les realizó una prueba de aliento con 50 g de lactosa para detectar MA, se observó que aquellos con IL presentaban una peor percepción de su calidad de vida en comparación con los pacientes en los que únicamente se demostró MA (p < 0,01),17 y esto influía en la decisión de restringir alimentos como los lácteos.
● La hipolactasia, la malabsorción de lactosa y la intolerancia a los lácteos: conceptos confusos y difusos
Debido a la compleja y heterogénea respuesta clínica a la exposición a lactosa en las distintas etapas del desarrollo humano, se han impulsado investigaciones sobre su metabolismo y los factores genéticos que lo regulan, la prevalencia de los diferentes genotipos y fenotipos a nivel global, y una nomenclatura específica para aplicar en la evaluación de pacientes con sospecha de MA e IL. A continuación, se presentan conceptos de utilidad y, más adelante, presentamos un esquema para el mejor entendimiento de los fenotipos relacionados con MA e IL (Figura 3).
A) Alactasia: ausencia de actividad enzimática de lactasa. En sentido estricto, solo ocurre como consecuencia de la deficiencia congénita de lactasa, una enfermedad rara y de herencia autosómica recesiva, caracterizada por diarrea acuosa grave en lactantes alimentados con leche materna o con cualquier fórmula que contenga lactosa.18
B) Hipolactasia o deficiencia de lactasa: estado de expresión reducida de lactasa en comparación con los recién nacidos a término. Se puede dividir en dos tipos: primaria (fenotipo de no persistencia de la lactasa o hipolactasia primaria del adulto) o secundaria (estados patológicos que se enumeran en la Figura 4 y causan reducción en la expresión de lactasa por lesión del borde en cepillo y del epitelio intestinal). Los conceptos MA, maldigestión de lactosa e IL no son sinónimos de este concepto ni son sinónimos entre sí.
Figura 3. Fenotipos relevantes del metabolismo de la lactosa
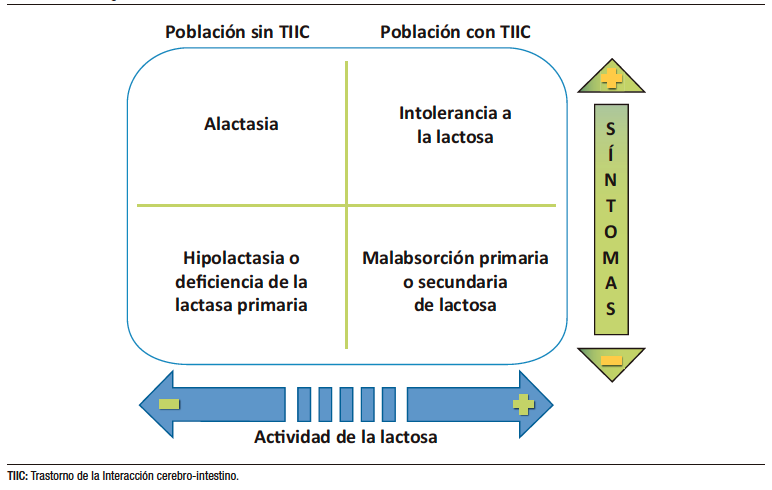
Figura 4. Causas primarias y secundarias de deficiencia de lactasa
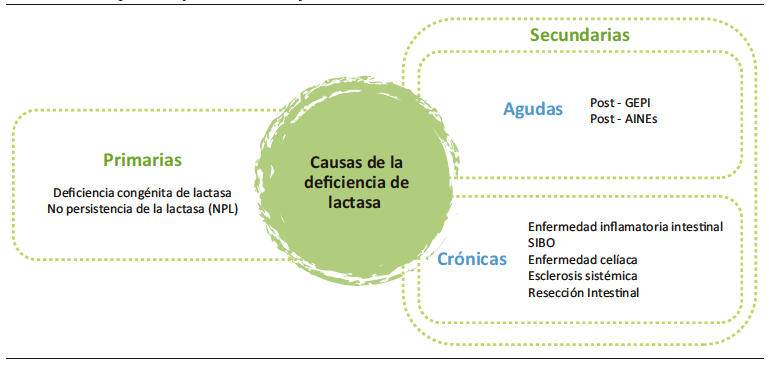
C) Malabsorción de lactosa (MA): paso de lactosa hacia el colon (falla en la digestión y/o absorción de monosacáridos en el intestino delgado). Existen causas primarias y secundarias. La causa más frecuente es la hipolactasia primaria del adulto. Entre las causas secundarias de MA, se enumeran condiciones en las que hay daño epitelial con destrucción de vellosidades intestinales y, por ende, disminución de lactasa, por ejemplo: enfermedad celíaca, gastroenteritis, esclerosis sistémica, resección intestinal (tránsito acelerado), sobrecrecimiento bacteriano del intestino delgado (SIBO), enfermedad de Crohn. La identificación de MA de carbohidratos, y específicamente de lactosa, se puede realizar con métodos objetivos, como se explicará más adelante. Los pacientes con MA pueden estar asintomáticos, es decir sin presentar IL, ya que habitualmente una dosis de 12 g de lactosa (250 mL de leche) se tolera bien si se consume combinada con otros alimentos o se distribuye a lo largo de un día.8
D) Intolerancia a la lactosa (IL): se define como la aparición de síntomas gastrointestinales (borborigmo, meteorismo, dolor abdominal, distensión abdominal, bloating y diarrea) luego de la exposición a lactosa en personas con MA (factor necesario).
● La discordancia entre los síntomas y el metabolismo de la lactosa
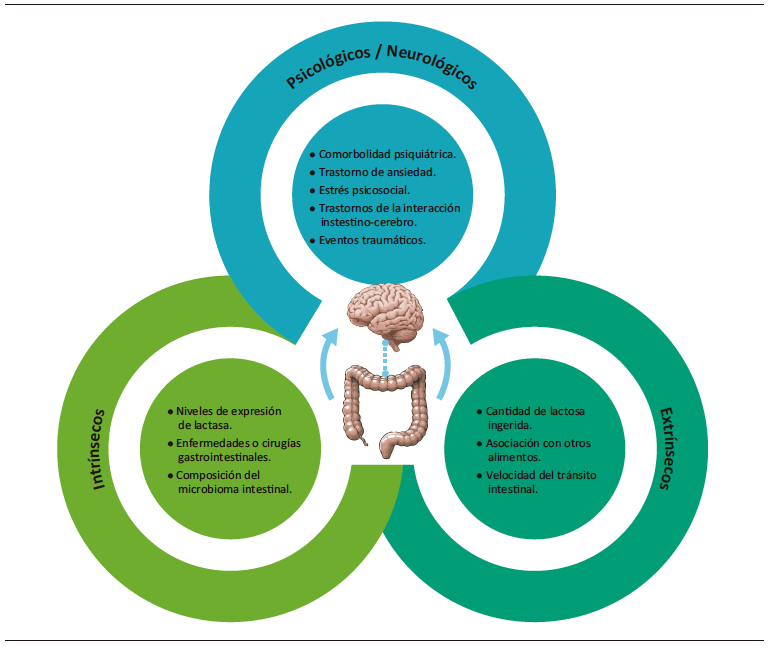
La causa de los síntomas asociados con la ingestión de lactosa es multifactorial,8 como se resume en la Figura 5. Existen factores extrínsecos que contribuyen al desarrollo de síntomas, como la cantidad de lactosa ingerida, el consumo de lácteos junto con otros alimentos que modifican el tránsito intestinal y, en consecuencia, la velocidad de llegada de la lactosa al colon. Entre los factores intrínsecos se incluyen la expresión de lactasa en el borde en cepillo, antecedentes de trastornos gastrointestinales o cirugías abdominales, y la composición de la microbiota intestinal. Asimismo, se han identificado factores inherentes al paciente que modulan el desarrollo e intensidad de los síntomas relacionados con el consumo de lactosa, como la presencia de trastornos de ansiedad, niveles elevados de estrés psicosocial y trastornos de la interacción cerebro-intestino (TICI), como el SII.19 Algunas publicaciones utilizan el término “intolerancia a la lactosa funcional” para describir la aparición de síntomas tras el consumo de lactosa sin evidencia de malabsorción en las pruebas diagnósticas. Además, deben considerarse factores individuales en la aparición de síntomas extraintestinales en los pacientes que refieren intolerancia a la lactosa. En un estudio con 1422 pacientes con TICI, a quienes se les realizaron pruebas para detectar malabsorción de lactosa, los síntomas extraintestinales más frecuentes fueron fatiga (67%), problemas de concentración (35%), depresión (28%), artralgias (26%) y mialgias (24%). Se observó una correlación positiva entre el número de síntomas intestinales y extraintestinales (r = 0,35; p < 0,001). Sin embargo, la coexistencia de MA fue inversamente proporcional a la cantidad de síntomas referidos, lo que sugiere que los síntomas gastrointestinales posteriores a la ingesta de lactosa se asocian con distensión mecánica, mientras que los síntomas extraintestinales podrían estar relacionados con la estimulación química por productos de fermentación, metabolitos de la microbiota intestinal y somatización.20
• Abordaje del paciente con sospecha de malabsorción e intolerancia a lactosa
Un interrogatorio dirigido para investigar la relación entre los síntomas y el consumo de leche y sus derivados es fundamental. Posteriormente, se debe realizar alguno de los métodos objetivos disponibles para confirmar o descartar la presencia de MA, ya que de ello dependerá el tratamiento adecuado del paciente o la necesidad de considerar otros diagnósticos concomitantes o diferenciales.
• Cuadro clínico
El paciente con sospecha de MA y/o IL suele presentar un cuadro clínico que aparece entre 60 minutos y 4 horas después de ingerir alimentos con lactosa. Los síntomas incluyen dolor abdominal (64,1%), distensión abdominal (22,6%), náuseas (15,1%), flatulencia, borborigmo y diarrea.6 En algunos casos, la producción exagerada de metano puede provocar estreñimiento en lugar de diarrea.21 Cuando los síntomas se presentan pocos minutos después de la ingesta (< 10 minutos), es probable que se trate de dispepsia funcional inducida por distensión gástrica, en lugar de una intolerancia alimentaria específica.22 Como se mencionó previamente, la presencia de síntomas extraintestinales sugiere la coexistencia de un trastorno funcional, más que una MA aislada. Hasta la fecha, solo existe una herramienta validada para cuantificar la intensidad de los síntomas relacionados con MA/IL. Esta se basa en una escala visual análoga y ha mostrado una sensibilidad de 75% y una especificidad de 67%, para un punto de corte de 7.23
Figura 5. Factores participantes en el desarrollo de intolerancia a la lactosa
• Pruebas diagnósticas
Además de la sospecha clínica de MA e IL, se pueden emplear métodos bioquímicos para evaluar la MA. Junto con las pruebas bioquímicas, o de forma alternativa, el análisis genético del gen de la lactasa también se utiliza para establecer la susceptibilidad genética a la hipolactasia. A continuación se describirán las pruebas invasivas y no invasivas más utilizadas a nivel global.
No invasivas
1. Pruebas genéticas
Son estudios costosos, utilizados principalmente en investigación. No requieren la administración oral de una carga de lactosa y no permiten establecer una correlación directa con los síntomas clínicos. Estas pruebas buscan polimorfismos de un solo nucleótido en el gen de la lactasa mediante reacción en cadena de la polimerasa (PCR) en tiempo real o secuenciación de ADN extraído de una muestra de sangre venosa o hisopado bucal. Los polimorfismos C/C-13910, G/A-22018 y G/G-13915 son compatibles con el fenotipo de DPL. El genotipo CC indica fenotipo con no persistencia de lactasa (NPL), el genotipo TT indica PLP y la heterocigosis CT caracteriza por una actividad enzimática intermedia. Publicaciones recientes sugieren que C/T-13910 es el polimorfismo dominante.24 En personas caucásicas esta prueba es precisa para detectar el genotipo; sin embargo, su rendimiento es menor en otras poblaciones debido a la presencia de polimorfismos regionales, lo que puede llevar a una alta tasa de falsos negativos.8 Por esta razón, no se recomienda su uso de forma generalizada. Cabe señalar que la MA secundaria no puede ser detectada mediante pruebas genéticas. Existen estudios que han tratado de investigar la correlación entre los resultados de las HAE y las pruebas genéticas para simplificar el algoritmo diagnóstico. La prueba genética es un buen predictor de la persistencia o no persistencia de la lactasa en una población específica, pero su uso está limitado por la alta prevalencia de polimorfismos regionales en individuos normales.24, 25
2. Prueba de medición de hidrógeno en aire espirado o prueba de aliento con lactosa
Las pruebas de aliento se basan en la medición de gases producidos en el intestino, que se difunden hacia la circulación sistémica y se eliminan a través de los pulmones. En sujetos sanos, el volumen promedio de gas intestinal es de aproximadamente 100 mL (rango de 30 a 200 mL), compuesto principalmente por H2, CO2 y CH4, con menores proporciones de oxígeno (O2), nitrógeno (N2), sulfuro de hidrógeno (H2S), indol, escatol y amoníaco (NH3). De estos, el H2 y el CH4 se generan exclusivamente por fermentación microbiana intestinal, principio en el que se basan las pruebas clínicas del aliento. La microbiota intestinal fermenta carbohidratos no absorbidos, lo que resulta en la producción de estos gases, que se difunden a la circulación venosa abdominal, se transportan a los pulmones y pueden detectarse en el aire espirado.26 En el diagnóstico de MA e IL, esta prueba es la más aceptada a nivel mundial debido a su reproducibilidad y baja complejidad. Su correcta ejecución requiere seguir las recomendaciones actuales de las sociedades americana y europea sobre indicaciones clínicas, rendimiento e interpretación.27 La prueba mide la excreción de H2 en el aire espirado tras la administración oral de una dosis estándar de lactosa (25 g disueltos en una taza de agua), con una duración mínima de observación de 3 horas, hasta
5 horas, dependiendo del lapso en el que se demuestre MA o IL. Las mediciones de H2 en partes por millón (ppm) se deben realizar cada 30 minutos. Un valor basal de H2 < 20 ppm es un requisito, y un aumento ≥ 20 ppm en un lapso de 3 horas es diagnóstico de MA, con sensibilidad del 60% y especificidad del 100%. Para documentar IL, se recomienda evaluar la aparición de síntomas abdominales asociados, preferiblemente mediante cuestionarios validados específicos para la prueba.28 Dado que el H2 no se produce por enzimas de mamíferos, su detección en el aire espirado indica la fermentación bacteriana del azúcar,28 es decir, la presencia de malabsorción. Una microbiota con baja producción de H2 puede generar falsos negativos en la HAE, al igual que un predominio de bacterias metanogénicas (por ejemplo, Methanobrevibacter smithii), que convierten el H2 en CH4. La tasa de falsos positivos es de aproximadamente un 20%, principalmente por la dificultad para discriminar entre una prueba positiva debida a tránsito orocecal acelerado inducido farmacológicamente, o por la presencia de SIBO, frente a una MA e IL genuina. Por ello, es fundamental descartar la presencia de SIBO previo a la realización de la prueba, con el fin de reducir la probabilidad de obtener falsos positivos.26 Se ha descrito una prueba que mide ¹³C/H2/CH4 en el aliento como un marcador más preciso de la digestión de lactosa, en comparación con las pruebas de aliento convencionales; sin embargo, esta solo está disponible en centros especializados.29
3. Prueba de tolerancia a la lactosa
Se basa en el principio de administrar una carga de lactosa y evaluar el incremento en los niveles plasmáticos de glucosa, lo que permite demostrar de forma indirecta la capacidad del individuo para digerir y absorber este carbohidrato. La prueba se optimiza mediante la correlación con los síntomas clínicos. Consiste en medir la glucosa plasmática en los tiempos 0, 30, 60 y 120 minutos tras la ingestión de 50 g de lactosa. La necesidad de realizar múltiples venopunciones limita su utilidad. Aunque el uso de glucómetros portátiles para mediciones en sangre capilar reduce la invasividad, se ha demostrado que no ofrece la misma precisión diagnóstica.30 Es una prueba económica, pero presenta limitaciones en cuanto a precisión y comodidad. Los resultados pueden verse afectados en pacientes con enfermedades del metabolismo de la glucosa o con alteraciones anatómicas del intestino.8
4. Test de gaxilosa (4-galactosil-xilosa)
Esta prueba consiste en administrar un sustrato análogo a la lactosa, la gaxilosa (4-galactosilxilosa), que conserva intactos la galactosa y el enlace β-glicosídico característicos de la lactosa, y difiere únicamente en el aglicón, que es una molécula de xilosa. La lactasa reconoce este análogo como sustrato y lo hidroliza, produciendo galactosa (que será metabolizada por el hígado) y xilosa. Esta última se absorbe en la mucosa intestinal, no se modifica por metabolismo hepático o renal y, posteriormente, aparece en orina, donde puede ser cuantificada (LacTEST®), o en sangre. La cantidad total de xilosa en la orina se relaciona con la actividad enzimática de la lactasa, de forma que un valor anormalmente bajo de xilosuria traduce una situación de hipolactasia. Los sujetos con fenotipo de PLP deberían eliminar cantidades significativamente mayores de xilosa que aquellos con fenotipos intermedios o con DPL.18 Para su realización, el paciente debe acudir en ayunas. Luego de la micción para vaciado vesical, recibe 0,45 g de gaxilosa disueltos en 100 ml de agua. A continuación, debe recoger toda la orina emitida durante 5 horas, cuantificándose la xilosa excretada que, en condiciones normales, debe ser superior a 37,8 mg cuando se mide por el método manual de Floroglucinol; o 19,18 mg cuando se mide por el método automatizado con Xylossay. Por tanto, en los pacientes con MA será inferior. Se recomienda evitar la toma de ácido acetilsalicílico o indometacina en los dos días previos a la prueba. La sensibilidad, la especificidad y los valores predictivos de esta prueba son del 93,5%, 91,8%, 92,7% y 92,7%, respectivamente, con un área bajo la curva de 0,93.21 Entre las ventajas de este método se destacan que evalúa la actividad de la lactasa a lo largo de todo el intestino, que es una prueba simple que no requiere la preparación previa necesaria para las HAE ni múltiples mediciones secuenciales, y que es altamente efectiva y segura para el paciente. Su principal desventaja es que no evalúa los síntomas, por lo que únicamente permite detectar MA, sin distinguir entre formas primarias o secundarias.31 En un ensayo clínico patrocinado por el fabricante, la precisión diagnóstica de la prueba con gaxilosa (AUC 0,93) fue superior a la de la HAE con lactosa (AUC 0,85) y a la prueba de tolerancia a la lactosa (AUC 0,79), en comparación con biopsias duodenales como referencia.32 No obstante, estos resultados aún no han sido confirmados en estudios multicéntricos o prospectivos. Aunque el test de la gaxilosa es una prueba no invasiva, está desaconsejado en caso de enfermedad renal grave, hipertensión portal, mixedema, diabetes con complicaciones crónicas o antecedentes de gastrectomía total y/o vagotomía.31
Invasivos
1.- Prueba de actividad enzimática de la lactasa en biopsias de mucosa duodenal
Se considera el método estándar de oro para el diagnóstico de hipolactasia, ya que permite una medición directa de la actividad de la lactasa. Es una prueba costosa que no se recomienda de forma rutinaria, salvo que se deba realizar un estudio endoscópico por otra indicación clínica. Esta prueba permite diferenciar entre MA primaria y secundaria, como en el caso de pacientes con SIBO.33 Sin embargo, la lactasa presenta una distribución parcheada en la mucosa intestinal, por lo que se requieren múltiples muestras de biopsia para aumentar la precisión diagnóstica.
• ¿Cuál es la mejor estrategia para evaluar a los pacientes con intolerancia a la lactosa?
Considerando que la aparición de síntomas digestivos inmediatos, intensos y acompañados de manifestaciones extraintestinales sugiere con mayor probabilidad la presencia de un trastorno funcional (IL funcional) más que MA propiamente dicha, la estrategia más costo-efectiva y simple consiste en ofrecer una prueba de provocación con consumo de lactosa, junto con la aplicación de un cuestionario de síntomas. Es fundamental identificar el tiempo de inicio de los síntomas y educar al paciente sobre la baja concordancia entre los síntomas y la presencia de MA, así como sobre la posibilidad de padecer un trastorno funcional digestivo. Además, se debe informar sobre los efectos benéficos de los lácteos en la salud. Una restricción innecesaria, basada en un diagnóstico no confirmado, podría privar al paciente de estos beneficios.21 Una prueba de provocación con dosis múltiples y a ciegas permitiría no solo evaluar la capacidad de digestión de la lactosa, sino también determinar la cantidad tolerada por cada individuo. En la práctica clínica, la autodeclaración de IL por los pacientes es frecuente y predice sus elecciones alimentarias, no así los resultados objetivos de las pruebas de diagnóstico ni la respuesta al tratamiento.8, 34
• Principios terapéuticos generales y recomendaciones para el manejo de la malabsorción e intolerancia a la lactosa
En el manejo de la intolerancia a un alimento, existen las siguientes recomendaciones generales previas al establecimiento de la intervención terapéutica: a) explicar la diferencia entre las reacciones adversas a los alimentos (alergia vs. intolerancia); b) considerar y optimizar el tratamiento de todos los potenciales mecanismos (orgánicos vs. funcionales) responsables de los síntomas del paciente, incluyendo comorbilidades con el SII; c) considerar el rol de otros carbohidratos fermentables en la dieta distintos a la lactosa; d) evaluar la posibilidad de tener un falso positivo en la HAE para lactosa y brindar tratamiento para SIBO; e) explicar al paciente las diferencias entre MA e IL; y, por último, f) si el paciente es candidato a tratamiento por MA/IL, debe ser referido con un profesional de la salud especialista en nutrición clínica y llevar seguimiento periódico.35 El objetivo del tratamiento de la MA e IL es conseguir el control y remisión de los síntomas, evitar restricciones dietéticas innecesarias y prevenir la malnutrición.28 Actualmente, las opciones terapéuticas disponibles incluyen: a) una dieta baja en lactosa y el uso de sustitutos de los lácteos, b) suplementación oral de lactasa exógena y c) uso de terapia basada en microbiota: suplementación biótica.8 A continuación, se describen los aspectos más destacados de estas estrategias terapéuticas.
• Dieta baja en lactosa
La mayoría de las personas con MA e IL pueden tolerar hasta 12-15 g de lactosa por día.36 Aquellos pacientes que presentan síntomas intensos con cantidades menores a este umbral deben ser orientados respecto de la probable concomitancia con el SII19 y se les debe sugerir reducir el consumo vs. la restricción absoluta de lactosa. Existen algunas estrategias para aumentar la tolerancia a los alimentos que contienen lactosa con el objetivo de mejorar la adecuación nutricional, evitar deficiencias y mejorar los síntomas. Estas son: la introducción gradual de 30-60 ml de leche por día hasta alcanzar 250 ml por día, el consumo diario de lácteos junto con otros alimentos (preferentemente con grasa para un mayor tiempo de vaciamiento gástrico), el consumo de quesos duros o añejos así como de lácteos fermentados por su menor contenido de lactosa.37, 38
• Alimentos lácteos libres de lactosa y sustitutos de los lácteos
Los alimentos lácteos libres de lactosa contienen preparados de la enzima lactasa. Estos aditivos reducen la cristalización de la lactosa, incrementando la dulzura de la leche y la fermentación para la producción de yogur. A su vez, la actividad proteolítica residual de la lactasa puede degradar la caseína, lo que puede alterar aún más el sabor original de los alimentos.8 Respecto de su valor nutricional, en comparación con los lácteos no modificados, son similares. Los alimentos sustitutos de los lácteos son derivados de plantas como la soja (el más disponible), el arroz, la avena, el coco, y las almendras. El aditivo más utilizado en estos productos es la sal.39 Pueden estar fortificados con calcio, vitaminas D, A, B12 y riboflavina, o sin fortificación. En comparación con los lácteos, el valor nutricional del aporte de aminoácidos y proteínas, así como de la vitamina D3, es menor. Cuando se consumen como bebidas principales pueden tener consecuencias para la salud, tales como provocar saciedad temprana, reducir el hambre y desplazar a otros alimentos más nutritivos, además de que una variedad amplia de estos sustitutos se endulzan con azúcar, miel, agave, jugo de caña u otros edulcorantes y aportan calorías vacías a la dieta.38 Por esta razón deben ser recomendados y supervisados por un experto en nutrición clínica.
• Suplementación oral de lactasa exógena
Los suplementos de lactasa exógena son producidos a partir de hongos (Aspergillus niger) o levaduras (Kluyveromyces lactis). Existen diferentes fórmulas farmaceúticas de venta libre disponibles alrededor del mundo (gel, suspensión, cápsulas o tabletas masticables). Se deben consumir un poco antes o junto con el lácteo.8, 38, 40 En México, se encuentra disponible el suplemento enzimático D-Lactase®, que aporta 10.000 UI de actividad enzimática de lactasa por cada tableta. En cuanto a la dosis y la eficacia terapéutica, diferentes estudios que compararon las formulaciones disponibles en los Estados Unidos y en Europa demuestran la equivalencia relativa de estos productos (3000 UI y > 30.000 UI)40
y sugieren un efecto benéfico modesto en la digestión de una dosis determinada de lactosa (disminución en la excreción total de hidrógeno en la HAE) y en los síntomas intestinales en pacientes con MA e IL. En un estudio se observó que con una dosis de 20 g de lactosa y 6000 UI de lactasa, se redujo significativamente la producción total de hidrógeno (p < 0,05) por debajo de lo observado con una dosis de 3000 UI. Sin embargo, los síntomas mejoraron significativamente (p < 0,05) con ambas dosis. Con la administración de dosis de 50 g de lactosa, ninguna de las posologías pudo mejorar la MA e IL.41 En un estudio italiano de 2014, se evaluó a 96 pacientes genéticamente deficientes en lactasa para establecer la dosis estándar idónea de lactasa que mejoraba el resultado en la HAE y la puntuación de la escala visual analóga para los síntomas digestivos relacionados con el consumo de lactosa (dolor, distensión y diarrea). El reto de lactosa fue de 25 g en agua (equivalente a 500 mL de leche) y la dosis evaluada de lactasa fue de 1500 UI. Los resultados fueron variables, ya que en el 22% de los pacientes la prueba de aliento se convirtió en negativa, en el 18% hubo una reducción significativa en el H2 espirado y en el 60% restante no hubo una diferencia significativa respecto del valor inicial. De modo interesante, en los pacientes que presentaron reducción en la producción de H2, no se observó correlación con la mejoría sintomática (p = 0,01, p = 0,02 y p = 0,003, respectivamente), similar en toda la cohorte evaluada, lo que sugiere la potencial implicación de un efecto placebo.41 Por último, es importante mencionar que el uso de suplementos exógenos de lactasa se considera seguro en la mayoría de los casos. Sin embargo, en la literatura se ha reportado al menos un caso de anafilaxia asociado a un suplemento de lactasa.42
• Terapias basadas en microbiota: suplementación biótica
Como se ha mencionado previamente, la exposición a los lácteos de forma gradual y con una cantidad específica de lactosa (12-15 g/día) se ha asociado al desarrollo de tolerancia a estos alimentos ya que las bacterias colónicas pueden adaptarse o modularse para mejorar la digestión de la lactosa sin que la expresión innata de la enzima lactasa se modifique.43 La modulación de la microbiota a través de la suplementación con bióticos (es decir, prebióticos y probióticos) es un tópico que se ha evaluado en varios escenarios clínicos dentro y fuera de la gastroenterología. Sin embargo, su objetivo es auxiliar en el manejo sintomático de la MA y la IL, y no sustituyen las opciones terapéuticas previamente descritas. Estudios previos sugieren que los prebióticos como los galactooligosacáridos (GOS) y, potencialmente, las dosis bajas de lactosa44 pueden mejorar la proliferación de Bifidobacterium y Lactobacillus, microorganismos metabolizadores de lactosa, y disminuir los síntomas asociados con la IL.43 Desde una base farmacéutica, se ha demostrado que la ingestión del prebiótico GOS RP-G28, en dosis bajas y altas por 30 días, redujo el dolor abdominal en el 50% de los pacientes al finalizar el tratamiento y de forma sostenida 30 días después de este (p = 0,019), con un buen perfil de seguridad. Además, los pacientes tratados con RP-G28 tuvieron una probabilidad seis veces menor de reportar IL tras la reintroducción de productos lácteos vs. los pacientes que recibieron placebo (p = 0,039). Adicionalmente RP-G28, no así el placebo, produjo aumentos significativos en cinco cepas de Bifidobacterium.40 Las bacterias que poseen lactasa producen ácido láctico al exponerse a la lactosa en el colon y se consideran probióticos, dado que contribuyen en la digestión del exceso de lactosa, evitando los síntomas de la IL.38 Las cepas más clásicas son Lactobacillus y Bifidobacterium.45 Los probióticos pueden encontrarse de forma natural en alimentos lácteos fermentados como el yogur y el kéfir o pueden adicionarse a estos y a otros alimentos. La evidencia disponible sobre su efectividad es heterogénea. En una revisión sistemática reciente que incluyó ensayos clínicos controlados de pacientes con IL, se evaluó el efecto del prebiótico RP-G28 y de varios probióticos de una o tres cepas de Lactobacillus: acidophilus, bulgarico, plantarum, reuteri o rhamnosus; Bifidobacterium: animalis, longum y Streptococcus thermophilus, sobre las modificaciones en el H2 exhalado en HAE con dosis variables de lactosa (2-50 g/kg) y en la puntuación de síntomas digestivos (dolor abdominal, diarrea y distensión). La dosis de probiótico utilizada osciló entre 107 UFC (unidades formadoras de colonias) y 1010 UFC; la duración de la intervención osciló entre seis días y seis semanas (media 24,83 + 12,86 días). De los estudios incluidos, en 6 de 7 se demostró mejoría en la puntuación de los síntomas globales, y solo en un estudio no se observaron diferencias significativas entre el grupo de intervención vs. el grupo control.46 Respecto de las HAE, en 3 de 5 estudios se observó disminución en la fracción de H2 posterior a la intervención, en 1 de 5 estudios se negativizó la HAE y en 1 de 5 estudios no se observaron diferencias significativas entre el grupo de intervención vs. el grupo control.47 Estos resultados sugieren que los probióticos pueden mejorar los resultados en la HAE y los síntomas. En cuanto al rol de los prebióticos, los resultados sugieren utilidad en la mejoría de los síntomas gastrointestinales pero no en la fracción de H2 exhalado. Cabe mencionar que una fuerte limitación para los hallazgos de esta revisión es la alta heterogeneidad en los estudios incluidos (edad, duración de la intervención, duración del seguimiento).48 A pesar de que la evidencia disponible sugiere efectos beneficiosos, no se consideran una línea de tratamiento para IL, sino un coadyuvante. Se requieren más estudios controlados y cegados que definan pautas para la estandarización en el uso de bióticos en el contexto de MA e IL.
• Perlas para el manejo: un algoritmo práctico
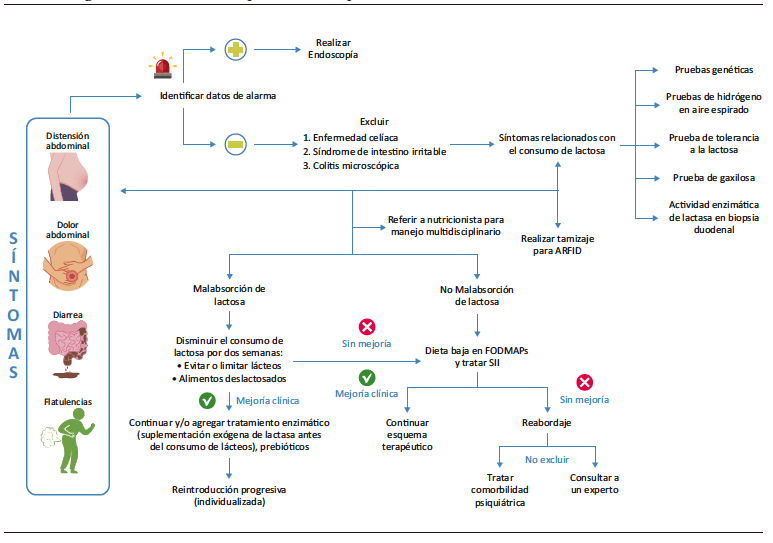
Como último punto de esta revisión, dedicaremos esta sección al abordaje terapéutico sugerido por nuestro grupo, el cual se resume gráficamente en la Figura 6. El paciente que acude con síntomas malabsortivos debe ser interrogado en detalle para detectar datos de alarma y/o de causas orgánicas de los síntomas digestivos. Sobre la base de los datos clínicos, deberán realizarse estudios complementarios, como serologías, imágenes e incluso estudios endoscópicos. Durante el interrogatorio es necesario cuestionar sobre los hábitos dietéticos y las restricciones alimentarias, así como la respuesta clínica a dichas restricciones. Los pacientes que tengan un tamizaje positivo con herramientas validadas, como la prueba de detección de nueve ítems del trastorno por evitación o restricción de la ingesta alimentaria (S-NIAS)49 deben ser referidos a psiquiatría/nutrición clínica para manejo multidisciplinario. Posteriormente, si se sospecha de IL se debe realizar una prueba que confirme o descarte MA: genotipo (en poblaciones europeas), HAE (más disponible), actividad de lactasa duodenal (si se realiza una endoscopía por otra indicación), o gaxylosa-4, considerando las limitaciones y la disponibilidad de las pruebas en cada centro. De confirmarse MA, se debe referir el paciente a un especialista en nutrición clínica para implementar una dieta baja en lactosa (12-15 g/día) y revalorar la sintomatología en un lapso no menor a dos semanas. Si la respuesta es favorable, pueden incorporarse suplementos de lactasa y probióticos como coadyuvantes, a demanda del paciente. De no existir mejoría clínica tras dos semanas de dieta baja en lactosa, se debe sospechar la presencia de un trastorno funcional intestinal como el SII, y podría ser útil el inicio de una dieta baja en FODMAPs. Cualquier modificación dietética, aunque es parte del manejo no farmacológico del paciente, amerita un seguimiento estrecho similar al que se recomienda en cualquier intervención terapéutica. La persistencia de síntomas a pesar de los cambios dietéticos obliga a replantear el diagnóstico clínico.
Figura 6. Algoritmo de atención de los pacientes con sospecha de Malabsorción e Intolerancia a la lactosa
Conclusión
Comprender las bases genéticas y la fisiología del metabolismo de la lactosa es fundamental para un abordaje adecuado del paciente con síntomas relacionados con MA e IL, dos entidades clínicas que a menudo se confunden entre sí y pueden coexistir con otras patologías digestivas, tanto orgánicas como funcionales. La elección de métodos diagnósticos, considerando la disponibilidad en cada centro, es recomendable para confirmar la necesidad de modificaciones dietéticas, y evitar restricciones innecesarias que podrían privar al paciente de los beneficios nutricionales de los lácteos y aumentar el riesgo de trastornos alimentarios como el ARFID. La ausencia de mejoría clínica con una dieta baja en lactosa debe orientar la evaluación hacia otras posibles causas de malabsorción de carbohidratos.
Fuentes de financiamiento. Los autores declaran que no hubo financiación externa.
Propiedad intelectual. Los autores declaran que los datos, figuras y tablas en el presente manuscrito son originales provenientes de sus instituciones.
Conflictos de interés. Los autores declaran no tener conflictos de interés con relación a este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Ordoñez-Vázquez A L, Fuentes-Montalvo A y Enrique Coss-Adame E. Malabsorción e intolerancia a la lactosa. Acta Gastroenterol Latinoam. 2025;55(2):88-102. https://doi.org/ 10.52787/agl.v55i2.495
Referencias
- Melchior C, Fremaux S, Jouët P, Macaigne G, Raynaud JJ, Facon S, et al. Perceived Gastrointestinal Symptoms and Association With Meals in a French Cohort of Patients With Irritable Bowel Syndrome. J Neurogastroenterol Motil. 2021;27(4):574-80.
- Perino A, Cabras S, Obinu D, Sforza LC. Lactose intolerance: a non-allergic disorder often managed by allergologists.
- Catanzaro R, Sciuto M, Marotta F. Lactose Intolerance-Old and New Knowledge on Pathophysiological Mechanisms, Diagnosis, and Treatment. SN Compr Clin Med. 2021;3(2):499-509.
- Rosado JL. Intolerancia a la lactosa. Gac Médica México.
- Hauster SC. Mayo Clinic Gastroenterology and Hepatology Board Review. 6a edición. Oxford University Press. 2024.496 p. (Mayo Clinic Scientific Press).
- Heine RG, AlRefaee F, Bachina P, De Leon JC, Geng L, Gong S, et al. Lactose intolerance and gastrointestinal cow’s milk allergy in infants and children – common misconceptions revisited. World Allergy Organ J. 2017;10:41.
- Antonowicz I, Lebenthal E. Developmental Pattern of Small Intestinal Enterokinase and Disaccharidase Activities in the Human Fetus. Gastroenterology. 1977;72(6):1299-303.
- Misselwitz B, Butter M, Verbeke K, Fox MR. Update on lactose malabsorption and intolerance: pathogenesis, diagnosis and clinical management. Gut. 2019;68(11):2080-91.
- Chen Z, Ahmed M, Ha V, Jefferson K, Malik V, Ribeiro PAB, et al. Dairy Product Consumption and Cardiovascular Health: A Systematic Review and Meta-analysis of Prospective Cohort Studies. Adv Nutr. 2022;13(2):439-54.
- Gallo A, Marzetti E, Pellegrino S, Montalto M. Lactose malabsorption and intolerance in older adults. Curr Opin Clin Nutr Metab Care. 2024;27(4):333-7.
- Kato K, Ishida S, Tanaka M, Mitsuyama E, Xiao J zhong, Odamaki T. Association between functional lactase variants and a high abundance of Bifidobacterium in the gut of healthy Japanese people. Wilson BA (ed.). PLOS ONE. 2018;13(10):e0206189.
- Järvelä I, Torniainen S, Kolho KL. Molecular genetics of human lactase deficiencies. Ann Med. 2009;41(8):568-75.
- Itan Y, Jones BL, Ingram CJ, Swallow DM, Thomas MG. A worldwide correlation of lactase persistence phenotype and genotypes. BMC Evol Biol. 2010;10(1):36.
- Swallow DM, Troelsen JT. Escape from epigenetic silencing of lactase expression is triggered by a single-nucleotide change. Nat Struct Mol Biol. 2016;23(6):505-7.
- Dewiasty E, Setiati S, Agustina R, Roosheroe AG, Abdullah M, Istanti R, et al. Prevalence of lactose intolerance and nutrients intake in an older population regarded as lactase non-persistent. Clin Nutr ESPEN. 2021;43:317-21.
- Nybacka S, Kinnander A, Augustin H, Bärebring L. Perceived healthiness of foods, food avoidance and diet-related anxiety in individuals with self-reported irritable bowel syndrome: a cross-sectional study. BMC Nutr. 2024;10(1):134.
- Casellas F, Aparici A, Pérez MJ, Rodríguez P. Perception of lactose intolerance impairs health-related quality of life. Eur J Clin Nutr. 2016;70(9):1068-72.
- Villanueva Torregrosa D, Mendoza Torres E, Varela Prieto L, Villarreal Camacho J. Conceptual basis of the diagnosis of lactose intolerance, hypolactasia and lactose maldigestion. Salud Uninorte. 2015;31(1):101-17.
- Yang J, Deng Y, Chu H, Cong Y, Zhao J, Pohl D, et al. Prevalence and Presentation of Lactose Intolerance and Effects on Dairy Product Intake in Healthy Subjects and Patients With Irritable Bowel Syndrome. Clin Gastroenterol Hepatol. 2013;11(3):262-268.e1.
- Wilder-Smith CH, Drewes AM, Materna A, Olesen SS. Extragastrointestinal Symptoms and Sensory Responses During Breath Tests Distinguish Patients With Functional Gastrointestinal Disorders. Clin Transl Gastroenterol. 2020;11(8):e00192.
- Martínez Vázquez SE, Nogueira De Rojas JR, Remes Troche JM, Coss Adame E, Rivas Ruíz R, Uscanga Domínguez LF. Importancia de la intolerancia a la lactosa en individuos con síntomas gastrointestinales. Rev Gastroenterol México. 2020;85(3):321-31.
- Führer M, Hammer J. Lack of an Effect of Gastric Capsaicin on the Rectal Component of the Gastrocolonic Response. Dig Dis Sci. 2017;62(12):3542-9.
- Casellas F, Varela E, Aparici A, Casaus M, Rodríguez P. Development, Validation, and Applicability of a Symptoms Questionnaire for Lactose Malabsorption Screening. Dig Dis Sci. 2009;54(5):1059-65.
- Santonocito C, Scapaticci M, Guarino D, Annicchiarico EB, Lisci R, Penitente R, et al. Lactose intolerance genetic testing: Is it useful as routine screening? Results on 1426 south-central Italy patients. Clin Chim Acta. 2015;439:14-7.
- Pimentel M, Kong Y, Park S. Breath Testing To Evaluate Lactose Intolerance in Irritable Bowel Syndrome Correlates With Lactulose Testing and May Not Reflect True Lactose Malabsorption. Am J Gastroenterol. 2003;98(12):2700-4.
- Rezaie A, Buresi M, Lembo A, Lin H, McCallum R, Rao S, et al. Hydrogen and Methane-Based Breath Testing in Gastrointestinal Disorders: The North American Consensus. Am J Gastroenterol. 2017;112(5):775-84.
- Scalese G, Cesarini A, Pallotta L, Ribichini E, Spina L, Diofebi M, et al. Lactose Breath Test: Possible Strategies to Optimize Test Performance, Accuracy, and Clinical Impact. Nutrients. 2024;16(20):3516.
- Hammer HF, Fox MR, Keller J, Salvatore S, Basilisco G, Hammer J, et al. European guideline on indications, performance, and clinical impact of hydrogen and methane breath tests in adult and pediatric patients: European Association for Gastroenterology, Endoscopy and Nutrition, European Society of Neurogastroenterology and Motility, y European Society for Paediatric Gastroenterology Hepatology and Nutrition consensus. United Eur Gastroenterol J. 2022;10(1):15-40.
- Houben E, De Preter V, Billen J, Van Ranst M, Verbeke K. Additional Value of CH4 Measurement in a Combined 13C/H2 Lactose Malabsorption Breath Test: A Retrospective Analysis. Nutrients. 2015;7(9):7469-85.
- Domínguez Jiménez JL, Fernández Suárez A. Correlation Between Capillary and Venous Blood Glucose in the Lactose Tolerance Test. Dig Dis Sci. 2016;61(1):208-14.
- Arias DFA, Álvarez DFC, Muñoz DED. Grupo de trabajo de la SEPD en hipolactasia/intolerancia a la lactosa/ malabsorción de lactosa.
- Aragón JJ, Hermida C, Martínez-Costa OH, Sánchez V, Martín I, Sánchez JJ, et al. Noninvasive Diagnosis of Hypolactasia With 4-Galactosylxylose (Gaxilose): A Multicentre, Open-Label, Phase
IIB-III Nonrandomized Trial. J Clin Gastroenterol. 2014;48(1):29-36. - Jo IH, Paik CN, Kim YJ, Lee JM, Choi SY, Hong KP. Lactase Deficiency Diagnosed by Endoscopic Biopsy-based Method is Associated With Positivity to Glucose Breath Test. J Neurogastroenterol Motil. 2023;29(1):85-93.
- Zingone F, Bertin L, Maniero D, Palo M, Lorenzon G, Barberio B, et al. Myths and Facts about Food Intolerance: A Narrative Review. Nutrients. 2023;15(23):4969.
- Hammer HF, Hammer J, Fox M. Mistakes in the management of carbohydrate intolerance and how to avoid them.
- Shaukat A, Levitt MD, Taylor BC, MacDonald R, Shamliyan TA, Kane RL, et al. Systematic Review: Effective Management Strategies for Lactose Intolerance. Ann Intern Med. 2010;152(12):
797-803. - Silanikove N, Leitner G, Merin U. The Interrelationships between Lactose Intolerance and the Modern Dairy Industry: Global Perspectives in Evolutional and Historical Backgrounds. Nutrients. 2015;7(9):7312-31.
- Szilagyi A, Ishayek N. Lactose Intolerance, Dairy Avoidance, and Treatment Options. Nutrients. 2018;10(12):1994.
- Fructuoso I, Romão B, Han H, Raposo A, Ariza-Montes A, Araya-Castillo L, et al. An Overview on Nutritional Aspects of Plant-Based Beverages Used as Substitutes for Cow’s Milk. Nutrients. 2021;13(8):2650.
- Ianiro G, Pecere S, Giorgio V, Gasbarrini A, Cammarota G. Digestive Enzyme Supplementation in Gastrointestinal Diseases. Curr Drug Metab. 2016;17(2):187-93.
- Ibba I, Gilli A, Boi MF, Usai P. Effects of Exogenous Lactase Administration on Hydrogen Breath Excretion and Intestinal Symptoms in Patients Presenting Lactose Malabsorption and Intolerance. BioMed Res Int. 2014;2014:1-7.
- Voisin MR, Borici-Mazi R. Anaphylaxis to supplemental oral lactase enzyme. Allergy Asthma Clin Immunol. 2016;12(1):66.
- Angima G, Qu Y, Park SH, Dallas DC. Prebiotic Strategies to Manage Lactose Intolerance Symptoms. Nutrients. 2024;16 (7):1002.
- Li X, Yin J, Zhu Y, Wang X, Hu X, Bao W, et al. Effects of Whole Milk Supplementation on Gut Microbiota and Cardiometabolic Biomarkers in Subjects with and without Lactose Malabsorption. Nutrients. 2018;10(10):1403.
- Oak SJ, Jha R. The effects of probiotics in lactose intolerance: A systematic review. Crit Rev Food Sci Nutr. 2019;59(11):1675-83.
- Roškar I, Švigelj K, Štempelj M, Volfand J, Štabuc B, Malovrh Š, et al. Effects of a probiotic product containing Bifidobacterium animalis subsp. animalis IM386 and Lactobacillus plantarum MP2026 in lactose intolerant individuals: Randomized, placebo-controlled clinical trial. J Funct Foods. 2017;35:1-8.
- Savaiano DA, Ritter AJ, Klaenhammer TR, James GM, Longcore AT, Chandler JR, et al. Improving lactose digestion and symptoms of lactose intolerance with a novel galacto-oligosaccharide (RP-G28): a randomized, double-blind clinical trial. Nutr J. 2013;12(1):160.
- Leis R, De Castro MJ, De Lamas C, Picáns R, Couce ML. Effects of Prebiotic and Probiotic Supplementation on Lactase Deficiency and Lactose Intolerance: A Systematic Review of Controlled Trials. Nutrients. 2020;12(5):1487.
- Medina-Tepal KA, Vazquez-Arevalo R, Trujillo-ChiVacuán EM, Zickgraf HF, Mancilla-Díaz JM. Cross-cultural adaptation and validation of the Nine Item ARFID Screen (NIAS) in Mexican youths. Int J Eat Disord. 2023;56(4):721-6.
Correspondencia: Enrique Coss-Adame
Correo electrónico: enriquecossmd@gmail.com
Acta Gastroenterol Latinoam 2025;55(2):88-102
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE


