Sara Noemí Schaab1 ID· María Cielo Gutiérrez2 ID
1 Licenciada en Nutrición. Universidad Nacional de La Matanza. Buenos Aires, Argentina.
2 Licenciada en Nutrición. División Gastroenterología. Hospital de Clínicas José de San Martín, Universidad de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2025;55(2):103-111
Recibido: 13/05/2025 / Aceptado: 22/06/2025 / Publicado online: 30/06/2025 / https://doi.org/10.52787/agl.v55i2.504
Resumen
El síndrome de intestino irritable es el trastorno gastrointestinal funcional más frecuente y afecta significativamente la calidad de vida. Si bien la intervención nutricional con mayor respaldo científico y más recomendada por las guías internacionales es la dieta baja en FODMAP, un número relevante de pacientes (entre 20% y 50%) no responde adecuadamente. Esto ha impulsado la exploración de otras alternativas de intervención nutricional, como son la dieta reducida en almidón y sacarosa y la dieta Mediterránea. El objetivo de este estudio es revisar la evidencia científica disponible acerca de las nuevas estrategias nutricionales para el manejo del síndrome de intestino irritable, con foco en la dieta reducida en almidón y sacarosa y la dieta mediterránea.
Palabras claves. Síndrome de intestino irritable, terapia dietética, dieta mediterránea, dieta reducida en almidón y sacarosa.
Emerging Nutritional Interventions for Irritable Bowel Syndrome: Starch- and Sucrose-Reduced Diet and Mediterranean Diet
Summary
Irritable bowel syndrome is the most common functional gastrointestinal disorder significantly affecting quality of life. The nutritional intervention with the greatest scientific support and most recommended by international guidelines is the low-FODMAPs diet, however, a relevant proportion of patients (between 20% and 50%) do not adequately respond to this intervention. This has prompted the exploration of alternative nutritional interventions, such as the starch- and sucrose-reduced diet and the Mediterranean diet. The aim of this study is to review the scientific evidence on new nutritional strategies for the management of irritable bowel syndrome, focusing on the the starch-sucrose reduced diet and the Mediterranean diet.
Keywords. Irritable bowel syndrome, dietary therapy, Mediterranean diet, starch- and sucrose reduced diet.
Abreviaturas
DBF: Dieta baja en FODMAP.
DLG: Dieta libre de gluten.
DM: Dieta mediterránea.
FODMAP: Oligosacáridos, disacáridos, monosacáridos y polioles fermentables.
IBS-SSS: Escala de gravedad de los síntomas del síndrome del intestino irritable.
SII: Síndrome de intestino irritable.
SNC: Sistema nervioso central.
SSRD: Dieta reducida en almidón y sacarosa.
Introducción
El síndrome de intestino irritable (SII) es el trastorno funcional gastrointestinal más frecuente y puede tener un gran impacto en la calidad de vida del paciente.1 En un estudio multinacional a gran escala, se reporta una prevalencia del 4,1% (3,9% – 4,2%) a nivel mundial y de 3,5% (2,7% – 4,3%) en Argentina, según los criterios de Roma IV.2 Estos criterios, que actualizaron los criterios de Roma III en el 2016,3-4 definen el diagnóstico de SII ante la presencia de dolor abdominal recurrente en promedio al menos 1 día a la semana en los últimos 3 meses (con inicio de los síntomas al menos 6 meses antes del diagnóstico), asociado a 2 o más de los siguientes criterios: relacionado con la defecación, asociado con un cambio en la frecuencia de las deposiciones y/o asociado con un cambio en la forma de las heces.
Aunque el mecanismo fisiopatológico del SII es complejo y aún tiene que ser esclarecido, está bien establecido que existe una alteración en la comunicación entre el cerebro y el intestino que genera alteraciones en la motilidad, hipersensibilidad visceral y alteración en el procesamiento del sistema nervioso central (SNC).5 Otros posibles factores de riesgo podrían incluir asociaciones genéticas, factores dietéticos, infecciones, alteraciones en la microbiota intestinal y la presencia de estrés, ansiedad y/o depresión.6
Una vez realizado el diagnóstico de SII, se requiere un enfoque empático que conduzca al paciente a mejorar la calidad de vida y los síntomas, además de reducir el gasto sanitario.5 Más del 80% de los pacientes con SII asocian sus síntomas (como gases, diarrea, distensión abdominal) al consumo de ciertos alimentos que actúan como gatillos, siendo las intervenciones dietéticas una pieza fundamental en el manejo terapéutico.7, 8 Entre los alimentos considerados «culpables» se encuentran la leche y otros productos lácteos, las legumbres, las verduras crucíferas, algunas frutas y los cereales, especialmente el trigo y el centeno.9 Al momento de la ingesta de alimentos, se producen cambios en la motilidad gastrointestinal, secreción gastrointestinal y pancreática, así como en la liberación de hormonas gastrointestinales con el objetivo de favorecer el proceso digesto absortivo adaptado a la naturaleza y composición de los nutrientes que se han ingerido.10 Existen múltiples mecanismos por los cuales los alimentos pueden desencadenar síntomas en el SII. Pueden actuar tanto de forma primaria (por ejemplo, a través de mecanismos osmóticos, químicos, inmunológicos, mecánicos o neuroendocrinos) como secundaria (por ejemplo, a través de subproductos de la fermentación, alteraciones en el pH luminal o efectos en el microbioma intestinal).11
Cada vez hay más evidencia que apoya las modificaciones dietéticas como tratamiento primario para los síntomas del SII.1 Por otra parte, hay factores que se deben tener en cuenta a la hora de instaurar un tratamiento dietético: la demografía del paciente, el costo y la disponibilidad de los alimentos, así como también la aceptabilidad del manejo dietético y su impacto en la calidad de vida relacionada con la alimentación. Tanto el costo como la disponibilidad del tratamiento son dos determinantes importantes que influyen en la aceptabilidad y la adherencia al abordaje nutricional.12
En la práctica clínica, el interés se ha centrado en el uso de tres dietas para el SII: el consejo dietético tradicional, la dieta baja en FODMAP (por su acrónimo Fermentables Oligosacáridos, Disacáridos, Monosacáridos y Polioles, DBF) y una dieta libre de gluten (DLG). El objetivo de esta revisión es evaluar la evidencia disponible sobre las nuevas estrategias nutricionales para el manejo del SII, enfocándose en la dieta reducida en almidón y sacarosa (SSRD) y la dieta mediterránea (DM).
Tratamiento dietético tradicional para el SII
Según las últimas guías de manejo del SII de la British Society of Gastroenterology publicadas en 2021,11 el consejo dietético tradicional se considera de primera línea para el tratamiento nutricional y se basa en las directrices elaboradas por NICE (del inglés National Institute for Health and Care Excellence) y la BDA (del inglés British Dietetic Association).13 Sus principios incluyen la adopción de patrones de alimentación saludables, como realizar comidas regulares, tomarse el tiempo para comer, reducir la ingesta de almidón resistente, evitar la ingesta de sorbitol en personas con diarrea, limitar la ingesta de alcohol y cafeína, ajustar la ingesta de fibra y reducir el consumo de alimentos grasos y picantes. Tales indicaciones se basan más en una combinación de la experiencia clínica y los posibles mecanismos por los cuales estos alimentos pueden inducir síntomas gastrointestinales (GI) en el SII, que en la evidencia de ensayos clínicos aleatorizados que comparen este enfoque con un tratamiento de control.
De acuerdo con las mismas guías, se recomienda la DBF como terapia nutricional de segunda línea, aunque consideran que cada vez hay más evidencia a favor para considerarla de primera línea. De hecho, las guías de la American Gastroenterological Association de 2022 consideran a la DBF como tratamiento nutricional de primera línea del SII.1 El beneficio de DBF se ha observado en el 50% al 80% de los pacientes con SII; sin embargo, un 20% a 50% de los pacientes no responden a una DBF y se beneficiarían con otros enfoques terapéuticos.14
Los FODMAP son una serie de carbohidratos altamente fermentables y/o activos osmóticamente que generan distensión luminal, siendo este último el mecanismo principal por el cual inducen síntomas en individuos que presentan hipersensibilidad visceral. La DBF implica una estrategia dietética de tres fases: i) fase de restricción o eliminación, que reduce temporalmente la ingesta de FODMAP por debajo de un límite arbitrario durante un período variable, de 2 a 6 semanas; ii) fase de reintroducción, que ayuda a identificar el impacto de cada FODMAP de forma específica y las cantidades que generan impacto en los síntomas; y iii) fase de personalización, con el objetivo final de mantener el control de los síntomas y maximizar la ingesta de FODMAP según la tolerancia individual.15, 16 Se han sugerido otras alternativas menos restrictivas que la DBF para situaciones específicas, por ejemplo cuando existe compromiso del estado nutricional, embarazo o falta de adherencia a la DBF tradicional.17 Este enfoque se ha denominado “DBF simplificada” (en inglés ‘gentle’ FODMAP diet)18 y tiene como objetivo restringir un número específico de alimentos que son fuentes altamente concentradas de FODMAP y/o restringir alimentos específicos con alto contenido de FODMAP si se sospecha que desencadenan síntomas a partir de una anamnesis alimentaria.
Por su parte, la DLG se centra en la eliminación de alimentos con alto contenido de gluten, como el trigo, la cebada y el centeno. Según las guías británicas,11 hasta el momento de su publicación, no se contaba con evidencia suficiente para su recomendación como terapia nutricional en el manejo del SII. El papel del gluten en la patogénesis y los síntomas del SII no se ha dilucidado por completo, y la evidencia sobre su efectividad sigue siendo incierta. En diferentes revisiones sistemáticas y metaanálisis se han encontrado estudios que reportan una mejoría en la severidad de los síntomas y en la calidad de vida con la DLG en comparación con una dieta estándar o con la DBF, pero las diferencias no fueron estadísticamente significativas, y por lo tanto la evidencia sobre la DLG no es lo suficientemente robusta como para recomendarla rutinariamente en los pacientes con SII.19 – 22 Se ha sugerido que el beneficio de la DLG no se debe en general a la eliminación del gluten en sí, sino a la exclusión del trigo, que conlleva una reducción del contenido de fructanos de la dieta, siendo este un FODMAP. Además, el trigo tiene otros componentes que también podrían estar implicados en los síntomas, como los inhibidores de la tripsina y la amilasa (ATI) y la lectina.23, 24
Intervenciones dietéticas emergentes para el SII
En junio del 2025, se publicó en The Lancet21 por Cuffe y col. una revisión sistemática y metaanálisis en red que incluyó 28 ensayos clínicos aleatorizados (ECA), cuyo objetivo fue evaluar la eficacia relativa de diversas intervenciones dietéticas para el tratamiento del SII (con al menos dos semanas de duración). La mayoría de las comparaciones a través de la red fueron calificadas con un nivel de confianza bajo o muy bajo, a excepción de las comparaciones directas entre la DBF o la dieta reducida en almidón y sacarosa, que fueron clasificadas con un nivel de confianza moderado.
Si bien los autores destacaron que la DBF es la intervención con mayor evidencia científica actual, han surgido otras alternativas prometedoras para las que faltan aún más estudios, entre ellas la dieta reducida en almidón y sacarosa y la dieta Mediterránea, que se desarrollarán a continuación.
Dieta reducida en almidón y sacarosa
La dieta reducida en almidón y sacarosa (o en inglés, starch- and sucrose-reduced diet – SSRD) se centra en la reducción de sacarosa, almidón y azúcar añadido. A diferencia de la DBF, permite la ingesta de fructanos, fructosa, lactosa y edulcorantes, caracterizándose por ser una alternativa menos restrictiva.25 Esta dieta ha ganado interés en los últimos años como una posible herramienta terapéutica en pacientes con SII, especialmente en aquellos pacientes que no responden a otras estrategias dietéticas. Esto podría deberse en parte a que algunos pacientes con SII podrían estar predispuestos a tener una actividad reducida de la enzima sacarasa-isomaltasa, en particular el tipo con predominio de diarrea (SII-D).26
La SSRD forma parte del grupo de dietas bajas en hidratos de carbono y se ha aplicado principalmente en pacientes con deficiencia congénita de sacarasa-isomaltasa (por sus siglas en inglés congenital sucrase-isomaltase deficiency, CSID).27
El primer estudio que evaluó la implementación de SSRD en pacientes con SII fue publicado por Nilholm y col. en 2019.28 En este estudio prospectivo, 105 pacientes con SII fueron asignados aleatoriamente a una intervención dietética de dos semanas con SSRD o a un grupo control que continuó con su dieta habitual. La intervención resultó en que el 66,3% de los pacientes respondieron con diferencias en la variación de la escala de gravedad de los síntomas del síndrome del intestino irritable (por sus siglas en inglés IBS-SSS) (p < 0,001), dolor abdominal (p = 0,001), diarrea (p = 0,002), distensión abdominal y flatulencia (p = 0,005), bienestar psicológico (p = 0,048) e influencia de los síntomas GI en la vida diaria (p < 0,001), en comparación con el grupo control. Asimismo, se observó que muchos pacientes con SII presentan malos hábitos alimentarios, con una ingesta irregular de comidas, un alto consumo de cereales, dulces y gaseosas y un bajo consumo de verduras, frutas y pescado. Por otra parte, se observó una mejoría de los síntomas extraintestinales luego de 4 semanas de SSRD en comparación con la dieta habitual, incluyendo la reducción del dolor muscular/articular (p = 0,029), la urgencia urinaria (p = 0,017) y el cansancio (p = 0,011).29
Años más tarde, en 2024, el mismo grupo de investigación Roth y col.25 publicaron un estudio aleatorizado de no inferioridad que incluyó a 155 pacientes con SII, con el objetivo de comparar la SSRD con la DBF tras una intervención de 4 semanas. Se estableció un margen de no inferioridad predefinido de hasta un 20% de diferencia en la tasa de respondedores a favor del tratamiento DBF. La tasa de respuesta en los síntomas GI fue comparable entre ambas dietas en la semana 2 (79,2% frente a 73,1%; p = 0,661; intervalo de confianza (IC) del 95% = −20 – 7,2) y en la semana 4 (79,2% frente a 78,2%; p = 1,000; IC del 95% = −14 – 12). Se observaron reducciones similares de los síntomas extraintestinales en ambos grupos, aunque la SSRD se asoció con mayor impacto en la reducción del peso, el índice de masa corporal (IMC) y el antojo del consumo de azúcar. Estos hallazgos sugieren que la SSRD puede llegar a ser una alternativa posible para el manejo del SII, con beneficios metabólicos adicionales.
La intervención dietética de SSRD de la mayoría de los estudios25, 30 que evaluaron su impacto en SII se basó en la reducción del consumo de sacarosa (comúnmente conocido como azúcar de mesa) y de almidón, así como evitar productos con azúcar añadido, favoreciendo un mayor consumo de ciertos vegetales y frutas (se les entregó una lista con selección de frutas y verduras a los participantes), carnes y productos lácteos. (Tabla 1)
Tabla 1. Generalidades de elección de alimentos para SSRD
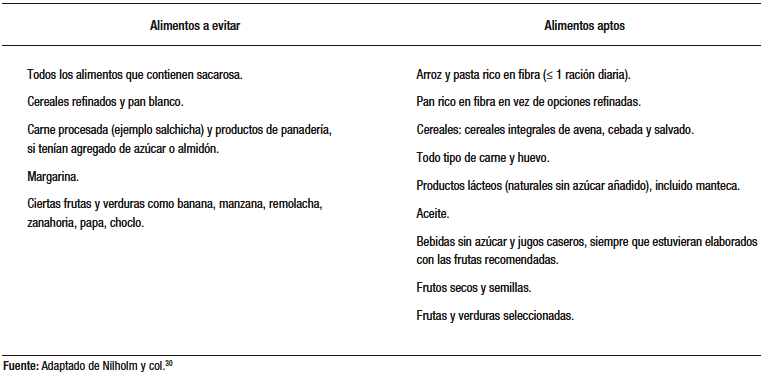
Cuffe y col.21 posicionó a la SSRD en el primer lugar en comparación con otras intervenciones dietéticas para la mejoría de los síntomas globales del SII (RR 0,41 [IC 95% 0,26 – 0,67], 2 estudios), mientras que una DBF ocupó el cuarto lugar (RR 0,51 [IC 95% 0,37 – 0,70], 24 estudios) y las recomendaciones BDA/NICE el décimo (RR 0,62 [IC 95% 0,43 – 0,90], 8 estudios). Es importante destacar que sólo se incluyeron 2 estudios de intervención SSRD.
Aunque los mecanismos que explican el efecto de la SSRD sobre los síntomas GI en el SII no están completamente dilucidados, se han propuesto tres teorías diferentes: posible deficiencia de la enzima sacarasa-isomaltasa, sobrecarga del sistema fisiológico de absorción o una disfunción del sistema nervioso inducida por los alimentos.31
Como estrategia terapéutica emergente, la SSRD podría ser prometedora para el abordaje nutricional de los pacientes con SII, con potencial para mejorar la adherencia al tratamiento si se acompaña con recomendaciones nutricionales personalizadas.32
Dieta Mediterránea
La dieta Mediterránea (DM) puede definirse como aquellos hábitos alimenticios tradicionales de las personas que viven en los países ribereños del mar Mediterráneo. Se caracteriza por un alto consumo de cereales integrales, frutas, verduras, frutos secos y semillas. Se consumen pescados, mariscos, aves y lácteos con moderación, la carne roja y los alimentos ricos en azúcares ocasionalmente, y el aceite de oliva es la principal fuente de grasa.33
En SII hay una elevada prevalencia de síntomas de ansiedad y depresión, los cuales han sido reportados en el 29% y 39% de los pacientes, respectivamente.34 La DM podría influir en los síntomas GI de dos maneras. Por un lado, el contenido de fibra, polifenoles y ácidos grasos puede influir en la composición de la microbiota, que a su vez produce metabolitos que pueden actuar sobre la función intestinal.35-37 Por otro lado, al reducir los síntomas de ansiedad y/o depresión, podría modular de forma descendente el eje intestino-cerebro y aliviar los síntomas GI, al mejorar la desregulación del eje. Estudios clínicos controlados y aleatorizados hallaron que la DM mejora los síntomas depresivos y la ansiedad38-39 y esto podría deberse a mecanismos directos e indirectos que interactúan entre sí, como el estrés inmunitario y oxidativo, la microbiota, la plasticidad cerebral, la producción de neurotransmisores y la función mitocondrial.40
La dieta baja en FODMAP es restrictiva y podría no ser apropiada para algunas personas con trastornos psiquiátricos, a diferencia de la DM que es un patrón de alimentación saludable y no restrictivo que ha sido asociado con un menor riesgo de padecer enfermedades.
En el 2023, Staudacher y col.41 llevaron a cabo un ECA, abierto en 59 individuos con SII según Roma IV que padecían ansiedad y/o depresión, leves o moderadas. En el mismo evaluaron el impacto de la DM en los síntomas GI y psicológicos (ansiedad y depresión). Hubo un mayor porcentaje de respuesta significativa en los síntomas GI en el grupo que realizó la DM que en el grupo control (83% frente a 37%; p < 0,001). Las puntuaciones específicas de los síntomas GI, evaluadas mediante el IBS-SSS en la semana 6, fueron más bajas en pacientes con DM en comparación con los controles, incluyendo la severidad del dolor abdominal (p < 0,001) y la distensión abdominal (p = 0,001); la consistencia de las heces fue diferente en el grupo de la DM que en los controles (p = 0,012), pero no hubo diferencias significativas entre los grupos en cuanto a la frecuencia de heces normales (p = 0,055) ni en la frecuencia de las deposiciones (p = 0.304). Sin embargo, las debilidades del estudio fueron el reducido número de pacientes con los cuales realizar un análisis comparativo, la falta de control con placebo (el grupo control siguió su dieta habitual) y el período de seguimiento corto (6 semanas) como para evaluar sus efectos a largo plazo. Además esos hechos podrían sobrestimar los efectos clínicos.
En el 2024, Chen y col.,42 llevaron a cabo un estudio transversal que incluyó un análisis retrospectivo de 106 adultos con SII (criterios Roma III o IV) y 108 sujetos sanos como grupo control. En el mismo se realizó una evaluación dietética detallada de la DM incluyendo grupos de alimentos y alimentos individuales “pro-DM” (como legumbres, cereales integrales, frutas y verduras) y “anti-DM» (como azúcar y manteca). La adherencia a la DM fue similar en los sujetos con SII y en los sanos y no se correlacionó con la severidad de los síntomas según IBS-SSS (p = 0,62), ni con el dolor (p = 0,24) ni la distensión abdominal (p = 0,10). Entre los participantes con SII, un mayor consumo de frutas (p = 0,0005), azúcar añadida (p = 0,08) y manteca (p = 0,02) se asoció con una mayor gravedad de los síntomas. El análisis multivariado identificó que varios alimentos de la DM se asociaron a un aumento de los síntomas, por ejemplo, el consumo de frutas aumentó el dolor abdominal (p = 0.009) y la distensión (p = 0.004) y el consumo de vegetales aumentó la distensión (p = 0,072). Los participantes con SII consumieron menos porotos/legumbres/soja en comparación con los sujetos sanos (p = 0,048), sin embargo, en el grupo SII un mayor consumo de estos se asoció con una menor gravedad de los síntomas GI (p = 0,02). Los autores concluyeron que era posible que los participantes con SII con síntomas más graves evitaran estos alimentos por el efecto en la sintomatología GI y que los consumieran aquellos con una sensibilidad visceral relativamente menor o una microbiota intestinal con menor producción de gases. En resumen, una DM estándar no se asoció con la gravedad de los síntomas del SII, pero ciertos alimentos se asociaron con un aumento de los síntomas. Dentro de las múltiples limitaciones del estudio se encuentra en primer lugar el hecho de ser un estudio transversal por lo que los participantes no fueron aleatorizados a intervenciones dietéticas específicas y los resultados solo demostraron asociación, pero no causalidad. Además, la evaluación de la ingesta dietética se basó en un cuestionario de tipo registro dietético que se basa en un recordatorio de la dieta del último año.
Cuffe y col.21 posicionó a la DM en el sexto lugar en comparación con otras intervenciones dietéticas para la mejoría de los síntomas globales del SII (RR 0,54 [IC 95% 0,30 – 1], 2 estudios), mientras que una DBF ocupó el cuarto lugar y las recomendaciones BDA/NICE el décimo, como se mencionó previamente. Sin embargo, dado que el límite superior del IC 95% incluye al valor nulo 1, este resultado no alcanza significancia estadística y debe interpretarse con cautela.
Teniendo en cuenta la escasa evidencia disponible sobre el uso de la DM en el SII, así como las limitaciones metodológicas de los estudios realizados hasta el momento, se requieren nuevos ECA, ciegos y de mayor tamaño en los que se compare la DM con una dieta placebo o un comparador activo como la DBF para minimizar el sesgo de expectativa. A su vez el análisis de subgrupos basado en el perfil psicológico basal ayudará a determinar el fenotipo de SII más adecuado.
Por otro lado, muchos de los principales componentes de la DM como frutas, verduras, cereales integrales y legumbres, se han asociado con un aumento de los síntomas del SII. Estos alimentos también se asocian con mayores cantidades de FODMAP, por lo que no serían adecuados para el SII y deberían reducirse a una cantidad tolerable, sobre todo en quienes presentan síntomas de SII más graves.41 Además, cada persona puede tener diferentes desencadenantes de síntomas alimentarios, por lo que una DM estándar puede no ser adecuada para todos los pacientes con SII o debe personalizarse. Por este motivo, se está estudiando el uso de una DM baja en FODMAP para reducir la gravedad de los síntomas del SII,43-44 que toma criterios de ambas dietas; significa volver, en parte, a la intervención que actualmente tiene mayor evidencia científica como tratamiento nutricional del SII, la dieta baja en FODMAP.
Limitaciones metodológicas en estudios de intervención nutricional en SII
El mayor desafío al desarrollar una intervención dietética es producir evidencia de calidad sobre su eficacia. Los ensayos clínicos con intervenciones dietéticas enfrentan varias limitaciones y desafíos para el diseño metodológico del estudio, la implementación y la interpretación de los resultados. Esto se ve influenciado principalmente por la naturaleza compleja de las intervenciones nutricionales, la interacción entre los diferentes componentes de la dieta, los efectos simultáneos de las intervenciones, los diversos comportamientos alimentarios, así como también la cultura alimentaria de las diversas regiones.45
A pesar de que los ECA doble ciego con placebo siguen siendo el estándar de oro metodológico en investigaciones de intervención, su aplicación en el ámbito de la nutrición presenta limitaciones, por ejemplo, la dificultad en el enmascaramiento adecuado de los alimentos del estudio, la elección inadecuada de alimentos o dietas placebo, el control de confundidores, así como también la evaluación de la adherencia. Los alimentos no son compuestos aislados, sino que son una matriz alimentaria compleja, es decir, una mezcla diversa de nutrientes y componentes bioactivos que interactúan entre sí. Sumado a que una persona consume una combinación de alimentos a lo largo del día dentro de un patrón alimentario, las ingestas están altamente correlacionadas, lo que también dificulta su interpretación.46 Como consecuencia de estas dificultades metodológicas, la mayoría de las intervenciones dietéticas carecen de evidencia de alto nivel, como se espera en los ensayos farmacológicos. El diseño de ECA a largo plazo con el objetivo de evaluar la eficacia sostenida de una dieta terapéutica resulta prácticamente inviable.47
Otra limitación es el reclutamiento y la retención de pacientes durante el estudio. En este caso, Roth y Ohlsson48 describieron los procesos de reclutamiento de pacientes con SII para estudios de intervención dietética que comparaban a la DBF con la SSRD y resaltaron el gran desafío que supone motivar a los pacientes a participar en este tipo de estudios. Más de un tercio de los pacientes asignados inicialmente no estaban dispuestos a participar al momento de ser contactados por el investigador, y un tercio de los participantes aleatorizados no acudió a la cita para su inclusión. Destacaron que la convocatoria a través de las redes sociales sería la forma más eficiente de reclutar pacientes para intervenciones dietéticas.
Reconocer las limitaciones metodológicas a las que nos enfrentamos al momento de analizar un estudio de intervención nutricional es crucial para evaluar críticamente su contenido y por lo tanto su potencial aplicabilidad en la práctica clínica.
Medidas conductuales para el SII
Como parte del equipo multidisciplinario, el nutricionista con experiencia en el área de la gastroenterología tiene múltiples roles en el abordaje del paciente con SII, como la evaluación nutricional, la instauración del tratamiento dietético, la educación alimentaria y el seguimiento continuo. La intervención especializada es fundamental para garantizar tanto la adecuación nutricional como también la practicidad del plan alimentario, aspectos fundamentales para favorecer la adherencia.15, 47
No existe una dieta única que funcione para todas las personas con SII y, más allá del abordaje terapéutico elegido, se deben tener en cuenta medidas conductuales como una adecuada masticación, comer despacio, evitar comidas de grandes volúmenes, comer con regularidad evitando grandes intervalos entre las comidas durante el día, asegurar una ingesta adecuada de líquidos (8 vasos de agua al día), reducir el consumo de té o café a no más de 3 tazas al día y de bebidas gaseosas y alcohol; también promover un ejercicio físico regular y utilizar herramientas para la gestión emocional.13
Conclusión
Si bien la DBF continúa siendo la estrategia más recomendada y con mayor evidencia disponible, la SSRD y la DM emergen como opciones terapéuticas prometedoras. Sin embargo, aún se requieren más estudios que consoliden la evidencia sobre su eficacia y aplicabilidad clínica. Más allá de la estrategia dietética implementada, un enfoque individualizado, basado en la evidencia y en la experiencia clínica, es fundamental para seleccionar la estrategia más adecuada para cada paciente, reconociendo que no existe una única solución posible que sea efectiva en todos los pacientes con SII.
Propiedad intelectual. Las autoras declaran que los datos presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Las autoras declaran que no hubo fuentes de financiación externas.
Conflicto de intereses. Las autoras declaran no tener conflictos de intereses en relación con este artículo.
Aviso de derechos de autor
© 2025 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Schaab S N y Gutiérrez M C. Intervenciones nutricionales emergentes para el síndrome de intestino irritable: dieta reducida en almidón y sacarosa, y dieta Mediterránea. Acta Gastroenterol Latinoam. 2025;55(2):103-111. https://doi.org/10.52787/agl.v55i2.504
Referencias
- Chey WD, Hashash JG, Manning L, Chang L. AGA Clinical Practice Update on the Role of Diet in Irritable Bowel Syndrome: Expert Review. Gastroenterology. 2022 May;
162(6):1737-45.e5. - Sperber AD, Bangdiwala SI, Drossman DA, Ghoshal UC, Simren M, Tack J, et al. Worldwide Prevalence and Burden of Functional Gastrointestinal Disorders, Results of Rome Foundation Global Study. Gastroenterology. 2021 Jan;160(1):99-114.e3.
- Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology [Internet]. 2016 Feb 19; Available from: http://dx.doi.org/10.1053/j.gastro.2016.02.032
- Drossman DA, Hasler WL. Rome IV-Functional GI Disorders: Disorders of Gut-Brain Interaction. Gastroenterology. 2016 May;
150(6):1257-61. - Ford AC, Sperber AD, Corsetti M, Camilleri M. Irritable bowel syndrome. Lancet. 2020 Nov 21;396(10263):1675-88.
- Zhang H, Su Q. Low-FODMAP Diet for Irritable Bowel Syndrome: Insights from Microbiome. Nutrients [Internet]. 2025 Jan 31;17(3). Available from: http://dx.doi.org/10.3390/nu17030544
- Böhn L, Störsrud S, Törnblom H, Bengtsson U, Simrén M. Self-reported food-related gastrointestinal symptoms in IBS are common and associated with more severe symptoms and reduced quality of life. Am J Gastroenterol. 2013 May;108(5):634-41.
- Ford AC, Staudacher HM, Talley NJ. Postprandial symptoms in disorders of gut-brain interaction and their potential as a treatment target. Gut. 2024 Jun 6;73(7):1199-211.
- Gibson PR. History of the low FODMAP diet. J Gastroenterol Hepatol. 2017 Mar;32 Suppl 1:5-7.
- Farré R, Tack J. Food and symptom generation in functional gastrointestinal disorders: physiological aspects. Am J Gastroenterol. 2013 May;108(5):698-706.
- Vasant DH, Paine PA, Black CJ, Houghton LA, Everitt HA, Corsetti M, et al. British Society of Gastroenterology guidelines on the management of irritable bowel syndrome. Gut. 2021 Jul;70(7):1214-40.
- Whelan K, Ford AC, Burton-Murray H, Staudacher HM. Dietary management of irritable bowel syndrome: considerations, challenges, and solutions. Lancet Gastroenterol Hepatol. 2024 Dec;9(12):1147-61.
- McKenzie YA, Bowyer RK, Leach H, Gulia P, Horobin J, O’Sullivan NA, et al. British Dietetic Association systematic review and evidence-based practice guidelines for the dietary management of irritable bowel syndrome in adults (2016 update). J Hum Nutr Diet. 2016 Oct;29(5):549-75.
- Mitchell H, Porter J, Gibson PR, Barrett J, Garg M. Review article: implementation of a diet low in FODMAPs for patients with irritable bowel syndrome-directions for future research. Aliment Pharmacol Ther. 2019 Jan;49(2):124-39.
- Sultan N, Varney JE, Halmos EP, Biesiekierski JR, Yao CK, Muir JG, et al. How to Implement the 3-Phase FODMAP Diet Into Gastroenterological Practice. J Neurogastroenterol Motil. 2022 Jul 30;28(3):343-56.
- Whelan K, Martin LD, Staudacher HM, Lomer MCE. The low FODMAP diet in the management of irritable bowel syndrome: an evidence-based review of FODMAP restriction, reintroduction and personalisation in clinical practice. J Hum Nutr Diet. 2018 Apr;31(2):239-55.
- Halmos EP, Gibson PR. Controversies and reality of the FODMAP diet for patients with irritable bowel syndrome. J Gastroenterol Hepatol. 2019 Jul;34(7):1134-42.
- Halmos E. A FODMAP gentle approach [Internet]. Monash Fodmap; 2020 [cited 2025 Jun 9]. Available from: http://www.monashfodmap.com/blog/gentle-fodmap-diet/
- Dionne J, Ford AC, Yuan Y, Chey WD, Lacy BE, Saito YA, et al. A Systematic Review and Meta-Analysis Evaluating the Efficacy of a Gluten-Free Diet and a Low FODMAPS Diet in Treating Symptoms of Irritable Bowel Syndrome. Official journal of the American College of Gastroenterology | ACG. 2018 Sep;113(9):1290.
- Haghbin H, Hasan F, Gangwani MK, Zakirkhodjaev N, Lee-Smith W, Beran A, et al. Efficacy of Dietary Interventions for Irritable Bowel Syndrome: A Systematic Review and Network Meta-Analysis. J Clin Med [Internet]. 2024 Dec 11;13(24). Available from: http://dx.doi.org/10.3390/jcm13247531
- Cuffe MS, Staudacher HM, Aziz I, Adame EC, Krieger-Grubel C, Madrid AM, et al. Efficacy of dietary interventions in irritable bowel syndrome: a systematic review and network meta-analysis. Lancet Gastroenterol Hepatol. 2025 Jun;10(6):520-36.
- Arabpour E, Alijanzadeh D, Sadeghi A, Khoshdel S, Hekmatdoost A, Kord-Varkaneh H, et al. Gluten restriction in irritable bowel syndrome, yes or no?: a GRADE-assessed systematic review and meta-analysis. Front Nutr. 2023 Nov 1;10:1273629.
- Biesiekierski JR, Peters SL, Newnham ED, Rosella O, Muir JG, Gibson PR. No effects of gluten in patients with self-reported non-celiac gluten sensitivity after dietary reduction of fermentable, poorly absorbed, short-chain carbohydrates. Gastroenterology. 2013 Aug;145(2):320-8.e1-3.
- Skodje GI, Sarna VK, Minelle IH, Rolfsen KL, Muir JG, Gibson PR, et al. Fructan, Rather Than Gluten, Induces Symptoms in Patients With Self-Reported Non-Celiac Gluten Sensitivity. Gastroenterology. 2018 Feb;154(3):529-39.e2.
- Roth B, Nseir M, Jeppsson H, D’Amato M, Sundquist K, Ohlsson B. A Starch- and Sucrose-Reduced Diet Has Similar Efficiency as Low FODMAP in IBS-A Randomized Non-Inferiority Study. Nutrients [Internet]. 2024 Sep 9;16(17). Available from: http://dx.doi.org/10.3390/nu16173039
- Henström M, Diekmann L, Bonfiglio F, Hadizadeh F, Kuech EM, von Köckritz-Blickwede M, et al. Functional variants in the sucrase-isomaltase gene associate with increased risk of irritable bowel syndrome. Gut. 2018 Feb;67(2):263-70.
- CSID Cares [Internet]. 2024 [cited 2025 Jun 6]. Choosing Your Foods. Available from: https://www.csidcares.org/treatment/diet/
- Nilholm C, Larsson E, Roth B, Gustafsson R, Ohlsson B. Irregular Dietary Habits with a High Intake of Cereals and Sweets Are Associated with More Severe Gastrointestinal Symptoms in IBS Patients. Nutrients [Internet]. 2019 Jun 5;11(6). Available from: http://dx.doi.org/10.3390/nu11061279
- Nilholm C, Roth B, Ohlsson B. A Dietary Intervention with Reduction of Starch and Sucrose Leads to Reduced Gastrointestinal and Extra-Intestinal Symptoms in IBS Patients. Nutrients [Internet]. 2019 Jul 20;11(7). Available from: http://dx.doi.org/10.3390/nu11071662
- Nilholm C, Larsson E, Sonestedt E, Roth B, Ohlsson B. Assessment of a 4-Week Starch- and Sucrose-Reduced Diet and Its Effects on Gastrointestinal Symptoms and Inflammatory Parameters among Patients with Irritable Bowel Syndrome. Nutrients [Internet]. 2021 Jan 28;13(2). Available from: http://dx.doi.org/10.3390/nu13020416
- Ohlsson B. Theories behind the effect of starch- and sucrose-reduced diets on gastrointestinal symptoms in irritable bowel syndrome (Review). Mol Med Rep [Internet]. 2021 Oct;24(4). Available from: http://dx.doi.org/10.3892/mmr.2021.12372
- Gayoso L, Garcia-Etxebarria K, Arzallus T, Montalvo I, Lizasoain J, D’Amato M, et al. The effect of starch- and sucrose-reduced diet accompanied by nutritional and culinary recommendations on the symptoms of irritable bowel syndrome patients with diarrhoea. Therap Adv Gastroenterol. 2023 Apr 28;16:17562848231156682.
- Davis C, Bryan J, Hodgson J, Murphy K. Definition of the Mediterranean Diet; a Literature Review. Nutrients. 2015 Nov 5;7(11):9139-53.
- Zamani M, Alizadeh-Tabari S, Zamani V. Systematic review with meta-analysis: the prevalence of anxiety and depression in patients with irritable bowel syndrome. Aliment Pharmacol Ther. 2019 Jul;50(2):132-43.
- So D, Whelan K, Rossi M, Morrison M, Holtmann G, Kelly JT, et al. Dietary fiber intervention on gut microbiota composition in healthy adults: a systematic review and meta-analysis. Am J Clin Nutr. 2018 Jun 1;107(6):965-83.
- Edwards CA, Havlik J, Cong W, Mullen W, Preston T, Morrison DJ, et al. Polyphenols and health: Interactions between fibre, plant polyphenols and the gut microbiota. Nutr Bull. 2017 Dec;42(4):356-60.
- Wan Y, Wang F, Yuan J, Li J, Jiang D, Zhang J, et al. Effects of dietary fat on gut microbiota and faecal metabolites, and their relationship with cardiometabolic risk factors: a 6-month randomised controlled-feeding trial. Gut. 2019 Aug;68(8):1417-29.
- The effect of a Mediterranean diet on the symptoms of depression in young males (the “AMMEND: A Mediterranean Diet in MEN with Depression” study): a randomized controlled trial. The Ame-
rican Journal of Clinical Nutrition. 2022 Aug 1;116(2):572-80. - Shafiei F, Salari-Moghaddam A, Larijani B, Esmaillzadeh A. Mediterranean diet and depression: reanalysis of a meta-analysis. Nutr Rev. 2023 Mar 16;81(7):889-90.
- Marx W, Lane M, Hockey M, Aslam H, Berk M, Walder K, et al. Diet and depression: exploring the biological mechanisms of action. Molecular Psychiatry. 2020 Nov 3;26(1):134-50.
- Staudacher HM, Mahoney S, Canale K, Opie RS, Loughman A, So D, et al. Clinical trial: A Mediterranean diet is feasible and improves gastrointestinal and psychological symptoms in irritable bowel syndrome. Aliment Pharmacol Ther. 2024 Feb;
59(4):492-503. - Chen EY, Mahurkar-Joshi S, Liu C, Jaffe N, Labus JS, Dong TS, et al. The Association Between a Mediterranean Diet and Symptoms of Irritable Bowel Syndrome. Clin Gastroenterol Hepatol. 2024 Jan;22(1):164-72.e6.
- Kasti AN, Katsas K, Pavlidis DE, Stylianakis E, Petsis KI, Lambrinou S, et al. Clinical Trial: A Mediterranean Low-FODMAP Diet Alleviates Symptoms of Non-Constipation IBS-Randomized Controlled Study and Volatomics Analysis. Nutrients [Internet]. 2025 Apr 30;17(9). Available from: http://dx.doi.org/10.3390/nu17091545
- Rustom JN. The Efficacy of the Low-FODMAP Diet to Alleviate Symptoms of Irritable Bowel Syndrome in Adults: A Systematic Review. 2021.
- Mirmiran P, Bahadoran Z, Gaeini Z. Common Limitations and Challenges of Dietary Clinical Trials for Translation into Clinical Practices. Int J Endocrinol Metab. 2021 Jul;19(3):
e108170. - Yao CK, Gibson PR, Shepherd SJ. Design of clinical trials evaluating dietary interventions in patients with functional gastrointestinal disorders. Am J Gastroenterol. 2013 May;108
(5):748-58. - Gibson PR, Halmos EP, So D, Yao CK, Varney JE, Muir JG. Diet as a therapeutic tool in chronic gastrointestinal disorders: Lessons from the FODMAP journey. J Gastroenterol Hepatol. 2022 Apr;37(4):644-52.
- Roth B, Ohlsson B. Challenges of recruitment processes to a randomized dietary trial in irritable bowel syndrome. F1000Res. 2024 Jun 24;13:323.
Correspondencia: Sara Noemí Schaab
Correo electrónico: schaabsara@gmail.com
Acta Gastroenterol Latinoam 2025;55(2):103-111
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE


