Fernando Lobos, Pablo Barros Schelotto, Diego Ramisch, Santiago Rubio, Leonardo Montes, Gabriel Gondolesi
Instituto de Trasplante multiorgánico y Cirugía HPB.
Hospital Universitario Fundación Favaloro. Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2020;50(2):101-108
Recibido: 19/03/2019 / Aprobado: 17/01/2020 / Publicado en www.actagastro.org el 29/06/2020
Resumen
A pesar de que la mortalidad de la cirugía pancreática ha disminuido en las últimas décadas, la morbilidad permanece alta. Una de las causas más importantes de esta es la fístula pancreática postoperatoria. Estudios recientes han demostrado la influencia de la fluidoterapia perioperatoria en los resultados postoperatorios de cirugías abdominales mayores. Esto se evidenció fundamentalmente en cirugía de colon, demostrando que la sobrecarga hídrica aumenta las complicaciones postoperatorias. Objetivo. Evaluar la influencia de la fluidoterapia en la morbilidad post pancreatectomía distal videolaparoscópica. Material y métodos. Estudio retrospectivo, de una base de datos prospectiva de pacientes sometidos a pancreatectomía distal videolaparoscópica de noviembre de 2011 a septiembre de 2018. Se evaluaron 30 pacientes que se dividieron en dos grupos según la fluidoterapia administrada (restrictiva o liberal). Los datos se recolectaron de los protocolos de anestesia y de los controles en sala de internación (hasta el 3° día postoperatorio). Se analizaron variables demográficas, tiempo de estadía hospitalaria, tipo de fluidoterapia y complicaciones. Para el análisis estadístico se utilizó SPSS® v.21. (p < 0,05 fue considerado significativo). Resultados. De los 30 pacientes, el 17% eran hombres, edad media de 54 ± 18 años; 17 pacientes (57%) pertenecían a grupo liberal y 13 (43%) al grupo restrictivo. Veintitrés pacientes presentaron complicaciones, 16 (53%) fueron del grupo liberal y 7 (23%) del grupo restrictivo, (p = 0,01). Catorce pacientes del grupo liberal presentaron fístula pancreática postoperatoria vs. 6 pacientes del grupo restrictivo (p = 0,04). En 7 pacientes del grupo liberal (23%) y en 4 pacientes del grupo restrictivo se presentó fistula pancreática clínicamente relevante (13%) (p = NS). La mortalidad de la serie fue de 3,3 %, no habiendo diferencias entre los grupos de estudio. Conclusión. Nuestros resultados sugieren que la restricción de líquidos en el perioperatorio reduce considerablemente la tasa de complicaciones y el desarrollo de fístula pancreática postoperatoria, después de la pancreatectomía distal videolaparoscópica.
Palabras claves. Fluidoterapia, complicaciones postoperatorias, fístula pancreática, pancreatectomía laparoscópica.
Perioperative fluid management and postoperative complications after laparoscopic distal pancreatectomy
Summary
Despite mortality in pancreatic surgery has decreased over the last decade, morbidity remains high. One of the most important causes is pancreatic fistula. Recent studies have demonstrated the importance of fluid therapy management during the perioperative period in major abdominal surgeries. This finding was observed first in colonic surgery, demonstrating that overload of fluids increases postoperative complications. Objective. To evaluate the impact of fluid management on postoperative complications after laparoscopic distal pancreatectomy. Material and methods. Descriptive, retrospective study of a prospective database of patients whom underwent laparoscopic distal pancreatectomy from November 2011 to September 2018. Thirty patients were evaluated and divided in two groups depending on the fluid management (restrictive, or liberal). The data were collected from the anesthesia protocols and nursery reports (until 3rd postoperative day). Demographics, length of stay, kind of fluid management and complications were analyzed. For statistical analysis SPSS®v.21 was used (p < 0.05 was considered significant). Results. Out of 30 patients, 17% were male, mean age was 55 ± 18 years (r 19-82); 17 patients (57%) were included in the liberal group and 13 (43%) in the restrictive group. Twenty-three patients developed complications; 16 (53%) belonged to liberal group whereas 7 (23%) to restrictive group. (p = 0.01). Fourteen patients of liberal group vs. 6 patients of restrictive group had postoperative pancreatic fistula (p = 0.04). There were 7 patients (23%) in liberal group. and 4 (13%) patients in restrictive group with clinically relevant pancreatic fistula (13%, p = NS). Ninety day-mortality was 3.3, with no differences between groups. Conclusion. After laparoscopic distal pancreatectomy, liberal fluid administration at the perioperative period is associated with an increase in the incidence of complication, specially favoring the development of pancreatic fistula.
Key words. Fluid management, postoperative complications, pancreatic fistula, laparoscopic pancreatectomy.
Abreviaturas
PDV: Pancreatectomía distal videolaparoscópica.
POP: Postoperatorio.
FpPOp: Fístula pancreática postoperatoria.
FpPOp-Cr: Fístula pancreática postoperatoria clínicamente relevante.
D-C: Dindo-Clavien.
GR: Grupo restrictivo.
GL: Grupo liberal.
Introducción
En las últimas décadas se ha visto un gran progreso de la cirugía pancreática, que se vio reflejado en la reducción de la tasa de mortalidad, alcanzando valores menores al 5% en centros de alto volumen. Sin embargo, la morbilidad, a diferencia de la mortalidad, continúa siendo alta, con tasas de entre 30 y 50%, incluso en los centros de alto volumen.1, 2
El desarrollo de la cirugía videolaparoscópica pancreática ha llevado a que hoy se considere que el abordaje laparoscópico es el “gold standard” para la realización de la pancreatectomía distal (PDV).3
La complicación responsable de la principal causa de morbimortalidad postoperatoria (POP) continúa siendo la fístula pancreática postoperatoria (FpPop). La tasa reportada varía entre 5 y 40%. Las complicaciones que siguen en frecuencia son la sepsis secundaria a abscesos intraabdominales y hemorragia. La aparición de complicaciones tendrá además el impacto económico asociado a la prolongación de la hospitalización en forma temprana y al retraso en el inicio del tratamiento adyuvante en los pacientes oncológicos, que incrementa el riesgo de recurrencia del cáncer a largo plazo.4, 5
Durante todo procedimiento quirúrgico y en el período perioperatorio la administración de líquidos intravenosos se constituye como una de las bases del manejo de estos pacientes. La corrección de las pérdidas sensibles e insensibles de agua y poder preservar una adecuada diuresis tanto como la perfusión tisular son algunos de los objetivos primarios buscados.6, 7 Las recomendaciones respecto de la forma del manejo de los fluidos han variado en las últimas décadas, pasando de la restricción a la sobreexpansión.6 Estudios recientes sugieren que la cantidad de volumen administrado durante la cirugía y en el perioperatorio afecta los resultados de las cirugías abdominales mayores, teniendo injerencia en la aparición de complicaciones.8-12 No existen aún protocolos para estandarizar la cantidad óptima de volumen intravenoso administrado para mantener una adecuada hidratación en el período perioperatorio de una PDV. La excesiva administración de volumen puede generar edema pulmonar, disfunción cardíaca, edema a nivel de órganos abdominales e íleo, además de prolongar la inmovilización del paciente y por lo tanto incrementar el riesgo de desarrollar trombosis venosa profunda, una patología ya de alta prevalencia en esta entidad.13 También causa alteraciones en la difusión de O2, que llevan a la hipoxia tisular.11, 14
La evidencia disponible a nivel mundial del efecto de la fluidoterapia sobre las complicaciones POP de la cirugía abdominal mayor deriva principalmente de la cirugía colorrectal.7, 9, 11, 12 En ella puede observarse una menor tasa de complicaciones cuando la fluidoterapia es más restrictiva. En el manuscrito de Abraham-Nordling y col. se muestra que, en pacientes sometidos a cirugía colorrectal, un régimen restrictivo de fluidos administrados en el primer día de cirugía (media 3050 ml) reduce de forma significativa la tasa de complicaciones POP, en comparación con los pacientes que recibieron un régimen estándar de fluidos (media 5.775 ml).15
Pero aún es un tema de controversia el impacto potencial que tiene la restricción hídrica en los resultados de la cirugía pancreática. Hay que tener presente que el manejo del fluido intraoperatorio es complejo y está afectado por varios factores, tanto durante el procedimiento como durante el cuidado inmediato en las unidades de cuidados intermedios o críticos. Durante los procedimientos de alta complejidad, como son los casos de la cirugía pancreática, es complejo mantener un equilibrio hídrico cercano a cero. Estudios recientes presentan diferencias en la definición del régimen de fluidos, haciendo difícil la comparación de estos. La mayoría de ellos se dan en POP de duodenopancreatectomía cefálica (DPC), además de que la mayoría evalúa el efecto de los líquidos administrados en el IO, sin evaluar los efectos que estos pueden tener en el POP inmediato. La complejidad del análisis se ve aumentada por el hecho de que hay profesionales de distinto nivel de formación en las unidades críticas. Esto genera la necesidad establecer guías de manejo que permitan desarrollar estándares sobre la base de evidencia científica.
El objetivo de este trabajo es evaluar la influencia de la fluidoterapia en la presentación de complicaciones en el período postoperatorio de una PDV.
Material y métodos
Estudio descriptivo, que realiza un análisis retrospectivo de una base de datos prospectiva de pacientes sometidos a PDV en el período comprendido entre noviembre de 2011 y septiembre de 2018, en el Hospital Universitario-Fundación Favaloro, Buenos Aires, Argentina.
Se evaluaron 30 pacientes. Se consideraron criterios de inclusión para el estudio a quienes se les realizó una PDV, independientemente de la etiología que motivo el procedimiento. Los pacientes incluidos fueron divididos en dos grupos según la fluidoterapia administrada. Se consideró grupo restrictivo (GR) a aquellos pacientes que durante el perioperatorio (definido como el período que incluye el intraoperatorio y los 3 primeros días POP) el volumen administrado fue < 2,5 ml/kg/h. Los pacientes del grupo liberal (GL) fueron aquellos que recibieron un volumen > 2,5 ml/kg/h. El tipo de fluidos que se utilizó fue cristaloides y coloides. El flujo y el tipo de fluido administrado en cada procedimiento y durante los primeros días de internación estuvieron a cargo del anestesiólogo y los médicos clínicos de la sala, quienes regularon su administración según el estado hemodinámico del paciente y la experiencia en el manejo de estos casos. Los datos se recolectaron de los protocolos de anestesia y de los controles en sala de internación.
Se analizaron variables demográficas, la presencia de complicaciones, según la clasificación de Dindo-Clavien (D-C), considerándose para el análisis principalmente las complicaciones mayores a D-C IIIB y su severidad, lo mismo que su relación con la fluidoterapia utilizada.12, 16, 17 Las complicaciones analizadas en la serie fueron FpPop, hemorragia, infarto esplénico, perforación, complicaciones respiratorias y tromboembolismo pulmonar (TEP). En cuanto a la FpPop, se definió y clasificó según el International Study Group Pancreatic Surgery (ISGPS), que define la FpPop como la presencia de secreción pancreática, independientemente del volumen, a través del drenaje colocado. Para ser considerada positiva debió tener un dosaje de amilasa superior a 3 veces el sérico a partir del 3 día POP.3, 18 Además de definirla, esta clasificación propone 3 grados de FpPop, según su severidad, dividiéndolas en FpPop Grado A o clínicamente no relevantes (también llamadas fuga bioquímica), y FpPop clínicamente relevantes (FpPop-Cr), que comprenden a las Grado B y C, las cuales se definieron como aquellas que producen un cambio en la evolución clínica de los pacientes, requiriendo en el caso de las fístulas tipo B la administración de antibióticos o análogos de somastostatina e incluso la colocación de drenajes percutáneos, y en el caso de la fístula tipo C, el requerimiento de reintervención quirúrgica.18, 19 Se evaluaron, además, la duración de las cirugías, el requerimiento de hemoderivados, el tipo y volumen de fluidos administrados y la mortalidad dentro de los primeros 90 días después de la cirugía, la estadía hospitalaria y la readmisión de los pacientes.
Para el análisis estadístico se utilizó SPSS® v.21. (p < 0,05 fue considerado significativo utilizando el Chi-cuadrado de Person).
Resultados
De los 30 pacientes sometidos a PDV, n = 5 (17%) eran hombres. Con una media de edad de 54 ± 18 años. La media de índice de masa corporal (IMC) fue de 27 ± 5 kg/m2. Las características demográficas de los pacientes se presentan en la Tabla 1. Solo n = 2 (7%) se convirtieron a cirugía abierta.
Tabla 1. Características demográficas.
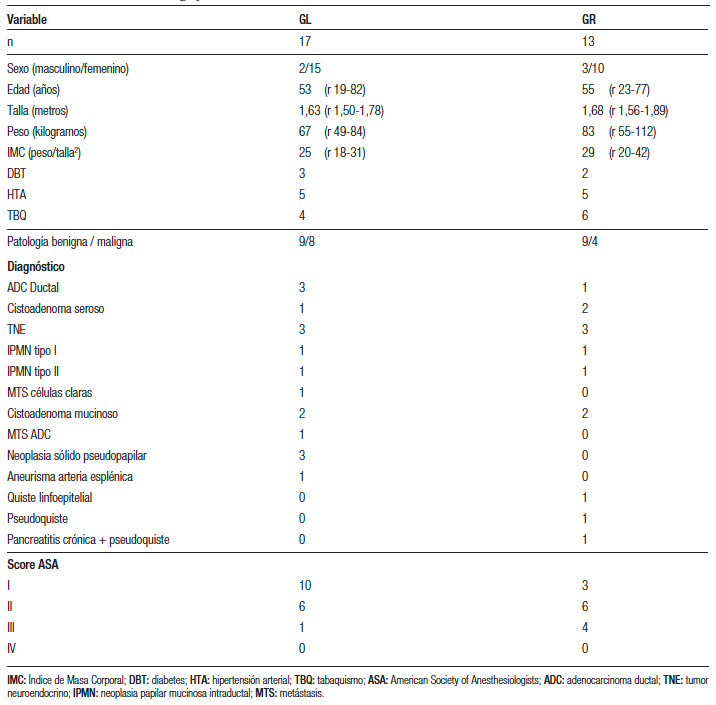
La media de duración de las cirugías fue de 268 ± 58 min. Según la fluidoterapia administrada, hubo 17 pacientes (57%) dentro del GL y 13 (43%) en el GR. Se realizaron 24 (80%) esplenopancreatectomías (EP) y 6 pancreatectomías con preservación de bazo (20%). En el GR hubo 12 EP (92%) y una sola resección con preservación del bazo (8%). En GL fueron 12 fueron EP (71%) y en 5 ocasiones se preservó el bazo (29%). La sección del parénquima se realizó con sutura mecánica en 28 casos (93%, 15 pacientes del GL y 13 del GR), el resto fue realizado con dispositivo de energía (2 casos del GL, 7%). El requerimiento de transfusiones fue necesario en 3 pacientes (todos del GL), 2 de ellos recibieron 1 UGR, y uno recibió 2 UGR, sin otro tipo de hemoderivados utilizados. El líquido administrado durante la cirugía y el postoperatorio fue cristaloides en todos los pacientes, excepto en dos del GR, que recibieron 500 ml y 1000 ml de coloides. En el GL solamente un paciente recibió coloides (1100 ml) en el POP.
Ningún paciente presentó falla renal aguda. La media de valor de creatinina en el preoperatorio fue de 0,8 mg/dl ± 0,2 mg/dl, siendo en el POP inmediato de 0,8 mg/dl ± 0,3 mg/dl y en el 3° día POP de 0,7 mg/dl ± 0,2 mg/dl, no existiendo diferencias entre los grupos (p = NS). La media de ritmo diurético fue de 112 ml/h ± 52 ml/h durante el POP. Ningún paciente requirió inotrópicos durante la cirugía ni en los primeros 3 días POP. Tampoco se observó alteración de los gases arteriales en ningún paciente durante dicho período.
Dieciséis (94%) pacientes del GL y 7 (54%) del GR presentaron algún tipo de complicación (Dindo-Clavien I-V,
p = 0,01). Véase la Tabla 2.
Tabla 2. Complicaciones según grupo y por paciente.
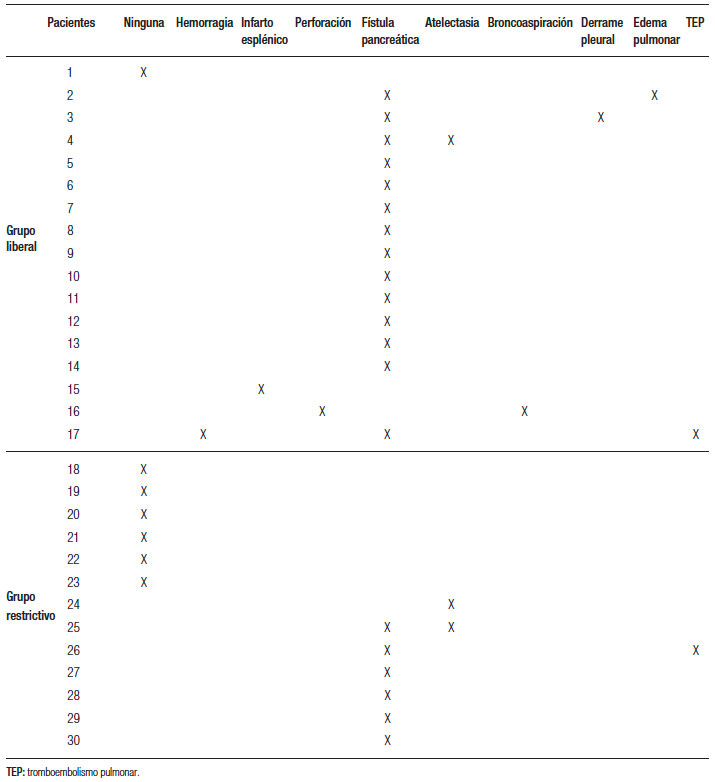
Hubo n = 8 (27%) pacientes que presentaron complicaciones mayores a D-C IIIb, de los cuales 6 (20%) se dieron en el GL y el resto (n = 2 pacientes, 7%) pertenecían al GR (p = NS). En el GR, en los 2 pacientes con complicaciones, estas fueron D-C IIIb. Mientras que en el GL hubo 5 con D-C IIIb (17%), y 1 con D-C IVb (3%) (p = NS). Un paciente del GL falleció dentro de los 90 días (3,3%).
Las FpPop se diagnosticaron en n = 14 (82%) pacientes del GL y en n = 6 (46%) pacientes del GR (p = 0,04). Si se tienen en cuenta solo las FpPop-Cr, en el GL se observaron en n = 7 (41%) casos y en n = 4 (31%) del GR (p = NS). De los n = 7 pacientes del GL, 2 (29%) se trataron de forma percutánea, y n = 5 (71%) requirieron reoperación (4 por vía laparoscópica y 1 por vía abierta). De los n = 4 pacientes del GR, 2 (50%) requirieron drenaje percutáneo, y el resto (n = 2 pacientes) se reoperaron (un paciente por vía laparoscópico y uno de forma abierta).
En cuanto a las reoperaciones por FpPop-Cr en el GL, 2 pacientes fueron intervenidos; uno por infarto esplénico (abordaje laparoscópico) y otro por perforación intestinal (abordaje abierto).
Con respecto a las complicaciones respiratorias, en el GL 5 (29%) pacientes presentaron alguna de ellas y fueron en un caso secundaria a TEP, en otros a atelectasia, derrame pleural, broncoaspiración y edema pulmonar. En el GR, 3 pacientes presentaron complicación respiratoria (23%), uno de ellos fue por TEP y dos casos fueron por atelectasia (p = NS). Véanse las Tablas 2 y 3.
Tabla 3. Valores estadísticos de complicaciones post pancreatectomía distal videolaparoscópica.
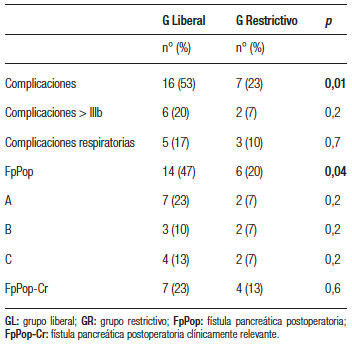
La estadía hospitalaria promedio fue de 6 ± 4 días, siendo de 5 ± 2 días para el GR, y de 7 ± 5 días para el GL (p = NS). La readmisión fue necesaria en 7 pacientes del GL (41%) y en 3 (23%) del GR (p = NS). La estadía hospitalaria durante la readmisión fue de 15 ± 11 días en el GR y en el GL 14 ± 12 días (p = NS).
Discusión
La cirugía pancreática ha evolucionado en las últimas décadas, principalmente por la centralización de estos pacientes en instituciones de alto volumen y por la estandarización de los procedimientos quirúrgicos.2, 3 Varios estudios han mostrado que diferentes estrategias pueden afectar el resultado del POP en pancreatectomía distal, por ejemplo la utilización o no de sutura mecánica,20 las diferentes vías de abordaje,21 la utilización de mallas biológicas o adhesivos en la superficie de corte,22, 23 pero poco se sabe del efecto de la fluidoterapia sobre el POP.12
Trabajos como el del grupo de In Woong Han y col., que evaluaron pacientes sometidos a DPC, encontraron un aumento significativo en la tasa de FpPop en los pacientes con fluidoterapia mayor de 15 ml/kg/h IO, no así con respecto a las complicaciones globales.11 Wang y col. demostraron que la administración de un flujo mayor a 8,2 ml/kg/h en el IO de pacientes sometidos a DPC se asocia a una incidencia mayor de FpPop.24 En nuestra experiencia, se vio que la incidencia de FpPop se incrementó cuando el flujo establecido fue mayor a 2,5 ml/kg/h dentro de los primeros 3 días POP (p = 0,04).
En el trabajo presentado por Kulemann y col., que evaluó la fluidoterapia durante los primeros 5 días perioperatorios post DPC, se demostró que los pacientes que recibieron más de 14.000 ml de líquido durante este período presentaron mayor tasa de complicaciones, así como también mayor tasa de FpPop-Cr.4 El grupo de Andrianello y col. evaluó la fluidoterapia en pacientes sometidos tanto a DPC como a PD, demostrando un aumento en la tasa de complicaciones D-C IIIb en los pacientes que recibieron un régimen liberal de fluidos (9 ml/kg/h en DPC y 8 ml/kg/h en PD); este aumento fue estadísticamente significativo. En cuanto a las FpPop, mostraron un aumento estadísticamente significativo en el caso de los pacientes sometidos a DPC, pero no en el caso de la PD.16 Al igual que el grupo de Andrianello, nosotros evidenciamos un aumento en la incidencia de complicaciones globales en el GL (> 2,5 ml/kg/h) (p = 0,01).
Nuestro trabajo evalúa no solo la fluidoterapia IO, sino que también la administrada hasta el 3° día POP de PDV, momento en el que por definición se establece la FpPop. En nuestra serie observamos que a mayor carga hídrica (> 2,5 ml/kg/h) en el IO y en el POP inmediato (hasta el 3° POP), mayor es el riesgo de presentar complicaciones globales luego de la PDV, como también es mayor el riesgo de presentar FpPop.
El aumento del aporte hídrico podría ser causa de edema tisular y este influir en la aparición de la fístula postoperatoria. Debemos tener en cuenta que todas las fístulas pancreáticas tipo B o C comienzan siendo una fístula tipo A. Por lo cual, si somos capaces de disminuir la presencia de estas, probablemente, disminuyamos las FpPop-Cr.
También hemos mostrado que existe un aumento en las complicaciones generales mayores a D-C IIIb, pero sin un resultado estadísticamente significativo. Esto puede ser debido al tamaño muestral. Creemos que el impacto del aporte hídrico en el perioperatorio no debe ser subestimado.
Nuestros resultados mostraron que el GL (flujo 2,5 ml/kg/h) presenta mayor frecuencia de complicaciones POP, así como de FpPop. Interpretamos esto como una mayor tendencia de complicaciones POP en aquellos que recibieron sobrecarga hídrica. Debido a las limitaciones presentadas por el estudio, las cuales fueron su carácter retrospectivo, el número de la población estudiada, y también la falta de evaluación de la textura del parénquima pancreático y el tamaño del conducto principal, no se puede ser categórico con esta conclusión. Para ello harían falta más estudios de carácter prospectivos y con mayor número de pacientes.
Los índices de complicaciones presentados en este trabajo están por encima de los presentados en la literatura mundial, particularmente en lo que respecta a las FpPop, la cual se presenta con tasas de entre 10 y 30%, como en el trabajo presentado por Lillemone y col. en pancreatectomías distales abiertas,25 o como lo muestra el estudio de Shimizu y col. en cirugía pancreática laparoscópica, con tasas del 15%.26
Una de las explicaciones posibles a lo ocurrido es que estos resultados corresponden a una serie inicial, en la cual posiblemente la curva de aprendizaje tenga influencia. Cuando se comparan los resultados de la cirugía pancreática abierta de nuestro centro, como así también cuando analizamos las PDV en etapas iniciales y las últimas, la tasa de fístula se adecúa a las reportadas en las publicaciones mencionadas. Además, habría que considerar otros aspectos, como el hecho de que la mayoría de los pacientes presentaban patología benigna, por lo que es de esperarse que el parénquima pancreático en esos casos fuera más blando y que esto favoreciera el surgimiento de las FpPop. Siguiendo esta misma línea, la mayoría de los pacientes presentaban IMC > de 25, lo que indicaría mayor incidencia de páncreas blandos en estos pacientes.
A pesar de las limitaciones del trabajo, que no nos permiten ser determinantes en las conclusiones, creemos que una adecuada administración de fluidos puede reducir la tasa de complicaciones después de PDV. La mejor comprensión de los efectos de la administración de líquidos es necesaria para mejorar los resultados del POP. Se necesitan y se propone la realización de estudios multicéntricos, prospectivos y aleatorizados para lograr definir la verdadera relación entre la fluidoterapia y las complicaciones de la cirugía pancreática, y así confeccionar guías para su manejo.
Sostén financiero. Ninguno.
Referencias
- Bassi C, Dervenis C, Butturini G, Fingerhut A, Yeo C, Izbicki J, Neoptolemos J, Sarr M, Traverso W, Buchler M. Postoperative pancreatic fistula: an international study group (ISGPF) definition. Surgery 2005; 138: 8-13.
- Fujino Y. Perioperative management of distal pancreatectomy. World Journal of Gastroenterology 2015; 21: 3166-3169.
- Bassi C, Butturini G, Molinari E, Mascetta G, Salvia R, Falconi M, Gumbs A, Pederzoli P. Pancreatic fistula rate after pancreatic resection: the importance of definitions. Digestive Surgery 2004; 21: 54-59.
- Kulemann B, Fritz M, Glatz T, Marjanovic G, Sick O, Hopt UT, Hoeppner J, Makowiec F. Complications after pancreaticoduodenectomy are associated with higher amounts of intra and postoperative fluid therapy: A single center retrospective cohort study. Annals of Medicine and Surgery 2017; 16: 23-29.
- Nagai S, Fujii T, Kodera Y, Kanda M, Sahin TT, Kanzaki A, Hayashi M, Sugimoto H, Nomoto S, Takeda S, Morita S, Nakao A. Recurrence pattern and prognosis of pancreatic cancer after pancreatic fistula. Annals of Surgical Oncology 2011; 18: 2329-2337.
- Brandstrup B. Fluid therapy for the surgical patient. Best Practice & Research Clinical Anaesthesiology 2006; 20: 265-283.
- Shin CH, Long DR, Mc Lean D, Grabitz SD, Ladha K, Timm FP, Thevathasan T, Pieretti A, Ferrone C, Hoeft A, Scheeren TWL, Thompson BT, Kurth T, Eikermann M. Effects of Intraoperative Fluid Management on Postoperative Outcomes: A Hospital Registry Study. Annals of Surgery 2018; 267: 1084-1092.
- De Aguilar-Nascimento JE, Diniz BN, do Carmo AV, Silveira EAO, Silva RM. Clinical Benefits After the Implementation of a Protocol of Restricted Perioperative Intravenous Crystalloid Fluids in Major Abdominal Operations. World Journal of Surgery 2009; 33: 925-930.
- MacKay G, Fearon K, Mc Connachie A, Serpell MG, Molloy RG, O’Dwyer PJ. Randomized clinical trial of the effect of postoperative intravenous fluid restriction on recovery after elective colorectal surgery. British Journal of Surgery 2006; 93: 1469-1474.
- Prien T, Backhaus N, Pelster F, Pircher W, Biinte H, Lawin P. Effect of intraoperative fluid administration and colloid osmotic pressure on the formation of intestinal edema during gastrointestinal surgery. Journal of Clinical Anesthesia 1990; 2: 317-323.
- Han IW, Kim H, Heo JS, Oh MG, Choi YS, Lee SE, Lim CS. Excess intraoperative fluid volume administration is associated with pancreatic fistula after pancreaticoduodenectomy. A retrospective multicenter study. Medicine 2017; 96: e6893.
- Brandstrup B, Tønnesen H, Beier-Holgersen R, Hjortsø E, Ørding H, Lindorff-Larsen K, Rasmussen MS, Lanng C, Wallin L; The Danish Study Group on Perioperative Fluid Therapy (Iversen LH, Gramkow CS, Okholm M, Blemmer T, Svendsen PE, Rottensten HH, Thage B, Riis J, Jeppesen IS, Teilum D, Christensen AM, Graungaard B, Pott F). Effects of intravenous fluid restriction on postoperative complications: comparison of two perioperative fluid regimens: a randomized assessor-blinded multicenter trial. Annals of Surgery 2003; 238: 641-648.
- Rahbari NN, Zimmermann JB, Schmidt T, Koch M, Weigand MA, Weitz J. Meta-analysis of standard, restrictive and supplemental fluid administration in colorectal surgery. British Journal of Surgery 2009; 96: 331-341.
- Lobo DN, Bostock KA, Neal KR, Perkins AC, Rowlands BJ, Allison SP. Effect of salt and water balance on recovery of gastrointestinal function after elective colonic resection: a randomised controlled trial. The Lancet 2002; 359: 1812-1818.
- Abraham-Nordling M, Hjern F, Pollack J, Prytz M, Borg T, Kressner U. Randomized clinical trial of fluid restriction in colorectal surgery. British Journal of Surgery 2012; 99: 186-191.
- Andrianello S, Marchegiani G, Bannone E, Masini G, Malleo G, Montemezzi GL, Polati E, Bassi C, Salvia R. Clinical Implications of Intraoperative Fluid Therapy in Pancreatic Surgery. Journal of Gastrointestinal Surgery 2018; 22: 2072-2079.
- Eng OS, Goswami J, Moore D, Chen C, Gannon CJ, August DA, Carpizo DR. Intraoperative Fluid Administration Is Associated with Perioperative Outcomes in Pancreaticoduodenectomy: A Single Center Retrospective Analysis. Journal of Surgical Oncology 2013; 108: 242-247.
- Bassi C, Marchegiani G, Dervenis C, Sarr M, Abu Hilal M, Adham M, Allen P, Andersson R, Asbun HJ, Besselink MG, Conlon K, Del Chiaro M, Falconi M, Fernández-Cruz L, Fernández-del Castillo C, Fingerhut A, Friess H, Gouma DJ, Hackert T, Izbicki J, Lillemoe KD, Neoptolemos JP, Olah A, Schulick R, Shrikhande SV, Takada T, Takaori K, Traverso W, Vollmer CR, Wolfgang CL, Yeo CJ, Salvia R, Buchler M. The 2016 update of the International Study Group (ISGPS) definition and grading of postoperative pancreatic fistula: 11 Years After. Surgery 2017; 16: 584-591.
- Hackert T, Hinz U, Pausch T, Fesenbeck I, Strobel O, Schneider L, Fritz S, Beuchler MW. Postoperative pancreatic fistula: We need to redefine grades B and C. Surgery 2016; 159: 872-877.
- Diener MK, Seiler CM, Rossion I, Kleeff J, Glanemann M, Butturini G, Tomazic A, Bruns CJ, Busch ORC, Farkas S, Belyaev O, Neoptolemos JP, Halloran C, Keck T, Niedergethmann M, Gellert K, Witzigmann H, Kollmar O, Langer P, Steger U, Neudecker J, Berrevoet F, Ganzera S, Heiss MM, Luntz SP, Bruckner T, Kieser M, Büchler MW. Efficacy of stapler versus hand-sewn closure after distal pancreatectomy (DISPACT): a randomised, controlled multicentretrial. The Lancet 2011; 377: 1514-1522.
- Riviere D, Gurusamy KS, Kooby DA, Vollmer CM, Besselink MG, Davidson BR, van Laarhoven CJ. Laparoscopic versus open distal pancreatectomy for pancreatic cancer. Cochrane Data base of Systematic Reviews 2016; 4: CD011391.
- Jang JY, Shin YC, Han Y, Park JS, Han HS, Hwang HK, Yoon DS, Kim JK, Yoon YS, Hwang DW, Kang CM, Lee WJ, Heo JS, Kang MJ, Chang YR, Chang J, Jung W, Kim SW. Effect of Polyglycolic Acid Mesh for Prevention of Pancreatic Fistula Following Distal Pancreatectomy: A Randomized Clinical Trial. JAMA Surgery 2017; 152: 150-155.
- Montorsi M, Zerbi A, Bassi C, Capussotti L, Coppola R, Sacchi M; The Italian Tachosil Study Group. Efficacy of an Absorbable Fibrin Sealant Patch (TachoSil) After Distal Pancreatectomy. A Multicenter, Randomized, Controlled Trial. Annals of Surgery 2012; 256: 853-860.
- Wang S, Wang X, Dai H, Han J, Li N, Li J. The effect of intraoperative fluid volumen administration on pancreatic fistulas after pancreaticoduodenectomy. Journal of Investigative Surgery 2014; 27: 88-94.
- Lillemoe KD, Kaushal S, Cameron JL, Sohn TA, Pitt HA, Yeo CJ. Distal Pancreatectomy: Indications and Outcomes in 235 Patients. Ann Surg 1999; 229 (5): 693-700.
- Shimizu S, Tanaka M, Konomi H, Mizumoto K, Yamaguchi K. Laparoscopic pancreatic surgery. Surg Endosc 2004; 18: 402-406.
Correspondencia: Pablo Barros Schelotto
Av. Belgrano 1782 (C1093AAS). Ciudad Autónoma de Buenos Aires, Argentina
Tel.: (54) 11 43781200 – Int: 1707
Correo electrónico: pbarros@ffavaloro.org
Acta Gastroenterol Latinoam 2020;50(2):101-108
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE


