Daniela Caamaño1 ID· Carolina Dutto2 ID· José Adi2 ID
1 Hospital J. J. Pose. Zapala, Provincia de Neuquén.
2 Hospital Lagomaggiore. Ciudad de Mendoza, Provincia de Mendoza.
Argentina.
Acta Gastroenterol Latinoam 2022;52(2):281-287
Recibido: 17/01/2022 / Aceptado: 10/05/2022 / Publicado online el 27/06/2022 / https://doi.org/10.52787/agl.v52i2.159
Resumen
La colecistitis aguda es causada mayormente por la obstrucción del conducto cístico o del cuello de la vesícula por cálculos biliares. El manejo habitual es la colecistectomía de emergencia o urgencia, dependiendo de la severidad de la enfermedad. En los pacientes de alto riesgo quirúrgico, se opta por el drenaje de la vesícula biliar, cuyo abordaje es tradicionalmente percutáneo o bien con métodos endoscópicos a través la colocación de tubos nasobiliares, stents transpapilares o stents transmurales por ecoendoscopía. El abordaje endoscópico cuenta con la ventaja de proteger la integridad de la barrera cutánea, es menos doloroso y tiene un menor impacto en la calidad de vida del paciente. Se presentan dos casos clínicos de drenaje endoscópico: el de una paciente con colecistitis aguda y shock séptico en contexto de quemaduras graves y el de un paciente añoso con similar deterioro clínico, a quienes se les realizó drenaje endoscópico con colocación de sonda nasovesicular, con buena respuesta clínica y resolución quirúrgica posterior.
Palabras claves. Colecistitis aguda grave, drenaje nasovesicular, pacientes de alto riesgo.
Nasogallbladder Drainage: Endoscopic Alternative for Severe Acute Cholecystitis
Summary
Acute cholecystitis is mainly caused by the obstruction of the cystic duct or the gallbladder neck by stones. The usual management is emergency or urgent cholecystectomy, depending on the severity of the disease. In patients at high surgical risk, gallbladder drainage is chosen, which is traditionally approached percutaneosly or with endoscopic methods through the placement of nasobiliary tubes, transpapillary stents or transmural stents by endoscopic ultrasound. The endoscopic approach has the advantage of maintaining the integrity of the skin barrier, is less painful and has less impact on the patient’s quality of life. Two clinical cases of endoscopic drainage are presented: that of a young woman with acute cholecystitis and septic shock in the context of severe burns, and that of an elderly man with similar clinical deterioration, both of whom underwent endoscopic drainage with placement of a nasogallbladder tube, with good clinical response and subsequent surgical resolution.
Keywords. Severe acute cholecystitis, nasogallbladder drainage, high-risk patients.
Abreviaturas
CA: Colecistitis aguda.
DP: Drenaje percutáneo.
DE: Drenaje endoscópico.
CPRE: Colangiografía retrógrada endoscópica.
EUS-DE: Drenaje transmural, guiado por ecoendoscopía.
Introducción
La colecistitis aguda (CA) es una enfermedad de gran incidencia, cuya principal etiología es la obstrucción del conducto cístico debido a la presencia de cálculos biliares. La resolución habitual es la colecistectomía laparoscópica. En los pacientes de alto riesgo quirúrgico, ya sea por comorbilidades o condiciones clínicas, las guías de Tokio 2018 sobre el manejo de colecistitis aguda recomiendan el drenaje paliativo de la vesícula biliar.1 El abordaje es tradicionalmente percutáneo (DP), y puede realizarse una colecistectomía en forma diferida una vez que mejora el estado clínico del paciente. Si bien el abordaje percutáneo es seguro y efectivo, tiene algunas limitaciones técnicas y, además, el tubo de drenaje externo genera un impacto negativo en la calidad de vida de los pacientes, y debe esperarse un tiempo para poder retirarlo sin complicaciones.2
Desde 1984 en adelante, se han descrito métodos endoscópicos de drenaje de la vesícula biliar (DE), a través la colocación de sondas nasobiliares, stents transpapilares o transmurales por ecoendoscopía. La vía endoscópica cuenta con la ventaja de ofrecer un drenaje interno, sin punciones, lo que resulta especialmente útil en pacientes con trastornos de la coagulación, ascitis u otras alteraciones anatómicas que dificulten el acceso percutáneo. La evidencia acerca de la factibilidad de la implementación de estas técnicas va en aumento. El éxito técnico y clínico, así como la seguridad del DE, se han evaluado en numerosos trabajos científicos. En un metaanálisis en el que se evaluaron los distintos métodos de DE, la tasa combinada ponderada para el éxito técnico fue del 83% (IC del 95%, 78%-87%), el éxito clínico fue del 93% (IC del 95%, 89%-96%), la tasa de eventos adversos fue del 10% (IC del 95%, 7%-13%) y la recurrencia de la colecistitis se registró en el 3% de los casos (IC del 95%, 1%-5%).14
Presentamos dos casos clínicos de colocación endoscópica de drenaje nasobiliar en pacientes con shock séptico a punto de partida de una colecistitis litiásica, que tuvieron una evolución favorable y resolución del cuadro de sepsis. En una paciente, el uso del abordaje endoscópico sumó a las ventajas previamente mencionadas la conservación de los sitios con compromiso cutáneo debido a quemaduras graves.
Caso clínico
Caso 1: Mujer de 19 años, cursando puerperio inmediato, que, a raíz de un accidente doméstico, sufrió quemaduras AB y B en cara, tórax y miembros, que comprometían el 20% de la superficie corporal total. Se realizaron curaciones locales, antibioticoterapia sistémica y toilette de lesiones cutáneas, con buena evolución. A las dos semanas presentó fiebre, taquicardia, taquipnea, insuficiencia respiratoria aguda e inestabilidad hemodinámica, por lo que requirió cuidados intensivos, asistencia respiratoria mecánica invasiva y vasopresores. Presentaba mala evolución, con disfunción orgánica múltiple y aparición clínica de ictericia. En la analítica se observó: hematocrito 29,6%; leucocitos 15750/mm3, NS 76%, NC 3%, L 20%, M 1%; plaquetas 99000/mm3, VSG 46 mm/1°hora, bilirrubina total 6,53 mg/dL; bilirrubina directa 5,54 mg/dL; TGO 34 UI/L, TGP 30 UI/L, FAL 564 UI/L, GGT 62 UI/L, amilasa 38 UI/L. En la ecografía abdominal se informó vesícula biliar con paredes en el límite de la normalidad y con litiasis múltiple en su interior. La vía biliar extrahepática se encontraba levemente dilatada, sin observarse imagen compatible con cálculo en esta. Debido a la condición clínica de la paciente y la sospecha de colecistitis aguda litiásica, se decidió realizar Colangiografía retrógrada endoscópica (CPRE).
El procedimiento se llevó a cabo con endoscopio de visión lateral; se observó papila de aspecto normal, no se observo salida de cálculos luego del paso de la canastilla. Al contrastar el cístico se observo la presencia de un lito en su interior (Figura 1) con vesícula biliar completamente ocupada por cálculos (Figura 2). Se dejó un drenaje nasovesicular (Figura 3), se aspiró bilis para cultivo y se realizaron lavados reglados (Figura 4).
Figura 1. CPRE, canulación transpapilar del conducto cístico con litiasis cística.
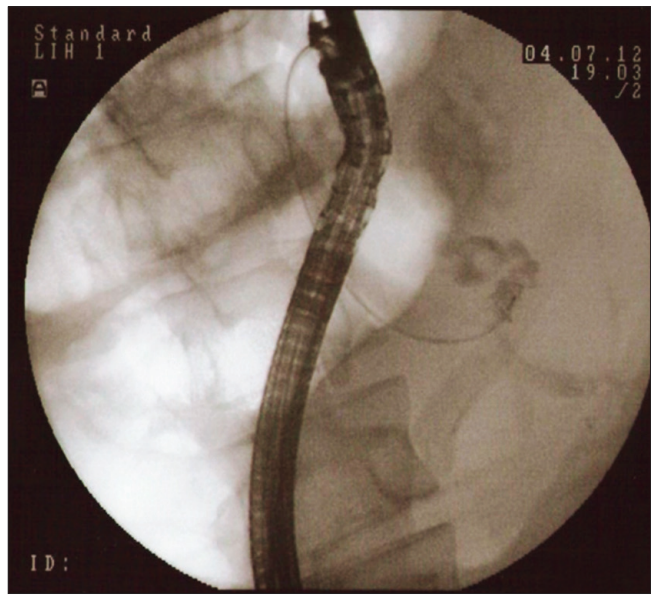
Figura 2. CPRE, se tiñe vesícula biliar, evidenciando presencia de litiasis múltiple.

Figura 3. CPRE, catéter para drenaje colocado en vesícula biliar.
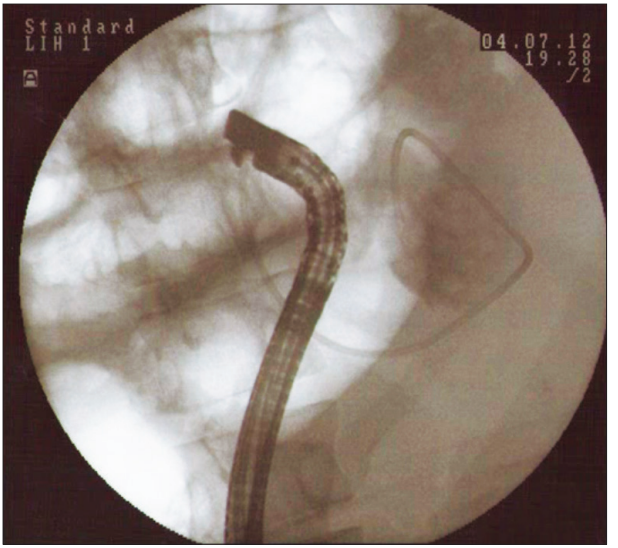
Figura 4. Lavado de catéter de drenaje nasovesicular.
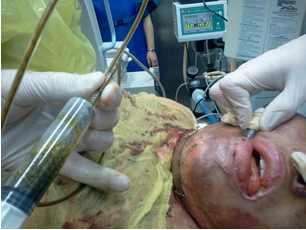
Posterior al procedimiento, la paciente presentó una rápida mejoría clínica y de los resultados de laboratorio, encontrándose afebril. En cultivo se aisló Stenotrophomonas maltophilia. Fue trasladada a sala común en las 72 horas siguientes y, posteriormente, se realizó la colecistectomía.
Caso 2: Hombre de 65 años con antecedentes de lupus eritematoso sistémico e hipertensión arterial que acudió por dolor abdominal en hipocondrio derecho, fiebre de 38,5° y deterioro del estado general. En la analítica se observó: leucocitosis, TGO 249 UI/L, TGP 196 UI/L, FAL 183 U/L, bilirrubina total 4,0 mg/dL, bilirrubina directa 3,3 mg/dL, ácido láctico 9,3 mmol/l. La ecografía abdominal evidenció hígado aumentado de tamaño y vía biliar intrahepática sin dilatación; colédoco de 8,3 mm de diámetro, con litiasis de 7 mm de diámetro a nivel de su tercio medio; vesícula distendida y de paredes engrosadas y, en su interior, imagen ecogénica de 8 mm de diámetro mayor. El paciente evolucionó con deterioro progresivo con shock séptico y requerimiento de ARM.
Se realizó procedimiento con endoscopio de visión lateral, en el que se observó la papila de aspecto normal. Se canuló selectivamente la vía biliar con un papilótomo y una guía. En la colangiografía, se evidenció la vía biliar levemente dilatada con lito a nivel del colédoco medio. Se realizó papilotomía observándose salida de bilis clara. Se extrajo un lito con balón. Se canularon el conducto cístico y la vesícula (Figura 5). Se dejó el drenaje nasovesicular (Figura 6), se aspiró bilis para cultivo y se indicaron lavados reglados (Figura 7).
Figura 5. CPRE, canulación transpapilar de la vesícula biliar a través del conducto cístico.

Figura 6. CPRE, catéter para drenaje colocado en vesícula biliar.
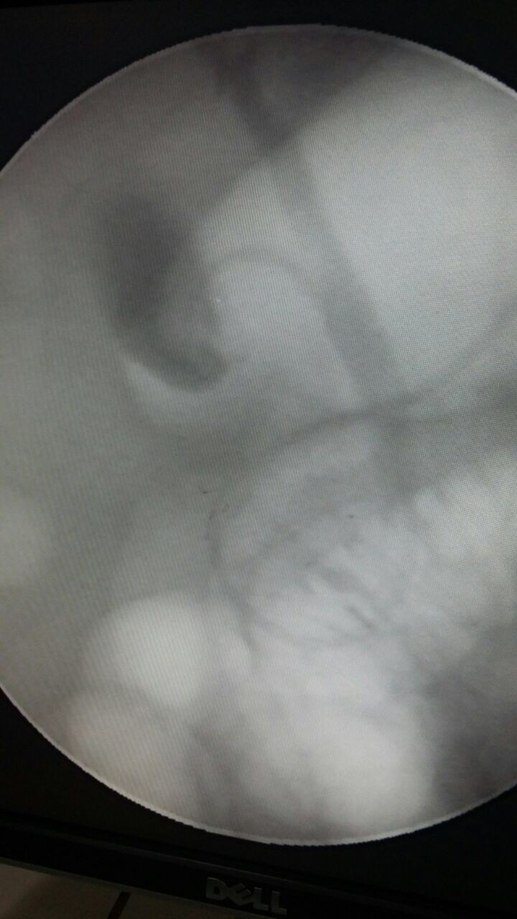
Figura 7. Lavado de catéter de drenaje nasovesicular.
El paciente presentó una sustancial mejoría clínica, pasando a sala general a las 48 horas. Se aisló Escherichia coli en los cultivos. Se realizó colecistectomía laparoscópica al quinto día post-CPRE, y se le otorgó el alta hospitalaria al séptimo día de internación.
Discusión
El tratamiento de primera línea para la colecistitis aguda es la colecistectomía laparoscópica; sin embargo, en pacientes críticamente enfermos, la morbilidad y mortalidad postoperatoria aumentan, con tasas del 40% y del 5% respectivamente.1, 15-16 En estos casos, el DP o simplemente la punción-aspiración de la vesícula biliar son los tratamientos estándar, que sirven como puente hasta la resolución quirúrgica definitiva. No obstante, en ciertas circunstancias, como en pacientes con coagulopatías, uso de anticoagulantes y antiplaquetarios, síndrome de Chilaiditi, ascitis, anormalidades anatómicas o falta de disponibilidad, el riesgo de complicaciones del DP, tales como hemorragia o peritonitis biliar, aumenta. En un estudio de gran población, se demostró que el antecedente del uso de agentes antiplaquetarios puede aumentar el sangrado severo después del DP (780/34.606, 2,3% de los pacientes), siendo el DE sin esfinterotomía una buena alternativa.12
Desde la introducción, en 1984, de la canulación transpapilar de la vesícula,3 se han desarrollado alambres guías y catéteres que han facilitado la canulación selectiva del conducto cístico y la vesícula biliar. Cada vez se reportan más casos en la bibliografía, encontrándose actualmente más de treinta estudios que informan su experiencia, con alrededor de 1500 pacientes sometidos a DE.4-13
Una revisión reciente de ASGE demostró resultados aceptables de las técnicas de DE de VB en comparación con DP. Las técnicas endoscópicas pueden ser tanto transpapilar, con colación de catéter nasovesicular o stent vesicular por CPRE, como transmural con EUS. Los datos publicados sugieren que las técnicas de DE de la VB pueden estar asociadas con tasas más bajas de eventos adversos y una mejor calidad de vida. Sin embargo, hay consideraciones clínicas importantes para elegir entre estas opciones de tratamiento, que requieren un enfoque colaborativo multidisciplinario para el manejo terapéutico en estos pacientes.15
Una de las mayores dificultades en el DE transpapilar es la canulación selectiva del conducto cístico. La presencia de litiasis cística, la dilatación del colédoco y la dirección del conducto cístico fueron reportadas como factores de riesgo que propician fallas técnicas.12 En el trabajo de Maruta y col., se estudió la tasa de éxito técnico de la canulación del cístico según su dirección, siendo más factible cuando su inserción en el conducto colédoco es de disposición distal y a la derecha.12
Pese a estos desafíos técnicos, en una serie de casos de China, se reportó el tiempo de entrada del alambre guía a la vesícula biliar. Este varió de 3 a 28 minutos (con un promedio de 12,7 minutos), con una tasa de éxito técnico del 100%.10
Si el conducto cístico no puede ser encontrado, puede ser útil el uso de la colangioscopía.
En relación con la colocación de drenajes nasovesiculares, generalmente se utilizan de 5F y 7F; si bien el uso de drenajes de mayor calibre podría resultar en un mejor drenaje vesicular, es posible que estos sean más difíciles de insertar y, además, si el paciente tiene coagulopatía y no se realiza papilotomía, podría conllevar un mayor riesgo de pancreatitis.
En nuestro caso, utilizamos un drenaje nasovesicular de 7F, con éxito.
Otra alternativa en el drenaje transpapilar es la utilización de prótesis plásticas, aunque estas impiden el lavado de la vesícula. La colocación de un stent colecistoduodenal se tolera mejor y no conlleva los riesgos adicionales de desalojo e infecciones de los senos nasales a largo plazo como en el caso de los drenajes nasovesiculares.5 Accesoriamente, Mutignani y col. encontraron una tasa de recurrencia de CA del 10% en pacientes sometidos a DE con drenajes nasobiliares, con un seguimiento medio de diecisiete meses.8
Por esto, en pacientes cuyo estado general los excluye completamente de una resolución quirúrgica posterior, es pertinente considerar la colocación de stents transpapilares y/o trasmurales por sobre el drenaje nasovesicular.
El EUS-DE, por su parte, aparece como una terapia emergente, con publicaciones recientes que evidencian excelentes tasas de éxito clínico y técnico.16-17 Se trata de una técnica novedosa que permite la formación de un trayecto fistuloso entre la vesícula biliar y la luz gastrointestinal (principalmente el duodeno, estómago y yeyuno), permitiendo el drenaje interno. Su complicación más relevante ha sido el sangrado y la perforación,19 así como la migración de prótesis y posterior bilirragia, pero esto se ha ido superando con la aparición de stents autoexpandibles antimigratorios.16 Kalva y col.,18 en un metaanálisis que incluyó 13 estudios con 233 pacientes sometidos a EUS-DE, encontraron un éxito técnico combinado del 93,86 % (IC del 95% = 90,56-96,49) y un éxito clínico del 92,48 % (IC 95% = 88,9-95,42), con una tasa de eventos adversos del 18,31% (IC 95% = 13,49-23,68). Mohan y col.,6 en un metanálisis que incluyó 72 estudios, compararon los tres métodos de drenaje vesicular en pacientes con colecistitis aguda de alto riesgo y concluyeron que el EUS-DE sería el método de elección para el manejo de estos pacientes con la mayor tasa de éxito técnico y clínico: 95,3% (95% CI 92,8-96,9) y 96,7% (95% CI 94,0-98,2) respectivamente, comparado con DE transpapilar, con 83% (95% CI 80,1-85,5, I 2 = 29) y 88,1% (95% CI 83,6-91,4) respectivamente, y con el DE PC 98,7 % (95% CI 98,0-99,1) y 89,3% (95% CI 86,6-91,5) respectivamente.
En cuanto a las complicaciones de cada procedimiento, un metaanálisis reciente mostró que, si bien el riesgo de pancreatitis post-CPRE en pacientes sometidos a DE (5,1%) es superior a la de los pacientes sometidos a EUS-DE (1,4%) y DP (1,1%), las incidencias de hemorragia y de fuga biliar son significativamente menores en pacientes sometidos a DE (1,9% y 1,4%, respectivamente) que en aquellos sometidos a EUS-DE (4,3% y 2,9%, respectivamente) y DP (2,0% y 2,7%, respectivamente).6
Otro punto a considerar es la resolución quirúrgica posterior. Es sencillo pensar que los métodos percutáneos cuentan con la aparente desventaja de alterar los planos anatómicos por la consecuente formación de la fístula colecistocutánea. Pese a esto, se ha demostrado que las colecistectomías post-DP son seguras. Kaura y col. evaluaron los resultados de la colecistectomía de intervalo en 52 pacientes con DE y 140 pacientes con DP y encontraron una tendencia hacia menores complicaciones postoperatorias con DE (30,7% vs. 43,5%; p = 0,07). No se hallaron diferencias significativas ni en la tasa de conversión a colecistectomía abierta OR 1,5 (IC del 95%: 0,68-3,65; p = 0,28) ni en la gravedad de las complicaciones (grado de Clavien-Dindo> 2) OR 0,60, (IC del 95%: 0,19-1,87; p = 0,38)8. Saumoy y col. tampoco encontraron diferencias en la tasa de conversión a colecistectomía abierta y eventos adversos postoperatorios entre 13 pacientes sometidos a DE, en comparación con 21 pacientes sometidos a DP.9
El DE es seguro y efectivo. Su importancia cobra especial valor en aquellos pacientes que no pueden someterse a DP y no está asociada a la aparición de complicaciones graves, tanto como de hematoma y peritonitis biliar como de neumotórax e, incluso, de diseminación de células tumorales en casos de colecistitis secundaria a cáncer vesicular. Otra condición desfavorable es el tiempo que se requiere para poder retirar el drenaje externo, que ronda entre las tres y seis semanas, ya que se espera la formación de una fístula segura para evitar complicaciones intraperitoneales.
El DE constituye una alternativa útil dentro del arsenal terapéutico para drenar la vesícula en pacientes con colecistitis aguda grave, como puente en el caso de colocación de tubos nasovesiculares y como terapia definitiva con la colocación de stents.
Conclusión
En los casos presentados, se logró, con éxito y sin complicaciones relacionadas con el método, el drenaje endoscópico de la vesícula. Creemos que, si bien son necesarios estudios aleatorizados para definir el rol del DE y DP, el primero es una alternativa segura en pacientes con colecistitis aguda con indicación de drenaje de la vesícula biliar, en quienes el drenaje percutáneo esté contraindicado o sea técnicamente dificultoso, y, además, plantea interesantes ventajas al no generar alteraciones morfológicas, en vistas de una resolución quirúrgica posterior. En uno de los casos expuestos, se contó con el beneficio adicional de no atravesar la dañada barrera cutánea de la paciente, sin predisponerla a infecciones, dado el antecedente de quemaduras graves. En el otro caso, la ventaja del DE consistió en tratar la vía biliar por la sospecha asociada de colangitis. En ambos casos, se optó por la opción transpapilar con drenaje nasobiliar por tratarse de casos agudos que necesitaban contemporización. Si bien el EUS-DE parece imponerse como el tratamiento estándar en un futuro cercano, con ventajas especialmente visibles en casos en los que se intenta evitar una cirugía posterior, es todavía una limitación real la no disponibilidad de este método en todos los centros, como es nuestro caso, y la grave condición de los pacientes que impedía que fueran trasladados. Por estos motivos, consideramos al DE transpapailar con colocación de catéter nasobiliar una alternativa accesible, viable y efectiva en este tipo de pacientes.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos y las figuras presentes en el manuscrito son originales y fueron realizados en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2022 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Caamaño D, Dutto C, Adi J. Drenaje nasovesicular: alternativa endoscópica para la colecistitis aguda grave. Acta Gastroenterol Latinoam. 2022;52(2):281-287. https://doi.org/10.52787/agl.v52i2.159
Referencias
- Tokyo guidelines 2018: diagnostic criteria and severity grading of acute cholecystitis. Jhbps. 2018;25(1):41-54.
- Bundy J, et al. Percutaneous cholecystostomy: long-term outcomes in 324 patients. Cardiovasc Intervent Radiol. 2018;41(6):928-34.
- Kozarek RA. Selective cannulation of the cystic duct at time of ERCP. J Clin Gastroenterol. 1984;6:37-40.
- Sobani Z, Ling C, Rustagi T. Endoscopic Transpapillary Gallbladder Drainage for AcuteCholecystitis. Digestive Diseases and Sciences. 2021;66:1425-35.
- Khan MA, Atiq O, Kubiliun N, et al. Eficacy and safety of endoscopic gallbladder drainage in acute cholecystitis: is it better than percutaneous gallbladder drainage? Gastrointest Endosc. 2017;85(1):76-87.
- Mohan BP, Khan SR, Trakroo S, et al. Endoscopic ultrasound-guided gallbladder drainage, transpapillary drainage, or percutaneous drainage in high risk acute cholecystitis patients: a systematic review and comparative meta-analysis. Endoscopy. 2020;52(2):96-106.
- Mutignani M, Iacopini F, Perri V, et al. Endoscopic gallbladder drainage for acute cholecystitis: technical and clinical results. Endoscopy. 2009;41:539-46.
- Kaura K, Bazerbachi F, Sawas T, et al. Surgical outcomes of ERCP-guided transpapillary gallbladder drainage versus percutaneous cholecystostomy as bridging therapies for acute cholecystitis followed by interval cholecystectomy. HPB (Oxford) 2019. Disponible en: https://doi.org/10.1016/j.hpb.2019.10.1530
- Saumoy M, Tyberg A, Brown E, et al. Successful cholecystectomy after endoscopic ultrasound gallbladder drainage compared with percutaneous cholecystostomy, can it be done? J Clin Gastroenterol. 2019;53:231-5.
- Xiaoping S, Yiting L, Ging H, Xuyang Z, Xingjie L, Zhiping W. Endoscopic transpapillary gallbladder drainage for management of acute cholecystitis with coagulopathy.Journal of International Medical Research. 2021;49(3):1-6.
- Hamada T, Yasunaga H, Nakai Y, et al. Severe bleeding after percutaneous transhepatic drainage of the biliary system: effect of antithrombotic agents-analysis of 34 606 cases from a Japanese nationwide administrative database. Radiology. 2015;274:605-13.
- Maruta A, Iwata K, Iwashita T, Mizoguchi K, Kimura M, Takeyama H, Joh T. Factors affecting technical success of endoscopic transpapillary gallbladder drainage for acute cholecystitis. J. Hepato-Biliary-Pancreat. Sci. 2020;27:429-36.
- Thomas R, McCarty KE Hathorn, ANB, Kunal J, Marvin R, Christopher C Thompson. Endoscopic gallbladder drainage for symptomatic gallbladder disease: a cumulative systematic review meta‑analysis. Surgical Endoscopy. 2021;35:4964-85.
- Khan MA, Atiq O, Kubiliun N, Ali B, Kamal F, Nollan R, et al. Efficacy and safety of endoscopic gallbladder drainage in acute cholecystitis: is it better than percutaneous gallbladder drainage? Gastrointest Endosc. 2017;85:76-87.
- Saumoy M, Yang J, Bhatt A, Bucobo J, Chandrasekhara V, Copland A, Krishnan K, Law R, Pannala R, Parsi M, Rahimi M, Trikudanathan G, Trindade A, LichtensteinD. ASGE. Endoscopic therapies for gallbladder drainage. GIE. 2021;94:671-84.
- Sobani ZA, Ling, C, Rustagi T. Endoscopic Ultrasound-Guided Gallbladder Drainage. Dig Dis Sci. 2021;66:2154-61. Disponible en: https://doi.org/10.1007/s10620-020-06520-y
- Lisotti A, Linguerri R, Bacchilega I, et al. EUS-guided gallbladder drainage in high-risk surgical patients with acute cholecystitis-procedure outcomes and evaluation of mortality predictors. Surg Endosc. 2022;36:569-78. Disponible en: https://doi.org/10.1007/s00464-021-08318-z
- Kalva NR, Vanar V, Forcione D, Bechtold ML, Puli SR. Efficacy and Safety of Lumen Apposing Self-Expandable Metal Stents for EUS Guided Cholecystostomy: A Meta-Analysis and Systematic Review. Can J Gastroenterol Hepatol. 2018 Apr 12;2018:7070961. doi: 10.1155/2018/7070961 PMID: 29850458; PMCID: PMC5925026.
Correspondencia: Daniela Caamaño
Correo electrónico: daniela.s.caamanio@hotmail.com
Acta Gastroenterol Latinoam 2022;52(2):281-287
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE



