Ianina Belén Capaldi ID· Florencia Giraudo ID· María Laura Garbi ID· Martín Yantorno ID Nicolás Capurro ID· Damián Ezequiel Moavro ID· Fernando Baldoni ID· Francisco Tufare ID Gustavo Javier Correa ID
Servicio de Gastroenterología, HIGA San Martín de La Plata.
Provincia de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2024;54(3):268-272
Recibido: 09/02/2024 / Aceptado: 10/09/2024 / Publicado online el 30/09/2024 /
https://doi.org/10.52787/agl.v54i3.393
Resumen
La colitis ulcerosa es un tipo de enfermedad inflamatoria intestinal, caracterizada por una inflamación mucosa crónica, que se inicia en el recto y se extiende proximalmente de forma continua. Es considerada una condición de alto riesgo de desarrollar cáncer colorrectal, por lo cual es fundamental la vigilancia endoscópica. Presentamos el caso de un paciente de 80 años con diagnóstico de colitis ulcerosa extensa de 35 años de evolución. En la colonoscopía de vigilancia, se evidencia una lesión de crecimiento lateral, no granular, pseudodeprimida, de 30 mm de diámetro, en la topografía del recto medio. Dadas las características de lesión, se decide una resección mediante la técnica de disección submucosa endoscópica. El procedimiento se realizó sin complicaciones. La disección submucosa endoscópica es una técnica avanzada, que permite la resección completa y en bloque de lesiones con riesgo de invasión submucosa superficial, incluso en aquellas con alta probabilidad de fibrosis submucosa.
Palabras claves. Colitis ulcerosa, disección submucosa endoscópica, fibrosis mucosa.
Endoscopic Submucosal Dissection as a Therapeutic Option for Rectal Lesions in Patients with Ulcerative Colitis
Summary
Ulcerative colitis is a type of inflammatory bowel disease, characterized by chronic mucosal inflammation that begins distally at the level of the rectum and extends proximally continuously. It is considered a high-risk condition for the development of colorectal cancer; therefore, surveillance colonoscopy is mandatory. We present the case of an 80-year-old patient with a diagnosis of extensive ulcerative colitis of 35 years of evolution. In surveillance colonoscopy, a non-granular pseudo-depressed lateral growth lesion measuring 30 mm in diameter, located in the middle rectum. Whence, an endoscopic submucosal dissection was performed to remove the lesion. The procedure was completed without complications. Endoscopic submucosal dissection is an advanced endoscopic technique, which allows complete and bloc resection of lesions at risk of superficial submucosal invasion, even in those with a high probability of submucosal fibrosis.
Keywords. Ulcerative colitis, endoscopic submucosal dissection, mucosal fibrosis.
Abreviaturas
CU: Colitis ulcerosa.
EII: Enfermedad inflamatoria intestinal.
CCR: Cáncer colorrectal.
RME: Resección mucosa endoscópica.
DSE: Disección submucosa endoscópica.
FS: Fibrosis submucosa.
Introducción
La colitis ulcerosa (CU) es un tipo de enfermedad inflamatoria intestinal (EII), caracterizada por una inflamación mucosa crónica que se inicia en el recto, se extiende proximalmente de forma continua y simétrica, y presenta una línea de demarcación respecto a la mucosa no comprometida.1
La CU es considerada una condición con alto riesgo de desarrollar de cáncer colorrectal (CCR), el cual es considerado el resultado final de la secuencia “inflamación crónica-displasia-carcinoma” y está asociado a la extensión y al grado de inflamación de la enfermedad de base. Se estima que el riesgo de desarrollar CCR es del 7 % a los 20 años de la enfermedad, del 7 al 14 % a los 25 años y hasta el 30 % después de los 35 años.2,3 Por este motivo, las distintas guías recomiendan la vigilancia endoscópica de estos pacientes y el tratamiento de la displasia.4,5
Actualmente, la primera colonoscopía de vigilancia de CCR debe realizarse dentro de los 8 años posteriores al inicio de los síntomas. Los controles posteriores se programan según el riesgo estimado de cada paciente.6 (Tabla 1)
Tabla 1. Indicaciones de endoscopía de seguimiento según el riesgo del paciente

La colonoscopía de vigilancia debe realizarse, luego de lograr la curación mucosa, por endoscopistas con experiencia en EII y utilizando técnicas de cromoendoscopía vital.7,8,9 En las lesiones visibles pasibles de tratamiento endoscópico, este podría llevarse a cabo a través de técnicas de resección mucosa endoscópica (RME) o de disección submucosa endoscópica (DSE).7 La DSE, si bien presenta mayor número de complicaciones que la RME, es una opción de tratamiento eficaz que permite la resección en bloque de lesiones de gran tamaño, o que presentan riesgo de invasión submucosa superficial, e incluso de aquellas con alta probabilidad de presentar fibrosis submucosa (FS), que es frecuente observar en los pacientes con CU.3,9 Sin embargo, la DSE en pacientes con EII presenta desafíos significativos debidos, fundamentalmente, a la presencia de fibrosis en las capas mucosa y submucosa, secundaria a la inflamación crónica. La inflamación repetida y la fibrosis de las capas reducen el espacio submucoso, por lo que dificultan el acceso al tercer espacio. Como resultado, la visualización de los planos resulta más compleja y aumenta el riesgo de perforación. Por otro lado, los cambios inflamatorios pueden provocar una demarcación difícil de la lesión y el tejido circundante, y complicar aún más la resección endoscópica.10 Aunque la DSE es una técnica implementada en la actualidad, se requieren estudios a largo plazo para evaluar su eficacia y seguridad en el tratamiento de las lesiones displásicas, en los pacientes con EII.
A continuación, se presenta el caso clínico de un paciente con diagnóstico de CU y con una lesión rectal tratada con la técnica de DSE convencional.
Caso clínico
Se presenta el caso de un paciente de 80 años con diagnóstico de CU extensa, de 35 años de evolución. En la colonoscopía de vigilancia, se evidencian cambios crónicos e importante compromiso cicatrizal con áreas de retracción en la mucosa recto-colónica; en topografía del recto medio, sobre la cara lateral izquierda, se observa una lesión de crecimiento lateral no granular pseudodeprimida (tipo 0-IIa+IIc, según la clasificación de París), de 30 mm de diámetro. Se realiza la semiología endoscópica por medio de cromoendoscopía vital con índigo carmín, que muestra un patrón glandular IIIs, según la clasificación de Kudo y mediante cromoendoscopía digital con NBI, que muestra un patrón vascular tipo II, según la clasificación de Sano.
Dadas las características morfológicas y el riesgo de invasión submucosa superficial, se decide la resección mediante la técnica de DSE. Se ingresa con gastroscopio, con capuchón de mucosectomía y se ubica la lesión en hora 6. Se realiza una marcación de los márgenes de resección con knife (Flush Knife, Fujinon®), con corriente de coagulación suave, a 3 mm de distancia de la lesión. Se eleva la lesión, a través de la inyección submucosa con solución salina e índigo carmín y se registra un signo del lifting positivo.
Se lleva a cabo la técnica de disección submucosa clásica, con incisión circunferencial y posterior disección del plano submucoso; no se observa una capa submucosa azul claro, sino una estructura blanquecina de aspecto similar al músculo, lo cual es un indicador de fibrosis submucosa severa o de grado 2. Se realiza la coagulación de los vasos de mayor calibre con pinza hemostática (Coagrasper, Olympus®) y de los más pequeños con la punta del knife. Se utilizó una fuente electroquirúrgica controlada con microprocesador (ERBE VIO 300®), e insuflación con CO2.
Se logra la resección en bloque aproximadamente en 60 minutos. El procedimiento no presentó complicaciones inmediatas ni tardías. La anatomía patológica informó adenoma con displasia epitelial de alto grado, con márgenes de resección laterales y en profundidad libres de lesión (R0), con un tamaño de 25x20x0,3 mm. Se calculó el área de resección de 392,7 mm2 con una velocidad de disección de 6,54 mm2/min. (Figura 1 y Video 1)
Figura 1. Disección submucosa endoscópica de lesión rectal
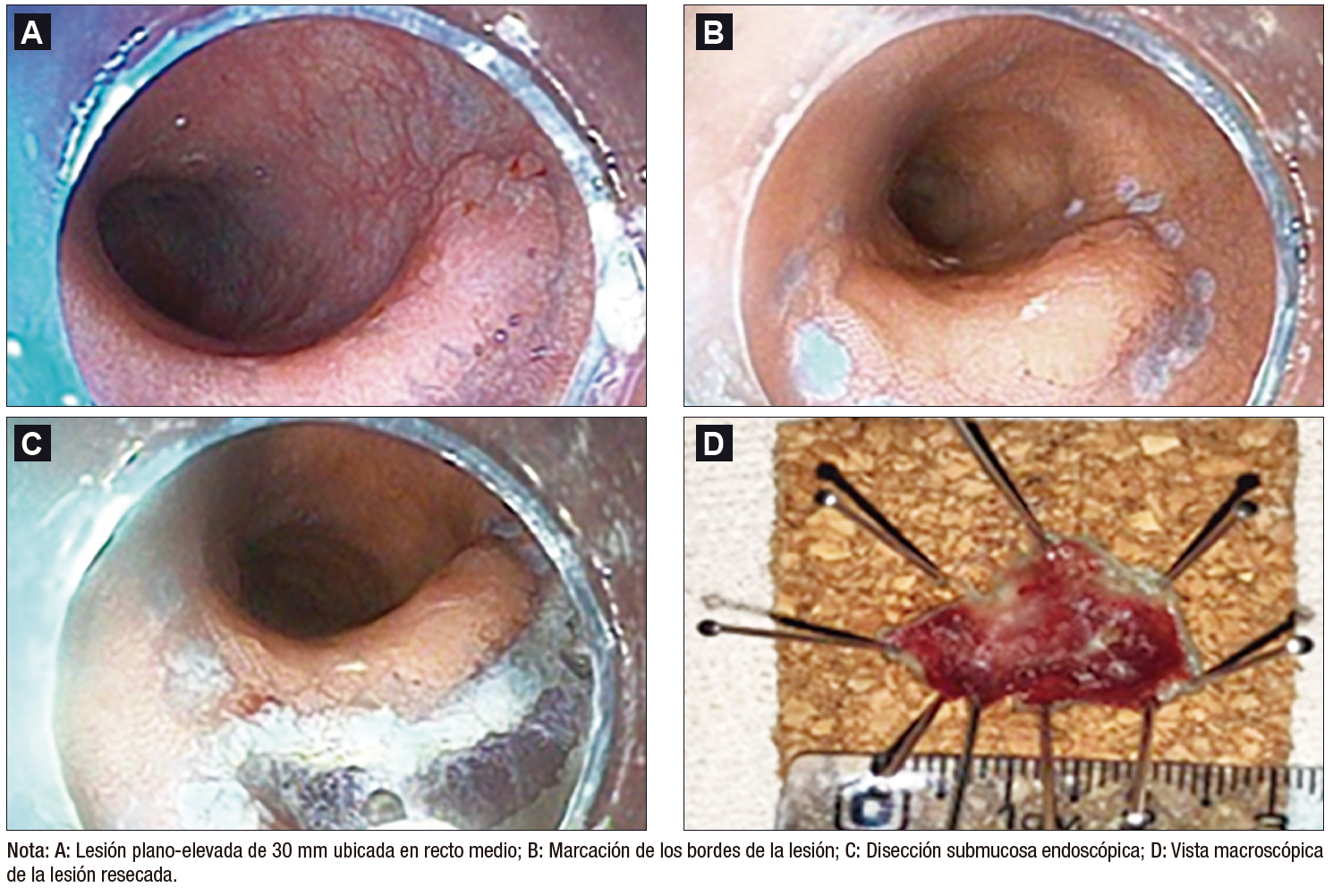
Se realizaron controles endoscópicos a los 6 y 12 meses, y se evaluó el lecho de resección con luz blanca y cromoendoscopía digital; no se encontró recurrencia endoscópica ni lesiones histológicas en las biopsias.
Discusión
La CU es un subtipo de EII que se caracteriza por la inflamación crónica de la mucosa recto-colónica.1 Los pacientes con CU presentan un mayor riesgo de desarrollar CCR en comparación con la población general. Este riesgo está relacionado con la extensión, la duración de la enfermedad, la presencia de colangitis esclerosante primaria y el antecedente familiar de CCR.4
En un estudio poblacional de gran tamaño realizado por Bernstein y col., que incluyó un seguimiento de 19.655 personas/año, se sugirió que los pacientes con CU tienen un riesgo tres veces mayor de desarrollar CCR.11 A su vez, Según Jess T. y col., en un estudio de cohortes poblacionales, se evidenció que la CU incrementa 2,4 veces el riesgo de CCR. Además, identificaron como factores de riesgo asociados, el sexo masculino, la colitis extensa y el diagnóstico a edad temprana.12
Distintos trabajos demuestran el impacto oncogénico de la inflamación colónica crónica en el desarrollo de CCR, de esta manera, la secuencia “inflamación-displasia-adenoma” estaría involucrada en el desarrollo de CCR en los pacientes con EII.13 Por lo tanto, la videocolonoscopía de vigilancia de alta definición con cromoendoscopía se recomienda para la detección temprana de la displasia.5
En relación con la displasia, ésta puede ser clasificada en dos grandes grupos: la displasia visible, que está asociada a una lesión visible por endoscopía, y la displasia invisible, diagnosticada mediante biopsias tomadas al azar, sin lesión endoscópica evidente.5 Actualmente, el 90% de las displasias detectadas corresponden a displasias visibles.14
En relación al manejo endoscópico, se recomienda la resección en bloque de las lesiones visibles por endoscopía, independientemente del grado de displasia, siempre que se trate de lesiones únicas, bien delimitadas, y sin signos sugestivos de invasión (depresión, ulceración, contornos irregulares, apariencia de masa o signo de no-lifting).14
En pacientes con EII, la actividad inflamatoria crónica puede causar fibrosis mucosa y submucosa significativa, que impediría la resección mediante técnicas de RME convencional. La utilización de la DSE, además de permitir una resección en bloque, posibilita una disección vertical adecuada del plano submucoso, aumenta las posibilidades de una resección potencialmente curativa de estas lesiones fibróticas y facilita un diagnóstico histopatológico más preciso, con la evaluación adecuada de los márgenes laterales y verticales.
La técnica de DSE es una valiosa herramienta para el tratamiento de las lesiones displásicas en los pacientes con EII, ya que permite la resección en bloque de lesiones de gran tamaño, incluso de aquellas con presencia de FS secundaria a la actividad inflamatoria de la enfermedad de base.2,9,15
En un estudio en 2016, Eun Kyoung Kim y col., analizaron de forma retrospectiva 158 pacientes con tumores colorrectales, los cuales habían sido tratados con DSE. En dicho trabajo, se determinó el grado de FS durante la inyección submucosa. Se clasificó la FS en 3 grados: sin fibrosis (F0), con una capa submucosa de aspecto azul transparente; fibrosis leve (F1), con presencia de una red blanquecina en la capa submucosa azul y fibrosis severa (F2), en la que se observa una estructura blanca, símil músculo, sin capa submucosa azul.16
Otro estudio, publicado en 2018, examinó los predictores endoscópicos de FS severa y su impacto. Este trabajo concluyó que la FS severa estaba asociada a una resección no curativa y a un tiempo mayor de procedimiento; los predictores de la FS serían el tamaño de la lesión (> 40 mm), la morfología (lesiones protruidas) y la presencia de convergencia de pliegues.17
Por un lado, en relación con los resultados de la DSE en este grupo de pacientes, se pueden destacar una serie de casos y una revisión sistemática con análisis de datos agrupados, publicada en el 2021, que mostró una tasa de éxito técnico del 88% y una tasa de efectos adversos (manejables endoscópicamente) menor al 10%.3
Por otro lado, Qi-Shan Zeng y col., en 2022, efectuaron una revisión sistemática y metaanálisis, en el que se evaluó la seguridad y eficacia de la DSE en la displasia en pacientes con CU. En este estudio se describió una tasa de recurrencia local del 5% y una tasa de tumores metacrónicos del 6%.9 Destacaron así, tanto la efectividad de esta técnica de resección como la necesidad de una vigilancia endoscópica continua posterior.
Conclusión
El avance en los programas de vigilancia de displasia en la EII ha contribuido a disminuir la incidencia de CCR y la necesidad de colectomía. La DSE es una técnica endoscópica avanzada, que permite la resección completa y en bloque de lesiones con riesgo de invasión submucosa superficial, incluso en aquellas con alta probabilidad de fibrosis submucosa. Asimismo, el entrenamiento continuo y el desarrollo de la técnica en otros segmentos colónicos permitirá la resolución endoscópica de lesiones rectales en una mayor cantidad de pacientes.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos, las figuras y los videos presentes en el manuscrito son originales y se realizaron en sus instituciones de pertenencia.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflictos de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2024 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Capaldi I B, Giraudo F, María Laura Garbi M L y col. Disección submucosa endoscópica como opción terapéutica de una lesión rectal en un paciente con colitis ulcerosa. Acta Gastroenterol Latinoam. 2024;54(3):268-272. https://doi.org/10.52787/agl.v54i3.393
Referencias
- Lamb CA., Kennedy NA., et al. British Society of Gastroenterology consensus guidelines on the management of inflammatory bowel disease in adults. Gut. 2019 Dec; 68(Suppl 3): S1-S106.
- Kinoshita S., Nishizawa T., et al. Endoscopic Submucosal Dissection in Patients with Ulcerative Colitis. Digestion. 2019; 99(1): 27-32.
- Manta R., Zullo A., et al. Endoscopic Submucosal Dissection for Visible Dysplasia Treatment in Ulcerative Colitis Patients: Cases Series and Systematic Review of Literature. J Crohn’s and Colitis. 2021 Jan 13; 15(1):165-168.
- Annese V., Beaugerie L., et al. European Evidence-based Consensus: Inflammatory Bowel Disease and Malignancies. J Crohn’s and Colitis. 2015 Nov; 9(11): 945-65.
- Laine L., Kaltenbach T., et al. SCENIC international consensus statement on surveillance and management of dysplasia in inflammatory bowel disease. Gastroenterology. 2015 Mar; 148(3): 639-651.e28.
- Murthy S., Feuerstein, J., et al. AGA Clinical Practice Update on Endoscopic Surveillance and Management of Colorectal Dysplasia in Inflammatory Bowel Diseases: Expert Review. Gastroenterology. 2021; 161: 1043-1051.
- Suzuki N., Toyonaga T., et al. Endoscopic submucosal dissection of colitis-related dysplasia. Endoscopy. 2017 Dec; 49(12): 1237-1242.
- Soetikno R., East J., et al. Endoscopic submucosal dissection for nonpolypoid colorectal dysplasia in patients with inflammatory bowel disease: in medias res. Gastrointest Endosc. 2018 Apr; 87(4): 1085-1094.
- Zeng QS., Zhao ZJ., et al. Efficacy and Safety of Endoscopic Submucosal Dissection for Dysplasia in Ulcerative Colitis Patients: A Systematic Review and Meta-Analysis. Gastroenterol Res Pract. 2022 Jan; 25:9556161.
- Maselli R., de Sire R., et al. Advancements in Endoscopic Resection for Colitis-Associated Colorectal Neoplasia in Inflammatory Bowel Disease: Turning Visible into Resectable. Diagnostics. 2024; 14(1), 9.
- Bernstein C., Blanchard J., et al. Cancer risk in patients with inflammatory bowel disease: a population-based study. Cancer. 2001; 91: 854-62.
- Jess T, Rungoe C, et al. Risk of colorectal cancer in patients with ulcerative colitis: a meta-analysis of population-based cohort studies. Clin Gastroenterol Hepatol. 2012; 10:639-45.
- Mescoli C., Albertoni L., et al. Dysplasia in inflammatory bowel diseases. Dig Liver Dis. 2013 Mar; 45(3): 186-94.
- Shah SC., Itzkowitz SH., et al. Management of Inflammatory Bowel Disease-Associated Dysplasia in the Modern Era. Gastrointest Endosc Clin N Am. 2019 Jul; 29(3): 531-548.
- Kinoshita S., Uraoka T., et al. The role of colorectal endoscopic submucosal dissection in patients with ulcerative colitis. Gastrointest Endosc. 2018 Apr; 87(4):1079-1084.
- Kim EK., Han DS., et al. The submucosal fibrosis: what does it mean for colorectal endoscopic submucosal dissection? Intest Res. 2016 Oct; 14(4): 358-364.
- Kaosombatwattana U., Yamamura T., et al. Preoperative endoscopic predictors of severe submucosal fibrosis in colorectal tumors undergoing endoscopic submucosal dissection. Endosc Int Open. 2019 Apr; 7(4): E421–E430.
Correspondencia: Ianina Belén Capaldi
Correo electrónico: ianinacapaldi@gmail.com
Acta Gastroenterol Latinoam 2024;54(3):268-272
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE


