Eduardo Fassio,1 Guillermo Mazzolini2 y la Asociación Argentina para el Estudio de las Enfermedades del Hígado
1 Jefe de la Sección Hígado, Vías Biliares y Páncreas, Hospital Nacional Profesor Alejandro Posadas, El Palomar. Buenos Aires, Argentina.
2 Miembro del Staff del Servicio de Hepatología y Trasplante Hepático, Hospital Universitario Austral, Pilar. Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2016;46: 350-374
Recibido: 03/07/2016 / Aprobado: 17/08/2016 / Publicado en www.actagastro.org el 01/01/2017
Participantes y responsables de los temas en el Consenso Argentino de Hepatocarcinoma 2015:
Gabriel Aballay, Raúl Adrover, José Allevato, Daniel Álvarez, Beatriz Ameigeiras, Margarita Anders, Oscar Andriani, Victoria Ardiles, Mario Arzeno, Alejandra Avagnina, Juan C Bandi, Fernando Barreyro, Fernando Bessone, Andrea Bosaleh, Gustavo Braslavsky, Andrés Bruno, Fernando Cairo, Cristina Cañero Velasco, Marcela Carballido, Rodolfo Cattaneo, Nora Cejas, Sara Chao, Daniel Cocozzella, Luis Colombato, Ariel Cubilla, Jorge Daruich, Valeria Descalzi, Melisa Dirchwolf, Claudio Estepo, Hugo Fainboim, José L Fernández, Nora Fernández, Sebastián Ferretti, Sebastián Figueroa, Bernardo Frider, Adrián Gadano, Omar Galdame, Adriana García, Daniel García, Mercedes García Lombardi, Ricardo García Mónaco, Carlos Garrocho Machado, Esteban González Ballerga, Fernando Gruz, Gisela Gualano, Carlos Guma, Shigeru Kozima, Diana Krasniansky, Graciela Landeira, Diana Levi, Oscar Mandó, Estela Manero, Ricardo Mastai, Lucas Mc Cormack, Manuel Mendizábal, Silvia Mengarelli, Carlos Míguez, Eduardo Mullen, Alberto Muñoz, Federico Orozco, Guillermo Ortiz, Florencia Perazzo, Roberto Pérez Ravier, Juan P Perotti, Federico Piñero, Gustavo Podestá, Daniel Poncino, Sebastián Raffa, María Virginia Reggiardo, Ezequiel Ridruejo, Gustavo Romero, Andrés Ruf, Gabriela Ruffillo, Pablo Sánchez, Teresa Schroder, Marcelo Silva, María Ester Sirotinsky, Juan A Sordá, Juan C Spina, Francisco Suárez Anzorena, Hugo Tanno, Guillermo Tsariktsian, Carlos Vigliano, Alejandra Villamil, Mariano Volpacchio.
Abreviaturas
HCC: hepatocarcinoma.
HCV: virus de la hepatitis C.
AAEEH: Asociación Argentina para el Estudio de las Enfermedades del Hígado.
HBV: virus de la hepatitis B.
EHNA: esteatohepatitis no alcohólica.
HIV: virus de la inmunodeficiencia humana.
HDV: virus de la hepatitis D.
OH: alcohol.
HGNA: hígado graso no alcohólico.
CBP: cirrosis biliar primaria.
CEP: colangitis esclerosante primaria.
AFP: alfa-feto proteína.
US: ultrasonografía.
ECR: ensayo controlado randomizado.
TC: tomografía computarizada.
RM: resonancia magnética.
PBH: punción biopsia hepática.
AASLD: American Association for the Study of Liver Diseases.
EASL: European Association for the Study of the Liver.
LIRADS: Liver Imaging Reporting and Data System.
EUA: Estados Unidos de Norteamérica.
MELD: model for end-stage liver disease.
HSP70: heat shock protein 70.
BCLC: Barcelona Clinic Liver Cancer.
ECOG: Eastern Cooperative Oncology Group.
TACE: transarterial chemoembolization.
EORTC: European Organization for Research and Treatment of Cancer.
GRETCH: Groupe d’Etude et de Traitement du Carcinome Hépatocellulaire.
CLIP: Cancer of the Liver Italian Program.
CUPI: Chinese University Prognostic Index.
JIS: Japan Integrated Staging.
ARF: ablación por radiofrecuencia.
IPE: inyección percutánea de etanol.
RQ: resección quirúrgica.
GPVH: gradiente de presiones de la vena suprahepática.
TH: trasplante hepático.
UCSF: University of California at San Francisco.
mRECIST: Modified Response Evaluation Criteria in Solid Tumors.
DEB: drug-eluting beads.
TARE: transarterial radioembolization.
VEGF: vascular endothelium growth factor.
PDGF: platelet-derived growth factor.
SHARP: Sorafenib HCC Assessment Randomized Protocol.
El hepatocarcinoma (HCC) es la tercera causa de muerte relacionada al cáncer en el mundo. Lamentablemente, la incidencia y la mortalidad de esta enfermedad se han incrementado en los últimos años a nivel mundial y, de acuerdo con estimaciones epidemiológicas, se espera que continúe en aumento debido al crecimiento poblacional, a la epidemia de obesidad y su consecuencia, la enfermedad hepática grasa no alcohólica; y al aumento en la incidencia de cirrosis y sus complicaciones en la gran cohorte de pacientes infectada por virus de la hepatitis C (HCV) hace 3-4 décadas. Además, debido a la dificultad en el acceso poblacional global a las nuevas y más costosas terapias antivirales, el beneficio clínico de los tratamientos para hepatitis B y C no se trasladan aún en una reducción de la incidencia del HCC.
En la Argentina no existen datos firmes acerca de la incidencia del HCC, aplicabilidad de los tratamientos y sobrevida obtenida tras su aplicación. A pesar del avance en el conocimiento de aspectos moleculares del HCC, de la accesibilidad a las herramientas para el diagnóstico temprano, del refinamiento de la técnica quirúrgica y del trasplante hepático, poco es lo que se ha podido hacer en cuanto al impacto sobre la mortalidad global de este tumor, por lo que sigue siendo un problema de salud pública en todo el mundo. En los últimos años se ha avanzado en forma sustancial en varios aspectos de esta patología como es la estadificación de los pacientes, el mejor entendimiento de la fisiopatología de la hepatocarcinogénesis y el desarrollo de nuevos procedimientos de diagnóstico y tratamiento. Otros aspectos que requieren aún mucha mejora e investigación son incrementar el número de pacientes con diagnóstico en estadios tempranos, la caracterización del perfil biológico o molecular del HCC, la disponibilidad de tratamientos más eficaces para pacientes con enfermedad avanzada, entre otros.
Este particular escenario motivó a la Asociación Argentina para el Estudio de las Enfermedades del Hígado (AAEEH) a convocar por primera vez el Consenso Argentino de Hepatocarcinoma, con el objetivo de estimular la discusión entre los expertos, aunar los conocimientos internacionales con la experiencia de nuestro medio, consensuar conductas a seguir en la vigilancia de los pacientes en riesgo, en el diagnóstico y en el tratamiento. Los coordinadores generales invitaron a reconocidos profesionales de nuestro país (hepatólogos de adultos y pediatras, radiólogos, hepatopatólogos, cirujanos hepáticos y de trasplante) a revisar (en ternas) diferentes aspectos del problema HCC, divididos en 4 módulos: epidemiología; screening y vigilancia; diagnóstico; estadificación y tratamiento; con el objetivo de responder a preguntas específicas como: ¿cuál es la incidencia del HCC en Argentina y cuáles son sus causas?, ¿qué pacientes deben ser involucrados en programas de vigilancia para HCC?, ¿cuáles son los mejores test de screening y cuál es el mejor programa de vigilancia?, ¿cuál es el mejor algoritmo diagnóstico en cirróticos con detección de un nódulo hepático?, ¿cuál es el mejor sistema de estadificación?, y ¿cuáles son las mejores opciones de tratamiento en los diversos estadíos del HCC? Los grupos asignados expusieron sus propuestas en una reunión abierta a la comunidad científica el día 16 de octubre de 2015, con un espacio de discusión abierta a todos los presentes. Durante la mañana del día 17 de octubre de 2015 los miembros del Consenso redactaron conclusiones preliminares que luego fueron leídas por la tarde en nueva reunión abierta a la comunidad científica, y discutidas y corregidas de acuerdo al Consenso entre los presentes. Este documento final plantea guías y recomendaciones para el manejo de los pacientes con HCC, con el objetivo de apoyar a los médicos, como así también a pacientes y otros actores (financiadores del sistema de obras sociales, instituciones públicas y privadas) que participan en el proceso de toma de decisiones, basándose en diferentes niveles de calidad de evidencia y fuerza de recomendación de acuerdo al sistema propuesto por el GRADE Working Group.1
Epidemiología
En el mundo
El hepatocarcinoma (HCC) es el 7º cáncer más frecuente a nivel mundial (5,6% del total de casos)2 pero asciende a la tercera posición como causa de muerte por cáncer,3 luego de los cánceres de pulmón y de mama. Entre los hombres, el HCC es la segunda causa de muerte por cáncer. Esto es consecuencia de que el pronóstico global continúa siendo muy pobre, con una relación de muertes/casos nuevos de aproximadamente 0,9, en relación a, entre otros factores, una elevada proporción de diagnósticos en estadíos avanzados y en países en vías de desarrollo. La obtención de información confiable sobre la incidencia del HCC a nivel mundial es muy dificultosa, ya que cerca de 3/4 de la población mundial no está cubierta por registros nacionales; además, hay problemas en la codificación de la enfermedad (por ejemplo, en algunas regiones no se distinguen claramente tumores primarios de secundarios hepáticos).
El mayor factor de riesgo para la ocurrencia de HCC es la presencia de cirrosis de cualquier etiología. Sin embargo, en una minoría de los casos puede desarrollarse en un hígado no cirrótico. Por ejemplo, el 15-20% de los casos de HCC en pacientes con infección crónica por el virus de la hepatitis B (HBV) ocurren en fases no cirróticas. A nivel mundial, las etiologías dominantes del HCC son la hepatitis crónica B (53%), la hepatitis crónica C (25%) y la cirrosis alcohólica.4 Se estima que un tercio de los pacientes cirróticos desarrollará HCC (con una incidencia anual que oscila de 1 a 8%), predominantemente en el sexo masculino (2:1 a 4:1).
La distribución e incidencia mundial del HCC es heterogénea. El 85% de los casos se presentan en Asia, África Subsahariana y Melanesia debido a la alta prevalencia de portadores crónicos del HBV5 y a la exposición en la dieta a elevadas concentraciones de aflatoxina B1 (una micotoxina derivada de los hongos Aspergillus flavus y Aspergillus parasiticus, que contaminan los utensilios de cocina), que podría actuar como un co-factor en el desarrollo de HCC.6 En cambio, en los países desarrollados de Occidente, la incidencia de HCC es baja (excepto en algunos países de la Europa mediterránea donde es intermedia) y su ocurrencia está asociada principalmente a la cirrosis por HCV, por alcohol y esteatohepatitis no alcohólica (EHNA).7-12 Sin embargo, recientemente se ha registrado en países occidentales un aumento significativo de la incidencia,13-17 en buena proporción asociado a casos de HCV,18 en relación con un fenómeno de cohortes (aumento en la incidencia de cirrosis y sus complicaciones entre la gran masa de pacientes infectados hace 3-4 décadas).
Argentina y Latinoamérica
La información acerca de la prevalencia, la incidencia y los factores de riesgo para el HCC en Latinoamérica es limitada. Se considera que la incidencia es baja y se relaciona con una escasa prevalencia de portadores crónicos del HBV en la región. La mayoría de los casos se originan por hepatitis crónica C o cirrosis alcohólica,19 excepto en Perú y en la cuenca amazónica de Brasil, donde aumenta la prevalencia del HBV.
En nuestro país, el HCC es diagnosticado casi exclusivamente en cirróticos (93%). La hepatitis crónica C y la cirrosis alcohólica son las 2 etiologías principales y representan el 76% de los casos.20 Habitualmente, la edad de presentación es entre los 60 y 70 años, siendo 2,6 veces más frecuente en varones.20 La tasa de incidencia cruda de cáncer hepático primario (ambos sexos) fue de 4.6/100.000 habitantes en el año 2012 de acuerdo al programa GLOBOCAN de la International Agency for the Research on Cancer de la Organización Mundial de la Salud,21 pero no existen datos sobre si se están produciendo cambios en la incidencia de HCC en nuestro país.
Hepatocarcinogénesis y factores de riesgo en el HCC por HBV
El mecanismo oncogénico del HBV se encuentra asociado a dos vías: indirecta y directa. La primera está relacionada con la presencia continua o recurrente de fases de necroinflamación hepática que promueve la fibrosis/ cirrosis y la hepatocarcinogénesis. La vía directa, que puede generar HCC en ausencia de cirrosis, está relacionada a la capacidad del HBV de integrarse al genoma del huésped permitiendo la persistencia viral, la inducción de alteraciones genéticas y la producción de proteínas como la X y la pre-S-S truncadas, todas con poder oncogénico.22 Los factores de riesgo para el desarrollo del HCC se relacionan al huésped (cirrosis,23 edad mayor a 40 años, sexo masculino, síndrome metabólico, alcoholismo crónico, historia familiar de HCC y la presencia de mutaciones genéticas) y al virus [carga viral,24 cuantificación del HBsAg, presencia del HBeAg,25 genotipo C26 y coinfecciones, ya sea con el virus de inmunodeficiencia humana (HIV),27 virus HDV o HCV].
En Argentina, la hepatitis crónica B está presente en 14% de los pacientes con HCC.20
Hepatocarcinogénesis y factores de riesgo en HCC por HCV
La acción carcinogenética del HCV se produciría a través de la acción conjunta de mecanismos directos (factores virales) e indirectos (respuesta necroinflamatoria y fibrosis). Algunas de las proteínas del HCV actúan directa o indirectamente sobre el genoma del huésped donde generan inestabilidad genética con activación de mutaciones oncogénicas, inactivación de genes supresores de tumores y desrregulación de las vías de transmisión de señales. Las alteraciones genéticas comenzarían con el proceso de necroinflamación crónica. Una vez instalada la cirrosis, se producen alteraciones fenotípicas de los hepatocitos que originan displasia y finalmente HCC.
En la hepatitis crónica C, algunas variables que aumentan el riesgo de HCC son la presencia de cirrosis,28 la primoinfección en mayores de 50 años, el género masculino, signos de hipertensión portal (plaquetopenia o várices esofágicas),29, 30 el alcoholismo crónico31 y la coinfección con HBV.32,33 Es discutido si la coinfección con HIV influencia el riesgo de HCC entre los cirróticos por HCV; en un estudio prospectivo de nuestro país no se demostraron diferencias significativas al comparar cohortes de coinfectados y monoinfectados.34 Entre los factores virológicos, la infección por genotipo 1b fue asociada a mayor riesgo de HCC en comparación con todos los otros, de acuerdo a un meta-análisis que incluyó 21 estudios previos;35 pero, en contraste, en una muestra de más de 110.000 veteranos con hepatitis C de EUA, el genotipo 3 se asoció a riesgo aumentado de cirrosis y HCC.36
Factores que han sido asociados a una disminución del riesgo de HCC en pacientes con hepatitis C son la erradicación viral luego del tratamiento antiviral37 (aunque el HCC aún puede ocurrir en pacientes con respuesta viral sostenida), el consumo de café38 y el uso de estatinas.39
Hepatocarcinogénesis y factores de riesgo en HCC por alcohol (OH)
La presencia de cirrosis es el principal factor de riesgo para el desarrollo de HCC en consumidores de OH, pero existe un 14 a 19% de los consumidores excesivos que lo presentan sin tenerla.
La incidencia anual de HCC en bebedores excesivos es de 0,01%, mientras que en cirrosis alcohólica oscila entre 0,6 a 2,0%. En un estudio de nuestro medio, la incidencia anual en cirrosis alcohólica compensada fue de 1,8%.40 Los factores de riesgo asociados a mayor incidencia de HCC entre alcoholistas crónicos, además de la presencia de cirrosis, son la edad, el sexo masculino, el nivel y el tiempo de consumo y el tabaquismo.41-43 Además, la presencia de infección por HBV y/o HCV, obesidad, diabetes y la hemocromatosis también incrementan significativamente el riesgo.42, 44, 45 En pacientes con cirrosis alcohólica que ingresan en abstinencia, el riesgo de HCC disminuye después de los primeros 5 años.
Los mecanismos de carcinogénesis están relacionados con el metabolismo del OH, siendo los más importantes el stress oxidativo y la cirrosis. El acetaldehído es conocido como un importante factor causal en neoplasias extrahepáticas, pero en el hígado tiene menos significancia como consecuencia de su efectivo sistema de metabolización, salvo que exista un consumo excesivo o alteraciones genéticas de la aldehído deshidrogenasa o la alcohol deshidrogenasa. Otros mecanismos implicados son la depleción del ácido retinoico, la deficiencia de metilación del ADN, la presencia de ciertos miRNAs y la genotoxicidad.
HCC por hígado graso no alcohólico (HGNA)
Existe amplia evidencia de la asociación de obesidad, diabetes y síndrome metabólico con HCC,47, 48 presumiblemente a través de la secuencia HGNA → esteatohepatitis no alcohólica → fibrosis avanzada/cirrosis.
La exacta prevalencia de HCC en pacientes con HGNA es desconocida, heterogénea en cuanto a las áreas geográficas y probablemente sea baja; pero, dada la tan elevada presencia de esta entidad en la población general, es esperable que se transforme en una de las causas más frecuentes en el futuro cercano.48, 49 La incidencia de HCC en cirrosis por HGNA ha sido comparada con la de cirróticos por HCV en varios estudios.50-52 Generalmente, se ha observado una incidencia levemente menor en cirróticos por HGNA, aproximadamente de 2,6% por año.51
En las series publicadas de HCC de Argentina y de Latinoamérica, la etiología HGNA/cirrosis criptogénica estuvo presente en 10-15% de los casos.19, 20
Varios estudios han propuesto que el HCC puede desarrollarse en pacientes con HGNA en ausencia de fibrosis avanzada o cirrosis,53-56 pero no sería costo-efectivo en la actualidad incluir a todos los individuos con esta entidad en programas de vigilancia, ya que el riesgo de HCC está significativamente aumentado en el estadío de cirrosis. Por otra parte, los HCCs asociados a HGNA pueden tener peor pronóstico, ya que suelen presentarse en pacientes de mayor edad, ser de mayor tamaño y es menos frecuente que sean detectados a través de programas de vigilancia cuando se los compara con los tumores relacionados a otras etiologías;48, 49, 56 quizás debido a una menor conciencia de parte de los médicos sobre el potencial que tiene la enfermedad de causar morbi-mortalidad hepática.
Incidencia de HCC y factores de riesgo en hepatopatías autoinmunes
En la hepatitis autoinmune, los factores que incrementan el riesgo de HCC son la presencia de cirrosis al momento del diagnóstico y el sexo masculino.57 La tasa de incidencia de HCC en el estadío de cirrosis es de 1,1% anual.58
Una revisión sistemática y metaanálisis han demostrado que los pacientes con cirrosis biliar primaria (CBP) tienen un riesgo significativamente mayor de cáncer en forma global (RR agrupado 1,55; IC95%: 1,28-1,83) y de HCC (RR agrupado 18,8; IC95%: 10,8-26,8) en comparación con la población control.59 Estudios recientes mostraron que la incidencia es significativamente mayor en hombres que en mujeres y que éstos pueden desarrollar HCC en cualquier estadio de CBP.60 Sin embargo, el estadío histológico avanzado es un factor de riesgo independiente para ocurrencia de HCC en mujeres con CBP.60, 61
Los pacientes con colangitis esclerosante primaria (CEP) tienen riesgo incrementado para desarrollar tumores hepatobiliares, cáncer de páncreas y colorrectal. La incidencia de HCC en pacientes con CEP y estadío de cirrosis no es bien conocida, pero, dado que existe riesgo aumentado de colangiocarcinoma y, en segundo lugar, de HCC, está justificado implementar estrategias de vigilancia en estos pacientes.
Profilaxis primaria y secundaria del hepatocarcinoma
La prevención del HCC debe estar dirigida a evitar la injuria hepática crónica y la progresión a cirrosis. Uno de los principales objetivos es lograr el cumplimiento de la vacunación de hepatitis B, de acceso libre y gratuito e incluida en el calendario de vacunación del adulto, para toda la población. Otros, son reducir el riesgo de ocurrencia de HCC identificando precozmente y tratando con terapia antiviral efectiva a todos los casos de hepatitis crónicas B y C; instaurar políticas sanitarias y educacionales en la población para evitar el contagio de las hepatitis B y C, y que apunten a la disminución del consumo de alcohol y a revertir o atenuar la epidemia de obesidad, insulino resistencia y diabetes.
Hepatocarcinoma en pediatría
El espectro de las enfermedades hepáticas que predisponen al HCC en niños es diferente al de los adultos. El HCC es el tumor hepático más frecuente en niños de alrededor de 10 años de edad (65%).
Los factores de riesgo para el desarrollo del HCC son la presencia de cirrosis; las enfermedades metabólicas con o sin cirrosis que afectan el hígado (entre ellas, las más estudiadas son el déficit de alfa-1-antitripsina y la tirosinemia); y entre las causas virales, la infección crónica por HBV. El screening del HCC en pediatría debe realizarse en pacientes cirróticos y en no cirróticos con enfermedades metabólicas con ecografía y alfa-feto proteína (AFP) cada 6 meses. Predomina el sexo masculino. En el tiempo del diagnóstico, la AFP está elevada en 70% de los pacientes; 30% de ellos pueden tener metástasis (pulmón, cerebro, médula ósea, riñón) y 20% compromiso vascular. Histológicamente, 75% de los HCCs son clasificados como epiteliales. El tipo fibrolamelar afecta a adolescentes y adultos jóvenes en hígados no cirróticos.
Recomendaciones
- La información sobre epidemiología del HCC en Argentina es limitada. Existen datos sobre la prevalencia relativa de las diferentes etiologías: cirrosis por HCV y por alcohol son las más frecuentes, seguidas a cierta distancia por HGNA/cirrosis criptogénica y HBV (calidad de la evidencia: baja).
- No se han efectuado estudios evaluando la incidencia del HCC en las diferentes hepatopatías crónicas en Argentina ni analizando si se están produciendo cambios en la misma. Se recomienda la organización de un registro nacional de casos de HCC con la participación de la AAEEH y del Instituto Nacional del Cáncer con el objetivo de contribuir a mejorar el conocimiento epidemiológico en nuestro medio, y con ello, la planificación del diagnóstico y tratamiento.
Screening y vigilancia
Un test de screening o cribaje es un estudio diagnóstico que se aplica en un paciente que está en riesgo de desarrollar una enfermedad determinada, pero en quien no existe razón alguna para sospechar que la tiene, ya que se encuentra asintomático. Vigilancia (surveillance) es la aplicación repetida, a intervalos bien sistematizados, de los test de screening.
El HCC es un tumor que muestra todas las condiciones que una enfermedad maligna debe tener para que un programa de vigilancia sea costo-efectivo:62 es un grave problema de Salud Pública, con elevada mortalidad; la población en riesgo está claramente identificada (pacientes con cirrosis); se dispone de un test de screening no invasivo, aceptable por los pacientes, con buena sensibilidad y especificidad y a un costo razonable, como es la ultrasonografía (US); existen buenos procedimientos para confirmar el diagnóstico (tomografía computarizada multifásica y/o resonancia nuclear magnética dinámica) y tratamientos efectivos (trasplante, resección, ablación) que pueden mejorar la sobrevida de la enfermedad en estadio temprano.
El objetivo de un programa de vigilancia es la detección del HCC en un estadío temprano, etapa en la que se podría aplicar un tratamiento con intención curativa, y así lograr una disminución significativa de la mortalidad. Un ensayo controlado randomizado (ECR) efectuado en China hace muchos años demostró, al estudiar una muestra de más de 18.000 individuos portadores del HBV, que aquellos que habían sido asignados al grupo screening tuvieron una reducción significativa, de 37%, en la mortalidad por HCC en comparación con el grupo control.63 En Occidente, donde un ECR evaluando la eficacia de la vigilancia para HCC no podrá ser efectuado porque los médicos especialistas confían en esta estrategia y los pacientes rehusarían ingresar en el estudio luego de conocer la información pertinente,64 varios estudios de cohorte han demostrado una sobrevida significativamente mayor en pacientes con HCC detectados por vigilancia que en los que tuvieron diagnóstico sintomático.65-68
Para mejorar la efectividad del programa de vigilancia se debe involucrar en el mismo a pacientes que tengan un riesgo reconocido (por encima de un umbral de incidencia de HCC predeterminado, de aproximadamente 1,5% anual), que estén en condición de recibir el tratamiento en caso de diagnóstico, elegir el/los mejor/es test de screening, realizarlos en los intervalos adecuados, tener un eficaz algoritmo de confirmación en caso de cribaje positivo y acceso a los tratamientos curativos.
Como resultado de la discusión durante el Consenso Argentino de HCC 2015, se concluyó que los candidatos a ser incluidos en programas de vigilancia para HCC deberían ser:
- Pacientes con cirrosis de cualquier etiologí
- Pacientes con hepatitis crónica C y fibrosis severa (estadio F3 de la clasificación de METAVIR).
- Pacientes portadores crónicos del HBV, independientemente del grado de fibrosis.
Los pacientes con hepatitis B o C en estadio de fibrosis severa/cirrosis que hayan alcanzado un estado de supresión viral mantenida o sostenida (hepatitis B) o erradicación viral (hepatitis C) con los tratamientos antivirales deben continuar con el esquema de vigilancia para HCC, ya que el riesgo de desarrollo del mismo disminuye en forma significativa pero no desaparece.
El método de imágenes que ha sido más investigado como test de screening para la detección del HCC es la ultrasonografía (US) abdominal. Presenta una precisión aceptable con una sensibilidad que oscila entre 60 y 89% y una especificidad mayor de 90%. Es un estudio no invasivo, ampliamente aceptado por los pacientes, de costo relativamente bajo y de gran accesibilidad. Un metaanálisis reciente incluyó 13 estudios que investigaron la utilidad de la US (con o sin AFP) en la vigilancia para HCC en cirróticos. Concluyó que la US fue capaz de detectar la mayoría de los HCCs antes de que se presentaran clínicamente con una sensibilidad agrupada de 94% (IC95%: 83-98) y una especificidad agrupada de 94% (IC95%: 89-97).69 Si el análisis se restringe a la detección de tumores tempranos dentro de los criterios de Milán, la sensibilidad agrupada disminuye a 63% (IC95%: 49-76%). Es importante enfatizar que la sensibilidad fue mayor en estudios donde el intervalo entre US fue ≤ 6 meses (70,1%) que en los que tuvieron intervalo > 6 meses (50,1%). Se analizó además la utilidad de agregar el estudio de AFP en conjunción con la US. La asociación de ambos estudios mostró una sensibilidad agrupada en la detección de HCC temprano de 69% (IC95%: 53-81%) (diferencia no significativa), concluyéndose que no había beneficio adicional en sumar el dosaje de AFP.69
El rango observado en la sensibilidad de la US en la detección del HCC (tanto en los estudios publicados como en la “vida real”) estaría relacionado a que el método es dependiente del operador y del equipamiento. El hígado cirrótico presenta habitualmente una ecoestructura heterogénea como resultado de las bandas de fibrosis y la existencia de nódulos de regeneración, por lo que se requiere de una cierta experiencia y entrenamiento para detectar las lesiones malignas más pequeñas.
Entre los biomarcadores serológicos, el más ampliamente investigado ha sido la AFP sérica, glucoproteína que es expresada por los hepatocitos fetales y también por células de HCC pobremente diferenciado. La AFP puede también elevarse en pacientes con hepatitis crónicas B y C en relación directa con brotes de actividad necroinflamatoria (“flares”), aunque no tengan un HCC; esta característica afecta la especificidad del test. El valor de corte más aceptado es el de 20 ng/ml, que es el que tiene la mejor relación entre sensibilidad y especificidad. Pero, aún con este cut-off, la sensibilidad para detectar HCC (considerando todos los estadíos), continúa siendo baja, oscilando entre 41 y 65%.70 Además, con este valor de corte, la especificidad desciende y el valor predictivo positivo es muy bajo, de aproximadamente 41%,71 lo que significa que en la mayoría de los pacientes cirróticos cuyo valor de AFP sea > 20 ng/ml, el diagnóstico final luego de concluido el algoritmo no será el de HCC (falso positivo). Pero además, esto implica que habrá que efectuar estudios contrastados [tomografía computarizada (TC) o resonancia magnética (RM)] antes de concluir que se trataba de un resultado falso positivo. Esto hace que aumenten los costos y se comprometa la relación costo-efectividad de la vigilancia y por esta razón el estudio de AFP no es recomendado dentro de las estrategias de surveillance en las guías de HCC de la American Association for the Study of Liver Diseases o la European Association for the Study of the Liver.72, 73
Un estudio retrospectivo de Taiwan analizando una serie de 363 pacientes con HCC mostró que la AFP (cut-off de 20 ng/ml) y la US tenían una sensibilidad de 53% y 92%, respectivamente, en la detección de los tumores;74 pero la combinación de US más AFP aumentaba la misma a un porcentaje de 99%, concluyéndose que ambos tests tenían un valor complementario.74 Una ventaja de la AFP como test de screening es que es un estudio sencillo, objetivo, reproducible, ampliamente disponible y de bajo costo. Algunos de los profesionales presentes durante la Discusión del Consenso Argentino argumentaron que en pequeñas ciudades de nuestro país podría no haber disponibilidad de operadores entrenados en la US del paciente cirrótico. Por esta razón, se consensuaron recomendaciones que difieren de las de las sociedades científicas más prestigiosas.
Con respecto a cuál es el mejor intervalo entre los tests de screening, este aspecto no ha sido estudiado en profundidad. Expertos opinan que el intervalo de 6 meses es adecuado, de acuerdo a lo que se conoce de viejos estudios que analizaron el tiempo de duplicación de los tumores tempranos no tratados. Un estudio retrospectivo afirmó que la vigilancia semianual se asoció a estadío menos avanzado y mejor sobrevida de los pacientes que la anual;75 mientras que un ECR europeo muy bien realizado no encontró diferencias significativas entre intervalos de 3 meses versus 6 meses en el diagnóstico de HCC ≤ 30 mm de diámetro.76
Recomendaciones
- Todos los pacientes cirróticos de cualquier etiología (incluyendo a los que están en lista de trasplante), los pacientes con hepatitis C y fibrosis severa, y los portadores crónicos del HBV, asintomáticos y que estén en condiciones de recibir tratamiento, deben ser incluidos en un programa de vigilancia para HCC con el objetivo de efectuar diagnóstico en un estadío temprano, aplicar un tratamiento curativo y reducir la mortalidad asociada a esta complicación (calidad de la evidencia: alta, recomendación fuerte).
- En centros que cuenten con operador entrenado, la vigilancia para HCC sería efectuada por medio de US abdominal (calidad de la evidencia: moderada). Ante la detección de una lesión nodular, se pasa al algoritmo diagnóstico (próxima sección).
- En centros que carezcan de operador entrenado en US, la vigilancia para HCC debería incluir la combinación de US abdominal más dosaje de AFP sérica (calidad de la evidencia: baja).
Ante la detección de AFP > 20 ng/ml (en paciente sin lesión nodular en la US simultánea), se debería derivar al paciente a un operador entrenado para una segunda evaluación de US. Si la segunda US no mostrara lesión nodular, se continuara con el esquema habitual de vigilancia.
Si en el siguiente control (6 meses más tarde) se demostrara una duplicación del valor de AFP, se debería realizar un estudio contrastado con TC o RM (pasar al algoritmo de diagnóstico de HCC), aunque la US continúe sin demostrar lesión nodular.
Si en cualquiera de los controles se observara una AFP > 200 ng/ml, sin lesión nodular en la UF simultánea, se debería realizar un estudio contrastado con TC o RM (pasar al algoritmo de diagnóstico de HCC).
- El intervalo recomendado para repetir los tests de screening es el de 6 meses (calidad de la evidencia: moderada).
Diagnóstico de hepatocarcinoma
En pacientes con fibrosis hepática severa o cirrosis, el diagnóstico de HCC puede hacerse en forma no invasiva por medio de estudios de imágenes contrastados o por el examen cito/histológico.
Los estudios de imágenes (TC o RM) deben ser multifásicos, analizando 4 fases: sin contraste y luego de la inyección del contraste IV, las fases arterial, venosa portal y de equilibrio. Los hallazgos característicos del HCC son la presencia de realce en fase arterial con «wash-out» o lavado y realce de una “cápsula” periférica durante la fase venosa portal/tardía.
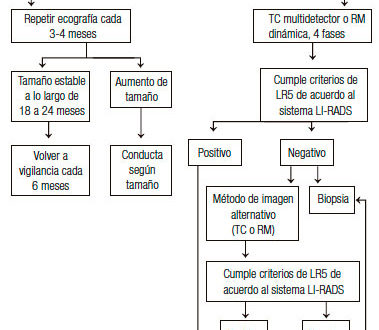
El diagnóstico no invasivo es posible porque el HCC tiene una irrigación predominantemente arterial, mientras que en el parénquima hepático no tumoral prevalece la irrigación venosa portal; pero esta característica del HCC se hace más evidente a partir de un cierto diámetro tumoral. Existe una relación directa entre los cambios histológicos que se van produciendo en la continuidad nódulo displásico de bajo grado → nódulo displásico de alto grado → HCC bien diferenciado de tipo “vagamente nodular” → HCC moderadamente diferenciado de tipo nodular (de acuerdo al International Consensus on Small Nodular Lesions in Cirrhotic Liver)77, 78 y la posibilidad de efectuar un diagnóstico no invasivo por criterios radiológicos. El último de los nombrados (HCC moderadamente diferenciado de tipo nodular) es el que se caracteriza por presentar ausencia de espacios porta y mayor número de arterias de neoformación, por lo que se comportará como hipervascular en la fase arterial (hiperdenso en la TC, hiperintenso en la RM) y presentará wash-out en las fases venosas (hipodenso o hipointenso con respecto al parénquima no tumoral). Lesiones más tempranas (HCC bien diferenciado de tipo “vagamente nodular”) pueden ser hipo o isovasculares en fase arterial. Este conocimiento da base racional al algoritmo recomendado ante la detección de lesiones nodulares por medio de la vigilancia con US en pacientes cirróticos (Figura 1):
Figura 1. Algoritmo recomendado ante la detección de un nódulo hepático por medio de la vigilancia con ultrasonografía abdominal.
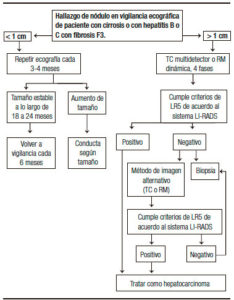
En pacientes cirróticos en quienes se haya detectado un nódulo < 1 cm por medio de la vigilancia ecográfica, no se indica la realización de un estudio contrastado (TC o RM), ya que la mayoría de estas lesiones no son HCCs sino nódulos de regeneración o nódulos displásicos. En cambio, se debe acortar el intervalo entre los tests de screening a 3-4 meses, si luego de 2 años de vigilancia reforzada no se hubiera constatado un aumento del diámetro por encima de 1 cm, se puede retornar al esquema cada 6 meses.
En pacientes cirróticos con nódulos ≥ 1 cm de diámetro, se debe efectuar un estudio por imágenes (RM o TC), dinámico, multifásico, con el equipamiento y la metodología adecuadas (Tabla 1) con el objetivo de verificar si presenta los rasgos característicos, y de ese modo, confirmar el diagnóstico de HCC en forma no invasiva.
Ante nódulos ≥ 1 cm de diámetro, si los estudios de imágenes (TC seguido de RM o viceversa) no muestran los rasgos característicos, se deberá efectuar una punción biopsia hepática (PBH) guiada para estudio cito/histológico.
Tabla 1.
En coincidencia con lo afirmado sobre la correlación histológica-radiológica, la sensibilidad del diagnóstico por imágenes se acerca a 100% en tumores > 2 cm de diámetro, de forma tal que la mayoría de estos casos se confirman no invasivamente. El mayor desafío está dado por las lesiones de 1-2 cm. En este grupo de tumores, se ha publicado que el diagnóstico radiológico (tomando en cuenta los 2 criterios reconocidos por las guías de AASLD y EASL, realce en la fase arterial más wash-out en la fase venosa portal/tardía) tiene una especificidad de 97-100% por medio de RM,79, 80 prácticamente sin falsos positivos; pero la sensibilidad cae a 44-62%, por lo que muchos de estos pacientes requerirán una PBH guiada. El uso secuencial de métodos contrastados (TC seguida de RM o viceversa) es complementario, aumenta la sensibilidad y permite evitar biopsias.80
Recientemente, el American College of Radiology desarrolló un sistema dinámico de terminología y criterios estandarizados para interpretar e informar estudios de imágenes hepáticas denominado LI-RADS (Liver Imaging Reporting and Data System).81 Se creó con el objetivo de estandarizar la evaluación y los informes de TC o RM en pacientes con cirrosis y otros factores de riesgo para HCC.
LI-RADS clasifica los hallazgos en 5 categorías: de LR1 a LR5, que reflejan la probabilidad de benignidad o de HCC en pacientes en riesgo. Una lesión LR1 es una lesión definitivamente benigna y una LR5 es definitivamente un HCC. Las categorías LR2 probablemente benigna, LR3 probabilidad intermedia de HCC y LR4 probable HCC son para lesiones indeterminadas. Para caracterizar a un nódulo se deben considerar: tamaño, crecimiento, realce arterial, wash-out o lavado y presencia de “cápsula” (Tabla 2).
Criterios del diagnóstico radiológico nóveles que están incluidos en el sistema LI-RADS como la presencia del realce de la “seudocápsula” en fases venosas o el aumento del diámetro tumoral ≥ 50% en un lapso de 6 meses (que no eran reconocidas aún en las guías de HCC de la AASLD o EASL) ya son aceptados dentro de los lineamientos que la OPTN/UNOS (Organ Procurement and Transplantation Network/United Network for Organ Sharing) en EUA considera para otorgar puntos de prioridad de MELD y alocación para trasplante hepático en un paciente cirrótico con lesión nodular.83
Los radiólogos expertos en imágenes hepáticas presentes en el Consenso Argentino de HCC coincidieron en apoyar el uso del sistema LI-RADS81, 82 para el diagnóstico no invasivo del HCC. Es muy importante enfatizar que se debe cumplir con los requerimientos técnicos adecuados en lo que hace al equipamiento y a los protocolos de estudio (volumen del contraste a infundir, uso de bomba de infusión, tiempo en que se evalúan las diversas fases, etc.) para poder optimizar las posibilidades del diagnóstico no invasivo (Tabla 1).83
Tabla 2. Sistema LI-RADS para la estandarización del reporte de imágenes de TC y RNM para diagnóstico de HCC.

El diagnóstico morfológico del HCC temprano en muestras de PBH es muy dificultoso y requiere de hepatopatólogos entrenados, siendo un verdadero desafío el diagnóstico diferencial con el nódulo displásico de alto grado, especialmente en lesiones de 1-2 cm de diámetro. La sensibilidad del primer examen histológico es de aproximadamente 60% en tumores < 2 cm79 y puede aumentar a aproximadamente 90% si se considera a todos los tamaños.
El diagnóstico se basa en las definiciones del International Consensus Group for Hepatocellular Neoplasia,77 siendo el hallazgo confirmatorio la presencia de invasión del estroma (invasión del mesénquima de los tractos portales por células neoplásicas), que puede ser difícil de reconocer en muestras de biopsia por aguja en un tejido que está perdiendo los espacios portales. Por lo tanto, un estudio patológico negativo no descarta el diagnóstico de HCC. Se recomienda el uso de un panel de inmunohistoquímica que incluya glipican-3, proteína de shock de calor 70 (HSP70) y glutamina sintetasa.77 Se ha descripto que si 2 de los 3 marcadores mencionados son positivos, esto tiene una sensibilidad de 68-72% y especificidad mayor de 92% para el diagnóstico de HCC.84, 85
Entre las desventajas del examen patológico, se debe recordar que existe un riesgo bajo (2,7%) de causar una diseminación tumoral en el trayecto de la aguja.86
Ante un estudio histológico negativo, se deberá continuar con la vigilancia reforzada, re-evaluar el diagnóstico por imágenes (TC o RM) en 3-6 meses y, de acuerdo a sus hallazgos, efectuar la repetición de la PBH guiada de la lesión nodular.
En el futuro, es probable que se estimule la obtención de muestras de tejido de lesiones nodulares en la mayoría de casos para elaborar bancos de tumores con el propósito de estudiar patrones moleculares de hepatocarcinogénesis, su relación con el pronóstico y la respuesta a nuevas terapias moleculares.
Recomendaciones
- Ante la detección de lesiones nodulares < 1 cm de diámetro, acortar el intervalo entre los tests de screening a 3-4 meses. Si no se constatara aumento del diámetro lesional luego de 2 años, retornar al esquema de vigilancia habitual (calidad de la evidencia: moderada).
- Ante la detección de lesión nodular ≥ 1 cm de diámetro, efectuar un estudio dinámico, multifásico (4 fases) con TC multidetector o RM de 1,5 T o mayor, con el equipamiento y la metodología adecuados (Tabla 1) para verificar si se observan los elementos característicos del diagnóstico no invasivo del HCC (calidad de la evidencia moderada, recomendación fuerte).
- En la evaluación de las lesiones nodulares en pacientes cirróticos o en riesgo para desarrollo de HCC, se considerarán todos los elementos incluidos en el sistema LI-RADS (tamaño, crecimiento, realce arterial, wash-out o lavado y presencia de “cápsula” o “seudocápsula”) (Tabla 2). Si se concluyera que cumple con los criterios de LR5 en un estudio que tenga la metodología adecuada, se debería indicar tratamiento para HCC (calidad de la evidencia moderada, recomendación fuerte).
- Si el primer estudio por imágenes (TC o RM) no mostrara los criterios de HCC, se recomienda efectuar el alternativo (RM o TC).
- Si la TC y la RM no fueran concluyentes, efectuar una PBH guiada que debería ser evaluada por un hepatopatólogo experto, utilizando, además de las coloraciones de rutina, marcadores de inmunohistoquímica como glipican-3, HSP70 y glutamina sintetasa, para aumentar la sensibilidad del estudio en el diagnóstico diferencial entre nódulo displásico de alto grado y HCC temprano (calidad de la evidencia moderada, recomendación fuerte).
- Si el examen histopatológico no confirmara la presencia de HCC, se deberá continuar con la vigilancia reforzada, reiterando estudios contratados (TC y/o RM) en lapso prudencial y eventualmente la PBH guiada hasta la obtención de un diagnóstico definitivo.
Estadificación y tratamiento
El HCC asienta habitualmente sobre un hígado cirrótico, por lo que la definición del pronóstico y la estadificación son complejas y deben considerar no solo la carga tumoral y los síntomas asociados al tumor, sino el grado de afección de la función hepática. El objetivo principal de la estadificación es definir la mejor estrategia terapéutica para cada paciente. El sistema Barcelona Clinic Liver Cancer (BCLC) es el más utilizado porque analiza las variables mencionadas y además, relaciona cada estadío con la modalidad de tratamiento más adecuada según la mejor evidencia científica.87, 88 Desde su descripción original en 1999,87 se ha ido actualizando para incorporar el estadío 0 (muy temprano) o avances en el tratamiento, a medida que metaanálisis o ECRs bien realizados permitían arribar a nueva evidencia científica (ejemplos, la recomendación de quimioembolización arterial para el estadío intermedio, en el año 2003; o de sorafenib para el estadío avanzado, en el año 2008).88
El sistema BCLC distingue los siguientes cinco estadíos o categorías de enfermedad:
Estadíos con intención curativa: El estadío muy temprano (BCLC 0) se define por la presencia de un tumor único < 2 de diámetro sin invasión vascular, en un paciente con clase A de Child-Pugh, sin hipertension portal y en buen estado de salud (ECOG-Performance Status 0);89, 90 las recomendaciones de tratamiento del sistema BCLC son la ablación o resección quirúrgica con una sobrevida a los 5 años mayor al 80%. El estadío temprano (BCLC A) incluye a pacientes con un tumor único o hasta 3 nódulos ≤ 3 cm de diámetro, clase de Child-Pugh A o B, con ECOG-PS 0. En el estadío BCLC A, el sistema recomienda tratamientos potencialmente curativos como la resección quirúrgica, la ablación percutánea o el trasplante hepático, con una sobrevida a 5 años de 50- 70%. La consideración de otros factores predictivos de sobrevida post-resección hepática, como el nivel de bilirrubina sérica (> o < 1 mg/dl) y la presencia o ausencia de hipertensión portal clínicamente significativa, permiten seleccionar a los mejores candidatos para la resección quirúrgica. La consideración de otros factores predictivos de sobrevida post-resección hepática, como el nivel de bilirrubina sérica (> o < 1 mg/dl) y la presencia o ausencia de hipertensión portal clínicamente significativa, permiten seleccionar a los mejores candidatos para la resección quirúrgica. La evaluación de comorbilidades puede determinar la decisión terapéutica en este estadio.
Estadíos con intención terapéutica paliativa: el estadío intermedio (BCLC B) comprende un grupo heterogéneo de pacientes con clase funcional A o B de Child Pugh, con HCC único de gran tamaño no pasible de tratamiento curativo, o con tumor multifocal, definido como más de 3 tumores de cualquier tamaño, o 2 ó 3 tumores > 3 cm de diámetro, en ausencia de síntomas relacionados con el cáncer, invasión macrovascular o diseminación extrahepática. En estos pacientes, el tratamiento recomendado es la quimioembolización transarterial (TACE, por transarterial chemoembolization). En pacientes bien seleccionados y con la aplicación de una técnica adecuada la sobrevida media alcanza los 20-40 meses. La población con estadío avanzado (BCLC C) comprende a pacientes con función hepática Child-Pugh A y B, con síntomas relacionados con el cáncer (ECOG-PS 1 ó 2), invasión macrovascular segmentaria o portal, y/o diseminación extrahepática (compromiso ganglionar o metástasis). La sobrevida mediana esperada de los pacientes en este grupo es de 25% a 1 año. En los pacientes con HCC avanzado (BCLC C) y función hepática preservada (Child-Pugh A), está recomendado el tratamiento sistémico con sorafenib. Los pacientes con HCC en estadío terminal (BCLC D) presentan tumores sintomáticos, con estado funcional malo (ECOG-PS 3-4) o compromiso de la función hepática (clase C de Child-Pugh) con tumores que superan los criterios de trasplantabilidad. Este grupo tiene una mediana de sobrevida de 11% al año y no tiene tratamiento específico, excepto los mejores cuidados paliativos.
El sistema BCLC es el más frecuentemente utilizado en Occidente para definir pronóstico, ha sido validado externamente en diferentes escenarios clínicos91-93 y es respaldado por la AASLD, la EASL y la European Organization for Research and Treatment of Cancer (EORTC). Uno de los mayores desafios del sistema BCLC es la incorporación de un marcador tumoral o perfil de expresión génica, que hasta la actualidad no ha podido realizarse por diversos motivos, como la heterogeneidad del HCC. Dado que la clasificación BCLC también se utiliza para la inclusión de pacientes en ECRs de nuevos tratamientos, algunos autores han propuesto subdivisiones en el estadío B o intermedio,94 que comprende a un grupo heterogéneo de enfermos con un rango de supervivencia que oscila de 11 a 45 meses. Sin embargo, éstas aún deben ser validadas.
Diversos sistemas de estadificación del HCC han sido desarrollados y validados en poblaciones específicas, como por ejemplo el GRETCH en Francia,95 CLIP en Italia,96 CUPI en China,97 JIS en Japón.98 Se caracterizan por una heterogénea selección de variables para determinar el pronóstico, incluyendo parámetros relacionados a la extensión tumoral y también a la reserva funcional hepática; pero no incluyen una recomendación de terapia específica para los diferentes estadíos, como lo hace el sistema BCLC. Recientemente, el Hong Kong Liver Center desarrolló, en base a un estudio retrospectivo sobre más de 3.850 pacientes, una nueva clasificación que incluyó (además de los usuales parámetros de extensión tumoral, función hepática y estado general) recomendaciones de tratamiento, demostrando una aparente mejor capacidad para identificar pacientes en estadíos intermedio y avanzado que se beneficiarían de un tratamiento más agresivo.99 Sin embargo, al evaluar la utilidad del sistema de Hong Kong en una cohorte europea, no se observó una optimización en la predicción del resultado con respecto al BCLC.100
Recomendaciones
- En pacientes con HCC, las principales variables pronósticas son la carga tumoral, la reserva funcional hepática y el estado general. Se recomienda efectuar los estudios necesarios para aplicar el sistema de estadificación BCLC, que permite una adecuada predicción del pronóstico y asignación de la mejor estrategia terapéutica para cada estadío (calidad de la evidencia: alta, recomendación fuerte). El uso de la clasificación BCLC posibilita, además, intercambio de información y comparación de nuevas terapias entre grupos de similar estadío.
Tratamiento del HCC
El manejo de los pacientes con HCC debería ser efectuado por un grupo multidisciplinario que incluya hepatólogos, cirujanos, radiólogos intervencionistas, hemodinamistas y oncólogos, teniendo en cuenta el amplio espectro de terapias disponibles. Sin embargo, dado que el hepatólogo clínico es habitualmente el médico tratante o “de cabecera” del paciente cirrótico que desarrolla el HCC, y teniendo en cuenta la complejidad de la enfermedad de base (cirrosis, con su potencial de presentar complicaciones asociadas a hipertensión portal o a insuficiencia hepatocelular), es fuertemente recomendado que sea este especialista quien coordine el manejo general del paciente afectado.
Tratamientos con intención curativa
Ablación percutánea del HCC
La ablación local con radiofrecuencia (ARF) y la inyección percutánea de etanol (IPE) son los tratamientos ablativos que han sido mejor investigados y se considera que son aplicables en los pacientes con tumores BCLC 0 o A no aptos para la cirugía. Otros tratamientos ablativos, como las microondas o la crioablación, se encuentran todavía en fase de investigación.
Cinco ECRs han comparado la eficacia de la ARF versus IPE en pacientes con HCC temprano y el metaanálisis de dichos estudios demostró que la ARF es superior tanto en términos de supervivencia global como en el porcentaje de necrosis completa del tumor y en la tasa de recurrencia local.101-106 Las tasas de recurrencia en el sitio de ablación fueron menores con ARF (2-14%) que con IPE (11-35%). En cambio, no hubo diferencias entre los resultados de ambos métodos en el subgrupo de pacientes con HCC < 2 cm de diámetro (tumores del estadio 0 de BCLC). En estos casos, ambas técnicas alcanzan respuestas completas en más del 90% de los casos, con buenos resultados a largo plazo.
La sobrevida global a 5 años en pacientes con estadio A tratados con ARF oscila entre 51 a 64% y puede ascender hasta 76% en aquellos que tienen criterios de resecabilidad (bilirrubina normal y sin hipertensión portal) de acuerdo a BCLC. Sin embargo, hay que mencionar que la tasa de respuesta completa es menor en lesiones > 3 cm o cuando el tumor se sitúa en la vecindad de un vaso de calibre ≥ 3 mm (debido a la pérdida del calentamiento del tejido por el enfriamiento asociado a la perfusión). Además, en tumores subcapsulares o adyacentes a la vesícula también se ha descripto riesgo aumentado de ablación incompleta o de complicaciones.107
La ablación por radiofrecuencia es recomendada como principal terapia ablativa en hasta dos nódulos menores de 3 cm de diámetro. En casos de abordaje técnicamente dificultoso (por proximidad de la vesícula, colon, estómago y lesiones subcapsulares con mayor riesgo de siembra tumoral), se puede considerar efectuar la ARF por vía laparoscópica. La inyección percutánea de etanol se recomienda en casos en los que la ablación por radiofrecuencia no es viable técnicamente o no está disponible (alrededor de 10-15%).
No está claro si las terapias ablativas pueden considerarse como alternativas competitivas a la resección quirúrgica en aquellos casos que son candidatos a ambas opciones. Muy pocos ECRs han comparado los resultados de la ARF y la resección quirúrgica (RQ) en pacientes con HCC en estadío A,108, 109 existiendo múltiples estudios que publicaron resultados de cohortes de pacientes tratados con ambas terapias, pero que no habían sido randomizadamente asignados. Ningún ECR ha analizado este aspecto en pacientes del estadío 0 de BCLC; pero estudios de tipo casos-controles y de modelamiento afirman que en este subgrupo la expectativa de vida es similar con ARF que con RQ, mientras que los costos son menores; de modo que la ARF sería la estrategia más costo-efectiva.110 En cambio, en tumores del estadío A, las revisiones sistemáticas y metaanálisis muestran que la RQ se asocia a mayor sobrevida global y sobrevida libre de recurrencia que la ARF.111
Resección quirúrgica del HCC
La RQ es el tratamiento de elección en los tumores que se desarrollan en hígado no cirrótico. En estos casos, es generalmente bien tolerada por la capacidad regenerativa del hígado remanente. Se pueden extirpar incluso lesiones grandes y un remanente hepático funcional > 20% sería suficiente para evitar complicaciones postoperatorias.
En pacientes cirróticos, la RQ del HCC está indicada en los estadios 0 o A y ante la comprobación de una adecuada reserva funcional hepática. En pacientes bien seleccionados, la RQ alcanza una supervivencia a 5 años de aproximadamente 50-60%. De acuerdo a la Japanese Nationwide Survey (una base de datos que comprende a más de 12.000 pacientes con HCC operados en Japón durante los años 1990 a 1999), la sobrevida a 5 años fue de 66% en tumores ≤ 2 cm de diámetro, 52% en lesiones de 2 a 5 cm y 37% en mayores de 5 cm.112
Tradicionalmente, se ha considerado como buenos candidatos para la RQ a aquellos pacientes cirróticos en clase funcional A de la clasificación de Child-Pugh. Sin embargo, existe una proporción de ellos que está en riesgo de presentar insuficiencia hepática, descompensación (ascitis, ictericia, etc) e incluso muerte en el período postoperatorio, especialmente luego de hepatectomías derechas; y el uso en forma exclusiva de la clasificación de Child-Pugh no permite identificar a dichos enfermos. En un estudio de 29 cirróticos de clase A de Child tratados con RQ, Bruix y col observaron descompensación hepática persistente en 38% de ellos.113 Entre múltiples variables analizadas, el gradiente de presiones de la vena suprahepática (GPVH) fue la única asociada con descompensación hepática no resuelta en el análisis multivariado (11 de 15 pacientes con GPVH ≥ 10 mm Hg presentaron descompensación versus ninguno de los 14 con GPVH < 10 mm Hg).113 En Oriente, se utiliza el test de retención de verde de indocianina para definir en forma más refinada la indicación/contraindicación de la RQ, pero es un estudio que no se ha adoptado en Occidente. Estudios tanto de Oriente como de Occidente han encontrado que el score de MELD puede ser de gran utilidad en discriminar pacientes con tumores únicos en mayor riesgo de insuficiencia hepática o mortalidad post-resección. Los valores de corte han variado, pero en general un cut-off ≥ 9 en el score de MELD se asoció a mayor porcentaje de morbilidad y mortalidad.114-116 La medición del GPVH tampoco se ha generalizado en las instituciones sanitarias de nuestro medio, pero se pueden utilizar marcadores subrogantes de hipertensión portal clínicamente significativa (presencia de várices esofágicas o esplenomegalia con recuento de plaquetas ≤ 100.000) para desaconsejar la indicación de la RQ, aunque se trate de un paciente Child A. Resultados de estudios recientes sugieren que la medición de la rigidez hepática (elastografía) por medio de FibroScan® podría ser útil en aproximadamente la mitad de los pacientes en identificar hipertensión portal clínicamente significativa117 o en predecir desarrollo de insuficiencia hepática en el postoperatorio.118
El riesgo de presentar una insuficiencia hepática post-hepatectomía no sólo depende de la reserva funcional hepática sino también de la extensión o complejidad de la RQ. Resecciones hepáticas mayores (≥ 3 segmentos) o complejas (segmentos posteriores 7, 8 ó 1) se asocian a mayor riesgo de disfunción hepática en el postoperatorio. La localización del tumor también influye: nódulos con una ubicación central o profunda en el hígado requieren una resección técnicamente compleja, mientras que nódulos superficiales pueden ser extirpados mediante resecciones en cuña. Un estudio prospectivo reciente de Italia, incluyendo 70 HCC consecutivamente resecados con mortalidad nula a 90 días, mostró que la RQ puede ser efectuada en pacientes con hipertensión portal moderada y tumores superficiales, por vía laparoscópica, con un riesgo bajo de insuficiencia hepática postoperatoria.119
Una desventaja del tratamiento del HCC con RQ (con respecto al trasplante hepático) es que la sobrevida libre de recurrencia a 5 años es de aproximadamente 30%, ya que hasta 70% de los pacientes presentarán una recurrencia tumoral, ya sea temprana (dentro de los 2 años), generalmente por nódulos satélites no reconocidos, o tardía, por la aparición de HCC de novo.
La Tabla 3 muestra recomendaciones sobre la evaluación de la operabilidad de un paciente cirrótico con HCC, y su manejo en los períodos pre, intra y postoperatorio.
Tabla 3. Recomendaciones para el manejo pre, intra y postoperatorio de un paciente cirrótico con HCC, potencialmente candidato a tratamiento con resección quirúrgica.
Trasplante hepático
Los criterios de Milán deben considerarse como los criterios de selección de referencia para pacientes cirróticos con HCC que son candidatos a trasplante hepático (TH). Se asocian a una sobrevida del 70% y una recurrencia acumulativa de 10% a los 5 años post-trasplante. Estos criterios contemplan: un nódulo único ≤ 5 cm de diámetro mayor o hasta 3 nódulos cada uno ≤ 3 cm de diámetro, sin evidencias de invasión macrovascular ni de compromiso extrahepático.120 Una revisión sistemática reciente que incluyó más de 17.000 pacientes con un seguimiento de hasta 15 años confirmó que aquellos que son trasplantados dentro de los criterios de Milán tienen una sobrevida a 5 años (65-78%), que es similar a la de pacientes que reciben TH por patología no tumoral.121
Otros autores propusieron la extensión de dichos criterios (“criterios extendidos”) en distintas cohortes y tanto los pacientes que cumplían con los criterios de UCSF (University of California at San Francisco)122 como los criterios “up-to-seven” 123 mostraron resultados comparables a los de Milán en la sobrevida global, aunque con mayor riesgo de recurrencia. Sin embargo, en ambas cohortes, la identificación de los criterios estuvo basada en los hallazgos patológicos del explante, y no en los estudios radiológicos pre-trasplante, que pueden subestimar la extensión tumoral y son los que serán utilizados para seleccionar a los pacientes. En una serie independiente que analizó 467 pacientes que recibieron TH luego de un breve tiempo de espera, la sobrevida a 5 años fue de 60,1% en aquellos que cumplían con los criterios de Milán y de 45,6% en los que cumplían con los de UCSF, de acuerdo a las imágenes pre-trasplante.124
La indicación de trasplante fuera de los criterios de Milán y dentro de los criterios extendidos debiera ser individualizada, contemplar el aspecto de la escasez de órganos y los criterios de alocación contemplados por la Sociedad Argentina de Trasplante.
La AFP es un marcador biológico de riesgo de recurrencia. Distintos niveles de corte de AFP pre-trasplante se han propuesto como criterios de selección de pacientes para trasplante.125, 126 Asimismo, valores en ascenso de AFP y modificaciones dinámicas durante el seguimiento en lista de espera se han asociado a mayor riesgo de recurrencia en otros estudios.127-129 Valores superiores a 1.000 ng/ml se asocian a un riesgo de recurrencia superior al 40% en distintas series.130 En Argentina, existe un estudio de cohorte retrospectivo que incluye pacientes trasplantados por HCC entre los años 2005-2011, en el cual el nivel de AFP >200 ng/ml identificó pacientes con mayor riesgo de recurrencia, incluso dentro de los criterios de Milán.131 El dosaje de AFP permite un refinamiento de los criterios de selección. En aquellos pacientes con valor de AFP pre-trasplante > 1.000 ng/ml, dado su peor pronóstico, debería considerarse aplicar un tratamiento locorregional mientras se encuentran en lista de espera.
Tratamientos locorregionales y downstaging
Está demostrado que en los pacientes con HCC dentro de los criterios de Milán existe un riesgo aumentado de progresión de la enfermedad cuando el tiempo en lista de espera es mayor a 6-12 meses.132, 133 Por lo tanto, los tratamientos locorregionales o “puente” están recomendados en los pacientes con HCC estadío T2 en quienes la expectativa de tiempo en lista de espera es mayor a 6 meses.134 Existen varios tratamientos propuestos como puente al trasplante, siendo los principales quimioembolización arterial (TACE, por su sigla en inglés transarterial chemoembolization), ARF y RQ.
El objetivo de estas terapias es evitar la progresión tumoral y consecuente salida de lista de espera, y además, evitar la recurrencia tumoral post-trasplante y mejorar la sobrevida global. La tasa de salida de lista sin tratamiento puente es de 30% a un año, lográndose un significativo descenso de la misma (3-9,3%) en los pacientes tratados.135-137
La respuesta a los tratamientos puente es un marcador subrogante de la agresividad biológica del tumor.
Los tratamientos locorregionales en pacientes con HCC que excede los criterios de Milán pueden además lograr el downstaging hacia dichos criterios. Los pacientes que logran el downstaging tienen una sobrevida a 5 años comparable a aquellos que se trasplantan dentro de los criterios de Milán.138, 139
Los criterios para considerar a un caso de HCC como candidato a downstaging no están definitivamente consensuados pero se podría utilizar este abordaje en pacientes con un nódulo único ≤ 8 cm o 2 ó 3 nódulos c/u menores de 5 cm con una suma tumoral total ≤ 8 cm, sin invasión macrovascular, con AFP < 1.000 ng/ml, sin manifestaciones extrahepáticas. No es recomendado en pacientes con más de 3 tumores. Se considera que el downstaging ha sido exitoso cuando la carga tumoral retorna dentro de los criterios de Milán, evaluado por TC o RM contrastadas de acuerdo a criterios de mRECIST.140 Si el caso en estudio hubiera presentado inicialmente un nivel de AFP > 1.000 ng/ml, debe descender a < 500 ng/ ml al momento de la inclusión en lista. De acuerdo a los resultados de los estudios, no existe evidencia para recomendar un tratamiento locorregional sobre otro. La respuesta al tratamiento de downstaging es un predictor de la evolución post-trasplante por lo que algunos autores sugieren esperar 3 meses antes de otorgar al paciente en estudio puntos adicionales para trasplante con el objetivo de identificar tumores con mayor riesgo de recurrencia.
Resección versus trasplante
La resección quirúrgica y el trasplante hepático son las técnicas que han demostrado mejores resultados en términos de sobrevida en pacientes bien seleccionados. La elección del tratamiento no solo va a estar determinada por las características del tumor (número, tamaño y localización de las lesiones), sino que también dependerá de la enfermedad hepática subyacente y del grado de compromiso de la funcionalidad hepática y del estado general del paciente. En aquellos pacientes con estadios iniciales y mala reserva funcional hepática, el tratamiento ideal es el trasplante hepático, ya que con el mismo se logra una resección tumoral completa, se elimina la hipertensión portal, se restaura la funcionalidad hepática y se evita la formación de “novo” de HCC (carcinogénesis multicéntrica), al eliminarse el factor predisponente, que es la cirrosis.
Las eventuales ventajas del trasplante hepático en pacientes con tumores que son considerados como pasibles de resección no han sido evaluadas en estudios prospectivos randomizados. Es de destacar que si este beneficio no está establecido, el trasplante no debiera ser llevado a cabo en buenos candidatos a RQ ya que, debido a la escasez de donantes, podría perjudicar a otros pacientes en quienes dicho tratamiento es la única alternativa terapéutica.
Tratamiento de la recurrencia
Para el tratamiento de la recurrencia del HCC luego de una terapia con intención curativa, no existen hasta el momento modelos pronósticos ni algoritmos de decisión que hayan sido consensuados en relación con la modalidad de tratamiento inicial aplicada. Ante la aparición de una recurrencia intrahepática, se debe efectuar una re-estadificación del caso teniendo en cuenta todos los parámetros comprendidos en BCLC.
Las opciones terapéuticas más aceptadas para recurrencias intrahepáticas son: 1) re-ablación para las recurrencias post-ARF y ante su falla o imposibilidad, resección hepática o trasplante; 2) re-resección, ARF o trasplante hepático de salvataje para recurrencias luego de la resección quirúrgica (en casos bien seleccionados, el trasplante hepático de salvataje alcanza resultados similares que el trasplante primario);141 3) en recurrencias post-trasplante, cirugía, ARF o TACE. En casos de recurrencia post-trasplante que no sean pasibles de tratamiento quirúrgico o locorregional, el uso de sorafenib se asoció a sobrevida mejorada con respecto a un grupo control histórico.142
En casos seleccionados de recurrencia extrahepática (presencia de uno o dos nódulos, HCC intrahepático controlado, reserva funcional hepática adecuada y buen performance status), la resección quirúrgica parecería ser una opción útil. La recurrencia extrahepática múltiple se asocia a mal pronóstico, con una sobrevida media de 4-5 meses.
Recomendaciones sobre tratamiento del HCC con intención curativa
- El manejo y tratamiento del HCC debe ser abordado por un grupo multidisciplinario (cirujanos, trasplantólogos, radiólogos intervencionistas, hemodinamistas, oncólogos) con la coordinación del hepatólogo clínico que asiste al paciente.
- Los tratamientos con intención curativa son indicados en los estadios 0 y A de la clasificación BCLC.
- La resección quirúrgica es la opción de primera línea en el tratamiento del HCC en pacientes no cirróticos (calidad de la evidencia baja, recomendación fuerte).
- En pacientes cirróticos, la resección quirúrgica es la primera opción terapéutica ante la presencia de tumor solitario y la comprobación de una adecuada reserva funcional hepática (clase A de Child-Pugh y ausencia de ictericia e hipertensión portal clínicamente significativa) (calidad de la evidencia moderada, recomendación fuerte).
- En pacientes con HCC en estadio 0 de BCLC, las terapias ablativas como ablación por radiofrecuencia o inyección percutánea de etanol se asocian a respuesta completa en más de 90% de los casos y alcanzan resultados similares a la resección quirúrgica en términos de supervivencia global (calidad de la evidencia baja, recomendación débil).
- En pacientes con HCC en estadío A de BCLC, la resección quirúrgica se asocia a mayor supervivencia global y libre de recurrencia que las terapias ablativas (calidad de la evidencia moderada, recomendación fuerte).
- Entre las terapias ablativas, la ARF se asocia a una mayor supervivencia global y a una menor tasa de recurrencia que la IPE (calidad de la evidencia alta, recomendación fuerte); aunque en tumores ≤ 2 cm de diámetro ambas técnicas obtienen una eficacia terapéutica similar.
- Durante el seguimiento post-resección quirúrgica o ablación percutánea, la incidencia de recurrencia del HCC es elevada. Ante dicha eventualidad, se debe proceder a la re-estadificación y tratamiento adecuado a la misma.
- El trasplante hepático debe ser indicado en pacientes con una carga tumoral dentro de los criterios de Milán (un nódulo único ≤ 5 cm de diámetro mayor o hasta 3 nódulos cada uno ≤ 3 cm de diámetro, sin evidencias de invasión macrovascular ni de compromiso extrahepático) y que no sean candidatos a resección quirúrgica (calidad de la evidencia moderada, recomendación fuerte).
- Ante la posibilidad de un tiempo en lista de espera mayor a 6 meses, se puede indicar un tratamiento locorregional (ARF, quimioembolización arterial, resección) con el objetivo de evitar la progresión tumoral y consecuente salida de la lista (calidad de la evidencia moderada, recomendación fuerte).
- El tratamiento locorregional pre-trasplante también es recomendado en tumores dentro de los criterios de Milán pero con niveles elevados de AFP, dado el mayor riesgo de recurrencia post-trasplante (calidad de la evidencia moderada, recomendación fuerte).
- En tumores que exceden los criterios de Milán, se puede intentar el downstaging por medio de tratamiento locorregional con el objetivo de disminuir la carga tumoral hacia dentro de dichos límites. La respuesta al tratamiento locorregional debe ser evaluada por medio de TC o RM contrastados multifásicos, siguiendo los criterios de RECIST modificados. La carga tumoral debería permanecer estable durante al menos 3 meses luego de alcanzado el downstaging antes de solicitar puntos de prioridad para la alocación de trasplante hepático (calidad de la evidencia moderada, recomendación fuerte).
Tratamientos con intención paliativa
Quimioembolización arterial (TACE)
La TACE es un tratamiento que consiste en la administración intra-arterial de drogas quimioterapéuticas (principalmente doxorrubicina, cisplatino, mitomicina C) junto con el medio de contraste oleoso Lipiodol ® y agentes embolizantes (luego de la infusión del quimioterápico se efectúa la embolización superselectiva de la arteria que irriga al tumor). Existe una amplia heterogeneidad respecto a los agentes quimioterapéuticos y de embolización utilizados, la selectividad terapéutica y los intervalos de tratamiento. Ello explica el diferente rango de efectividad clínica descripto en la literatura.143 Los mejores resultados reportados en términos de sobrevida global son actualmente de 48 meses en poblaciones bien seleccionadas.144
Es muy importante hacer una correcta selección de los pacientes a tratar ya que esta terapia puede ser riesgosa si no se respetan ciertos criterios de exclusión. No deberían ser tratados con TACE los pacientes que tengan un deterioro del flujo venoso portal (obstrucción venosa o flujo portal hepatófugo), o aquellos que no tengan una adecuada reserva funcional hepática. En ambos casos, la isquemia arterial puede precipitar insuficiencia hepática, ictericia, ascitis o incluso la muerte (en aproximadamente 1% de los casos).
Se consideran contraindicaciones absolutas143 para TACE:
– La presencia de tumores masivos con compromiso de ambos lóbulos.
– Cirrosis descompensada (score de Child-Pugh ≥ 8).
– Ausencia completa de flujo portal.
– Contraindicación técnica al tratamiento intra-arterial.
Se consideran contraindicaciones relativas para TACE:
– Tumores grandes (> 10 cm de diámetro).
– Várices gastroesofágicas sin tratamiento y con riesgo de sangrado.
– Trombosis venosa de rama o segmentaria portal.
– Obstrucción de la vía biliar o papila incompetente por cirugía o stent.
La sobrevida a 2 años en pacientes con HCC irresecable tratados con TACE fue reportada como significativamente mayor en comparación con el tratamiento de sostén;145, 146 lo que fue confirmado posteriormente en un metaanálisis.147 Las guías europeas recomiendan TACE para pacientes con HCC en estadio intermedio, tumor grande o multinodular, asintomáticos, con buena función hepática y sin invasión vascular ni metástasis extrahepática; o en aquellos pacientes en los que la ablación percutánea no es posible o está contraindicada.73 En el ECR de LLovet y col, el tratamiento con TACE obtuvo una sobrevida a 2 años de 63% comparada con 27% en el grupo control (p = 0,009).146 Las sobrevidas reportadas en los pacientes tratados son ampliamente variables, oscilando desde 53% a 90% al primer año, de 11% a 67% a los dos años y de 8% a 26% a los cinco años, en relación probable a la ya mencionada heterogeneidad de los pacientes del estadio B o intermedio de BCLC.
El uso de microesferas cargadas con drogas (DEB, por “drug-eluting beads”) como la doxorrubicina tiene el objetivo de alcanzar una obstrucción arterial calibrada y una liberación lenta (durante aproximadamente una semana) del citostático, proveyendo una mayor concentración intratumoral del mismo y una menor exposición sistémica,148 y por lo tanto, una menor incidencia de efectos adversos. En ECRs, se demostró en pacientes tratados con DEB una marcada reducción de la toxicidad hepática y de los efectos adversos de la quimioterapia en comparación con la quimioembolización convencional.149, 150
El ensayo controlado randomizado multicéntrico PRECISION V comparó la TACE convencional con la TACE con DEB en 212 cirróticos con HCC irresecable, clases de Child A o B y sin compromiso extrahepático; siendo el end point primario la respuesta tumoral a los 6 meses. La Respuesta Objetiva en la población global tendió a ser mejor en el grupo TACE con DEB que en TACE convencional (52% versus 44%, respetivamente), aunque la diferencia no fue estadísticamente significativa y la hipótesis de superioridad no fue confirmada (p = 0,11).149 En el subgrupo de pacientes con enfermedad más avanzada (Child Pugh B, Performance Status ECOG 1, enfermedad bilobar y enfermedad recurrente), la Respuesta Objetiva fue significativamente mejor en pacientes tratados con DEB que con la técnica convencional (p = 0,038). Se requieren más estudios prospectivos para determinar fehacientemente si una técnica ofrece mayor sobrevida que la otra.
La utilización de DEB permite un tratamiento más reproducible que con la técnica convencional ofreciendo la oportunidad de estandarizar el procedimiento. Existe una tendencia hacia la generalización del uso de microesferas cargadas con doxorubicina (DEB) ya que ofrece menor toxicidad hepática, menores efectos adversos de los citostáticos y permite un tratamiento reproducible y estandarizado. Los mejores resultados reportados en la literatura reciente sobre TACE (con sobrevida global a los 3 y 5 años de 62% y 22,5%, respectivamente, y sobrevida media de 44 meses) se obtuvieron con la técnica de DEB.151
Radioembolizacion arterial hepática (TARE, por “transarterial radioembolization”)
La terapia con Ytrio 90 (Y90) por vía intraarterial consiste en la implantación de microesferas radioactivas para realizar radioterapia hepática interna.152 En este procedimiento se administran partículas muy pequeñas de resina o vidrio que contienen Ytrio 90, un emisor de radiación beta pura que posee una penetración tisular de 2,5 mm y que, una vez inyectadas, se alojan dentro del tumor. La dosis estipulada se administra de acuerdo a la extensión y localización tumoral así como a la presencia o no de shunts pulmonares y/o portales, previamente estudiados. El cálculo de dosis debe ajustarse a cada paciente en particular. El mismo puede obtenerse a partir de la superficie corporal, o bien por el volumen corporal.
La energía que contienen las micropartículas es emitida durante las primeras dos semanas tras la inyección. Para evitar la localización fuera del hígado es necesario realizar un procedimiento angiográfico de mapeo muy meticuloso dentro de las dos semanas previas al procedimiento y que implica la administración de partículas de albúmina marcadas con Tc99 que tienen un tamaño similar a las partículas cargadas con Y90. Una vez finalizado el examen, se efectúa un centellograma corporal total determinando la localización de la albúmina marcada con tecnecio 99, tanto en parénquima sano como en el área del tumor. El shunt hepato-pulmonar debe ser menor al 20% para evitar la neumonitis actínica. Realizado el centellograma corporal total, se ajustará la dosis de Y 90 a colocar, de acuerdo al porcentaje de captación por el tumor. Los pacientes deberían presentar bilirrubina total menor a 2 mg/dl, AST/ALT que no superen más de cinco veces los valores normales y tener una función hepática preservada, clase A de Child-Pugh. La presencia de trombosis portal o invasión no es una contraindicación para la TARE, dada la mínima capacidad embolizante de las partículas.
Son susceptibles de recibir TARE pacientes con HCC que no sean pasibles de tratamiento quirúrgico o trasplante, y pacientes que hayan recibido otras terapias loco regionales que hayan fracasado como quimioembolización o ablación por radiofrecuencia.153 También se podría aplicar radioembolización hepática para downstaging,154 y en pacientes del estadio B que podrían ser candidatos a TACE pero con contraindicaciones a la misma como trombosis segmentarias o de la vena porta.153, 155
Los resultados dependen de las características de los pacientes, estadio de la enfermedad BCLC, del ECOG Performance Status, presencia de obstrucción de la vena porta o metástasis a distancia.156 Un estudio retrospectivo comparativo entre TARE y TACE incluyendo 245 pacientes mostró que en pacientes con estadio B o intermedio de BCLC, la sobrevida global es similar alcanzando los 17 meses, con un tiempo hasta la progresión significativamente mayor entre los tratados por radioembolización.157 Es necesario enfatizar que estos resultados no provienen de estudios controlados randomizados. Actualmente, están en fase de reclutamiento activo estudios clínicos comparativos entre TACE y radioembolizacion, incluyendo un estudio en fase 3 para HCC unilobar.158, 159
Tratamiento sistémico del HCC
Sorafenib
Sorafenib es una molécula pequeña con capacidad de inducir la apoptosis, inhibir la proliferación de las células tumorales y la formación de nuevos vasos. Su mecanismo de acción implica la inhibición de la actividad de las quinasas Raf-B y Raf-1, además de bloquear los receptores del factor de crecimiento del endotelio vascular (VEGF) de tipo 1, 2 y 3, así como también del receptor del factor de crecimiento derivado de plaquetas beta (PDGF). Es el único tratamiento sistémico que ha sido aprobado para el tratamiento del HCC avanzado en base a dos estudios randomizados controlados frente a placebo, en los cuales se demostró un aumento significativo en la sobrevida de los pacientes tratados.160, 161 Estos estudios son el SHARP (Sorafenib HCC Assessment Randomized Protocol), efectuado en Occidente y el de la región Asia-Pacífico; los pacientes que fueron incluidos tenían función hepática preservada (Child-Pugh A) y estadio C de BCLC. En el estudio SHARP, la sobrevida global mediana fue de 10,7 meses en el grupo sorafenib y de 7,9 meses en el grupo placebo (hazard ratio en el grupo sorafenib: 0,69; IC95%: 0,55-0,87; p < 0,001); lo que implica un descenso de 31% en el riesgo de muerte.160 Una diferencia similar en términos de sobrevida global se observó en el estudio de Oriente entre los grupos sorafenib y placebo.161
Los efectos adversos más frecuentes son diarrea (39%), fatiga (22%) y eventos cutáneos, como la reacción mano-pie (21%), rash (16%), alopecia (14%) o piel seca (8%). Ante reacciones cutáneas severas se debe reducir la dosis o discontinuar el sorafenib y luego intentar la reintroducción gradual. Se ha descripto que la aparición de eventos adversos dermatológicos tempranos luego del inicio de sorafenib se asocia a una mejor sobrevida, por lo que habría que intentar sostener la terapia.162
No se puede aún hacer una recomendación clara en cuanto al uso de sorafenib en pacientes con clase B de Child Pugh, aunque algunos estudios sugieren que la seguridad y tolerancia sería similar a la de los pacientes con clase A.163, 164 Sin embargo, en el estudio GIDEON, que incluyó más de 3.000 pacientes, el porcentaje de eventos adversos serios fue mayor en pacientes Child B que en A (60 versus 36%, respectivamente).163
La eficacia de sorafenib como terapia adyuvante luego del tratamiento del HCC con resección quirúrgica o ablación fue investigada en el ECR de fase 3, a doble ciego, STORM, que incluyó 1.114 pacientes, no observándose diferencia significativa en la sobrevida mediana libre de recurrencia.165 En un estudio ramdomizado más pequeño de Oriente, tampoco se observó un beneficio del tratamiento con sorafenib en pacientes con HCC irresecable que habían respondido a la quimioembolización arterial.166
La dosis de sorafenib es de 400 mg, 2 veces por día y se recomienda continuar hasta la progresión de la enfermedad o la aparición de efectos adversos severos que no puedan ser manejados con la reducción de la dosis.
Diferentes moléculas que tienen acción potencial sobre diversos mecanismos implicados en el complejo proceso de la hepatocarcinogénesis han sido probadas en ensayos de fase 3 en pacientes con HCC en estadío avanzado, ya sea como primera o segunda línea (luego del fracaso terapéutico de sorafenib) pero ninguna de ellas ha demostrado hasta el momento actual una mejoría significativa (con respecto al sorafenib en la primera línea o con respecto al placebo en la segunda).
Recomendaciones sobre tratamiento del HCC con intenciones paliativas
- La quimioembolización arterial (TACE) es la opción de primera línea en pacientes del estadío B o intermedio de la clasificación BCLC, asintomáticos, con tumor único grande o multinodular, irresecable, sin invasión vascular o enfermedad extra-hepática (calidad de la evidencia alta, recomendación fuerte).
- La técnica de la quimioembolización arterial utilizando microesferas que liberan doxorubicina (drug-eluting beads) permite obtener tasas de respuesta similares a la quimioembolización convencional, pero con menor incidencia de efectos adversos hepáticos y sistémicos (calidad de la evidencia alta, recomendación débil).
- El procedimiento de TACE con DEB es más reproducible, aunque no se ha demostrado hasta el momento actual que aumente la sobrevida global con respecto a la técnica de TACE convencional.
- La quimioembolización arterial no está recomendada en pacientes con cirrosis descompensada o reserva funcional hepática pobre (Child-Pugh ≥ 8) u obstrucción de la vena porta.
- TACE podría indicarse en pacientes del estadio A o temprano cuando, por diversas razones, las terapias curativas (ARF, RQ o trasplante) no puedan ser aplicadas.
- La radioembolización transarterial (TARE) ha mostrado resultados antitumorales promisorios y similares a los de TACE con mejor tolerancia pero no es considerada aún como estándar de cuidado por la falta de evidencia científica apoyatoria.
- TARE podría ser indicada en pacientes con contraindicaciones a la TACE como la presencia de tumores grandes, bilobares múltiples o con trombosis de la vena porta, así como también en aquellos casos en los que ha fracasado la TACE. Se esperan resultados de ensayos controlados randomizados para definir su eficacia en comparación con TACE en el estadío B o intermedio de BCLC.
- TARE no debe ser indicado en pacientes con deterioro de la función hepática (bilirrubina > 2 mg/dl), shunt hepato-pulmonar mayor del 20%, ECOG > 2.
- En pacientes con HCC en estadio C o avanzado de la clasificación BCLC que conserven una buena función hepática (Child Pugh clase A) y un buen estado funcional (ECOG Performance Status 0-2), la opción de primera línea es el tratamiento sistémico con sorafenib (calidad de la evidencia alta, recomendación fuerte).
- En pacientes con HCC del estadio B o intermedio que tengan contraindicaciones a la TACE o que hayan sido tratados con TACE y no hayan tenido respuesta objetiva, se puede indicar terapia sistémica con sorafenib (calidad de la evidencia baja, recomendación débil).
- No existen por el momento terapias de segunda línea para los pacientes con HCC en estadio C o avanzado con falta de respuesta al sorafenib o intolerancia al mismo.
- En los pacientes con HCC en estadio D de BCLC, se deben utilizar cuidados paliativos, incluyendo terapia del dolor, apoyo nutricional y psicoterapé
Sostén financiero. Todos los gastos relativos a la organización del Consenso Argentino de Hepatocarcinoma 2015 fueron solventados por la Asociación Argentina para el Estudio de las Enfermedades del Hígado. Los Dres Eduardo Fassio y Guillermo Mazzolini no tienen ningún conflicto de intereses que declarar.
Referencias
- Grading quality of evidence and strenght of recommendations. Grades of Recommendation, Assessment, Development, and Evaluation (GRADE) Working Group. Brit Med J 2004; 328: 1490-1494.
- http://globocan.iarc.fr/Pages/bar_sex_site_prev_sel.aspx.
- http://globocan.iarc.fr/old/summary_table_pop-html.asp?selectio n=224900&title=World&sex=0&type=1&window=1&sort=0&s ubmit=%C2%A0Execute
- Perz JF, Armstrong GL, Farrington LA, Hutin YJ, Bell BP. The contributions of hepatitis B virus and hepatitis C virus infections to cirrhosis and primary liver cancer worldwide. J Hepatol 2006; 45: 529-538.
- Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin 2005; 55: 74-108.
- Qian GS, Ross RK, Yu MC, Yuan JM, Gao YT, Henderson BE, Wogan GN, Groopman JD. A follow-up study of urinary markers of aflatoxin exposure and liver cancer risk in Shangai, People’s Republic of China. Cancer Epidemiol Biomarkers Pre Prev 1994; 3: 3-10.
- Bruix J, Barrera JM, Calvet X, Ercilla G, Costa J, Sanchez Tapias, JM, Ventura M, Vall M, Bruguera M, Bru C. Prevalence of antibodies to hepatitis C virus in Spanish patients with hepatocellular carcinoma and hepatic cirrhosis. Lancet 1989; 2: 1004-1006.
- Colombo M, Kuo G, Choo QL, Donato MF, Del Ninno E, Tommasini MA, Dioquardi N, Houghton M. Prevalence of antibodies to hepatitis C virus in Italian patients with hepatocellular carcinoma. Lancet 1989; 2: 1006-1008.
- Bugianesi E, Leone N, Vanni E, Marchesini G, Brunello F, Carucci P, Musso A, De Paolis P, Capussotti L, Salizzoni M, Rizzetto M. Expanding the natural history of nonalcoholic steatohepatitis: from cryptogenic cirrhosis to hepatocellular carcinoma. Gastroenterology 2002; 123: 134-140.
- Donato F, Tagger A, Chiesa R, Ribero ML, Tomasoni V, Fasola M, Gellatti U, Portera G, Boffetta P, Nardi G. Hepatitis B and C virus infection, alcohol drinking, and hepatocellular carcinoma: a case-control study in Italy. Hepatology 1997; 26: 579-584.
- Hassan MM, Hwang L-Y, Hatten CJ, Swaim M, Li D, Abbruzzese JL, Beasley P, Patt YZ. Risk factors for hepatocellular carcinoma: synergism of alcohol with viral hepatitis and diabetes mellitus. Hepatology 2002; 36: 1206-1213.
- Marrero JA, Fontana RJ, Su GL, Conjeevaram HS, Emick DM, Lok AS. NAFLD may be a common underlying liver disease in patients with hepatocellular carcinoma in the United States. Hepatology 2002; 36: 1349-1354.
- El-Serag HB, Mason AC. Rising incidence of hepatocellular carcinoma in the United States. N Engl J Med 1999; 340: 745-750.
- Taylor-Robinson SD, Foster GR, Arora S, Hargreaves S, Thomas HC. Increase in primary liver cancer in the UK, 1979-94. Lancet 1997; 350: 1142-1143.
- Levi F, Lucchini F, Negri E, Boyle P, La Vecchia C. Cancer mortality in Europe, 1995-1999, and overview of trends since 1960. Int J Cancer 2004; 110: 155-169.
- Dyer Z, Peltekian K, van Zanten SV. Review article: the changing epidemiology of hepatocellular carcinoma in Canada. Aliment Pharmacol Ther 2005; 22: 17-22.
- Altekruse SF, McGlynn KA, Reichman ME. Hepatocellular carcinoma incidence, mortality, and survival trends in the United States from 1975 to 2005. J Clin Oncol 2009; 27: 1485-1491.
- El-Serag HB, Mason AC. Risk factors for the rising rates of primary liver cancer in the United States. Arch Intern Med 2000; 160: 3227-3230.
- Fassio E, Diaz S, Santa C, Reig ME, Martínez Artola Y, Alves de Mattos A, Míguez C, Galizzi J, Zapata R, Ridruejo E, de Souza FC, Hernández N, Pinchuk L; Multicenter Group for the Study of Hepatocarcinoma in Latin America; Asociación Latinoamericana para el Estudio del Hígado (ALEH). Etiology of hepatocellular carcinoma in Latin America: prospective, multicenter, international study. Ann Hepatol 2010; 9: 63-69.
- Fassio E, Míguez C, Soria S, Palazzo F, Gadano A, Adrover R, Landeira G, Fernández N, García D, Barbero R, Perelstein G, Ríos B, Isla R, Civetta E, Pérez Ravier R, Barzola S, Curciarello J, Colombato LA, Jmelnitzky A. Etiology of hepatocellular carcinoma in Argentina: results of a multicenter retrospective study. Acta Gastroenterol Latinoamer 2009; 39: 47-52.
- file:///C:/Documents%20and%20Settings/New/Escritorio/ GLOBOCAN%202012/GLOBOCAN%202012-Cancer%20 incidence,%20both%20sexes.htm
- Bréchot C, Gozuacik D, Murakami Y, Paterlini-Bréchot P. Molecular bases for the development of hepatitis B virus (HBV)-related hepatocellular carcinoma (HCC). Semin Cancer Biol 2000; 10: 211–231.
- Fattovich G, Bortolotti F, Donato F. Natural history of chronic hepatitis B: special emphasis on disease progression and prognostic factors. J Hepatol 2008; 48: 335-352.
- Chen CJ, Yang HI, Su J, Jen CL, You SL, Lu SN, et al. Risk of hepatocellular carcinoma across a biological gradient of serum hepatitis B virus DNA level. JAMA 2006; 295: 65-73.
- Yang HI, Lu SN, Liaw YF, You SL, Sun CA, Wang LY, Hsiao CK, Chen PJ, Chen DS, Chen CJ; Taiwan Community-Based Cancer Screening Project Group. Hepatitis B e antigen and the risk of hepatocellular carcinoma. N Engl J Med 2002; 347: 168-174.
- Yu MW, Yeh SH, Chen PJ, Liaw YF, Lin CL, Liu CJ, Shih WL, Kao JH, Chen DS, Chen CJ. Hepatitis B virus genotype and DNA level and hepatocellular carcinoma: a prospective study in men. J Natl Cancer Inst 2005; 97: 265-272.
- Bonacini M, Louie S, Bzowej N, Wohl AR. Survival in patients with HIV infection and viral hepatitis B or C: a cohort study. AIDS 2004; 18: 2039–2045.
- Yoshida H, Shiratori Y, Moriyama M, Arakawa Y, Ide T, Sata M, Inoue O, Yano M, Tanaka M, Fujiyama S, Nishiguyi S, Kuroki T, Imazeki F, Yokosuka O, Kinoyama S, Yamada G, Omata M. Interferon therapy reduces the risk for hepatocellular carcinoma: national surveillance program of cirrhotic and noncirrhotic patients with chronic hepatitis C in Japan. Ann Intern Med 1999; 131: 174-181.
- Lok AS, Seef LB, Morgan TR, di Biscegli AM, Sterling RK, Curto TM, Everson GT, Lindsay KL, Lee WM, Bonkovsky HL, Dienstag JL, Ghany MG, Morishima C, Goodman ZD; HALT-C Trial Group. Incidence of hepatocellular carcinoma and associated risk factors in hepatitis C-related advanced liver disease. Gastroenterology 2009; 136: 138-148.
- Degos F, Christidis C, Ganne-Carrie N, Farmachidi JP, Degott C, Guettier C, Trinchet JC, Beaugrand M, Chevret S. Hepatitis C virus related cirrhosis: time to occurrence of hepatocellular carcinoma and death. Gut 2000; 47: 131-136.
- Aizawa Y, Shibamoto Y, Takagi I, Zeniya M, Toda G. Analysis of factors affecting the appearance of hepatocellular carcinoma in patients with chronic hepatitis C. A long term follow up study after histologic diagnosis. Cancer 2000; 89: 53-59.
- Chiaramonte M, Stroffolini T, Vian A, Stazi MA, Floreani A, Lorenzoni U, Lobello S, Farinati F, Naccarato R. Rate of incidence of hepatocellular carcinoma in patients with compensated viral cirrhosis. Cancer 1999; 85: 2132-2137.
- Donato F, Boffetta P, Puoti M. A meta-analysis of epidemiological studies on the combined effect of hepatitis B and C virus infections on causing hepatocellular carcinoma. Int J Cancer 1998; 75: 347-354.
- Di Benedetto N, Peralta M, Alvarez E, Schroder T, Estepo CR, Paz S, Fainboim H. Incidence of hepatocellular carcinoma in hepatitis C cirrhotic patients with and without HIV infection: a cohort study, 1999-2011. Ann Hepatol 2014; 13: 38-44.
- Raimondi S, Bruno S, Mondelli MU, Maisonneve P. Hepatitis C virus genotype 1b as a risk factor for hepatocellular carcinoma development: a meta-analysis. J Hepatol 2009; 50: 1142-1154.
- Kanwal F, Kramer JR, Ilyas J, Duan Z, El-Serag HB. HCV genotype 3 is associated with an increased risk of cirrhosis and hepatocellular cancer in a national sample of U.S. veterans with HCV. Hepatology 2014; 60: 98-105.
- Morgan RL, Baack B, Smith BD, Yartel A, Pitasi M, Falck-Itter Y. Eradication of hepatitis C virus infection and the development of hepatocellular carcinoma. A meta-analysis of observational studies. Ann Intern Med 2013; 158: 329-337.
- Bravi F, Bosetti C, Tavani A, Gallus S, La Vecchia C. Coffee reduces risk for hepatocellular carcinoma: an updated meta-analysis. Clin Gastroenterol Hepatol 2013; 11: 1413-1421.
- Tsan YT, Lee CH, Ho WC, Lin MH, Wang JD, Chen PC. Statins and the risk of hepatocellular carcinoma in patients with hepatitis C virus infection. J Clin Oncol 2013; 31: 1514-1521.
- García D, Poncino D, Martínez Artola Y, et al. Incidencia del hepatocarcinoma en pacientes con cirrosis por alcohol y hepatitis C. Acta Gastroent Latinoamer 2005; 35: A62.
- Jepsen P, Ott P, Andersen P, Sorensen HT, Vilstrup H. Risk for hepatocellular carcinoma in patients with alcoholic cirrhosis. A Danish nationwide cohort study. Ann Intern Med 2012; 156: 841-847.
- Donato F, Tagger A, Gelatti U, Parrinello G, Bofetta P, Albertini A, Decarli A, Trevisi P, Ribero ML, Martelli C, Porru S, Nardi G. Alcohol and hepatocellular carcinoma: the effect of lifetime intake and hepatitis virus infections in men and women. Am J Epidemiol 2002; 155: 323-331.
- Hassan M, Spitz M, Thomas M, El-Deeb AS, Glover KY, Nguyen NT, Chan W, Kaseb A, Curley SA, Vauthey JN, Ellis LM, Abdalla E, Lozano RD, Patt YZ, Brown TD, Abbruzzese JL, Li D. Effect of different types of smoking and synergism with Hepatitis C virus on risk of hepatocellular carcinoma in American men and women: Case-control study. Int J Cancer 2008; 123: 1883-1891.
- Balbi M, Donadon V, Ghersetti M, Grazioli S, Valentina GD, Gardenal R, Mas MD, Casarin P, Zanette G, Miranda C, Cimarosti P. Alcohol and HCV chronic infection are risk cofactors of type 2 diabetes mellitus for hepatocellular carcinoma in Italy. Int J Environ Res Public Health 2010; 7: 1366-1378.
- Nahon P, Sutton A, Rufat P, Ziol M, Thabut G, Schischmanoff PO, Vidaud D, Charnaux N, Couvert P, Ganne-Carrie N, Trinchet JC, Gattegno L, Beaugrand M. Liver iron, HFE gene mutations, and hepatocellular carcinoma occurrence in patients with cirrhosis. Gastroenterology 2008; 134: 102-110.
- Morgan T, Mandayan S and Jamal M. Alcohol and hepatocellular carcinoma. Gastroenterology 2004; 127: S87-S96.
- Welzel TM, Graubard BI, Zeuzem S, El-Serag HB, Davila JA, Mc Glynn KA. Metabolic syndrome increases the risk of primary liver cancer in the United States: a study in the SEER-Medicare Database. Hepatology 2011; 54: 463-471.
- Dyson J, Jaques B, Chattopadyhay D, Lochan R, Graham J, Das D, Aslam T, Patanwala I, Gaggar S, Cole M, Sumpter K, Stewart S, Rose J, Hudson M, Manas D, Reeves HL. Hepatocellular cancer: the impact of obesity, type 2 diabetes and a multidisciplinary team. J Hepatol 2014; 60: 110-117.
- Younossi ZM, Otgonzuren M, Henry L, Venkatesan C, Mishra A, Erario M, Hunt S. Association of nonalcoholic fatty liver disease (NAFLD) with hepatocellular carcinoma (HCC) in the United States from 2004 to 2009. Hepatology 2015; 62: 1723-1730.
- Sanyal AJ, Banas C, Sargeant C, Luketic VA, Sterling RK, Stravitz RT, Shiffman ML, Heuman D, Coterrell A, Fisher RA, Contos MJ, Mills AS. Similarities and differences in outcomes of cirrhosis due to nonalcoholic steatohepatitis and hepatitis C. Hepatology 2006; 43: 682-689.
- Ascha MS, Hanouneh IA, López R, Tamimi TA, Feldstein AF, Zein NN. The incidence and risk factors of hepatocellular carcinoma in patients with nonalcoholic steatohepatitis. Hepatology 2010; 51: 1972-1978.
- Bhala N, Angulo P, van der Poorten D, Lee E, Hui JM, Saracco G, Adams LA, Charatcharoenwitthaya P, Topping JH, Bugianesi E, Day CP, George J. The natural history of nonalcoholic fatty liver disease with advanced fibrosis or cirrhosis: an international collaborative study. Hepatology 2011; 54: 1208-1216.
- Paradis V, Zalinski S, Chelbi E, Guedj N, Degos F, Vilgrain V, Bedossa P, Belghiti J. Hepatocellular carcinomas in patients with metabolic syndrome often develop without significant liver fibrosis: a pathological analysis. Hepatology 2009; 49: 851-859.
- Ertle J, Dechêne A, Sowa JP, Penndorf V, Herzer K, Kaiser G, Schlaak JF, Gerken G, Syn WK, Canbay A. Non-alcoholic fatty liver disease progresses to hepatocellular carcinoma in the absence of apparent cirrhosis. Int J Cancer 2011; 128: 2436-2443.
- Mittal S, El-Serag HB, Sada YH, Kanwal F, Duan Z, Temple S, May SB, Kramer JR, Richardson PA, Davila JA. Hepatocellular carcinoma in the absence of cirrhosis in United States veterans is associated with nonalcoholic fatty liver disease. Clin Gastroenterol Hepatol 2016; 14: 124-131.
- Reddy SK, Steel JL, Chen HW, DeMateo DJ, Cardinal J, Behari J, Humar A, Marsh JW, Geller DA, Tsung A. Outcome of curative treatment for hepatocellular cancer in nonalcoholic steatohepatitis versus hepatitis C and alcoholic liver disease. Hepatology 2012; 55: 1809-1819.
- Grømbǽk L, Vilstrup H, Jepsen P. Hepatitis autoimmune in Denmark: incidence, prevalence, prognosis, and causes of death. A nationwide registry-based cohort study. J Hepatol 2014; 60: 612-617.
- Yeoman AD, Al-Chalabi T, Karani JB, Quaglia A, Devlin J, Mieli-Vergani G, Bomford A, O’Grady JG, Harrison PM, Henegham MA. Evaluation of risk factors in the development of hepatocellular carcinoma in autoimmune hepatitis: implications for follow-up and screening. Hepatology 2008; 48: 863-870.
- Liang Y, Yang Z, Zhong R. Primary biliary cirrosis and cancer risk: a systematic review and meta-analysis. Hepatology 2012; 56: 1409-1417.
- Harada K, Hirohara J, Ueno Y, Nakano T, Kakuda Y, Tsubouchi H, Ichida T, Nakanuma Y. Incidence of and risk factors for hepatocellular carcinoma in primary biliary cirrhosis: national data from Japan. Hepatology 2013; 57: 1942-1949.
- Tomiyama Y, Takenaka K, Kodama T, Kawanaka M, Sasaki K, Nishina S, Yoshioka N, Hara Y, Hino K. Risk factors for survival and the development of hepatocellular carcinoma in patients with primary biliary cirrhosis. Intern Med 2013; 52: 1553-1559.
- Prorok PC. Epidemiologic approach for cancer screening. Problems in design and analysis of trials. Am J Pediatr Hematol Oncol 1992; 14: 117-128.
- Zhang BH, Yang BH, Tang ZY. Randomized controlled trial of screening for hepatocellular carcinoma. J Cancer Res Clin Oncol 2004; 130: 417-422.
- Poustchi H, Farrell GC, Strasser SI, Lee AU, McCaughan GW, Jacob G. Feasibility of conducting a randomized controlled trial for liver cancer screening: is a randomized controlled trial for liver cancer screening feasible or still needed? Hepatology 2011; 54: 1998-2004.
- Trevisani F, De Notariis S, Rapaccini G, Farinati F, Benvegnù L, Zoli M, Grazi GL, Del PP, Di N, Bernardi M; Italian Liver Cancer Group. Semiannual and annual surveillance of cirrhotic patients for hepatocellular carcinoma: effects on cancer stage and patient survival (Italian experience). Am J Gastroenterol 2002; 97: 734-744.
- Todd Stravitz R, Heuman DM, Chand N, Sterling RK, Shiffman RL, Luketic VA, Sanyal AJ, Habib A, Mihas AA, Giles HC, Maluf DG, Coterrell AH, Posner MP, Fisher RA. Surveillance for hepatocellular carcinoma in patients with cirrhosis improves outcome. Am J Med 2008; 121: 119-126.
- Chan ACY, Poon RTP, Ng KKC, Lo CM, Fan ST, Wong J. Changing paradigm in the management of hepatocellular carcinoma improves the survival benefit of early detection by screening. Ann Surg 2008; 247: 666-673.
- Yang JD, Harmsen WS, Slettedahl SW, Chaiteerakij R, Enders FT, Therneau TM, Orsini L, Kim WR, Roberts LR. Factors that affect risk for hepatocellular carcinoma and effects of surveillance. Clin Gastroenterol Hepatol 2011; 9: 617-623.
- Singal A, Volk ML, Waljee A, Salgia R, Higgins P, Rogers MAM, Marrero JA. Meta-analysis: surveillance with ultrasound for early-stage hepatocellular carcinoma in patients with cirrhosis. Aliment Pharmacol Ther 2009; 30: 37-47.
- Gupta S, Bent S, Kohlwes J. Test characteristics of α-fetoprotein for detecting hepatocellular carcinoma in patients with hepatitis C. A systematic review and critical analysis. Ann Intern Med 2003; 139: 46-50.
- Trevisani F, D’Intino PE, Morselli-Labate AM, Mazzella G, Accogli E, Caraceni P, Domenicale M, De Notariis S, Roda E, Bernardi M. Serum alpha-fetoprotein for diagnosis of hepatocellular carcinoma in patients with chronic liver disease: influence of HBsAg and anti-HCV status. J Hepatol 2001; 34: 570-575.
- Bruix J, Sherman M. American Association for the Study of Liver Diseases. Management of hepatocellular carcinoma: an update. Hepatology 2011; 53: 1020-1022.
- EASL-EORTC Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol 2012; 56: 908-943.
- Chang TS, Wu YC, Tung SY, Wei KL, Hsieh YY, Huang HC, Chen WM, Shen CH, Lu CH, Wu CS, Tsai YH, Huang YH. Alpha-fetoprotein measurement benefits hepatocellular carcinoma surveillance in patients with cirrhosis. Am J Gastroenterol 2015; 110: 836-844.
- Santi V, Trevisani F, Gramenzi A, Grignaschi A, Mirici-Cappa F, Del Poggio P, Di Nolfo MA, Benvegnú L, Farinati F, Zoli M, Giannini EG, Borzio F, Caturelli E, Chiaramonte M, Bernardi M; Italian Liver Cancer (ITA.LI.CA) Group. Semiannual surveillance is superior to annual surveillance for the detection of early hepatocellular carcinoma and patient survival. J Hepatol 2010; 53: 291-297.
- Trinchet JC, Chaffaut C, Bourcier V, Degos F, Henrion J, Fontaine H, Roulot D, Mallat A, Hillaire S, Cales P, Ollivier I, Vinel JP, Mathurin P, Bronowicki JP, Vilgrain V, N’Kontchou G, Beaugrand M, Chevret S; Groupe d’Etude et de Traitement du Carcinome Hépatocellulaire (GRETCH). Ultrasonographic surveillance of hepatocellular carcinoma in cirrhosis: a randomized trial comparing 3- and 6-month periodicities. Hepatology 2011; 54: 1987-1997.
- International Consensus Group for Hepatocellular Neoplasia. Pathologic diagnosis of early hepatocellular carcinoma: a report of the International Consensus Group for Hepatocellular Neoplasia. Hepatology 2009; 49: 658-664.
- Roskams T, Kojiro M. Pathology of early hepatocellular carcinoma: conventional and molecular diagnosis. Semin Liv Dis 2010; 30: 17-25.
- Forner A, Vilana R, Ayuso C, Bianchi L, Solé M, Ayuso JR, Boix L, Sala M, Varela M, Llovet JM, Brú C, Bruix J. Diagnosis of hepatic nodules 20 mm or smaller in cirrhosis: prospective validation of the noninvasive diagnostic criteria for hepatocellular carcinoma. Hepatology 2008; 47: 97-104.
- Sangiovanni A, Manini MA, Iavarone M, Romeo R, Forzenigo LV, Fraquelli M, Massironi S, Della Corte C, Ronchi G, Rumi MG, Biondetti P, Colombo M. The diagnostic and economic impact of contrast imaging techniques in the diagnosis of small hepatocellular carcinoma in cirrhosis. Gut 2010; 59: 638-644.
- http://www.acr.org/quality-safety/resources/LIRADS
- Santillan CS; Tang A, Cruite I, Shah A, Sirlin CB. Understanding LI-RADS. A primer for practical use. Magn Reson Imaging Clin N Am 2014; 22: 337-352.
- Wald C, Russo MW, Heimbach JK, Hussain HK, Pomfret EA, Bruix J. New OPTN/UNOS policy for liver transplant allocation: standardization of liver imaging, diagnosis, classification, and reporting of hepatocellular carcinoma. Radiology 2013; 266: 376-382.
- Di Tommaso L, Franchi G, Park YN, Fiamengo B, Destro A, Morenghi E, Montorsi M, Torzilli G, Tommasini M, Terracciano L, Tornillo L, Vecchione R, Roncalli M. Diagnostic value of HSP70, glypican 3, and glutamine synthetase in hepatocellular nodules in cirrhosis. Hepatology 2007; 45: 725-734.
- Di Tommaso L, Destro A, Seok JY, Balladore E, Terracciano L, Sangiovanni A, Iavarone M, Colombo M, Janq JJ, Yu E, Jin SY, Morenghi E, Park YN, Roncalli M. The application of markers (HSP70, GPC3 and GS) in liver biopsies is useful for detection of hepatocellular carcinoma. J Hepatol 2009; 50: 746-754.
- Silva MA, Hegab B, Hyde C, Guo B, Buckels JA, Mirza DF. Needle track seeding following biopsy of liver lesions in the diagnosis of hepatocellular cancer: a systematic review and meta-analysis. Gut 2008; 57: 1592-1596.
- Llovet JM, Brú C, Bruix J. Prognosis of hepatocellular carcinoma: the BCLC staging classification. Semin Liver Dis 1999; 19: 329-338.
- Llovet JM, Di Bisceglie AM, Bruix J, Kramer BS, Lencioni R, Zhu AX, Sherman M, Schwartz M, Lotze M, Talwarkar J, Gores GJ; Panel of Experts in HCC-Design Clinical Trials. Design and endpoints of clinical trials in hepatocellular carcinoma. J Natl Cancer Inst 2008; 100: 698-711.
- Oken MM, Creech RH, Tormey DC, Horton J, Davis TE, McFadden ET, Carbone PP. Toxicity and response criteria of the Eastern Cooperative Oncology Group. Am J Clin Oncol 1982; 5: 649-655.
- http://www.npcrc.org/files/news/ECOG_performance_status.pdf
- Marrero J, Fontana RJ, Barrat A, Askari F, Conjeevaram HS, Su GL, Lok AS. Prognosis of hepatocellular carcinoma: comparison of 7 staging systems in an American cohort. Hepatology 2005; 41: 707-716.
- Cillo U, Vitale A, Grigoletto F, Farinati F, Brolese A, Zanus G, Neri D, Boccagni P, Srsen N, D’Amico F, Ciarleglio FA, Bridda A, D’Amico DF. Prospective validation of the Barcelona Clinic Liver Cancer staging system. J Hepatol 2006; 44: 723-731.
- Guglielmi A, Ruzzenente A, Pachera S, Valdegamberi A, Sandri M, D’Onofrio M, Iacono C. Comparison of seven staging systems in cirrhotic patients with hepatocellular carcinoma in a cohort of patients who underwent radiofrequency ablation with complete response. Am J Gastroenterol 2008; 103: 597-604.
- Bolondi L, Burroughs A, Dufour JF, Galle P, Mazzaferro V, Piscaglia F, Raoul JL, Sangro B. Heterogeneity of patients with intermediate (BCLC B) hepatocellular carcinoma: proposal for a subclassification to facilitate treatment decisions. Semin Liver Dis 2012; 32: 348-359.
- Chevret S, Trinchet JC, Mathieu D, Rached AA, Beaugrand M, Chastang C. A new prognostic classification for predicting survival in patients with hepatocellular carcinoma. Groupe d’Etude et de Traitement du Carcinome Hepatocellulaire. J Hepatol 1999; 31: 133-141.
- A new prognostic system for hepatocellular carcinoma: a retrospective study of 435 patients: the Cancer of the Liver Italian Program (CLIP) investigators. Hepatology 1998; 28: 751-755.
- Leung TW, Tang AM, Zee B, Lau WY, Lai PB, Leung KL, Lau JT, Yu SC, Johnson PJ. Construction of the Chinese University Prognostic Index for hepatocellular carcinoma and comparison with the TNM staging system, the Okuda staging system, and the Cancer of the Liver Italian Program staging system: a study based on 926 patients. Cancer 2002; 94: 1760-1769.
- Kudo M, Chung H, Osaki Y. Prognostic staging system for hepatocellular carcinoma (CLIP score): its value and limitations, and a proposal for a new staging system, the Japan Integrated Staging Score (JIS score). J Gastroenterol 2003; 38: 207-215.
- Yau T, Tang VY, Yao TJ, Fan ST, Lo CM, Poon RT. Development of Hong Kong Liver Cancer staging system with treatment stratification for patients with hepatocellular carcinoma. Gastroenterology 2014; 146: 1691-1700.
- Adhoute X, Penaranda G, Bronowicki JP, Raoul JL. Usefulness of the HKLC vs. the BCLC staging system in a European HCC cohort. J Hepatol 2015; 62: 492-493.
- Lencioni RA, Allgaier HP, Cioni D, Olschewski M, Deibert P, Crocetti L, Frings H, Laubenberger J, Zuber I, Blum HE, Bartolozzi C. Small hepatocellular carcinoma in cirrhosis: randomized comparison of radio-frequency thermal ablation versus percutaneous ethanol injection. Radiology 2003; 228: 235-240.
- Lin SM, Lin CJ, Lin CC, Hsu CW, Chen YC. Radiofrequency ablation improves prognosis compared with ethanol injection for hepatocellular carcinoma < or = 4 cm. Gastroenterology 2004; 127: 1714-1723.
- Lin SM, Lin CJ, Lin CC, Hsu CW, Chen YC. Randomised controlled trial comparing percutaneous radiofrequency thermal ablation, percutaneous ethanol injection, and percutaneous acetic acid injection to treat hepatocellular carcinoma of 3 cm or less. Gut 2005; 54: 1151-1156.
- Shiina S, Teratani T, Obi S, Sato S, Tateishi R, Fujishima T, Ishikawa T, Koike Y, Yoshida H, Kawabe T, Omata M. A randomized controlled trial of radiofrequency ablation with ethanol injection for small hepatocellular carcinoma. Gastroenterology 2005; 129: 122-130.
- Brunello F, Veltri A, Carucci P, Pagano E, Ciccone G, Moretto P, Sacchetto P, Gandini G, Rizzetto M. Radiofrequency ablation versus ethanol injection for early hepatocellular carcinoma. Scand J Gastroenterol 2008; 43: 727-735.
- Germani G, Pleguezuelo M, Gurusamy K, Meyer T, Isgrò G, Burroughs AK. Clinical outcomes of radiofrequency ablation, percutaneous alcohol and acetic acid injection for hepatocellular carcinoma: a meta-analysis. J Hepatol 2010; 52: 380-388.
- Lencioni R. Loco-regional treatment of hepatocellular carcinoma. Hepatology 2010; 52: 762-773.
- Chen MS, Li JQ, Zheng Y, Guo RP, Liang HH, Zhang YQ, Lin XJ, Lau WY. A prospective randomized trial comparing percutaneous local ablative therapy and partial hepatectomy for small hepatocellular carcinoma. Ann Surg 2006; 243: 321-328.
- Huang J, Yan L, Cheng Z, Wu H, Du L, Wang J, Xu Y, Zeng Y. A randomized trial comparing radiofrequency ablation and surgical resection for HCC conforming to the Milan criteria. Ann Surg 2010; 252: 903-912.
- Cucchetti A, Piscaglia F, Cescon M, Colecchia A, Ercolani G, Bolondi L, Pinna AD. Cost-effectiveness of hepatic resection versus percutaneous radiofrequency ablation for early hepatocellular carcinoma. J Hepatol 2013; 59: 300-307.
- Dong W, Zhang T, Wang ZG, Liu H. Clinical outcome of small hepatocellular carcinoma after different treatments: a meta-analysis. World J Gastroenterol 2014; 20: 10174-10182.
- Ikai I, Arii S, Kojiro M, Ichida T, Makuuchi M, Matsuyama Y, Nakanuma Y, Okita K, Omata M, Takayasu K, Yamaoka Y. Reevaluation of prognostic factors for survival after liver resection in patients with hepatocellular carcinoma in a Japanese Nationwide Survey. Cancer 2004; 101: 796-802.
- Bruix J, Castells A, Bosch J, Feu F, Fuster J, García Pagán JC, Visa J, Bru C, Rodés J. Surgical resection of hepatocellular carcinoma in cirrhotic patients: prognostic value of preoperative portal pressure. Gastroenterology 1996; 111: 1018-1022.
- Hsu KY, Chau GY, Lui WY, Tsai SH, King KL, Wu CW. Predicting morbidity and mortality after hepatic resection in patients with hepatocellular carcinoma: the role of Model for End-Stage Liver Disease score. World J Surg 2009; 33: 2412-2419.
- Cucchetti A, Ercolani G, Vivarelli M, Cescon M, Ravaioli M, La Barba G, Zanello M, Grazi GL, Pinna AD. Impact of model for end-stage liver disease (MELD) score on prognosis after hepatectomy for hepatocellular carcinoma on cirrhosis. Liver Transpl 2006; 12: 966-971.
- Teh SH, Christein J, Donohue J, Que F, Kendrick M, Farnell M, Cha S, Kamath P, Nagorney DM. Hepatic resection of hepatocellular carcinoma in patients with cirrhosis: Model of End-Stage Liver Disease (MELD) score predicts perioperative mortality. J Gastrointest Surg 2005; 9: 1207-1215.
- Llop E, Berzigotti A, Reig M, Erice E, Reverter E, Seijo S, Abraldes JG, Bruix J, Bosch J, García Pagán JC. Assessment of portal hypertension by transient elastography in patients with compensated cirrhosis and potentially resectable liver tumors. J Hepatol 2012; 56: 103-108.
- Cescon M, Colecchia A, Cucchetti A, Peri E, Montrone L, Ercolani G, Festi D, Pinna AD. Value of transient elastography measured with Fibroscan in predicting the outcome of hepatic resection for hepatocellular carcinoma. Ann Surg 2012; 256: 706-713.
- Cucchetti A, Cescon M, Golfieri R, Piscaglia F, Renzulli M, Neri F, Cappelli A, Mazzotti F, Mosconi C, Colecchia A, Ercolani G, Pinna AD. Hepatic venous pressure gradient in the preoperative assessment of patients with resectable hepatocellular carcinoma. J Hepatol 2016; 64: 79-86.
- Mazzaferro V, Regalia E, Doci R, Andreola S, Pulvirenti A, Bozzetti F, Montalto F, Ammatuna M, Morabito A, Gennari L. Liver transplantation for the treatment of small hepatocellular carcinomas in patients with cirrhosis. New Engl J Med 1996; 334: 693-699.
- Mazzaferro V, Bhoori S, Sposito C, Bongini M, Langer M, Miceli R, Mariani L. Milan criteria in liver transplantation for hepatocellular carcinoma: an evidence-based analysis on 15 years of experience. Liver Transpl 2011; 17: S44-S57.
- Yao FY, Ferrell L, Bass NM, Watson JJ, Bacchetti P, Venook A, Ascher NL, Roberts JP. Liver transplantation for hepatocellular carcinoma: expansion of the tumor size limits does not adversely impact survival. Hepatology 2001; 33: 1394-1403.
- Mazzaferro V, Llovet JM, Miceli R, Bhoori S, Schiavo M, Mariani L, Camerini T, Roayaie S, Schwartz ME, Grazi GL, Adam R, Neuhaus P, Salizzoni M, Bruix J, Forner A, De Carlis L, Cillo U, Burroughs AK, Troisi R, Rossi M, Gerunda GE, Lerut G, Belghiti J, Boin I, Gugenheim J, Rochling F, Van Hoek B, Majno P; Metroticket Investigator Study Group. Predicting survival after liver transplantation in patients with hepatocellular carcinoma beyond the Milan criteria: a retrospective, exploratory analysis. Lancet Oncol 2009; 10: 35-43.
- Decaens T, Roudot-Thoraval F, Hadni-Bresson S, Meyer C, Gugenheim J, Durand F, Bernard PH, Boillot O, Sulpice L, Calmus Y, Hardwigsen J, Ducerf C, Pageaux GP, Dharancy S, Chazouilleres O, Cherqui D, Duvoux C. Impact of UCSF criteria according to pre and post-OLT tumor features: analysis of 479 patients listed for HCC with a short waiting time. Liver Transpl 2006; 12: 1761-1769.
- Toso C, Asthana S, Bigam DL, Shapiro AMJ, Kneteman NM. Reassessing selection criteria prior to liver transplantation for hepatocellular carcinoma utilizing the scientific registry of transplant recipients database. Hepatology 2008; 49: 832-838.
- Berry K, Ioannou GN. Serum alpha-fetoprotein level independently predicts posttransplant survival in patients with hepatocellular carcinoma. Liver Transpl 2013; 19: 634-645.
- Vibert E, Azoulay D, Hoti E, Iacopinelli S, Samuel D, Salloum C, Lemoine A, Bismuth H, Castaing D, Adam R. Progression of alphafetoprotein before liver transplantation for hepatocellular carcinoma in cirrhotic patients: a critical factor. Amer J Transpl 2009; 10: 129-137.
- Wong LL, Naugler WE, Schwartz J, Scott DL, Bhattacharya R, Reyes J, Orloff SL. Impact of locoregional therapy and alpha-fetoprotein on outcomes in transplantation for liver cancer: a UNOS Region 6 pooled analysis. Clin Transplant 2012; 27: E72-E79.
- Dumitra TC, Dumitra S, Metrakos PP, Barkun JS, Chaudhury P, Deschênes M, Paraskevas S, Hassanain M, Tchervenkov JI. Pretransplantation α-Fetoprotein slope and Milan criteria: strong predictors of hepatocellular carcinoma recurrence after transplantation. Transplantation 2013; 95: 228–233.
- Hameed B, Mehta N, Sapisochin G, Roberts JP, Yao FY. Alpha-fetoprotein level > 1000 ng/mL as an exclusion criterion for liver transplantation in patients with hepatocellular carcinoma meeting the Milan criteria. Liver Transpl 2014; 20: 945-951.
- Piñero F, Marciano S, Anders M, Orozco F, Zerega A, Cabrera CR, Baña MT, Gil O, Andriani O, de Santibañes E, McCormack L, Gadano A, Silva M. Screening for liver cancer during transplant waiting list. Eur J Gastroenterol Hepatol 2015; 27: 355-360.
- Llovet JM, Fuster J, Bruix J. Intention-to-treat analysis of surgical treatment for early hepatocellular carcinoma: resection versus transplantation. Hepatology 1999; 30: 1434-1440.
- Yao FY, Bass NM, Nikolai B, Davern TJ, Kerlan R, Wu V, Ascher NL, Roberts JP. Liver transplantation for hepatocellular carcinoma: analysis of survival according to the intention-to-treat principle and dropout from the waiting list. Liver Transpl 2002; 8: 873-883.
- Clavien PA, Lesurtel M, Bossuyt PM, Gores GJ, Langer B, Perrier A; OLT for HCC Consensus Group. Recommendations for liver transplantation for hepatocellular carcinoma: an international consensus conference report. Lancet Oncol 2012; 13: e11-e22.
- Millonig G, Graziadei IW, Freund MC, Jaschke W, Stadlmann S, Ladurner R, Margreiter R, Vogel W. Response to preoperative chemoembolization correlates with outcome after liver transplantation in patients with hepatocellular carcinoma. Liver Transpl 2007; 13: 272-279.
- Alba E, Valls C, Dominguez J, Martínez L, Escalante E, Lladó L, Serrano T. Transcatheter arterial chemoembolization in patients with hepatocellular carcinoma on the waiting list for orthotopic liver transplantation. Am J Roentgenol 2008; 190: 1341-1348.
- Mazzaferro V, Battiston C, Perrone S, Pulvirenti A, Regalia E, Romito R, Sarli D, Schiavo M, Garbagnati F, Marchianò A, Spreafico C, Camerini T, Mariani L, Miceli R, Andreola S. Radiofrequency ablation of small hepatocellular carcinoma in cirrhotic patients awaiting liver transplantation: a prospective study. Ann Surg 2004; 240: 900-909.
- Graziadei IW, Sandmueller H, Waldenberger P, Koenigsrainer A, Nachbaur K, Jaschke W, Margreiter R, Vogel W. Chemoembolization followed by liver transplantation for hepatocellular carcinoma impedes tumor progression while on the waiting list and leads to excellent outcome. Liver Transpl 2003; 9: 557-563.
- Yao FY, KerIan RK, Hirose R, Davern TJ 3rd, Bass NM, Feng S, Peters M, Terrault N, Freise CE, Ascher NL, Roberts JP. Excellent outcome following down-staging of hepatocellular carcinoma prior to liver transplantation: an intention-to-treat analysis. Hepatology 2008; 48: 819-827.
- Lencioni R, Llovet JM. Modified RECIST (mRECIST) assessment for hepatocellular carcinoma. Semin Liver Dis 2010; 30: 52-60.
- Majno P, Sarasin F, Mentha G, Hadengue A. Primary liver resection and salvage transplantation or primary liver transplantation in patients with single, small hepatocellular carcinoma and preserved liver function: An outcome-oriented decision analysis. Hepatology 2000; 31: 899-906.
- Sposito C, Mariani L, Germini A, Flores Reyes M, Bongini M, Grossi G, Bhoori S, Mazzaferro V. Comparative efficacy of sorafenib versus best supportive care in recurrent hepatocellular carcinoma after liver transplantation: a case-control study. J Hepatol 2013; 59: 59-66.
- Raoul JL, Sangro B, Forner A, Mazzaferro V, Piscaglia F, Bolondi L, Lencioni R. Evolving strategies for the management of intermediate-stage hepatocellular carcinoma: available evidence and expert opinion on the use of transarterial chemoembolization. Cancer Treat Rev 2011; 37: 212-220.
- Burrel M, Reig M, Forner A, Barrufet M, de Lope CR, Tremosini S, Ayuso C, Llovet JM, Real MI, Bruix J. Survival of patients with hepatocellular carcinoma treated by transarterial chemoembolisation (TACE) using Drug Eluting Beads. Implications for clinical practice and trial design. J Hepatol 2012; 56: 1330-1335.
- Lo CM, Ngan H, Tso WK, Liu CL, Lam CM, Poon RT, Fan ST, Wong J. Randomized controlled trial of transarterial lipiodol chemoembolization for unresectable hepatocellular carcinoma. Hepatology 2002; 35: 1164-1171.
- Llovet JM, Real MI, Montañá X, Planas R, Coll S, Aponte J, Ayuso C, Sala M, Muchart J, Solà R, Rodés J, Bruix J; Barcelona Liver Cancer Group. Arterial embolisation or chemoembolisation versus symptomatic treatment in patients with unresectable hepatocellular carcinoma: a randomised controlled trial. Lancet 2002; 359: 1734-1739.
- Llovet JM, Bruix J. Systematic review of randomized trials for unresectable hepatocellular carcinoma: chemoembolization improves survival. Hepatology 2003; 37: 429-442.
- Varela M, Real MI, Burrel M, Forner A, Sala M, Brunet M, Ayuso C, Castells L, Montañá X, Llovet JM, Bruix J. Chemoembolization of hepatocellular carcinoma with drug eluting beads: efficacy and doxorubicin pharmacokinetics. J Hepatol 2007; 46: 474-481.
- Lammer J, Malagari K, Vogl T Pilleul F, Denys A, Watkinson A, Pitton M, Sergent G, Pfammater T, Terraz S, Benhamou Y, Avajon Y, Gruenberger T, Pomoni M, Langerberger H, Schuchmann M, Dumortier J, Chevallier P, Lencioni R; PRECISION V Investigators. Prospective randomized study of doxorubicin-eluting-bead embolization in the treatment of hepatocellular carcinoma: results of the PRECISION V study. Cardiovasc Intervent Radiol 2010; 33: 41-52.
- Vogl TJ, Lammer J, Lencioni R, Malagari K, Watkinson A, Pilleul F, Denys A, Lee C. Liver, gastrointestinal and cardiac toxicity in intermediate hepatocellular carcinoma treated with PRECISION TACE with drug-eluting beads: results from the PRECISION V randomized trial. AJR Am J Roentgenol 2011; 197: W562-W570.
- Malagari K, Pomoni M, Moschouris H, Bouma E, Koskinas J, Stefaniotou A, Marinis A, Kelekis A, Alexopoulou E, Chatziioannou A, Chatzimichael K, Dourakis S, Kelekis N, Rizos S, Kelekis D. Chemoembolization with doxorubicin-eluting beads for unresectable hepatocellular carcinoma: five-year survival analysis. Cardiovasc Intervent Radiol 2012; 35: 1119-1128.
- Sangro B, Salem R. Transarterial chemoembolization and radioembolization. Semin Liver Dis 2014; 34: 435-443.
- Lau WY, Ho S, Leung TWT, Chan M, Ho R, Johnson PJ, Li AK. Selective internal radiation therapy for nonresectable hepatocellular carcinoma with intraarterial infusion of 90yttrium microspheres. Int J Radiat Oncol Biol Phys 1998; 40: 583-592.
- Lewandowski RJ, Kulik L, Riaz A, Senthilnathan S, Mulcahy MF, Ryu RK, Ibrahim SM, Sato KT, Baker T, Miller FH, Omary R, Abecassis M, Salem R. A comparative analysis of transarterial downstaging for hepatocellular carcinoma: chemoembolization versus radioembolization. Amer J Transplant 2009; 9: 1920-1928.
- Sangro B, Bilbao JI, Boan J, Martínez Cuesta A, Benito A, Rodriguez J, Panizo A, Gil B, Inarrairaegui M, Herrero I, Quiroga J, Prieto J. Radioembolization using 90Y-resin microspheres for patients with advanced hepatocellular carcinoma. Int J Radiat Oncol Biol Phys 2006; 66: 792-800.
- Sangro B, Carpanese L, Cianni R, Golfieri R, Gasparini D, Ezziddin S, Paprottka PM, Fiore F, Van Buskirk M, Bilbao JI, Ettorre GM, Salvatori R, Giampalma E, Geatti O, Wilhelm K, Hoffman RT, Izzo F, Inarrairaegui M, Maini CL, Urigo C, Cappelli A, Vit A, Ahmadzadehfar H, Jakobs TF, Lastoria S; European Network on Radioembolization with Yttrium-90 Resin Microspheres (ENRY). Survival after yttrium-90 resin microsphere radioembolization of hepatocellular carcinoma across Barcelona Clinic Liver Cancer stages: a European evaluation. Hepatology 2011; 54: 868-878.
- Salem R, Lewandowski RJ, Kulik L, Wang E, Riaz A, Ryu RK, Sato KT, Gupta R, Nikolaidis P, Miller FH, Yaghmai V, Ibrahim SM, Senthilnathan S, Baker T, Gates VL, Atassi B, Newman S, Memon K, Chen R, Vogelzang RL, Nemcek AA, Resnick SA, Chrisman HB, Carr J, Omary RA, Abecassis M, Benson AB 3rd, Mulcahy MF. Radioembolization results in longer time-to-progression and reduced toxicity compared with chemoembolization in patients with hepatocellular carcinoma. Gastroenterology 2011; 140: 497-507.
- https://clinicaltrials.gov/ct2/show/NCT01381211?term=radioe mbolization+hcc&rank=3.
- https://clinicaltrials.gov/ct2/show/NCT02004210?term=radioe mbolization+hcc&rank=5.
- Llovet JM, Ricci S, Mazzaferro V, Hilgard P, Gane E, Blanc JF, de Oliveira AC, Santoro A, Raoul JL, Forner A, Schwartz M, Porta C, Zeuzem S, Bolondi L, Greten TF, Galle PR, Seitz JF, Borbath I, Häussinger D, Giannaris T, Shan M, Moscovici M, Voliotis D, Bruix J; SHARP Investigators Study Group. Sorafenib in advanced hepatocellular carcinoma. N Engl J Med 2008; 359: 378-390.
- Cheng AL, Kang YK, Chen Z, Tsao CJ, Qin S, Kim JS, Luo R, Feng J, Ye S, Yang TS, Xu J, Sun Y, Liang H, Liu J, Wang J, Tak WY, Pan H, Burock K, Zou J, Voliotis D, Guan Z. Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma: a phase III randomised, double-blind, placebo-controlled trial. Lancet Oncol 2009; 10: 25-34.
- Reig M, Torres F, Rodríguez Lope C, Forner A, Llarch N, Rimola J, Darnell A, Ríos J, Ayuso C, Bruix J. Early dermatologic adverse events predict better outcome in HCC patients treated with sorafenib. J Hepatol 2014; 61: 318-324.
- Marrero JA, Lencioni R, Ye S-L et al. Final analysis of GIDEON (Global Investigation of Therapeutic Decisions in Hepatocellular Carcinoma [HCC] and of Its Treatment with Sorafenib [Sor]) in >3000 Sor-treated patients (pts): clinical findings in pts with liver dysfunction. J Clin Oncol 2013; 31(Suppl.); abstract 4126.
- Iavarone M, Cabibbo G, Piscaglia F, Zavaglia C, Grieco A, Villa E, Cammà C, Colombo M; SOFIA (SOraFenib Italian Assessment) study group. Field-practice study of sorafenib therapy for hepatocellular carcinoma: a prospective multicenter study in Italy. Hepatology 2011; 54: 2055-2063.
- Bruix J, Takayama T, Mazzaferro V, Chau GY, Yang J, Kudo M, Cai J, Poon RT, Han KH, Tak WY, Lee HC, Song T, Roayaie S, Bolondi L, Lee KS, Makuuchi M, Souza F, Berre MA, Meinhardt G, Llovet JM; STORM Investigators. Adjuvant sorafenib for hepatocellular carcinoma after resection or ablation (STORM): a phase 3, randomised, double-blind, placebo-controlled trial. Lancet Oncol 2015; 16: 1344-1354.
- Kudo M, Imanaka K, Chida N, Nakachi K, Tak WY, Takayama T, Yoon JH, Hori T, Kumada H, Hayashi N, Kaneko S, Tsubouchi H, Suh DJ, Furuse J, Okusaka T, Tanaka K, Matsui O, Wada M, Yamaguchi I, Ohya T, Meinhardt G, Okita K. Phase III study of sorafenib after transarterial chemoembolisation in Japanese and Korean patients with unresectable hepatocellular carcinoma. Eur J Cancer 2011; 47: 2117-2127.
Correspondencia: Eduardo Fassio
Av Presidente Illia y Marconi, s/n (CP 1684). El Palomar, Provincia de Buenos Aires, Argentina
Tel.: 4469-9300, Int. 1621-1615
Correo electrónico: efassio@intramed.net
Acta Gastroenterol Latinoam 2016;46(4): 350-374
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE