Jorge A Olmos,1 John E Pandolfino,2 María Marta Piskorz,3 Natalia Zamora,4 Miguel Ángel Valdovinos,5 José María Remes Troche,6 Mauricio J Guzmán,7 Albis Hani,8 Luis R Valdovinos,9 Hannah Pitanga Lukashok,10 Paulo Carvalho,11 Isaac Quintero,12 Eduardo Vesco,13 Ginés Martínez,14 Marcelo F Vela15
1 Jefe del sector de Neurogastroenterología del Hospital de Clínicas “José de San Martín”, Universidad de Buenos Aires, Ciudad Autónoma de Buenos Aires, Argentina.
2 Profesor de Medicina y Jefe de Gastroenterología y Hepatología en la Facultad de Medicina Feinberg de la Universidad Northwestern, Chicago, Estados Unidos.
3 Médica de planta del sector de Neurogastroenterología del Hospital de Clínicas “José de San Martín”, Universidad de Buenos Aires, Ciudad Autónoma de Buenos Aires, Argentina.
4 Médica reumatóloga en Centro Médico Kolff S.A., Pergamino. Coordinadora de guías de práctica clínica de la Sociedad Argentina de Reumatología. Ciudad Autónoma de Buenos Aires, Argentina.
5 Profesor titular de Gastroenterología, Universidad Nacional Autónoma de México. Jefe del Laboratorio de Motilidad GI. Director Training Center México WGO. Departamento de Gastroenterología, Instituto Nacional de Ciencias Médicas y Nutrición “Salvador Zubirán”, Ciudad de México, México.
6 Jefe del Laboratorio de Fisiología Digestiva y Motilidad Gastrointestinal. Director del Instituto de Investigaciones Médico Biológicas de la Universidad Veracruzana, Veracruz, México.
7 Jefe de Unidad de Neurogastroenterología, Servicio de Gastroenterología, Hospital San Martín de La Plata, Buenos Aires, Argentina.
8 Profesora titular de Medicina Interna y Gastroenterología, Hospital San Ignacio – Pontificia Universidad Javeriana, Bogotá, Colombia. Presidenta de la Sociedad Latinoamericana de Neurogastroenterología.
9 Médico Gastroenterólogo y Laboratorio de Motilidad Gastrointestinal, Fundación Clínica Médica Sur, Ciudad de México, México.
10 Jefa del Servicio de Motilidad Digestiva del Instituto Ecuatoriano de Enfermedades Digestivas (IECED), Guayaquil, Ecuador.
11 Coordinador del Curso de Posgrado en Neurogastroenterología IEP. Coordinador del NUFIG – Núcleo de Fisiología Gastrointestinal, Hospital Israelita “Albert Einstein” en San Pablo, Brasil.
12 Médico gastroenterólogo, Jefe de la Unidad de Motilidad del Hospital San Fernando, Ciudad de Panamá, Panamá.
13 Médico gastroenterólogo, Jefe de la Unidad de Neuromotilidad de la clínica Angloamericana. Profesor invitado de la Universidad Nacional Mayor de San Marcos, Lima, Perú.
14 Director de la Unidad de Endoscopía del Centro Comprensivo de Cáncer en San Juan, Puerto Rico. Presidente del Centro de Motilidad Gastrointestinal “Gastrolab”, Caguas, Puerto Rico.
15 Profesor de Medicina y Director de Trastornos Esofágicos. División de Gastroenterología y Hepatología, Mayo Clinic, Scottsdale, Arizona, Estados Unidos.
Acta Gastroenterol Latinoam 2020;50:8-41
Resumen
En los últimos años hubo importantes avances tecnológicos, particularmente en el desarrollo de la manometría esofágica de alta resolución, la impedanciometría y la tecnología FLIP. Este consenso fue desarrollado por un grupo de expertos a partir de una búsqueda sistemática de la literatura y utilizando la metodología GRADE (Grading of Recommendations Assessment, Development and Evaluation) para la evaluación de la calidad de la evidencia y la decisión de la fuerza de la recomendación. Se emitieron recomendaciones en cuanto a la utilidad de la manometría esofágica de alta resolución, la impedanciometría para la medición del tránsito del bolo y la peristalsis efectiva, las pruebas complementarias y la tecnología FLIP.
Palabras claves. Manometría esofágica de alta resolución, impedanciometría, tragos sólidos, tragos viscosos, multitragos, EndoFLIP.
Latin American consensus on esophageal motility
Summary
In recent years, there have been important technological advances, particularly in the development of high-resolution esophageal manometry, impedancemetry and FLIP technology. This consensus was developed by a group of experts from a systematic search of the literature and using the GRADE (Grading of Recommendations Assessment, Development and Evaluation) methodology for the evaluation of the quality of evidence and the decision of the recommendation strength. Recommendations were issued regarding the usefulness of high-resolution esophageal manometry, impedancemetry for the measurement of bolus transit and effective peristalsis, complementary tests and FLIP technology.
Key words. High resolution esophageal manometry, impedancemetry, solid swallows, viscous swallows, multi-swallows, EndoFLIP.
Abreviaturas
HRM: Manometría de alta resolución.
MC: Manometría convencional.
MII: Impedancia intraluminal multicanal.
BT: Tránsito del bolo.
NOD: Disfagia no obstructiva.
IEM: Motilidad esofágica inefectiva.
AIM-HRM: Manometría esofágica de alta resolución con análisis automático de impedancia.
PFI: Índice de flujo de presión.
IBP: Presión intra bolo.
MRS: Degluciones rápidas múltiples.
EEI: Esfínter esofágico inferior.
RDC: Desafío rápido con tragos líquidos.
POEM: Miotomía peroral endoscópica.
IRP: Presión de relajación integrada.
DCI: Contractilidad distal integrada.
DES: Espasmo esofágico distal.
EAV: Escala analógica visual.
IBH: Altura del bolo por impedancia.
AFSL: Air Flow Sphincter Locator.
HRIM: Manometría esofágica de alta resolución combinada con impedanciometría.
MAIpH: Manometría Ambulatoria con Impedanciometría más catéter de pH-metría.
UEG: Unión esófago gástrica.
RAC: Contracciones repetidas anterógradas.
RRC: Contracciones repetidas retrógradas.
DDCR: Contractilidad desordenada o disminuida.
EJGOO: Obstrucción al tracto de salida de la unión esofagogástrica.
Confección de preguntas PICO
Jorge A. Olmos
Marcelo F. Vela
John E. Pandolfino
Hannah Pitanga Lukashok
María Marta Piskorz
Grupo de metodología GRADE
Natalia Zamora
Búsqueda bibliográfica
María Concepción Chávez
Panel de expertos
Jorge A. Olmos (JO)
John E. Pandolfino (JP)
María Marta Piskorz(MMP)
Paulo Carvalho (PC)
Mauricio J. Guzmán (MG)
Albis Hani (AH)
Hannah Pitanga Lukashok (HPL)
Ginés Martínez (GM)
Isaac Quintero (IQ)
José María Remes Troche (JMRT)
Miguel Ángel Valdovinos (MAV)
Luis R. Valdovinos (LV)
Eduardo Vesco (EV)
Marcelo F. Vela (MV)
Redacción de las recomendaciones
Jorge A. Olmos
María Marta Piskorz
Natalia Zamora
Revisores
Marcelo F. Vela
John E. Pandolfino
Resumen de todas las recomendaciones

Introducción
Objetivo y metodología
Este consenso, basado en las mejores evidencias disponibles a la fecha, tiene como objetivo proveer recomendaciones acerca de la realización y utilidad de los métodos diagnósticos para la evaluación de la función motora del esófago, incluyendo la manometría convencional y de alta resolución, las pruebas complementarias efectuadas durante la manometría, la impedanciometría para la valoración del tránsito esofágico y la tecnología EndoFLIP (del inglés functional luminal imaging probe). Este documento está orientado a los médicos gastroenterólogos, los cirujanos y los enfermeros para el beneficio del paciente. No será tratado en esta guía el rol de la metodología antedicha en menores de 18 años.
Equipos involucrados
El consenso latinoamericano de motilidad fue desarrollado por dos grupos con diferentes funciones: un equipo de metodología, encargado de las búsquedas bibliográficas y desarrollo de las guías, y otro grupo compuesto por un panel de expertos, que realizó las preguntas de relevancia clínica y llevó a cabo el proceso de votación.
El equipo de metodología estuvo conformado por 3 metodólogos. Un grupo desarrolló las búsquedas bibliográficas y revisión sistemática de la literatura y un especialista en metodología GRADE (Grading of Recommendations Assessment, Development and Evaluation) lideró la tarea de la confección de las tablas y los apéndices.
El grupo del panel de expertos, conformado por 14 gastroenterólogos, no estuvo involucrado en el proceso de revisión de la literatura.
Ambos equipos declararon no presentar conflictos de intereses relevantes para el desarrollo de las guías.
Desarrollo de preguntas PICO
El panel de expertos llevó a cabo el proceso de la selección de las preguntas relevantes y su armado en formato PICO (población, intervención, comparador y outcomes o desenlaces). Con respecto a las intervenciones y los comparadores, fueron discutidos y seleccionados entre ambos equipos para poder contar con un adecuado balance entre la factibilidad y la relevancia clínica.
Revisión literaria
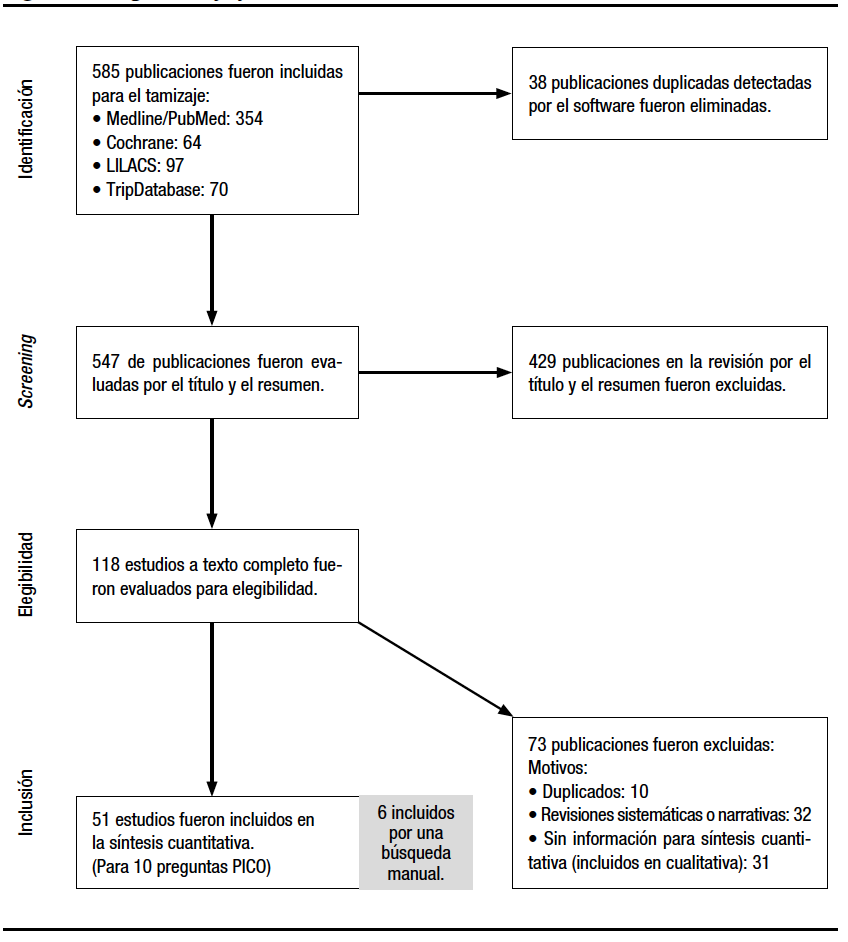
Se realizaron revisiones sistemáticas de la literatura para identificar la evidencia relevante sobre las preguntas PICO. Las bases de datos utilizadas fueron MedLine (PubMed), Lilacs, biblioteca Cochrane y TripDatabase. Las revisiones fueron efectuadas utilizando los términos específicos y las palabras claves (en inglés) relacionadas a los dominios de interés: Deglutition Disorders, High-resolution Manometry alone and with impedance, Conventional Manometry with Impedance, Achalasia, anti-reflux surgery, Multi swallow test, Dysphagia y FLIP Technology. Se excluyeron las revisiones narrativas, los reportes de casos y las editoriales. Las búsquedas fueron realizadas hasta marzo de 2020 (Figura 1).
Selección de estudios: el proceso de selección de artículos fue realizado en Excel. El proceso de tamizaje de los títulos, los resúmenes y los artículos completos, fue llevado a cabo por dos integrantes del equipo, de forma independiente trabajando de a pares, y un tercer revisor resolvió los conflictos de inclusión o exclusión. Los artículos incluidos fueron juzgados y seleccionados para cada pregunta PICO.
Extracción de datos y análisis: la extracción de datos para cada pregunta PICO fue realizada en el programa RevMan.1 La metodología GRADE fue seguida para la inclusión, teniendo en cuenta la mayor calidad de la evidencia, por ejemplo, entre los ensayos clínicos sobre los estudios observacionales. Los desenlaces continuos fueron analizados usando el método de inversa de la varianza en el modelo de efectos aleatorizados reportados como media con 95% del intervalo de confianza y desvío estándar. Los dicotómicos fueron incluidos y analizados por el método Mantel-Haenszel en el modelo de efectos aleatorizados reportados como riesgo de ratios (RR) con 95% del intervalo de confianza. Se adjunta el diagrama de flujo considerando el PRISMA2 para el reporte de los pasos de la revisión sistemática (Figura 1).
Evaluación de calidad y formulación del reporte de evidencia
Se exportó cada carpeta creada en el programa RevMan en el programa GRADE3 para la creación de las tablas con el resumen de la evidencia. La evaluación de la calidad fue realizada siguiendo los estándares de GRADE. Para cada desenlace se incluyó el análisis del riesgo de sesgo, la posibilidad de sesgo de publicación, la inconsistencia, la incongruencia en la dirección de la evidencia y la imprecisión. La metodología GRADE diferencia 4 niveles de calidad basados en el grado de confianza por la cercanía entre la medida de efecto alcanzada (luego del análisis de los estudios agrupados) al efecto real. Por este motivo, la calidad de la evidencia final de cada desenlace es: alta, moderada, baja o muy baja. En ausencia de la evidencia o solo obtenida a través de la opinión de expertos, el desenlace fue catalogado como de calidad muy baja.
De la evidencia a las recomendaciones: cada recomendación fue realizada teniendo en cuenta el balance entre los beneficios de cada tratamiento o método diagnóstico considerado sobre el daño que puede ejercer el uso mismo y la calidad de la evidencia brindada. Una recomendación puede ser a favor o en contra de la intervención y a su vez ser fuerte o débil. De acuerdo a GRADE, esta diferencia radica en que una recomendación es fuerte si la mayor parte del panel de expertos confía en que los beneficios superan ampliamente a los daños o viceversa. Una recomendación débil puede presentar algo de incertidumbre entre el beneficio y el daño o bien poseer una calidad de evidencia baja y muy baja a la hora de realizar la recomendación.
Consenso
El panel de expertos recibió oportunamente el reporte de la evidencia para ser revisado antes de la votación. En la reunión donde se realizaron las recomendaciones, los expertos recibieron, además, un resumen oral con la evidencia seleccionada de cada pregunta PICO. El proceso de votación y la elaboración de cada recomendación fueron realizados en una reunión con los expertos utilizando la plataforma Zoom4 la cual permite votar de forma independiente y anónima. Si en la votación no se alcanzó el consenso del 70% de acuerdo en la primera instancia, los miembros llevaron a cabo discusiones antes de votar nuevamente, con un máximo permitido de 3 votaciones para cada pregunta PICO.
Preguntas PICO
1. En los pacientes con sospecha de trastornos motores esofágicos, ¿es la manometría de alta resolución más eficaz que la manometría convencional en términos de reproducibilidad, velocidad e interpretación?
Calidad de la evidencia:
moderada ⨁⨁⨁○/ alta ⨁⨁⨁⨁
Fuerza de la recomendación: fuerte a favor
La manometría esofágica es una prueba útil para la evaluación de los trastornos motores esofágicos en los pacientes con disfagia, un dolor torácico o una enfermedad por reflujo gastroesofágico. Desde el primer registro de presión esofágica hacia finales de los años 50, el avance tecnológico en los sistemas de manometría ha sido significativo.5 Actualmente existen dos sistemas diferentes para realizar la manometría: la convencional (MC) y la de alta resolución (HRM).6 Asimismo, existen para cada uno de estos sistemas, dos tipos de catéteres: de estado sólido y por perfusión. Estos poseen diferentes características estructurales y mecanismos para lograr el trazado manométrico. El catéter de estado sólido tiene un diámetro de 4,2 mm. Consiste en 36 sensores de cobre, separados por 1 cm. Cada uno tiene 12 sensores integrados en la circunferencia. Esto significa que cada sensor realiza un registro circunferencial desde la hipofaringe hasta el estómago. El catéter por perfusión es un tubo de silicona fenestrado (con 22 a 36 orificios). Cada orificio funciona como un sensor de presión conectado a un transductor externo. El catéter de estado sólido es fácil de calibrar, pero caro; no es confortable para la mayor parte de los pacientes y es muy vulnerable al daño. La información provista por este catéter varía con la temperatura, por lo que se debe realizar una compensación térmica. El catéter por perfusión requiere de una bomba hidroneumática. La presión detectada por cada orificio del catéter es registrada por transductores externos. Este sistema requiere más tiempo de calibración, no es caro y el material es más flexible y confortable para el paciente.6
En la MC el estudio debe realizarse con el paciente en la posición supina, los transductores deben estar dispuestos horizontalmente a la altura del esófago, el agua debe perfundir a una velocidad de 0,5 ml/min y los registros de presión deben realizarse mediante la técnica de extracción por etapas (station pull-through). La HRM puede realizarse en la posición supina o con el paciente sentado. El catéter de HRM genera múltiples registros de la presión de todo el esófago, la hipofaringe y de la presión intragástrica de manera simultánea. Con un programa de cómputo, se generan imágenes a color de la topografía de la presión esofágica. Además, la desinfección del catéter y el mantenimiento del equipo de la HRM es más fácil que en la MC. Por estas diferencias tecnológicas, se ha considerado que la HRM tiene ventajas sobre la MC, ya que es mejor tolerada por el paciente, permite el registro en tiempo real de los eventos motores a lo largo del esófago y facilita el reconocimiento de los patrones anormales de la topografía de la presión esofágica.7 Sin embargo, es una técnica que por su costo más elevado, no está ampliamente disponible en Latinoamérica, en donde aún se sigue utilizando la MC. Por ello, es importante conocer la evidencia científica que demuestre que la HRM es superior a la MC en la evaluación diagnóstica de pacientes con los trastornos motores esofágicos.
Para la confección de la pregunta PICO, se tomó como población a los pacientes con la sospecha de trastornos motores esofágicos, como intervención a la manometría esofágica de alta resolución, como comparador a la manometría convencional y como evento o desenlace a la reproducibilidad, velocidad (el tiempo necesario para completar un estudio) e interpretación.
Esta pregunta fue contestada por seis estudios. Varios aspectos fueron evaluados para comparar el rendimiento de la HRM y la MC en los pacientes con la sospecha de trastornos motores del esófago: la sensibilidad, la especificidad, la precisión diagnóstica, la duración del procedimiento, la reproducibilidad y la facilidad en la interpretación.
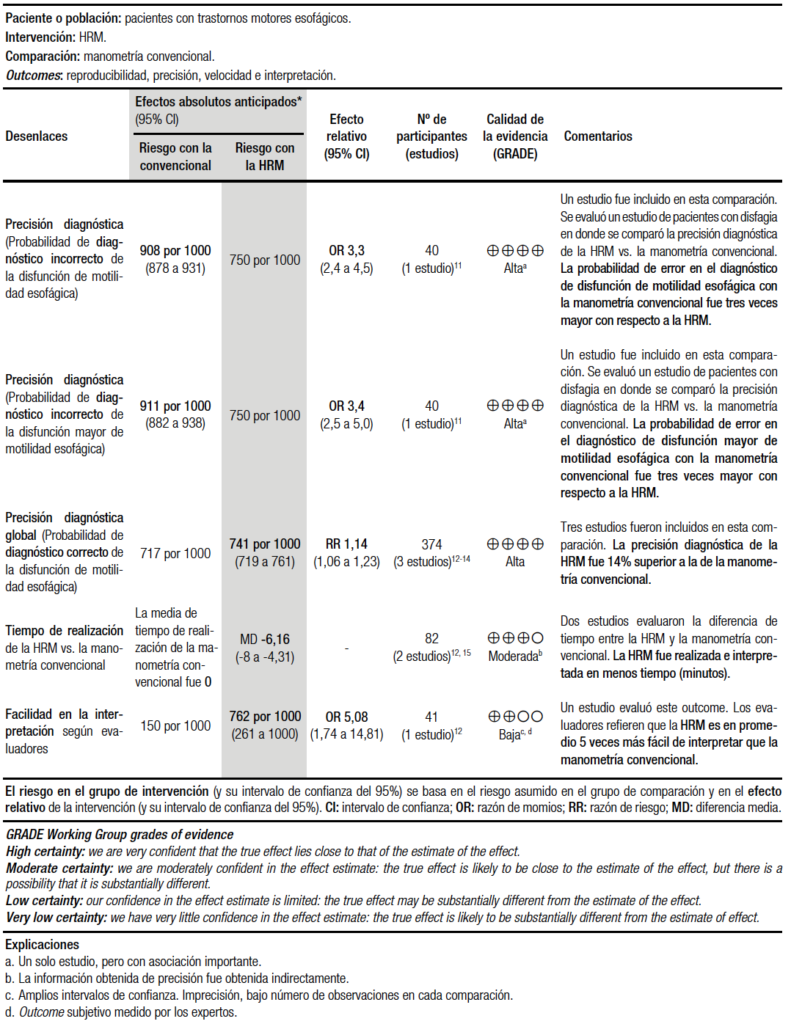
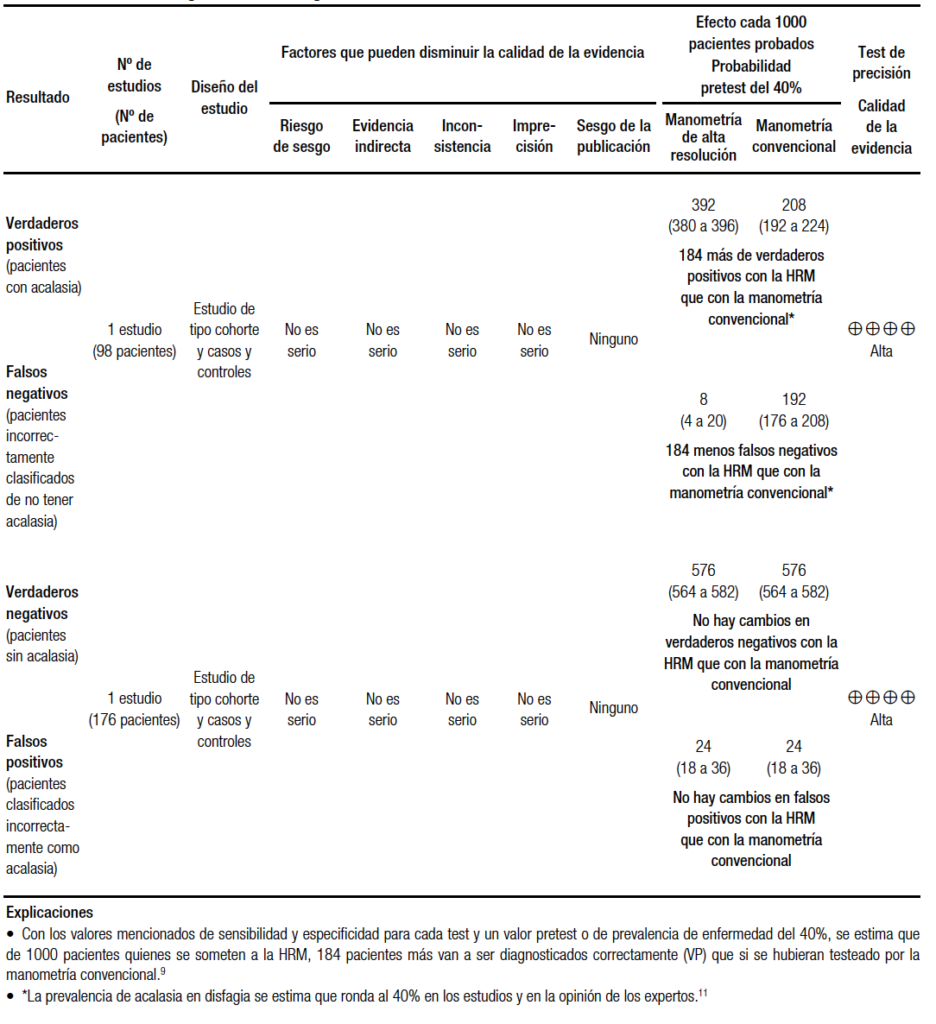
La sensibilidad y la especificidad se estimó en base a un estudio de cohorte de 400 pacientes y 75 controles. A su vez, la prevalencia de la acalasia utilizada fue del 40% según los datos publicados y la discusión entre los expertos.8 La sensibilidad promedio para la HRM fue del 98%, mientras que para la MC fue del 52%; la especificidad para ambos métodos fue del 96% en promedio.9 Esto determina que la HRM detectaría 184 casos más de acalasia que no podrían ser identificados por manometría convencional (Tabla 1a). Una de las razones por las que la HRM es superior a la MC para la detección de la relajación inapropiada de la UEG, es que el fenómeno de pseudorelajación que puede ocurrir con MC, no es visto durante la HRM.10 En otro estudio se demostró que la MC tiene aproximadamente tres veces más posibilidades de error en la precisión diagnóstica para la disfunción de la motilidad esofágica que la HRM.11 Además, basándose en la agrupación de otros tres estudios, la precisión diagnóstica global de la HRM fue 14% superior a la de la MC12-14 (Tabla 1b).
Tabla 1a. Resultados de precisión del test para acalasia
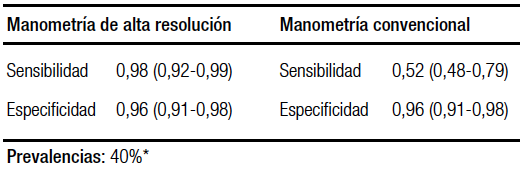
Tabla 1a. Resultados de precisión del test para acalasia
La facilidad en la interpretación y el tiempo de realización de la HRM versus la MC fue estimada en base a un estudio que evaluó a los estudiantes de medicina sin experiencia en las técnicas de manometría esofágica. A todos se les enseñó a interpretar los trazados lineales de la MC y los gráficos espacio-temporales de la topografía de la presión esofágica obtenidos con la HRM. La HRM demostró mayor precisión diagnóstica (89% frente a 86%, p = 0,002) y velocidad en la interpretación (25 frente a 31s, p < 0,001) que la MC.12 Además, en otro estudio, se informó que la duración total del procedimiento se redujo de 42 minutos con la MC a 31 minutos con la HRM.15
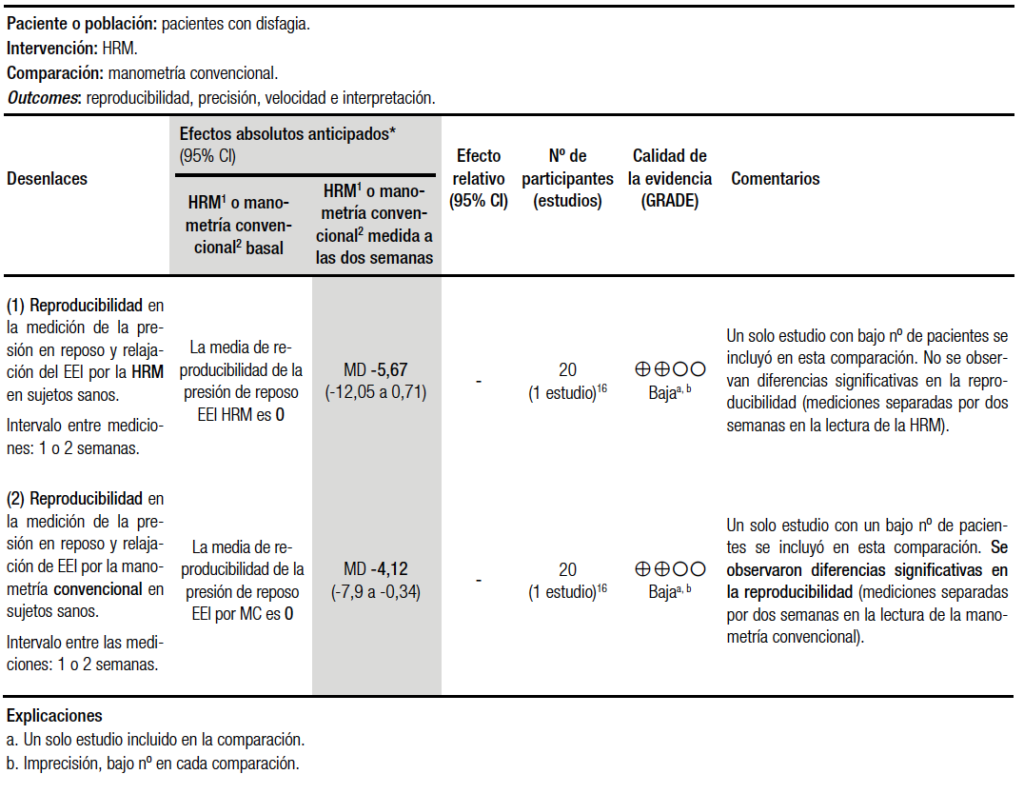
Respecto a la síntesis cuantitativa realizada para estos desenlaces, al agruparse estos dos estudios, se obtuvo que en promedio el tiempo de la realización de la HRM fue de seis minutos menos en comparación con la MC.12, 15 Por otro lado, los autores encontraron que los evaluadores de los gráficos y los trazados manométricos refirieron que la HRM fue en promedio 5 veces más fácil de interpretar que la MC12 (Tabla 1b). Por último, la reproducibilidad de ambas técnicas también fue superior para la HRM que para la MC. Al evaluar la presión en reposo y la relajación del esfínter esofágico inferior, utilizando los mismos gráficos de la HRM y la MC, con una diferencia de 15 días entre ambas mediciones, no se observaron diferencias significativas en ambas mediciones para la HRM. En cambio, con la MC, se encontró una diferencia significativa en el día 15 respecto al día 0, lo que indica menor reproducibilidad16 (Tabla 1b).
Con respecto a la comparación entre la HRM con un catéter por perfusión versus estado sólido, no se encontró información suficiente para realizar un análisis cuantitativo. Un estudio concluyó que las presiones del esfínter esofágico inferior (EEI) y la presión de relajación integrada (IRP) resultaron significativamente menores en el sistema de perfusión en comparación al estado sólido.6 Otro estudio encontró diferencias significativas entre las diferentes métricas evaluadas como la presión del EEI y esfínter esofágico superior, la amplitud y duración de la onda de contracción, IRP, DCI, la latencia distal (DL) por ambos sistemas y poco acuerdo interobservador entre los dos métodos.17 En el mismo sentido, se encontraron presiones del EEI más elevadas con el sistema de estado sólido en relación al sistema de perfusión.18 Por otro lado, en un estudio de la validación de la manometría de alta resolución por perfusión en 50 voluntarios, encontraron que los valores normales para este sistema solo eran algo diferentes a los publicados para el sistema de estado sólido, con un moderado a un buen acuerdo entre los dos sistemas.19
Hay que remarcar que la mayoría de los estudios importantes en la literatura citada en este consenso, fueron realizados con el catéter de alta resolución de estado sólido.
Se logró un grado de acuerdo del 100%, por lo que no hubo dudas entre los expertos, de que la manometría de alta resolución es superior a la convencional ante la sospecha de un trastorno motor del esófago. No existe la información suficiente para determinar si, en la HRM, el sistema de estado sólido es comparable al sistema por perfusión.
2. En los pacientes con la sospecha de trastornos motores esofágicos, ¿la manometría de alta resolución con impedancia (HRIM) aporta más información en la medición del tránsito del bolo y la peristalsis efectiva que la HRM sin impedanciometría?
Calidad de la evidencia: baja ⨁⨁○○
Fuerza de la recomendación: fuerte a favor
En la actualidad, la clasificación de Chicago v3.0 para la HRM permite clasificar los trastornos de la motilidad esofágica en función de los cambios de presión registrados al realizar 10 degluciones líquidas de 5 cc en la posición supina.20 Sin embargo, para evaluar el impacto del trastorno motor sobre el tránsito del bolo se requiere de otro método. El poder realizar simultáneamente la impedanciometría multicanal intraluminal (MII) en combinación con la HRM nos permitiría obtener esta información, ya que muestra una muy buena correlación intra e interobservador con la videofluoroscopia, sin la exposición radiológica de esta última.21, 22 Se han establecido, mediante la MII, parámetros de normalidad del tránsito del bolo completo e incompleto, tanto para los bolos líquidos como para los viscosos. La adición de la impedancia a la HRM puede ser un complemento útil para la evaluación del tránsito del bolo y la efectividad del peristaltismo. Sin embargo, la utilidad clínica y el impacto de los hallazgos de la impedancia sobre la toma de decisiones terapéuticas no son claros.23, 24 El último informe del International Manometry Working Group establece que la adición de la impedancia podría ayudar a complementar el análisis de la función esofágica, pero no se ha comprobado que proporcione nueva información y orientación terapéutica.20
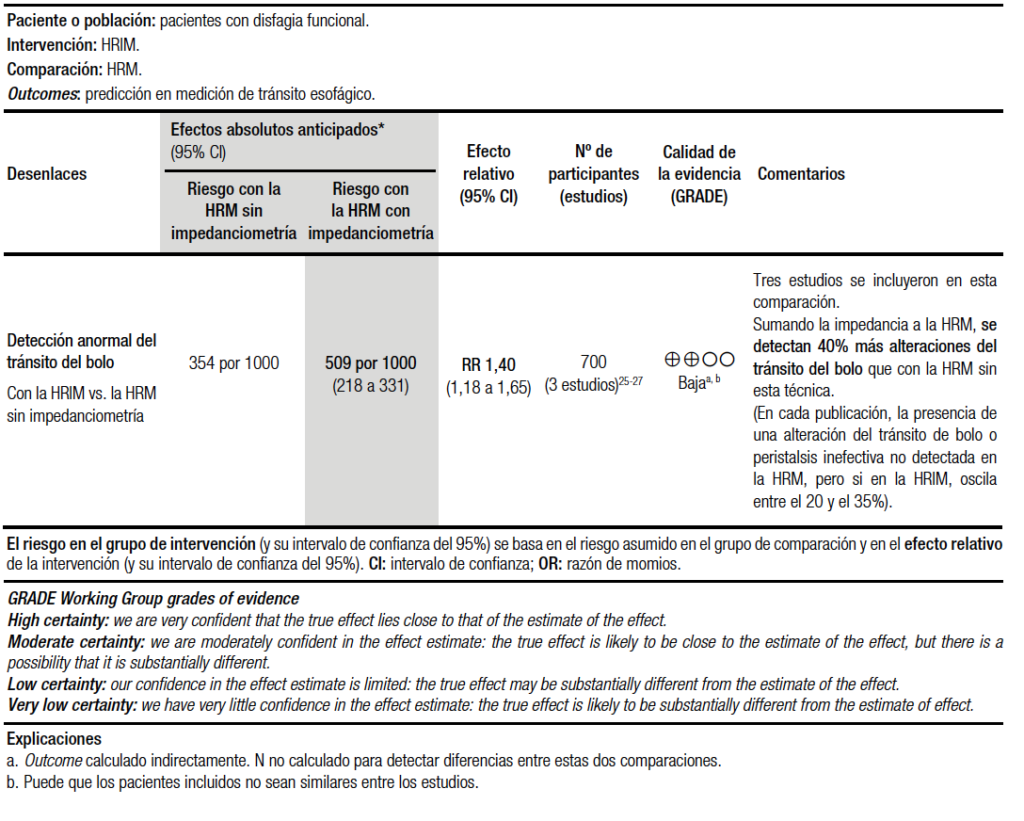
Para la confección de la pregunta PICO se tomó como población a los pacientes con la sospecha de trastornos motores esofágicos, como intervención a la HRM con impedanciometría (HRIM), como comparador a la HRM sin impedanciometría y como evento o desenlace a la medición del tránsito del bolo y la peristalsis efectiva. Con respecto a la síntesis cuantitativa para esta pregunta, se comparó la detección anormal del tránsito del bolo entre la HRIM y la HRM sin este complemento. Aunque con baja calidad de evidencia, tanto en las tres publicaciones independientes como en la agrupación de las mismas, se obtuvo que la HRIM fue capaz de detectar un 40% más de alteraciones del tránsito que la HRM sin impedanciometría25-27 (Tabla 2).
Se analizaron 3 estudios en la bibliografía para responder esta pregunta: en el primer trabajo Conchillo et al. se plantearon como objetivo determinar qué valor aporta la adición de la MII a la MC en la evaluación de los pacientes con disfagia no obstructiva (NOD) definida como disfagia sin anormalidad endoscópica o radiográfica. En este estudio compararon a 40 pacientes con NOD con 42 individuos sanos (controles). Los hallazgos de la manometría en los pacientes con NOD fueron: normal en 20 casos, motilidad esofágica inefectiva en 13, espasmo esofágico distal en 4 y acalasia en 3. La MII mostró el tránsito del bolo anormal, para tragos líquidos y viscosos, en el 35,3% de los pacientes con la manometría normal, en el 66,7% de los pacientes con espasmo esofágico difuso, en el 76,9% de los pacientes con motilidad esofágica inefectiva y en el 100% de los pacientes con acalasia. En estos últimos, la cuantificación del tránsito del bolo fue casi imposible debido a la baja impedancia por la estasis en la luz esofágica. De esta manera se concluye que la MII fue eficaz en identificar los cambios funcionales esofágicos en los pacientes con NOD tanto con la manometría normal como ante la presencia de los trastornos motores, no siendo tan adecuada en la evaluación del extremo más grave del espectro de la disfagia como son los pacientes con acalasia.27 El significado clínico del tránsito del bolo anormal en los pacientes con NOD y la manometría normal no fue evaluado en este estudio.
El segundo trabajo de Koya et al. planteó como objetivo valorar la relevancia clínica del hallazgo de impedanciometría anormal asociada con la manometría normal durante la evaluación de los pacientes con distintos síntomas esofágicos.25 Sobre un total de 576 pacientes con la manometría normal se encontraron 158 pacientes (27%) con impedanciometría anormal. El tránsito del bolo anormal se identificó con más frecuencia para las degluciones de los bolos viscosos que los líquidos (60% para los tragos viscosos, 19% para los tragos líquidos y 21% para ambos). De los pacientes con tránsito del bolo anormal el 23% presentaba como síntoma la disfagia en comparación con el 10% de los que tenían tránsito del bolo normal, siendo esta diferencia estadísticamente significativa (p = 0,0035). De esta manera, el trabajo concluye que el hallazgos de una impedanciometría anormal, incluso en pacientes con la manometría normal, puede ser un indicador sensible de la anormalidad funcional esofágica y se puede expresar con el síntoma de disfagia en estos pacientes.25
En el último trabajo de la evaluación, Nguyen et al. utilizan nuevos parámetros derivados del análisis automatizado de la manometría combinada con la impedanciometría, con el fin de valorar su utilidad en la evaluación de pacientes con NOD y la manometría normal.26 Los parámetros utilizados fueron: presión intrabolo media (IBP), pendiente de IBP, presión pico (PP) y el intervalo de tiempo entre el punto más declive de la impedancia y la presión máxima (TnadImp a Peack Pressure). El análisis automatizado de la impedancio-manometría (AIM) fue realizado mediante un software denominado MATLAB. Con estos parámetros, se determinó el índice del flujo de presión (PFI) el cual refleja la relación entre la fuerza de contracción de la peristalsis y la resistencia al flujo en el esófago distal en cada deglución. Se aplicaron estas mediciones a 42 pacientes con NOD y se las comparó con 24 individuos normales (controles). De los 42 pacientes con NOD, 11 presentaron la manometría normal y de estos, solamente 2 (18%) mostraron evidencias de un flujo anormal en el análisis convencional con la impedanciometría. Al realizar el AIM se encontraron diferencias significativas entre los pacientes y los controles en algunas de las variables explicadas: mayor PNadImp (p < 0,01), IBP (p < 0,01), pendiente de IBP (p < 0,05) y más corto TNadImp PP (p = 0,01). A su vez el PFI de los pacientes con NOD y la manometría normal fue significativamente mayor que en los controles tanto para los bolos líquidos (6,7 vs. 1,2; p = 0,02) como viscosos (27,1 vs. 5,6; p < 0,001) y 9 de los 11 pacientes con NOD y manometría normal tuvieron un PFI anormal. De esta manera, la adición del análisis AIM provee un diagnóstico y una explicación posible en el 95% (40/42) de los pacientes con NOD.26 Por lo tanto, comparando el análisis convencional de la manometría y la impedancia con el análisis integrado AIM, éste se muestra más sensible en la detección de anormalidades sutiles de la función esofágica en los pacientes con NOD y la manometría normal.
Del análisis cualitativo de estas tres publicaciones, se desprende que las mismas no son uniformes, porque utilizan diferentes metodologías en su evaluación como la manometría convencional vs. la HRM y diferentes análisis (habitual vs. AIM).
A su vez, el número limitado de datos y el hecho de que los pacientes incluidos no sean similares entre los estudios determinan una baja calidad de la evidencia para responder la pregunta PICO en cuestión. Además, es importante recalcar que ninguno de los estudios evaluó la respuesta a intervenciones terapéuticas en los pacientes con la manometría normal y la impedanciometría anormal.
En cuanto a la fuerza de la recomendación fuerte a favor, se llegó a un acuerdo del 86%. Los argumentos a favor tuvieron que ver con que, si los costos no son prohibitivos, la MII aporta información clínica y, en ciertas ocasiones, ayuda a definir la conducta terapéutica, a pesar de que existe un déficit en cuanto a la evidencia científica.
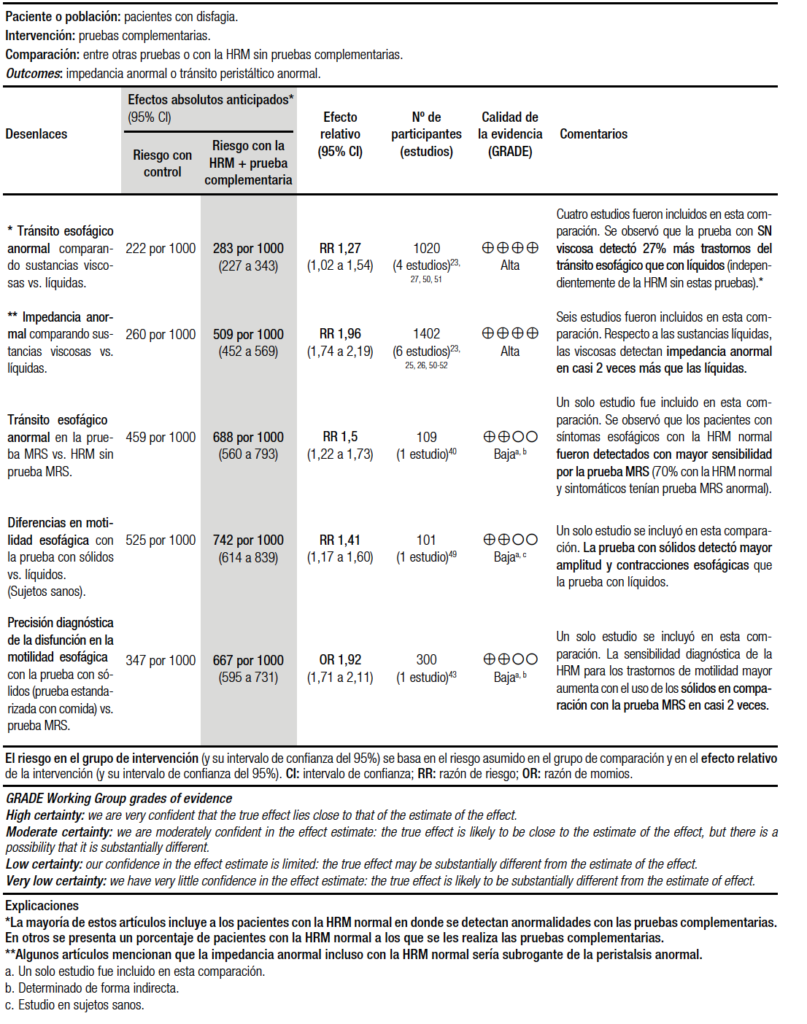
3. En pacientes con disfagia, las pruebas complementarias (los tragos viscosos, los sólidos y los multitrago*), ¿aportan valor diagnóstico y utilidad en comparación con la HRM sin estas pruebas o entre sí?
*Prueba de las degluciones rápidas múltiples (MRS) o desafío rápido con los tragos líquidos (RDC).
Calidad de la evidencia: moderada ⨁⨁⨁○
Fuerza de la recomendación: fuerte a favor
Las pruebas de provocación podrían proveer información clínica más allá de los protocolos habituales de manometría de alta resolución. Adicionalmente a las degluciones de agua tradicionales (5 cc cada 30 segundos), los bolos viscosos y sólidos son utilizados con un incremento en el rendimiento diagnóstico para los procesos obstructivos.28 La mejor indicación de las degluciones rápidas múltiples (200 ml de agua en 30 segundos) es actualmente el diagnóstico de la obstrucción de la unión gastroesofágica (UGE).29 La prueba de las degluciones rápidas múltiples (MRS por sus siglas en inglés) consiste en administrar 5 degluciones de 2 cc de agua con menos de 3 segundos de diferencia. La prueba de MRS provoca la inhibición deglutoria (una intensa inhibición neural periférica y central que resulta en la ausencia de contracción en la porción del músculo liso del cuerpo esofágico con la prolongada y completa relajación del esfínter esofágico inferior), seguida de una fuerte contracción peristáltica luego del último trago, junto con una contracción posterior a la relajación en el esfínter esofágico inferior (EEI). La presencia de una contracción peristáltica, con vigor aumentado inmediatamente después de la secuencia de tragos múltiples, indica la presencia de una buena reserva peristáltica. Al menos tres degluciones son necesarias para evaluar la reserva peristáltica.30 Estudios recientes han demostrado alteraciones en la reserva peristáltica en la enfermedad por reflujo no erosiva, la esclerosis sistémica y la disfagia posoperatoria luego de la cirugía antireflujo;31, 32 además, la respuesta a la prueba de MRS ayuda a diferenciar los subtipos de acalasia.33, 34 Para el desafío rápido con los tragos líquidos (RDC del inglés rapid drink challenge), se le pide al paciente que tome 200 ml de agua lo más rápido posible y se analiza el comportamiento del cuerpo esofágico y la EEI durante e inmediatamente después de la maniobra. La prueba RDC puede revelar anormalidades que no son aparentes durante el protocolo habitual de la HRM con los tragos individuales, como inducir la presurización esofágica en el contexto de una obstrucción sutil del flujo de salida.35
Para la confección de la pregunta PICO, se tomó como población a los pacientes con disfagia, como intervención a las pruebas complementarias (los tragos viscosos, los sólidos, los multitrago, el desafío rápido con tragos líquidos), como comparador a la HRM sin estas pruebas o entre sí y como evento o desenlace al valor diagnóstico y la utilidad.
Como fue establecido para la pregunta PICO número 1, se constató con buena calidad de evidencia que la HRM respecto a la MC proporciona más información y precisión en los pacientes con disfagia. Más aún, para replicar las condiciones fisiológicas de la deglución, se ha propuesto que los estudios que adicionan técnicas complementarias a la HRM (los tragos viscosos, los sólidos, la prueba multitrago o el desafío rápido con tragos líquidos), proporcionan información más certera que sin estos complementos. Varias publicaciones describieron que las pruebas complementarias con los coadyuvantes nombrados, comúnmente descubren nuevas patologías y acentúan las alteraciones subyacentes, especialmente en los pacientes con acalasia, espasmos y obstrucción funcional de la unión gastroesofágica.36-39 La solución viscosa detecta significativamente más anormalidades manométricas que una solución líquida. De hecho, una manometría con degluciones líquidas normal con una impedancia viscosa anormal en un paciente con disfagia indica motilidad esofágica anormal.36-39 En cuanto a la prueba de MRS, las publicaciones disponibles sugieren que la adición de esta técnica evidencia con mayor precisión la obstrucción a nivel de la unión gastroesofágica asociada tanto a la acalasia como a otros trastornos. Además, podría ser más sensible para identificar la reserva peristáltica en los pacientes que no pudieron ser detectados con otras pruebas.34-37, 39-42
Uno de estos estudios se incluyó en la síntesis cuantitativa. En el mismo se observó que los pacientes con síntomas esofágicos que presentaban HRM normal fueron diagnosticados luego de ser sometidos a la prueba MRS (70% con HRM normal y sintomáticos tenían prueba MRS anormal) (Tabla 3).40 Respecto al desafío rápido con los tragos líquidos (RDC), se postuló que de forma similar a las MRS, es una prueba de utilidad para evaluar con precisión la obstrucción de la unión gastro-esofágica en los pacientes con disfagia.43 Asimismo, resultó ser confiable para la medición de la estasis esofágica en los pacientes con acalasia, pudiendo también evaluar adecuadamente la respuesta al tratamiento médico.43-46 En otro estudio en pacientes con disfagia se determinó que en el 17% de los pacientes con la HRM normal y sintomáticos, la adición de RDC pudo detectar anormalidades.35 Tanto en la MC como en la HRM, el esófago responde al desafío de una mayor consistencia del bolo al aumentar la coordinación y la intensidad de las contracciones peristálticas.47, 48
En la presente síntesis cuantitativa, un solo estudio se incluyó en esta comparación. La prueba con sólidos detectó mayor amplitud de contracciones esofágicas cuando fue comparada con la prueba con líquidos en voluntarios sanos (Tabla 3).49 Respecto a la precisión diagnóstica de la disfunción en la motilidad esofágica con pruebas con sólidos, no está claro si se identifican los diagnósticos adicionales en comparación con otras pruebas. Sin embargo, cuando esta prueba fue comparada con la prueba MRS en los pacientes con trastornos de motilidad mayor, se observó en un estudio con moderada calidad de la evidencia que esta prueba aumentó la precisión diagnóstica en casi 2 veces en comparación con la prueba MRS (Tabla 3).43 Además, otras comparaciones fueron incluidas en la síntesis cuantitativa. Se comparó el tránsito esofágico anormal y la impedancia anormal frente a sustancias líquidas y viscosas. Se observó en la agrupación de los estudios incluidos, que la solución viscosa detectó 27% trastornos más del tránsito esofágico y dos veces más la impedancia anormal que con líquidos (Tabla 3).23, 27, 50-52 Es importante recalcar que estos estudios no permiten clarificar si las anormalidades detectadas únicamente con pruebas adicionales representan a patologías no diagnosticadas por los métodos habituales o falsos positivos.
La calidad de la evidencia difiere para las distintas pruebas: desde alta (para pruebas viscosas), hasta baja (para las demás incluidas en la síntesis cuantitativa). Debido a que para todas las pruebas disponibles existe mayor información cualitativa sobre la cuantitativa en forma de pregunta PICO, la calidad sumaria se determinó como moderada.
Se alcanzó un grado de acuerdo del 86%. Los argumentos en contra tuvieron que ver con la falta de sensibilidad de las pruebas complementarias, por lo que existiría una alta tasa de falsos positivos para establecer el diagnóstico de un trastorno motor. Por otro lado, son métodos con alta especificidad, por lo que serían adecuados para descartar un trastorno motor del esófago.
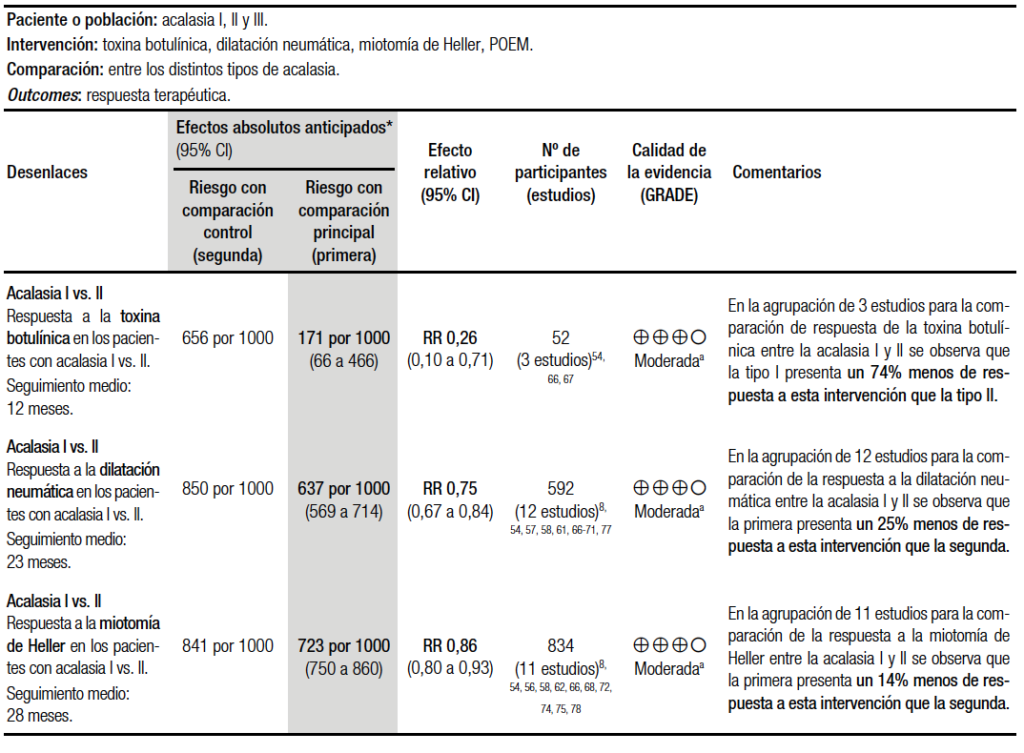
4. ¿Existen diferencias en las respuestas a los tratamientos según el subtipo de acalasia diagnosticada por la HRM?
Calidad de la evidencia: moderada ⨁⨁⨁○
Fuerza de la recomendación: fuerte a favor
La acalasia es un trastorno primario del esófago de etiología desconocida, caracterizada por la degeneración del plexo mientérico, que resulta en una alteración de la relajación de la unión gastroesofágica (UGE), junto con una pérdida de la peristalsis del cuerpo del esófago.53 El advenimiento de la HRM tuvo un fuerte impacto en la mejoría del rédito diagnóstico en la acalasia. En comparación con la MC (sensibilidad 52%), la IRP tiene una sensibilidad del 98% y una especificidad del 96% para diagnosticar la acalasia.9 Los criterios diagnósticos de la acalasia son la relajación incompleta de la unión gastroesofágica y la ausencia de la peristalsis organizada. Han sido definidos tres subtipos de acalasia en base a los hallazgos de la manometría esofágica de alta resolución: tipo I o clásica con baja presión intraesofágica, tipo II con pan presurización esofágica y tipo III con contracciones espásticas de gran amplitud.54
Aunque un 5% de los pacientes con acalasia puede llegar a necesitar una esofagectomía en los estadios finales de la enfermedad,55 la mayoría de los pacientes serán tratados bajo las siguientes modalidades: inyección de la toxina botulínica, dilatación neumática, miotomía de Heller y POEM (miotomía endoscópica peroral). Existen varios estudios que han demostrado que el resultado del tratamiento depende del subtipo de acalasia y esta información puede servir para guiar la elección del tratamiento.56-58
Para la confección de la pregunta PICO, se tomó como población a los pacientes con acalasia, como la intervención a las diferentes modalidades terapéuticas (dilatación neumática, miotomía de Heller, inyección de toxina botulínica y POEM), como comparador a los diferentes subtipos de acalasia y como evento o desenlace a la respuesta al tratamiento.
En resumen, en comparación con el tipo I, se ha demostrado que el tipo II tiene una mejor respuesta a cualquier forma de tratamiento (toxina botulínica, dilatación neumática, miotomía peroral o miotomía de Heller laparoscópica), mientras que el tipo III tiene la peor respuesta a todos los tratamientos.56-61 Por otro lado, un estudio con un análisis retrospectivo evidenció que los pacientes sometidos a la miotomía de Heller laparoscópica tuvieron respuesta similar entre los pacientes con acalasia tipo I y tipo II, mientras que aquellos con acalasia tipo III no tuvieron respuesta favorable.62
Un meta-análisis que incluyó 20 estudios analizó el resultado clínico después de los diferentes tratamientos en los subtipos manométricos. Se observó que las tasas de éxito terapéutico para la acalasia tipo I, II y III fueron del 61, 84 y 31% luego de la dilatación neumática, 81, 92 y 71% después de la miotomía de Heller, y 95, 97 y 93% luego de POEM respectivamente.63
Por otro lado, las guías de la Sociedad Británica de Gastroenterología publicadas en 2018 refieren que por el momento no hay suficiente información para recomendar tratamientos específicos basados en el subtipo, especialmente entre el tipo I o el tipo II.64 En contraste, las guías de la Sociedad Americana de Endoscopia Gastrointestinal (ASGE) publicadas en 2020 declaran que la dilatación neumática, la miotomía de Heller y POEM tienen efectividad comparable para la acalasia tipo I y II, pero POEM es el tratamiento de elección para tipo III.65 Ambas guías sugieren que las decisiones terapéuticas deben basarse en la disponibilidad de los tratamientos, la experiencia local y la elección del paciente.64, 65
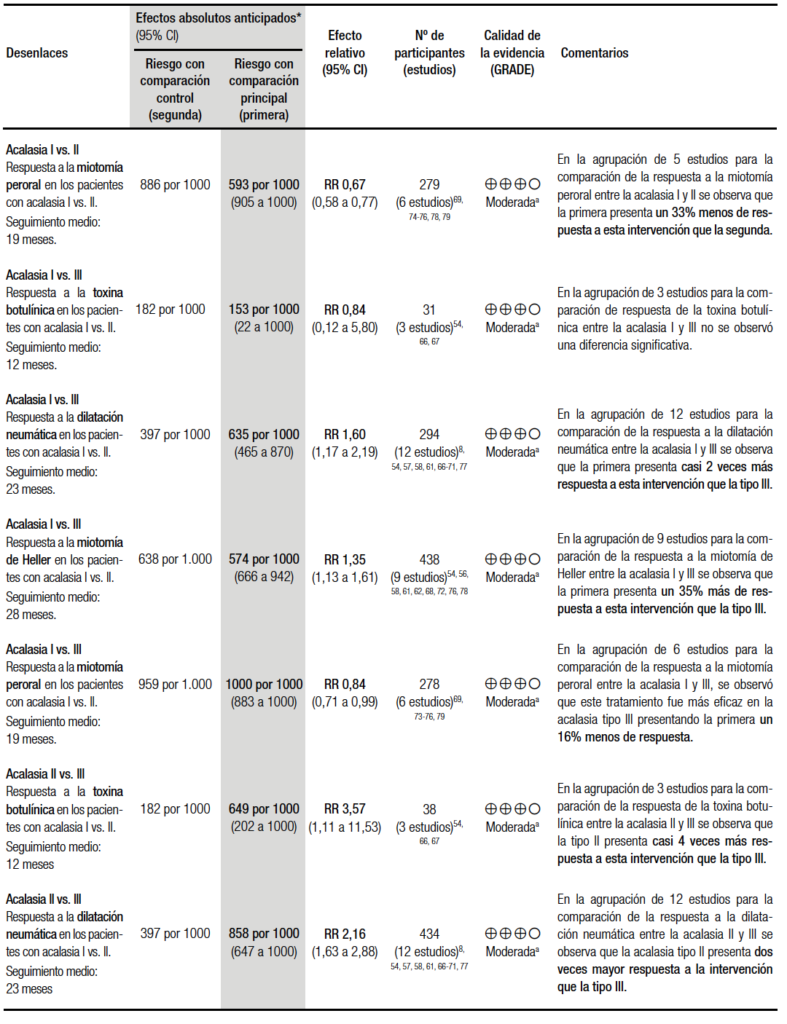
Para la síntesis cuantitativa se analizaron todas las opciones terapéuticas comparadas entre los diferentes subtipos de acalasia. Cuando se compararon los estudios agrupados que analizaron la acalasia tipo I vs. La tipo II, se halló que todas las opciones terapéuticas tuvieron mejor respuesta en la acalasia tipo II respecto a la I (Tabla 4).54, 56-58, 61, 62, 66-79
La comparación entre acalasia tipo I y la III no arrojó diferencias significativas en la respuesta a corto plazo al tratamiento con toxina botulínica.54, 66, 67 En cambio, en el resto de los tratamientos, presentaron significativamente mejor respuesta los demás procedimientos en la acalasia tipo I respecto a la III, salvo con el POEM donde se observó mejor respuesta en la acalasia tipo III (Tabla 4).54, 56-58, 61, 62, 66-78
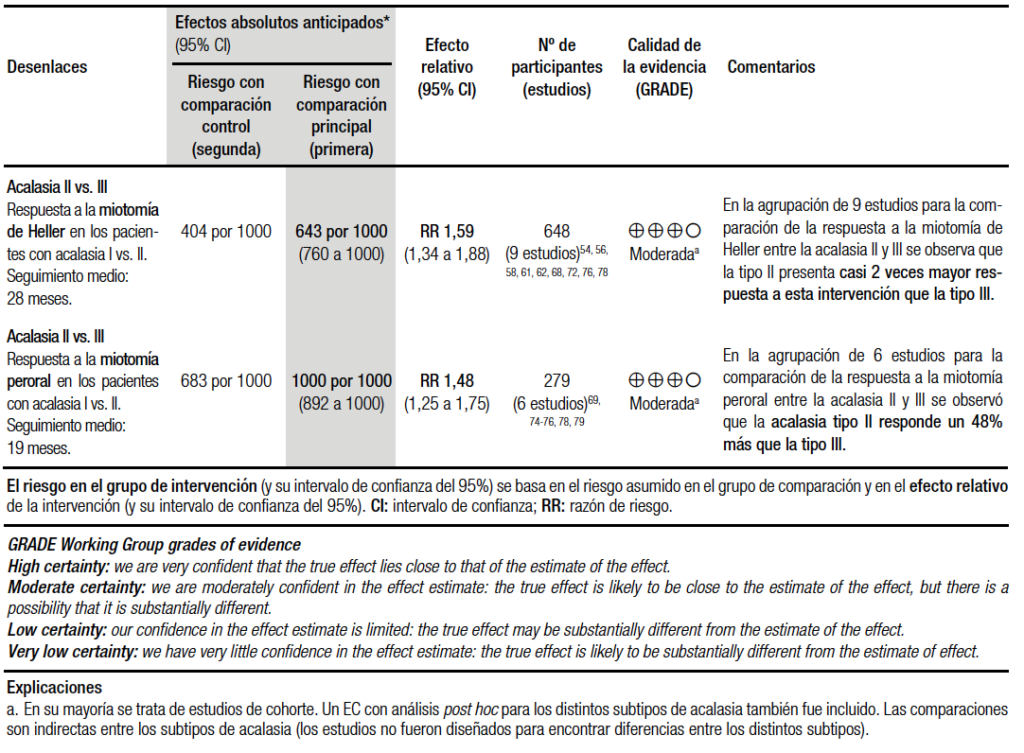
Por último, para la comparación de la acalasia tipo II y III se halló que las cuatro opciones terapéuticas tuvieron considerablemente mejores resultados para la acalasia tipo II que para la tipo III (Tabla 4).54, 56-58, 61, 62, 66-76
Hubo un acuerdo en la recomendación fuerte a favor de un 71% a pesar de que se trata de una pregunta con un adecuado grado de evidencia. Los que votaron en contra aducen que no existe la suficiente evidencia para indicar un tratamiento u otro en los diferentes subtipos, sobre todo en los I y II.
5. En los pacientes con trastornos motores mayores distintos a la acalasia (espasmo esofágico distal, hipercontractilidad o aperistalsis esofágica), ¿provee la manometría de alta resolución (HRM) mayor información funcional que la manometría convencional?
Calidad de la evidencia: moderada ⨁⨁⨁○
Fuerza de la recomendación: fuerte a favor
De acuerdo con la clasificación de Chicago v3.0, son tres los trastornos motores que se caracterizan por tener una IRP normal y cuyas alteraciones motoras se caracterizan por anormalidades en la DL, una DCI elevada o ausencia de peristalsis.20 Estas alteraciones no se observan en los sujetos sanos y, por lo tanto, se consideran trastornos motores mayores; son:
a) Espasmo esofágico distal (DES): es un trastorno de la motilidad poco frecuente y se considera que es consecuencia de las alteraciones en la inervación inhibitoria que produce la disfagia o el dolor torácico. Su definición actual se basa en la presencia de al menos 20% de contracciones prematuras (LD < 4,5 segundos) en presencia de una relajación de la UEG normal.20
b) Aperistalsis esofágica: la aperistalsis o la ausencia de contractilidad se caracteriza por la presencia del 100% de las degluciones fallidas en presencia de una IRP normal.20 Frecuentemente, esta entidad también se ha descrito con el término «esófago de la esclerodermia». Sin embargo, en una revisión reciente, se demostró que solo el 63% de estos pacientes tienen esclerosis sistémica, y que el resto puede tener otras enfermedades autoinmunes (ej. dermatomiositis, polimiositis) y sistémicas (ej. diabetes mellitus tipo 1, sarcoidosis).80 También es importante notar que en un estudio que incluyó a 200 pacientes con esclerodermia, el 25% tuvo una manometría normal.81 La aperistalsis esofágica tiene importancia clínica en los pacientes que se consideran para una funduplicatura o un trasplante de pulmón y es considerada una contraindicación relativa para estos procedimientos quirúrgicos, debido al alto riesgo de disfagia posquirúrgica o pérdida del injerto.82, 83
c) Hipercontractilidad esofágica: este trastorno, también denominado «esófago de Jackhammer», se caracteriza por la presencia de > 20% de degluciones que presenten peristalsis con vigor anormalmente alto, definido por una DCI > 8.000 mmHg/cm/s.20 Clínicamente, la mayoría de los pacientes presenta disfagia y dolor torácico.84 Un metaanálisis reciente demostró que esta entidad representa el 1,97% de los pacientes remitidos HRM y que clínicamente el 6% refiere disfagia, pero de forma interesante el 46% refiere síntomas de ERGE.85
Para la confección de la pregunta PICO, se tomó como población a los pacientes con trastornos motores mayores distintos a la acalasia (espasmo esofágico distal, hipercontractilidad o aperistalsis esofágica), como intervención a la manometría esofágica de alta resolución, como comparador a la manometría esofágica convencional y como evento o desenlace a la información funcional.
Los trastornos de motilidad esofágica distintos a la acalasia (espasmo esofágico distal, hipercontractilidad o aperistalsis esofágica) han evolucionado y han sido estudiado con mayor énfasis en los últimos años. Se postula que la HRM en comparación con la MC, puede proporcionar una mayor información diagnóstica y funcional. La HRM es de importancia ya que puede detectar la latencia distal para su diagnóstico y, por otro lado, evaluar la relajación del esfínter a través de la IRP con mayor confianza en comparación con la MC.13 Además, el DES no puede ocurrir con la obstrucción esofágica distal debido a que la ocurrencia de la misma confirmaría el diagnóstico diferencial de acalasia tipo III.86 De igual manera, las contracciones prematuras frecuentemente halladas en el DES9 y la discriminación entre pacientes con DES respecto de acalasia, también fueron detectados más fácilmente en la HRM que con la MC.87 Respecto al esófago hipercontráctil, la HRM aporta mayor precisión ya que permitió definir tres patrones: múltiples picos sincronizados con la respiración, múltiples picos no sincronizados con la respiración y sin múltiples picos. Los dos primeros se denominaron «esófago Jackhammer», mientras que el último se asoció a la obstrucción de la unión gastroesofágica.88 Por último, en la aperistalsis, que debe ser diferenciada de la acalasia tipo I para un correcto manejo, la HRM ha demostrado superioridad, ya que la relajación de la unión gastroesofágica se observa de manera más confiable que con la MC y el fenómeno de pseudorelajación, que puede resultar en falsos negativos con la MC, no es visto durante la HRM. A su vez, en pacientes donde la HRM y la MC no fueron definitorias, las pruebas complementarias (como la prueba MRS o la prueba con sólidos) pueden ayudar a identificar dicho diagnóstico con mayor precisión.35, 41
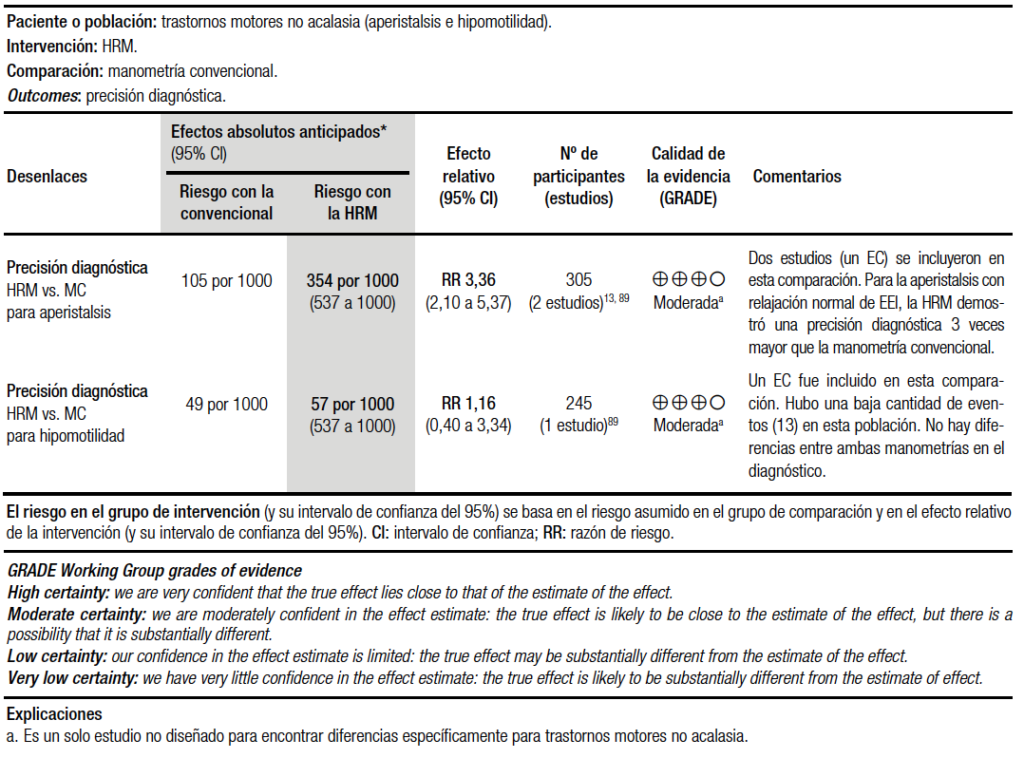
Respecto a la síntesis cuantitativa, solo se halló información extraíble y de calidad moderada para la aperistalsis y la hipomotilidad esofágica. Para la aperistalsis, dos estudios se agruparon en esta comparación. En pacientes con la relajación normal del esfínter esofágico inferior, la HRM demostró tres veces mayor precisión diagnóstica que la manometría convencional.13, 89 Para la hipomotilidad (definida como aperistalsis o motilidad esofágica inefectiva), el mismo ensayo clínico no detectó diferencias significativas entre la HRM y la MC, probablemente debido al bajo número de eventos detectados (Tabla 5).13
En el primer estudio13 36 estudiantes o «aprendices» de la HRM evaluaron 60 trazados, con 4 meses de diferencia, siguiendo un tutorial. Los alumnos calificaron los conocimientos previos de fisiopatología y MC y calificaron la facilidad y la velocidad de interpretación en escalas analógicas visuales (EAV) de 10 cm. Después del tutorial, la precisión del diagnóstico fue significativamente mayor con los gráficos de la HRM con la MC (p < 0,001). La precisión diagnóstica fue mayor con la HRM, particularmente en la aperistalsis (36,1%) y la hipomotilidad del cuerpo esofágico (25,8%).
En el segundo estudio89 245 pacientes con disfagia inexplicable fueron aleatorizados para ser analizados, ya sea con la MC (n = 122) o la HRM (n = 123). Inicialmente se logró un diagnóstico manométrico con mayor frecuencia con la HRM que con la MC (97% frente a 84%, p < 0,01) y se diagnosticaron más pacientes con hipomotilidad con la HRM que con la MC (27% vs. 7%, p < 0,05).
Así pues, de acuerdo a nuestro análisis, es claro que la HRM es una mejor técnica para el diagnóstico de la aperistalsis y la hipomotilidad. Respecto al DES y Jackhammer no hay evidencia suficiente, pero es evidente que son entidades de reciente aparición y que las métricas utilizadas para su comparación con la MC no están disponibles con esta tecnología.
Se logró un acuerdo del 86% con respecto a la fuerza de la recomendación. Se discutió sobre si debería desglosarse según el trastorno motor. Los expertos reconocieron que faltan evidencias. Los que votaron a favor adujeron que la HRM fue fundamental para el diagnóstico de los trastornos motores sin acalasia. El grupo, en general, tuvo la opinión de que Jackhammer es el trastorno motor más desafiante en cuanto a su manejo.
6. En los pacientes con disfagia, ¿son similares la manometría de alta resolución con impedancia versus vaciado radiológico con bario para la detección diagnóstica del vaciamiento esofágico?
Calidad de la evidencia: baja ⨁⨁○○
Fuerza de la recomendación: débil a favor
Disfagia es un síntoma descripto como la dificultad para la deglución o simplemente la presencia de problemas al tragar.44, 90-92 Existen dos tipos: la orofaríngea, que ocurre en el acto de la deglución, y la esofágica, que sucede durante el paso del bolo alimenticio en su camino por el esófago.44, 90, 91 Este síntoma puede presentarse en varias enfermedades que afectan la función motora del esófago de las cuales queremos distinguir a la acalasia. Esta enfermedad se caracteriza principalmente por la ausencia de la peristalsis en el esófago y trastornos en el EEI referentes a su tonicidad y relajación.90, 91 Estas características afectan el movimiento del bolo alimenticio, provocando ulteriormente la retención y su obstrucción, afectando de esta forma al vaciamiento del esófago.90-92 Como parte de las herramientas para el diagnóstico de la acalasia, se encuentran la endoscopía, el esofagograma y la manometría de esófago, la cual es considerada la prueba de elección para el diagnóstico definitivo de la enfermedad.90, 91 A pesar de los atributos de la manometría esofágica, su utilización sigue siendo controversial en el seguimiento de los pacientes con acalasia, papel que fundamentalmente ha jugado el esofagograma con vaciamiento cronometrado.92 La evolución, hoy en día, de la manometría convencional hacia la de alta resolución con impedancia, nos permite un análisis del movimiento del bolo alimenticio, la función del EEI, así como la clasificación (Chicago) en subtipos de los pacientes con acalasia.20 Su tratamiento persigue aliviar la obstrucción a nivel del EEI y, por ende, mejorar el vaciamiento esofágico así como la sintomatología de la disfagia.53, 92
Para la confección de la pregunta PICO, se tomó como población a los pacientes con disfagia, como intervención al vaciamiento esofágico con la manometría de alta resolución con impedancia (HRIM), como comparador al vaciamiento radiológico con bario y como evento o desenlace a la detección diagnóstica.
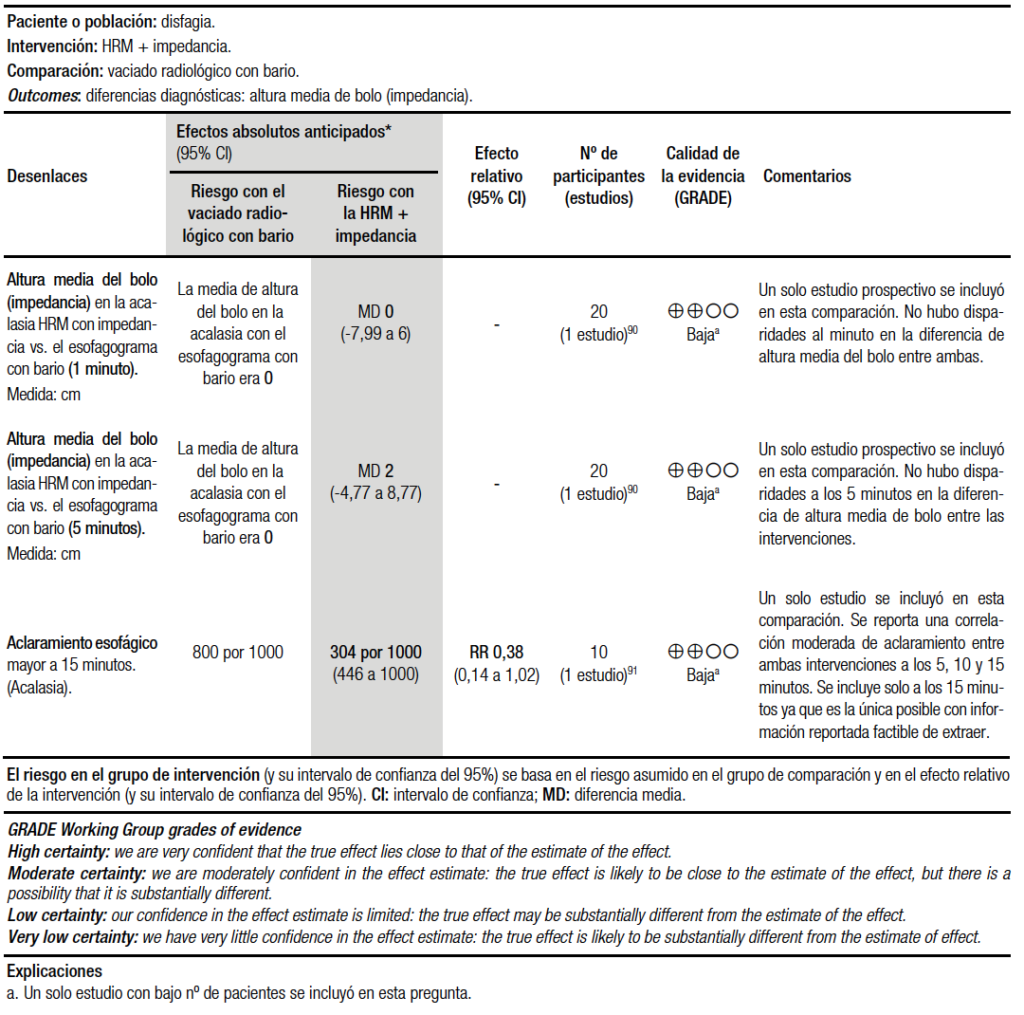
Para la revisión cuantitativa de esta pregunta, se incluyeron dos estudios.90, 91 Estos comparan el vaciamiento esofágico utilizando la HRIM, con el vaciado radiológico con bario. No se encontraron diferencias en la altura media del bolo en la acalasia entre ambas técnicas (Tabla 6). Estos estudios difieren considerablemente en sus fechas de publicación, donde la evolución de la tecnología juega un papel importante en las conclusiones. El bajo número de pacientes también fue un factor limitante en ambos.
El estudio de investigación publicado en el 2014,90 presenta una técnica para evaluar la altura del bolo por la impedancia (IBH), integrando la manometría de alta resolución con la impedanciometría. El análisis de la IBH se hizo mediante la unión de la topografía de la impedancia y su variante espacial. En este trabajo, de manera prospectiva, se incluyeron a 20 pacientes, todos con diagnóstico de acalasia e igualmente divididos en tratados y no tratados. Se les realizó una endoscopia, la manometría de alta resolución con impedancia, el esofagograma cronometrado y un cuestionario de los síntomas de disfagia. Tanto el protocolo del esofagograma cronometrado,92 como la manometría de alta resolución con impedancia, incluían cantidades similares de ingesta de líquido (200 ml de bario y 200 ml de salina respectivamente), seguido de evaluaciones manométricas y radiográficas al minuto y a los cinco minutos. No hubo diferencias significativas entre el promedio de la altura del bolo por impedancia (IBH) y la columna de bario al minuto, ni a los cinco minutos, y la correlación entre ambas medidas a los cinco minutos guardaba una concordancia de 95%.
El segundo estudio de investigación prospectivo, publicado en el 2006,91 incluyó a diez pacientes con acalasia, siete tratados con dilatación neumática y tres no tratados, a los cuales se les realizó simultáneamente la impedanciometría y la videofluoroscopia. Las imágenes fluoroscópicas fueron anotadas para el tiempo de aclaramiento del bolo, definido como el tiempo en que la columna de bario pasaba el segmento por encima del EEI. La altura de la columna de bario fue analizada al minuto, a los cinco, a los diez y a los quince. Hubo diferencias significativas en el tiempo de aclaramiento del bolo del esófago entre la impedanciometría y videofluoroscopia entre los observadores. A pesar de que se pudo observar en un 80% de los sujetos un aclaramiento del bolo mayor de 15 minutos por videofluoroscopia, esto variaba marcadamente en la impedanciometría con un promedio del 37%. En cuanto a la relación entre la altura de la columna de bario y el nivel del líquido por impedanciometría, esta resultó ser pobre a moderada, con un valor débil, pero significativo a los diez minutos.
El primer estudio90 trae a la mesa una metodología novedosa e interesante para integrar a los estudios manométricos de alta resolución con impedancia. Esta metodología, en los aspectos de retención y vaciamiento del bolo, incide favorablemente al compararla con el esofagograma cronometrado. Factores como el número reducido de los pacientes y la ausencia, al día de hoy, de reproducibilidad, mantienen bajo el nivel de evidencia (Tabla 6). Luego de revisar la poca literatura disponible, no pudimos concluir que la manometría de alta resolución con impedancia y el esofagograma sean comparables en cuanto al vaciado esofágico.
El acuerdo logrado en cuanto a la fuerza de la recomendación fue del 93% débil a favor. A pesar de que la impedanciometría es un método fácil de implementar durante la manometría, si se cuenta con la tecnología, aún falta evidencia sobre su utilidad y no brinda la información anatómica de los estudios radiológicos. Sin embargo, de contar con la tecnología, está recomendado implementarla.
7. En los pacientes con reflujo gastroesofágico (RGE), ¿es la manometría de alta resolución (HRM) el método más eficaz para la localización del esfínter esofágico inferior (EEI) comparado con el pH/impedanciometría o el Air-flow Sphincter Locator?
Calidad de la evidencia: baja ⨁⨁○○/ moderada ⨁⨁⨁○
Fuerza de la recomendación: fuerte a favor
Desde que se inició la medición del pH esofágico como herramienta diagnóstica de la enfermedad por reflujo gastroesofágico, esta se convirtió en un método indispensable cuyo resultado es fundamental para la toma de decisiones en el manejo de la enfermedad. Derivado de esta premisa, es importante obtener un registro con la mayor precisión posible y esto depende de colocar el catéter en el lugar correcto. Colocarlo muy lejos del EEI incrementa los resultados falsos negativos y a la inversa, muy cerca del EEI o dentro de la cavidad gástrica, los falsos positivos.
Por consenso, el electrodo de pH debe colocarse a 5 cm del borde superior del EEI, para prevenir el desplazamiento del catéter al estómago durante la deglución y evitar una reducción en la detección de reflujo ácido que ha sido demostrada con el posicionamiento más proximal.94, 95
Ya que el EEI es el punto de referencia para la colocación del electrodo de pH, se han utilizado varias técnicas de localización que incluyen la endoscopía, la radiografía y la fluoroscopia. Sin embargo, la manometría (inicialmente convencional y posteriormente de alta resolución) ha surgido como el método con mayor exactitud para localizar el EEI. Por esto, desde la década del 80 se recomienda colocar el catéter de pH previo estudio de manometría y desde 1996 la Asociación Americana de Gastroenterología (AGA) lo recomienda dentro de sus guías.96
Sin embargo, existen ciertas dificultades como los aumentos en el costo del procedimiento, la incomodidad del paciente y el tiempo del operador, aunado a la falta de disponibilidad de la manometría en todos los centros. Por estos motivos se han buscado métodos alternativos como el pH step up (retiro paulatino del catéter para colocarlo 5 cm por arriba de la distancia en la que se observa el cambio del pH) o el de incorporar un transductor de presión neumático al catéter de pH o pH/impedanciometría para identificar el EEI, conocido como el Air Flow Sphincter Locator (AFSL).97
Para la confección de la pregunta PICO, se tomó como población a los pacientes con ERGE, como intervención a la HRM, como comparador al pH/impedanciometría o AFSL y como evento o desenlace a la localización precisa del EEI.
Múltiples estudios han evaluado la colocación del catéter de pH por medio del método step up comparado a la manometría convencional, mostrando la variabilidad y la falta de exactitud, en algunos casos,98, 99 y de precisión suficiente, en otros.100 Un estudio más reciente mostró que el método step up tiene una precisión aceptable si se realiza con el paciente en posición supina, pero es muy inexacto si está sentado.101
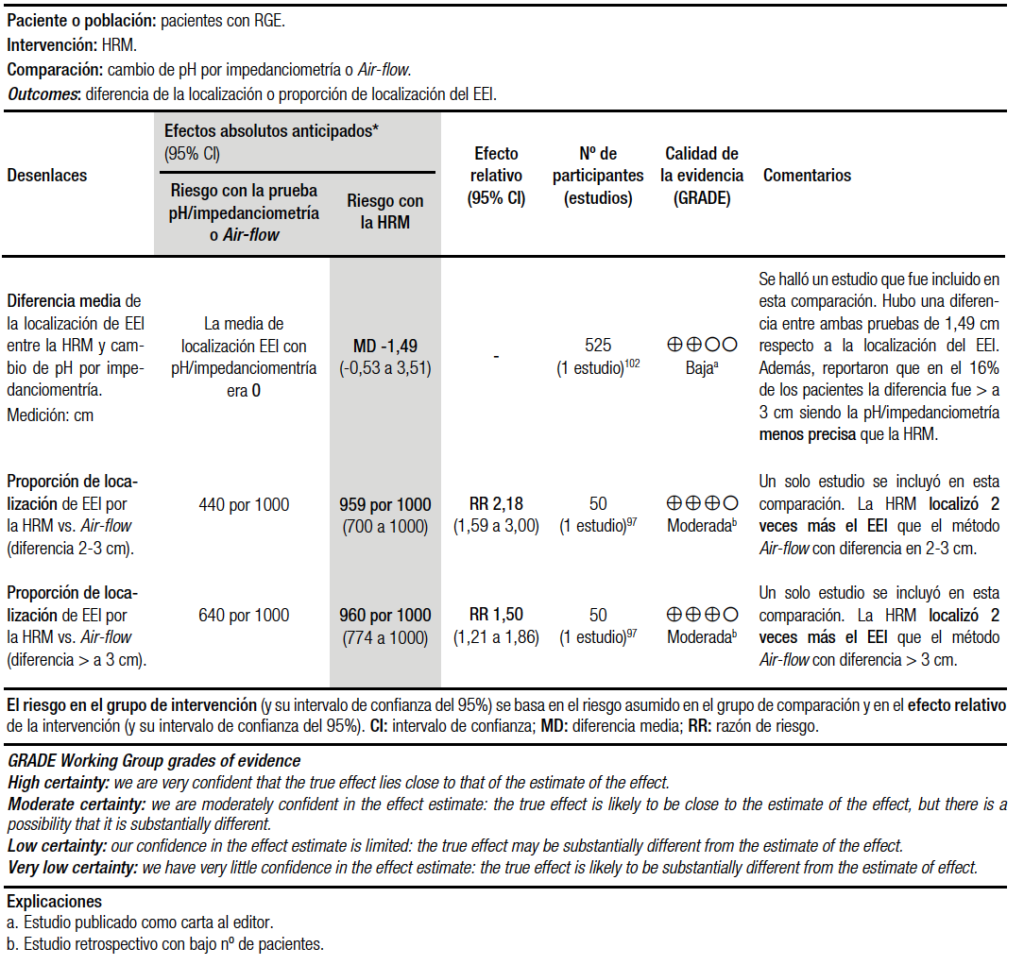
En la síntesis cuantitativa se incluyeron dos estudios. Uno de ellos comparó la HRM para localización del EEI respecto a la técnica step up con baja calidad de evidencia y en el otro se comparó la HRM vs. AFSL para determinar dicha localización con moderada calidad de evidencia. Respecto a la primera comparación, se observaron diferencias significativas. En cambio, la HRM fue superior que el método AFSL para la localización del EEI (Tabla 7).
En el primer estudio se analizaron retrospectivamente a 525 pacientes comparando la HRM y el step up en posición sentado.102 Los autores encontraron que en promedio sólo hubo una diferencia de -1,49 cm (DS 2,02 cm) en relación con la HRM. Sin embargo, ellos reportaron que en el 16% de los pacientes la diferencia fue mayor a 3 cm y que esta diferencia fue significativamente más frecuente en los pacientes más altos.102 Por esto, los autores recomendaron a la HRM como un método más preciso para localizar el EEI. Si bien es cierto que este estudio tiene una buena cantidad de pacientes, sólo fue publicado como una carta al editor lo cual dificulta su análisis, además el step up fue realizado en posición sentado y (como se mencionó anteriormente) es preferible hacerlo en posición supina.
El segundo estudio comparó a la HRM con el método AFSL en 50 pacientes.97 El resumen de la evidencia se puede apreciar en la tabla 2. Los autores encontraron que en el 52% de los pacientes hubo una diferencia entre 2 y 3 cm con relación a la HRM y esta diferencia fue mayor a 3 cm en el 32%. La mayor diferencia se produjo cuando el paciente era portador de una hernia hiatal. Los autores concluyeron que el AFSL no es una alternativa a la HRM para la ubicación del EEI.
En base a la bibliografía descrita, podemos concluir que aún no existe un método alternativo a la manometría de alta resolución para la localización del EEI. Sin embargo, cabe mencionar un estudio reciente publicado en el 2019 que utilizó pH/impedanciometría para localizar el EEI, basándose en cambios en el valor de la impedancia durante el retiro paulatino del catéter (step up por impedancia).103 Este estudio comparó al step up por impedancia con la HRM en 100 pacientes, encontrando una diferencia de ± 1 cm en el 62% y de ± 2 en el 84%, lo que llevó a los autores a concluir que este método, aunque menos preciso que la HRM, puede ser considerado cuando la manometría no está disponible o no es tolerada por el paciente.
El acuerdo logrado en cuanto a la fuerza de la recomendación fue del 85%. Los argumentos en contra tienen que ver con la incomodidad para el paciente de tener que realizarse un estudio adicional con un catéter. Los argumentos a favor se relacionan con la precisión del método, aunque no necesariamente se precisaría la HRM, pudiendo lograr un resultado similar con la MC.
8. En pacientes que van a ser sometidos a una cirugía antirreflujo, ¿una pobre respuesta a la prueba multitrago está asociada a la disfagia postquirúrgica?
Calidad de la evidencia: baja ⨁⨁○○
Fuerza de la recomendación: débil a favor
La disfagia es una de las complicaciones más temidas después de una cirugía antirreflujo. Su diagnóstico oportuno y su manejo representan un desafío, especialmente en el periodo posquirúrgico temprano. La prevalencia de la disfagia poscirugía antirreflujo se estima entre el 15 y el 20% en el período postquirúrgico temprano (primeras 6 semanas) y en un 10% en el período postquirúrgico tardío.104
La manometría esofágica previa a una cirugía antirreflujo es capaz de identificar situaciones donde es evidente que existen defectos peristálticos mayores. Sin embargo, también puede identificar secuencias motoras intermitentes con poca o baja amplitud intercaladas con secuencias fallidas, cuya significancia clínica aún no está claramente demostrada.105, 106
El origen de la disfagia poscirugía antirreflujo es multifactorial. Además de la motilidad del esófago, otros factores que pueden estar involucrados incluyen el tipo, la longitud y el diámetro de la fundoplicatura, así como la experiencia y volumen de procedimientos del cirujano. Por esto, no sorprende que múltiples estudios hayan demostrado que los hallazgos de la manometría con o sin impedancia no pueden predecir la disfagia posoperatoria.107-109 No obstante, estudios recientes sugieren que la prueba de degluciones rápidas múltiples (MRS) puede tener utilidad para predecir disfagia luego de la cirugía antirreflujo.40, 110
Para la confección de la pregunta PICO, se tomó como población a los pacientes que van a ser sometidos a una cirugía antirreflujo, como intervención a los resultados de las pruebas multitragos (MRS), como comparador a la buena vs. mala peristalsis y como evento o desenlace a la disfagia posquirúrgica.
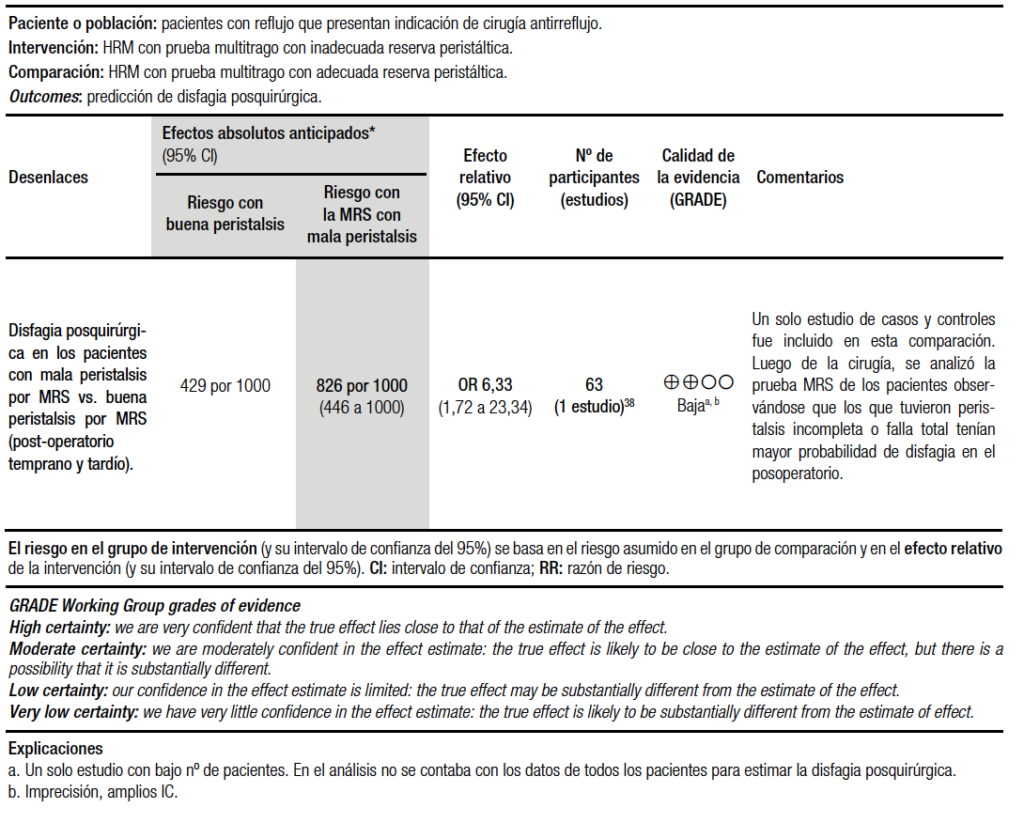
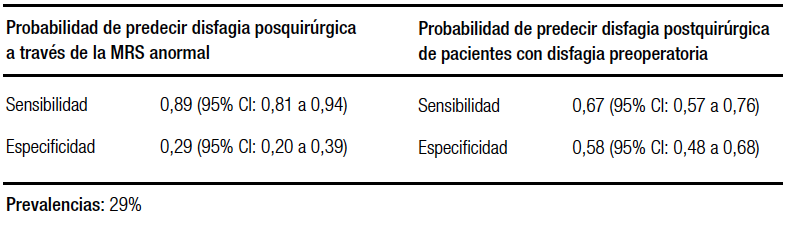
En el análisis cuantitativo, se incluyó un artículo realizado en una población de 63 pacientes.38 La prevalencia de la motilidad esofágica inefectiva considerada fue del 29% según Lee.111 Se realizó un análisis de precisión diagnóstica, en el que se comparó la precisión de tener una MRS anormal con la sensibilidad y especificidad conocidas de la disfagia prequirúrgica para predecir disfagia posquirúrgica. Los resultados evidenciaron que para una sensibilidad del 89% y especificidad del 29% para la prueba MRS anormal vs. una sensibilidad de 67% y especificidad de 58% para la disfagia prequirúrgica, la prueba MRS captó 64 más verdaderos positivos con mayor número de falsos positivos206 debido a su baja especificidad (Tabla 8b).24
A su vez, en este estudio de 63 pacientes sometidos a una cirugía antirreflujo a los que se les realizó la MRS luego de la cirugía, se evidenció que 14 pacientes (22,2%) presentaron la MRS normal (buena peristalsis). Los pacientes con MRS anormales (46/63) (peristalsis incompleta o falla total) tenían 6,33 veces de probabilidad de presentar disfagia en el período posquirúrgico (el análisis incluyó a pacientes tanto del período temprano como tardío) (Tabla 8a).38 Basándose en estos resultados, se puede decir que la respuesta anormal a la MRS se asocia a una probabilidad aumentada de la disfagia posoperatoria en los pacientes a quienes se les realiza la cirugía antirreflujo. Por lo tanto, las MRS son un complemento valioso al protocolo estándar de la HRM para las pruebas de función esofágica preoperatorias, antes de la cirugía antirreflujo.
El acuerdo en cuanto a la fuerza de recomendación fue del 71%. Se deja en claro que se trata de una información importante para el cirujano que debe realizar la funduplicatura, ya que podría modificar la técnica quirúrgica, a pesar de que aún hay bajo nivel de evidencia.
9. En los pacientes con la sospecha de rumiación, ¿es la manometría de alta resolución con impedancia (HRIM) con protocolo posprandial más efectiva que otra técnica o sin este protocolo?
Calidad de la evidencia: baja ⨁⨁○○
Fuerza de la recomendación: fuerte a favor
El síndrome de rumiación es un trastorno funcional gastrointestinal de etiología desconocida caracterizado por la regurgitación hacia la boca, muchas veces repetitiva, de la comida recientemente ingerida en ausencia de anormalidades estructurales.112
En los últimos años, este síndrome ha cobrado interés por ser uno de los trastornos funcionales a tener en cuenta en los diagnósticos diferenciales ante la presencia de pacientes con vómitos persistentes y reflujo gastroesofágico con regurgitación predominante.113 El diagnóstico de este síndrome se basa en datos clínicos (Criterios de Roma IV).114 Si bien los criterios clínicos permiten hacer el diagnóstico, éste se soporta con métodos objetivos. Los episodios de rumiación han sido demostrados y caracterizados mediante diferentes estudios funcionales digestivos, siendo la manometría esofágica de alta resolución combinada con impedancia (HRIM) uno de los métodos más utilizados actualmente.112 Mediante HRIM, se puede objetivar un aumento en la presión intragástrica, que debe ser mayor a 30 mmHg, coincidente con el inicio del movimiento retrógrado del contenido gástrico hacia el esófago en la impedanciometría.115 Se ha propuesto a la HRIM con protocolo posprandial como un método de elección para identificarlo. En estos pacientes, la pH/impedanciometria simultánea proporcionaría información adicional de confirmación y diagnóstico (confirmando la regurgitación posprandial de fluidos y diferenciaría las variantes asociadas con eructos y reflujo ácido verdadero).113, 115
Para la confección de la pregunta PICO, se tomó como población a los pacientes con la sospecha de rumiación, como intervención a la HRIM con protocolo posprandial, como comparador a otra técnica o sin este protocolo y como evento o desenlace a la efectividad para el diagnóstico.
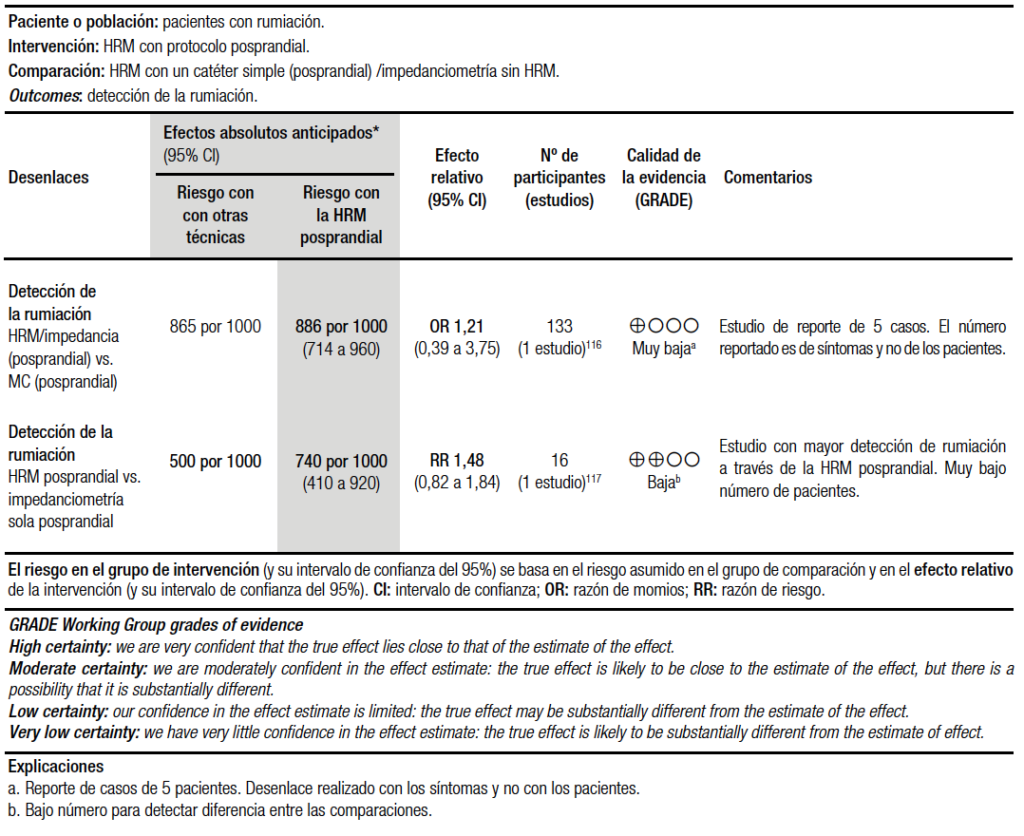
En la síntesis cuantitativa de esta pregunta se incluyeron dos estudios de baja calidad de la evidencia que compararon la HRIM posprandial vs. la manometría ambulatoria con la impedanciometría y pH-metría (MAIpH)116 o la HRM sin impedanciometría.117 En ambas comparaciones, la HRIM con protocolo posprandial marcó una tendencia a detectar más casos de rumiación que las dos técnicas de control, pero sin ser estadísticamente significativa (probablemente debido al bajo número de pacientes incluidos en los estudios, siendo, además, uno de ellos un reporte de casos) (Tabla 9).
En el primer trabajo de la tabla se analizan en 5 pacientes, con diagnóstico clínico de rumiación (Roma III), 96 síntomas reportados mediante la MAIpH y 37 síntomas reportados mediante la HRIM. La MAIpH identificó 85 de los 96 episodios reportados (índice sintomático: 89%) y la HRIM 32 de los 37 (índice sintomático: 86%). La HRIM permitió describir con más detalle los eventos de rumiación y los mecanismos involucrados con una buena correlación con los síntomas reportados por los pacientes. Una observación importante sobre este trabajo es que el desenlace fue medido con síntomas (133 síntomas) y no con pacientes.116
En el segundo trabajo que muestra la tabla, se logró confirmar el diagnóstico en 8 de los 16 pacientes con sospecha clínica de rumiación (Roma III) observando los cambios típicos en la HRIM después de someterlos al protocolo posprandial y observación durante 1 hora. Los autores establecieron que el diagnóstico clínico tendría un valor predictivo positivo del 50% para rumiación y la HRIM una especificidad del 50% con un valor predictivo positivo del 66,6%.117
La disponibilidad de la HRIM y la necesidad de considerar a la rumiación dentro de los diagnósticos diferenciales en los pacientes con regurgitación posprandial, vómitos y reflujo refractario nos exige un desafío en nuestra práctica clínica en los centros de referencia de neurogastroenterología. Si bien en nuestra revisión, en el análisis cuantitativo no se encontraron diferencias estadísticamente significativas para establecer a la HRIM como el método más efectivo para el diagnóstico de la rumiación, la bibliografía revisada y la experiencia de los diferentes centros sugieren a este estudio funcional con protocolo posprandial como el método objetivo que mejor nos permitiría confirmar y clasificar a la rumiación y de esta manera otorgar el tratamiento adecuado a cada subtipo.113, 115, 118
El acuerdo en cuanto a la fuerza de la recomendación fue del 71%. Los argumentos a favor tienen que ver con que es el único método que sirve para documentar objetivamente el problema, considerando que la clínica tiene un valor predictivo positivo de sólo el 50%. Además, el patrón manométrico de la rumiación es fácilmente reconocible. En cuanto a las limitaciones o los asuntos por resolver, se discutió la falta de estandarización del protocolo posprandial.
10. En los pacientes con disfagia con manometría de alta resolución (HRM) normal, ¿aporta información diagnóstica aplicar la sonda de imagen funcional luminal (FLIP)?
Calidad de la evidencia: moderada ⨁⨁⨁○
Fuerza de la recomendación: fuerte a favor
La disfagia esofágica es un síntoma frecuente.119 El primer paso en el abordaje de este síntoma consiste en descartar las causas obstructivas mediante una endoscopía de tubo digestivo superior. Una vez descartada una alteración obstructiva que explique la sintomatología, el paso a seguir es realizar los estudios de fisiología digestiva.119 Actualmente la HRM es el estándar de oro para la evaluación de la función motora del esófago y, además, nos permite su clasificación de acuerdo a Chicago v3.0.20 El sistema de EndoFLIP (por sus siglas en inglés: sonda de imagen luminal funcional) es una nueva tecnología. Tiene como objetivo evaluar en tiempo real las propiedades biomecánicas del cuerpo del esófago y la dinámica de la unión esófago gástrica (UEG) (incluye el comportamiento del esfínter esofágico inferior) en tiempo real mediante una imagen digital, utilizando planimetría por impedancia de alta resolución.120 A diferencia de la HRM que recaba información sobre las presiones endoluminales, durante la peristalsis primaria inducida por la deglución, el sistema del EndoFLIP mide el área de sección transversal durante la distensión controlada por volumen del esófago además de la presión, lo que permite evaluar el comportamiento de la UEG y las contracciones del cuerpo esofágico durante la peristalsis secundaria inducida por la distensión.121 El parámetro de mayor utilidad en el EndoFLIP es la distensibilidad de la UEG. Ésta es calculada con el área de sección transversal y la presión. Una distensibilidad < 2 mm2/Hg nos permite identificar las patologías relacionadas con la relajación incompleta de la UEG incluyendo la acalasia y la obstrucción del tracto de salida de la UEG.122 Además de la distensibilidad, el EndoFLIP nos permite valorar la peristalsis inducida por distensión o peristalsis secundaria. Se han descrito cuatro patrones de respuesta contráctil: las contracciones repetidas anterógradas (RAC), las contracciones repetidas retrógradas (RRC), la contractilidad desordenada o disminuida (DDCR) y ausencia de contractilidad.122 Las RAC son el patrón característico de los controles asintomáticos,123 mientras que las RRC se presentan con mayor frecuencia en las patologías esofágicas.124 El EndoFLIP se ha utilizado en: a) el estudio del paciente con disfagia no obstructiva, b) la valoración intraoperatoria del EEI en la ERGE con la finalidad de ajustar la funduplicatura reduciendo el riesgo de la disfagia posoperatoria o funduplicatura fallida, c) durante la miotomía laparoscópica o POEM con el fin de disminuir la incidencia de la miotomía incompleta o fallida, d) en la esofagitis eosinofílica. Existe además un balón de EndoFLIP modificado para el tratamiento que permite realizar la dilatación esofágica, conocido como el sistema EsoFLIP.122, 125
Para la confección de la pregunta PICO, se tomó como población a los pacientes con disfagia no obstructiva y manometría esofágica normal, como intervención al sistema EndoFLIP, como comparador la HRM y como evento o desenlace la información diagnóstica.
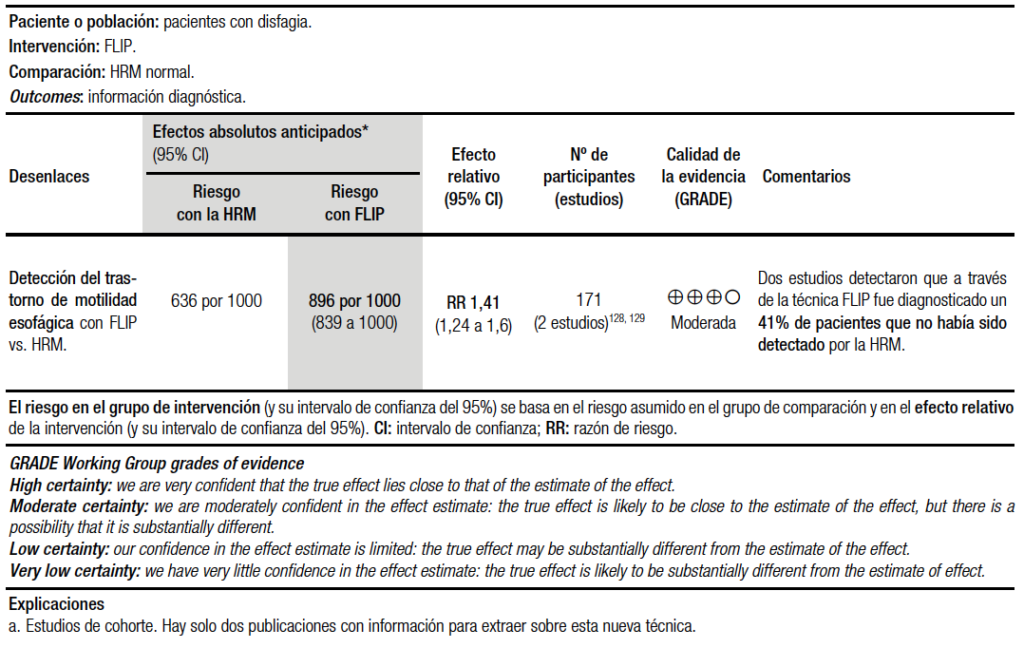
Dos estudios fueron incluidos en la síntesis cuantitativa con moderada calidad de la evidencia. De acuerdo a los criterios de Roma IV, en los pacientes con endoscopía y biopsias esofágicas normales y manometría normal se puede diagnosticar la disfagia funcional.126, 127 Se postula que en algunos de estos pacientes que presentan disfagia con la HRM normal, el EndoFLIP puede encontrar algunas alteraciones que no es posible detectar por la HRM con un RR 1,41 (IC 95% 1,24-1,60) explicando la sintomatología en algunos de estos pacientes (Tabla 10). Esto se puede explicar en parte debido a que los dos métodos evalúan la función esofágica desde puntos de vista distintos. La HRM se basa en las mediciones de presión en los múltiples sitios para evaluar la relajación de la UEG y la actividad contráctil del cuerpo esofágico durante la peristalsis primaria estimulada por degluciones voluntarias. En contraste, el EndoFLIP incorpora un solo transductor de presión en el balón y mide los cambios en el área de sección transversal en los múltiples sitios para evaluar la distensibilidad de la UEG y la peristalsis secundaria inducida por la distensión.
En el primer estudio el grupo del Carlson et al.,128 realizaron la endoscopia, la HRM y el EndoFLIP de 16 cm en 145 pacientes referidos por disfagia esofágica. Clasificaron los trazados de la manometría de acuerdo con Chicago v3.0 y el EndoFLIP fue considerado como anormal si presentaba una distensibilidad < 2,8 mm2/mmHg o un patrón de contracción de cuerpo esofágico retrógrado o ausente. Demostraron que hasta un 50% (17 pacientes) de los pacientes que presentan disfagia y una manometría sin alteraciones mayores (manometría normal o peristalsis esofágica inefectiva) presentó anormalidades en el EndoFLIP. De estos 17 pacientes, 13 (76%) presentaron una obstrucción al tracto de salida de la unión esofagogástrica (EJGOO por sus siglas en inglés) caracterizada por una distensibilidad menor de 2,8 mm2/mmHg. El segundo estudio realizado por el mismo grupo comparó los resultados de la HRM con los resultados obtenidos en tiempo real por el EndoFLIP durante una endoscopia.129 Se incluyeron a 40 pacientes que fueron referidos a endoscopía y tenían programada una HRM en dos centros. En total, en 18 pacientes no se encontró un diagnóstico manométrico de trastorno motor mayor del esófago. De estos, 10 (55,5%) presentaron un EndoFLIP anormal.
De esta manera, de acuerdo a nuestro análisis, el EndoFLIP es una herramienta que nos permite detectar alteraciones de la biomecánica esofágica que no pueden ser detectadas por la HRM. Se requieren más estudios con la finalidad de investigar la significancia clínica y clarificar la utilidad de los hallazgos por EndoFLIP.
El acuerdo en cuanto a la fuerza de recomendación fue del 71%. Hay dudas sobre cuánto añade el EndoFLIP al diagnóstico en los pacientes que tienen manometría normal. Sin embargo, otros expertos opinan que el EndoFLIP mide aspectos de la función esofágica distintos a lo que evalúa la HRM y, por lo tanto, provee información diferente.
Conflictos de interés
Se obtuvo financiamiento parcial de parte de Medtronic para la realización de este consenso. La empresa brindó apoyo logístico para organizar las reuniones del grupo de expertos. La empresa no influyó ni tuvo ninguna participación en el desarrollo de las preguntas, la búsqueda bibliográfica, el análisis de los datos, el proceso de votación, las recomendaciones finales o la preparación del manuscrito que describe el consenso. Además, este consenso se ha realizado con completa independencia editorial. Los conflictos de intereses de los expertos están enumerados al final del documento.
JO: declara haber participado como consultor o disertante de la empresa Medtronic.
JP: declara haber participado como speaker y consultor de Medtronik, Diversatek y Irongood, y haber recibido un grant de Takeda. Además refiere poseer propiedad intelectual en Crospon y Medtronik.
MMP: declara no tener conflictos de intereses.
PC: declara no tener conflictos de intereses.
MG: declara haber participado como consultor o disertante de la empresa Medtronic.
AH: declara no tener conflictos de intereses.
HPL: declara no tener conflictos de intereses.
GM: declara no tener conflictos de intereses.
IQ: declara no tener conflictos de intereses.
JMRT: declara no tener conflictos de intereses.
MAV: declara no tener conflictos de intereses.
LV: declara no tener conflictos de intereses.
EV: declara no tener conflictos de intereses.
MV: declara haber recibido apoyo no monetario en equipamiento, instalaciones, y haber participado como consultor de las empresas Medtronic y Diversatek.
Referencias
- Collaboration C, Others. Review Manager (RevMan) [Computer Program] Versión 5.2.3. Copenhagen: The Nordic Cochrane Centre; 2012. Health Psychol Rev 2014; 17.
- Moher D, Liberati A, Tetzlaff J, Altman DG, PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. PLoS Medicine 2009; 6 (7): e1000097. Disponible en: http://dx.doi.org/10.1371/journal.pmed.1000097
- GRADEpro GDT. GRADEpro Guideline Development Tool [Software]. McMaster University, 2015 (developed by Evidence Prime, Inc.). Disponible en: gradepro.org
- Blokdyk G. Zoom Software: A Complete Guide. 2020 ed. Emereo Publishing 2020.
- Code CF, Creamer B, Schlegel, Olsen AM, Donoghue FE, and Andersen H. An Atlas of Esophageal Motility in Health and Disease. Springfield: Thomas, 1958.
- Zavala-Solares M, Saleme-Cruz E, Coss-Adame E, Pinzon-Te L, Valdovinos MA. High Resolution Esophageal Pressure Topography (HREPT) in Asymptomatic Volunteers. A Comparative Study Between Solid-state and Water-perfused Systems. Gastroenterology & Hepatology Open Access 2015; 2(2): 00033. Disponible en: http://dx.doi.org/10.15406/ghoa.2015.02.00033
- Pandolfino JE, Kahrilas PJ; American Gastroenterological Association. AGA technical review on the clinical use of esophageal manometry. Gastroenterology 2005; 128 (1): 209-224.
- Lee JY, Kim N, Kim SE, Choi YJ, Kang KK, Oh DH, et al. Clinical characteristics and treatment outcomes of 3 subtypes of achalasia according to the chicago classification in a tertiary institute in Korea. J Neurogastroenterol Motil 2013; 19 (4): 485-494.
- Ghosh SK, Pandolfino JE, Rice J, Clarke JO, Kwiatek M, Kahrilas PJ. Impaired deglutitive EGJ relaxation in clinical esophageal manometry: a quantitative analysis of 400 patients and 75 controls. Am J Physiol Gastrointest Liver Physiol 2007; 293 (4): G878-G885.
- Bansal A, Kahrilas PJ. Has high-resolution manometry changed the approach to esophageal motility disorders? Curr Opin Gastroenterol 2010; 26 (4): 344-351.
- Carlson DA, Ravi K, Kahrilas PJ, Gyawali CP, Bredenoord AJ, Castell DO, et al. Diagnosis of Esophageal Motility Disorders: Esophageal Pressure Topography vs. Conventional Line Tracing. Am J Gastroenterol 2015; 110 (7): 967-977. Disponible en: http://dx.doi.org/10.1038/ajg.2015.159
- Grübel C, Hiscock R, Hebbard G. Value of Spatiotemporal Representation of Manometric Data. Clinical Gastroenterology and Hepatology 2008; 6: 525-530. Disponible en: http://dx.doi.org/10.1016/j.cgh.2008.02.006
- Soudagar AS, Sayuk GS, Gyawali CP. Learners favour high resolution oesophageal manometry with better diagnostic accuracy over conventional line tracings. Gut 2012; 61 (6): 798-803.
- Roman S, Huot L, Zerbib F, des Varannes SB, Gourcerol G, Roux A, et al. Tu1967 High Resolution Manometry Improves the Diagnosis of Esophageal Motility Disorders in Patients With Dysphagia: Preliminary Results of a Randomized Multicenter Trial [Internet]. Gastroenterology 2014; 146 (5): S-883-S884. Disponible en: http://dx.doi.org/10.1016/s0016-5085(14)63222-4
- Sadowski DC, Broenink L. High-resolution esophageal manometry: a time motion study. Can J Gastroenterol. 2008; 22 (4): 365-368.
- Bogte A, Bredenoord AJ, Oors J, Siersema PD, Smout AJPM. Reproducibility of esophageal high-resolution manometry. Neurogastroenterol Motil 2011; 23 (7): e271-e276.
- Capovilla G, Savarino E, Costantini M, Nicoletti L, Zaninotto G, Salvador R. Mo1884 Inter-Rater and Inter-Device Agreement for the Diagnosis of Primary Esophageal Motility Disorders Based on Chicago Classification Between Solid-State and Water-Perfused HRM System – A Prospective, Randomized, Double Blind, Crossover Study. Gastroenterology 2014; 146: S-681. Disponible en: http://dx.doi.org/10.1016/s0016-5085(14)62474-4
- Gehwolf P, Hinder RA, DeVault KR, Edlinger M, Wykypiel HF, Klingler PJ. Significant pressure differences between solid-state and water-perfused systems in lower esophageal sphincter measurement. Surg Endosc 2015; 29 (12): 3565-3569.
- Kessing BF, Weijenborg PW, Smout AJPM, Hillenius S, Bredenoord AJ. Water-perfused esophageal high-resolution manometry: normal values and validation. Am J Physiol Gastrointest Liver Physiol 2014; 306 (6): G491-G495.
- Kahrilas PJ, Bredenoord AJ, Fox M, Gyawali CP, Roman S, Smout AJPM, et al. The Chicago Classification of esophageal motility disorders, v3.0. Neurogastroenterol Motil 2015; 27 (2): 160-174. Disponible en: http://dx.doi.org/10.1111/nmo.12477
- Lin Z, Nicodème F, Lin C-Y, Mogni B, Friesen L, Kahrilas PJ, Pandolfino JE. Parameters for quantifying bolus retention with high-resolution impedance manometry. Neurogastroenterol Motil 2014; 26 (7): 929-936.
- Rohof WO, Myers JC, Estremera FA, Ferris LS, van de Pol J, Boeckxstaens GE, Omari TI. Inter- and intra-rater reproducibility of automated and integrated pressure-flow analysis of esophageal pressure-impedance recordings. Neurogastroenterol Motil 2014; 26 (2):168-175.
- Tutuian R, Castell DO. Combined multichannel intraluminal impedance and manometry clarifies esophageal function abnormalities: study in 350 patients. Am J Gastroenterol 2004; 99 (6): 1011-1019.
- Blom D, Mason R, Balaji N, Bremner C, Crookes P, Hagen J, et al. Esophageal bolus transport measured by simultaneous muttichannel intraluminal impedance and manofluorometry. Gastroenterology 2001; 120 (5): A220. Disponible en: http://dx.doi.org/10.1016/s0016-5085(01)81093-3
- Koya DL, Agrawal A, Freeman JE, Castell DO. Impedance detected abnormal bolus transit in patients with normal esophageal manometry. Sensitive indicator of esophageal functional abnormality? Dis Esophagus 2008; 21 (6): 563-569.
- Nguyen NQ, Holloway RH, Smout AJ, Omari TI. Automated impedance-manometry analysis detects esophageal motor dysfunction in patients who have non-obstructive dysphagia with normal manometry. Neurogastroenterol Motil 2013; 25 (3): 238-245. Disponible en: http://dx.doi.org/10.1111/nmo.12040
- Conchillo JM, Nguyen NQ, Samsom M, Holloway RH, Smout AJPM. Multichannel intraluminal impedance monitoring in the evaluation of patients with non-obstructive Dysphagia. Am J Gastroenterol 2005; 100 (12): 2624-2632.
- Yadlapati R. High-resolution esophageal manometry: interpretation in clinical practice. Curr Opin Gastroenterol 2017; 33 (4): 301-309.
- Carlson DA, Roman S. Esophageal provocation tests: Are they useful to improve diagnostic yield of high resolution manometry? Neurogastroenterol Motil 2018; 30 (4): e13321.
- Mauro A, Savarino E, De Bortoli N, Tolone S, Pugliese D, Franchina M, Gyawali CP, Penagini R. Optimal number of multiple rapid swallows needed during high-resolution esophageal manometry for accurate prediction of contraction reserve. Neurogastroenterol Motil 2018; 30 (4): e13253.
- Carlson DA, Crowell MD, Kimmel JN, Patel A, Prakash Gyawali C, Hinchcliff M, et al. Loss of Peristaltic Reserve, Determined by Multiple Rapid Swallows, Is the Most Frequent Esophageal Motility Abnormality in Patients With Systemic Sclerosis. Clinical Gastroenterology and Hepatology 2016; 14 (10): 1502-1506. Disponible en: http://dx.doi.org/10.1016/j.cgh.2016.03.039
- Martinucci I, Savarino EV, Pandolfino JE, Russo S, Bellini M, Tolone S, et al. Vigor of peristalsis during multiple rapid swallows is inversely correlated with acid exposure time in patients with NERD. Neurogastroenterology & Motility 2016; 28 (2): 243-250. Disponible en: http://dx.doi.org/10.1111/nmo.12719
- Kushnir V, Sayuk GS, Prakash Gyawali C. Multiple rapid swallow responses segregate achalasia subtypes on high-resolution manometry. Neurogastroenterology & Motility 2012; 24 (12): 1069-e561. Disponible en: http://dx.doi.org/10.1111/j.1365-2982.2012.01971.x
- Price LH, Li Y, Patel A, Prakash Gyawali C. Reproducibility patterns of multiple rapid swallows during high resolution esophageal manometry provide insights into esophageal pathophysiology. Neurogastroenterol Motil 2014; 26 (5): 646-653.
- Marin I, Serra J. Patterns of esophageal pressure responses to a rapid drink challenge test in patients with esophageal motility disorders. Neurogastroenterol Motil 2016; 28 (4): 543-553.
- Wang YT, Tai LF, Yazaki E, Jafari J, Sweis R, Tucker E, et al. Investigation of Dysphagia After Antireflux Surgery by High-resolution Manometry: Impact of Multiple Water Swallows and a Solid Test Meal on Diagnosis, Management, and Clinical Outcome. Clinical Gastroenterology and Hepatology 2015; 13 (9): 1575-1583. Disponible en: http://dx.doi.org/10.1016/j.cgh.2015.04.181
- Shaker A, Stoikes N, Drapekin J, Kushnir V, Brunt LM, Prakash Gyawali C. Multiple rapid swallow responses during esophageal high-resolution manometry reflect esophageal body peristaltic reserve. Am J Gastroenterol 2013; 108 (11): 1706-1712.
- Stoikes N, Drapekin J, Kushnir V, Shaker A, Brunt LM, Prakash Gyawali C. The value of multiple rapid swallows during preoperative esophageal manometry before laparoscopic antireflux surgery. Surg Endosc 2012; 26 (12): 3401-3407.
- Sanagapalli S, Roman S, Hastier A, Leong RW, Patel K, Raeburn A, et al. Achalasia diagnosed despite normal integrated relaxation pressure responds favorably to therapy. Neurogastroenterol Motil 2019; 31 (6): e13586.
- Fornari F, Bravi I, Penagini R, Tack J, Sifrim D. Multiple rapid swallowing: A complementary test during standard oesophageal manometry. Neurogastroenterol Motil 2009; 21 (7): 718-e41.
- Ang D, Misselwitz B, Hollenstein M, Knowles K, Wright J, Tucker E, et al. Diagnostic yield of high-resolution manometry with a solid test meal for clinically relevant, symptomatic oesophageal motility disorders: serial diagnostic study. Lancet Gastroenterol Hepatol 2017; 2 (9): 654-661.
- Elvevi A, Mauro A, Pugliese D, Bravi I, Tenca A, Consonni D, Conte D, Penagini R. Usefulness of low- and high-volume multiple rapid swallowing during high-resolution manometry. Dig Liver Dis 2015; 47 (2): 103-107.
- Ang D, Hollenstein M, Misselwitz B, Knowles K, Wright J, Tucker E, Swies R, Fox M. Rapid Drink Challenge in high-resolution manometry: an adjunctive test for detection of esophageal motility disorders. Neurogastroenterol Motil 2017; 29 (1). Disponible en: http://dx.doi.org/10.1111/nmo.12902
- Ponds FA, Oors JM, Smout AJPM, Bredenoord AJ. Rapid drinking challenge during high-resolution manometry is complementary to timed barium esophagogram for diagnosis and follow-up of achalasia. Neurogastroenterol Motil 2018; 30 (11): e13404.
- Sweis R, Anggiansah A, Wong T, Brady G, Fox M. Assessment of esophageal dysfunction and symptoms during and after a standardized test meal: development and clinical validation of a new methodology utilizing high-resolution manometry. Neurogastroenterol Motil 2014; 26 (2): 215-228.
- Woodland P, Gabieta-Sonmez S, Arguero J, Ooi J, Nakagawa K, Glasinovic E, Yazaki E, Sifrim D. 200 mL Rapid Drink Challenge During High-resolution Manometry Best Predicts Objective Esophagogastric Junction Obstruction and Correlates With Symptom Severity. Journal of Neurogastroenterology and Motility 2018; 24 (3): 410-414. Disponible en: http://dx.doi.org/10.5056/jnm18038
- Sweis R, Anggiansah A, Wong T, Kaufman E, Obrecht S, Fox M. Normative values and inter-observer agreement for liquid and solid bolus swallows in upright and supine positions as assessed by esophageal high-resolution manometry. Neurogastroenterol Motil 2011; 23 (6): 509-e198.
- Hasan Y, Go J, Hashmi SM, Valestin J, Schey R. Influence of everyday bolus consistencies in different body positions on high-resolution esophageal pressure topography (HREPT) parameters. Dis Esophagus 2015; 28 (3): 246-252.
- Xiang X, Wang A, Tu L, Xie X, Ke M, Yang Y, et al. The differences in the esophageal motility between liquid and solid bolus swallows: A multicenter high-resolution manometry study in Chinese asymptomatic volunteers . Neurogastroenterology & Motility 2019; 31: e13574. Disponible en: http://dx.doi.org/10.1111/nmo.13574
- Blonski W, Hila A, Jain V, Freeman J, Vela M, Castell DO. Impedance manometry with viscous test solution increases detection of esophageal function defects compared to liquid swallows. Scandinavian Journal of Gastroenterology 2007; 42 (8): 917-922. Disponible en: http://dx.doi.org/10.1080/00365520701245702
- Clayton SB, Rife C, Kalbfleisch JH, Castell DO. Viscous impedance is an important indicator of abnormal esophageal motility. Neurogastroenterol Motil 2013; 25 (7): 563-e455.
- Tutuian R, Castell DO. Review article: oesophageal spasm – diagnosis and management. Aliment Pharmacol Ther 2006; 23 (10): 1393-1402.
- Vaezi MF, Pandolfino JE, Vela MF. ACG clinical guideline: diagnosis and management of achalasia. Am J Gastroenterol 2013; 108 (8): 1238-1249.
- Pandolfino JE, Kwiatek MA, Nealis T, Bulsiewicz W, Post J, Kahrilas PJ. Achalasia: a new clinically relevant classification by high-resolution manometry. Gastroenterology 2008; 135 (5): 1526-1533.
- Vela MF, Richter JE, Wachsberger D, Connor J, Rice TW. Complexities of managing achalasia at a tertiary referral center: use of pneumatic dilatation, Heller myotomy, and botulinum toxin injection. Am J Gastroenterol 2004; 99 (6): 1029-1036.
- Salvador R, Costantini M, Zaninotto G, Morbin T, Rizzetto C, Zanatta L, et al. The Preoperative Manometric Pattern Predicts the Outcome of Surgical Treatment for Esophageal Achalasia. Journal of Gastrointestinal Surgery 2010; 14: 1635-1645. Disponible en: http://dx.doi.org/10.1007/s11605-010-1318-4
- Pratap N, Kalapala R, Darisetty S, Joshi N, Ramchandani M, Banerjee R, et al. Achalasia cardia subtyping by high-resolution manometry predicts the therapeutic outcome of pneumatic balloon dilatation. J Neurogastroenterol Motil 2011; 17 (1): 48-53.
- Rohof WO, Salvador R, Annese V, Bruley des Varannes S, Chaussade S, Costantini M, et al. Outcomes of treatment for achalasia depend on manometric subtype. Gastroenterology 2013; 144 (4): 718-725.
- Boeckxstaens G, Zaninotto G. Achalasia and esophago-gastric junction outflow obstruction: focus on the subtypes. Neurogastroenterology 2012. Disponible en: https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1365-2982.2011.01833.x
- Boeckxstaens GE, Zaninotto G, Richter JE. Achalasia. Lancet 2014; 383 (9911): 83-93.
- Moonen A, Annese V, Belmans A, Bredenoord AJ, Bruley des Varannes S, Costantini M, et al. Long-term results of the European achalasia trial: a multicentre randomised controlled trial comparing pneumatic dilation versus laparoscopic Heller myotomy. Gut 2016; 65 (5): 732-739.
- Hamer PW, Holloway RH, Heddle R, Devitt PG, Kiroff G, Burgstad C, et al. Evaluation of outcome after cardiomyotomy for achalasia using the Chicago classification. British Journal of Surgery 2016; 103: 1847-1854. Disponible en: http://dx.doi.org/10.1002/bjs.10285
- Andolfi C, Fisichella PM. Meta-analysis of clinical outcome after treatment for achalasia based on manometric subtypes. Br J Surg 2019; 106 (4): 332-341.
- Trudgill NJ, Sifrim D, Sweis R, Fullard M, Basu K, McCord M, et al. British Society of Gastroenterology guidelines for oesophageal manometry and oesophageal reflux monitoring. Gut 2019; 68 (10): 1731-1750.
- Khashab MA, Vela MF, Thosani N, Agrawal D, Buxbaum JL, Abbas Fehmi SM, et al. ASGE guideline on the management of achalasia. Gastrointest Endosc 2020; 91 (2): 213-227.
- Lee H, Chung H, Lee TH, Hong KS, Youn YH, Park JH, et al. Therapeutic Outcome of Achalasia Based on High-Resolution Manometry: A Korean Multicenter Study. Am J Ther 2019; 26 (4): e452-e461.
- Min M, Peng LH, Yang YS, Hou XH, Guo RB, Wang WF, et al. Characteristics of achalasia subtypes in untreated Chinese patients: a high-resolution manometry study. J Dig Dis 2012; 13 (10): 504-509.
- Hosaka H, Kusano M, Kawada A, Kuribayashi S, Shimoyama Y, Moki F, et al. Mo1900 The Long Term Outcome After the Treatment of Different Subtypes of Achalasia Using High Resolution Manometry. Gastroenterology 2014; 146: S-686. Disponible en: http://dx.doi.org/10.1016/s0016-5085(14)62490-2
- Meng F, Li P, Wang Y, Ji M, Wu Y, Yu L, et al. Peroral endoscopic myotomy compared with pneumatic dilation for newly diagnosed achalasia. Surgical Endoscopy 2017; 31: 4665-4672. Disponible en: http://dx.doi.org/10.1007/s00464-017-5530-0
- Müller M, Keck C, Eckardt AJ, Werling S, Wehrmann T, König J, et al. Outcomes of pneumatic dilation in achalasia: Extended follow-up of more than 25 years with a focus on manometric subtypes. Journal of Gastroenterology and Hepatology 2018; 33: 1067-1074. Disponible en: http://dx.doi.org/10.1111/jgh.14044
- Yamashita H, Ashida K, Fukuchi T, Nagatani Y, Koga H, Senda K, et al. Predictive factors associated with the success of pneumatic dilatation in Japanese patients with primary achalasia: a study using high-resolution manometry. Digestion 2013; 87 (1): 23-28.
- Crespin OM, Tatum RP, Xiao K, Martin AV, Khandelwal S, Pellegrini CA, et al. The relationship between manometric subtype and outcomes of surgical treatment for patients with achalasia. Surg Endosc 2017; 31 (12): 5066-5075.
- Kumbhari V, Tieu AH, El Zein MH, Ngamruengphong S, Abdelgelil A, Besharati S, et al. Tu1513 PerOral Endoscopic Myotomy (POEM) Achieves Similar Clinical Response but Incurs Lesser Charges Compared to Heller Myotomy (HM) for the Treatment of Achalasia. Gastrointestinal Endoscopy 2015; 81: AB492. Disponible en: http://dx.doi.org/10.1016/j.gie.2015.03.964
- Kim WH, Cho JY, Ko WJ, Hong SP, Hahm KB, Cho J-H, et al. Comparison of the Outcomes of Peroral Endoscopic Myotomy for Achalasia According to Manometric Subtype. Gut Liver 2017; 11 (5): 642-647.
- Kumbhari V, Tieu AH, Onimaru M, El Zein MH, Teitelbaum EN, Ujiki MB, et al. Peroral endoscopic myotomy (POEM) vs. laparoscopic Heller myotomy (LHM) for the treatment of Type III achalasia in 75 patients: a multicenter comparative study. Endosc Int Open 2015; 3 (3): E195-E201.
- Kim GH, Jung KW, Jung H-Y, Kim M-J, Na HK, Ahn JY, et al. Superior clinical outcomes of peroral endoscopic myotomy compared with balloon dilation in all achalasia subtypes. J Gastroenterol Hepatol 2019; 34 (4): 659-665.
- Park EJ, Lee JS, Lee TH, Bok GH, Hong SJ, Kim HG, et al. High-resolution Impedance Manometry Criteria in the Sitting Position Indicative of Incomplete Bolus Clearance. J Neurogastroenterol Motil 2014; 20 (4): 491-496.
- Khashab MA, Kumbhari V, Tieu AH, El Zein MH, Ismail A, Ngamruengphong S, et al. Peroral endoscopic myotomy achieves similar clinical response but incurs lesser charges compared to robotic Heller myotomy. Saudi J Gastroenterol 2017; 23 (2): 91-96.
- Worrell SG, Alicuben ET, Boys J, DeMeester SR. Peroral Endoscopic Myotomy for Achalasia in a Thoracic Surgical Practice. Ann Thorac Surg 2016; 101 (1): 218-224.
- Laique S, Singh T, Dornblaser D, Gadre A, Rangan V, Fass R, et al. Clinical Characteristics and Associated Systemic Diseases in Patients With Esophageal “Absent Contractility” – A Clinical Algorithm. J Clin Gastroenterol 2019; 53 (3): 184-190.
- Crowell MD, Umar SB, Griffing WL, DiBaise JK, Lacy BE, Vela MF. Esophageal Motor Abnormalities in Patients With Scleroderma: Heterogeneity, Risk Factors, and Effects on Quality of Life. Clin Gastroenterol Hepatol 2017; 15 (2): 207-213.e1.
- Rerych K, Kurek J, Klimacka-Nawrot E, Błońska-Fajfrowska B, Stadnicki A. High-resolution Manometry in Patients with Gastroesophageal Reflux Disease Before and After Fundoplication. Journal of Neurogastroenterology and Motility 2017; 23: 55-63. Disponible en: http://dx.doi.org/10.5056/jnm16062
- van Hoeij FB, Bredenoord AJ. Clinical Application of Esophageal High-resolution Manometry in the Diagnosis of Esophageal Motility Disorders. Journal of Neurogastroenterology and Motility 2015; 22: 6-13. Disponible en: http://dx.doi.org/10.5056/jnm15177
- Herregods TVK, Smout AJPM, Ooi JLS, Sifrim D, Bredenoord AJ. Jackhammer esophagus: Observations on a European cohort. Neurogastroenterol Motil. 2017; 29 (4). Disponible en: http://dx.doi.org/10.1111/nmo.12975
- Wahba G, Bouin M. Jackhammer esophagus: A meta-analysis of patient demographics, disease presentation, high-resolution manometry data, and treatment outcomes. Neurogastroenterology & Motility 2020; 32(11): e13870. Disponible en: http://dx.doi.org/10.1111/nmo.13870
- Bennett JR, Hendrix TR. Diffuse Esophageal Spasm: A Disorder with More Than One Cause. Gastroenterology 1970; 59: 273-279. Disponible en: http://dx.doi.org/10.1016/s0016-5085(19)33771-0
- Roman S, Kahrilas PJ. Distal Esophageal Spasm. Dysphagia 2012; 27: 115-123. Disponible en: http://dx.doi.org/10.1007/s00455-011-9388-3
- Roman S, Pandolfino JE, Chen J, Boris L, Luger D, Kahrilas PJ. Phenotypes and clinical context of hypercontractility in high-resolution esophageal pressure topography (EPT). Am J Gastroenterol 2012; 107 (1): 37-45.
- Roman S, Huot L, Zerbib F, des Varannes SB, Gourcerol G, Coffin B, et al. High-Resolution Manometry Improves the Diagnosis of Esophageal Motility Disorders in Patients With Dysphagia: A Randomized Multicenter Study. American Journal of Gastroenterology 2016; 111: 372-380. Disponible en: http://dx.doi.org/10.1038/ajg.2016.1
- Cho YK, Lipowska AM, Nicodème F, Teitelbaum EN, Hungness ES, Johnston ER, et al. Assessing Bolus Retention in Achalasia Using High-Resolution Manometry With Impedance: A Comparator Study With Timed Barium Esophagram. American Journal of Gastroenterology 2014; 109: 829-835. Disponible en: http://dx.doi.org/10.1038/ajg.2014.61
- Conchillo JM, Selimah M, Bredenoord AJ, Samsom M, Smout AJPM. Assessment of oesophageal emptying in achalasia patients by intraluminal impedance monitoring. Neurogastroenterology and Motility 2006; 18: 971-977. Disponible en: http://dx.doi.org/10.1111/j.1365-2982.2006.00814.x
- de Oliveira JM, Birgisson S, Doinoff C, Einstein D, Herts B, et al. Timed barium swallow: a simple technique for evaluating esophageal emptying in patients with achalasia. American Journal of Roentgenology 1997; 169(2): 473-479. Disponible en: http://dx.doi.org/10.2214/ajr.169.2.9242756
- Spencer J. Prolonged pH recording in the study of Gastro-oesophageal reflux. British Journal of Surgery 1969; 56: 912-914. Disponible en: http://dx.doi.org/10.1002/bjs.1800561211
- Anggiansah A, Sumboonnanonda K, Wang J, Linsell J, Hale P, Owen WJ. Significantly reduced acid detection at 10 centimeters compared to 5 centimeters above lower esophageal sphincter in patients with acid reflux. Am J Gastroenterol 1993; 88 (6): 842-846.
- Ruiz-De-León A, Sevilla-Mantilla C, Pérez-de-la-Serna J, Taxonera C, Rubio MD. Simultaneous two-level esophageal 24-hour pH monitoring in patients with mild and severe esophagitis. Digestive Diseases and Sciences 1995; 40: 1423-1427. Disponible en: http://dx.doi.org/10.1007/bf02285187
- Kahrilas PJ, Quigley EM. Clinical esophageal pH recording: a technical review for practice guideline development. Gastroenterology 1996; 110 (6): 1982-1996.
- Chen JW, Baker JR, Compton JM, McDermott M, Rubenstein JH. Accuracy of the Air Flow Sphincter Locator system in identifying the lower esophageal sphincter for placement of pH catheters. Dis Esophagus 2017; 30 (3): 1-5.
- Marples MI, Mughal M, Bancewicz J. Can an Oesophageal pH Electrode be Accurately Positioned Without Manometry?. Diseases of the Esophagus 1988: 789-791. Disponible en: http://dx.doi.org/10.1007/978-3-642-86432-2_172
- Mattox HE, Richter JE, Sinclair JW, Price JE, Douglas Case L. Gastroesophageal pH step-up inaccurately locates proximal border of lower esophageal sphincter. Digestive Diseases and Sciences 1992; 37: 1185-1191. Disponible en: http://dx.doi.org/10.1007/bf01296558
- Klauser AG, Schindlbeck NE, Müller-Lissner SA. Esophageal 24-h pH monitoring: is prior manometry necessary for correct positioning of the electrode? Am J Gastroenterol 1990; 85 (11): 1463-1467.
- Can MF, Yagci G, Cetiner S, Gulsen M, Yigit T, Ozturk E, et al. Accurate positioning of the 24-hour pH monitoring catheter: Agreement between manometry and pH step-up method in two patient positions. World Journal of Gastroenterology 2007; 13: 6197. Disponible en: http://dx.doi.org/10.3748/wjg.v13.i46.6197
- Haarala A, Linjamäki J-A, Tuominen H, Kähönen M. High Resolution Manometry and pH stepup method on the localisation of the lower esophageal sphincter. Journal of Gastrointestinal and Liver Diseases 2017; 26: 425-429. Disponible en: http://dx.doi.org/10.15403/jgld.2014.1121.264.haa
- Mauro A, Franchina M, Consonni D, Penagini R. Lower oesophageal sphincter identification for gastro-oesophageal reflux monitoring: The step-up method revisited with use of basal impedance. United European Gastroenterol J 2019; 7 (10): 1373-1379.
- Rohof WO, Bisschops R, Tack J, Boeckxstaens GE. Postoperative Problems 2011: Fundoplication and Obesity Surgery. Gastroenterology Clinics of North America 2011; 40: 809-821. Disponible en: http://dx.doi.org/10.1016/j.gtc.2011.09.002
- Chan WW, Haroian LR, Prakash Gyawali C. Value of preoperative esophageal function studies before laparoscopic antireflux surgery. Surgical Endoscopy 2011; 25: 2943-2949. Disponible en: http://dx.doi.org/10.1007/s00464-011-1646-9
- Ho S-C, Chang C-S, Wu C-Y, Chen G-H. Ineffective Esophageal Motility Is a Primary Motility Disorder in Gastroesophageal Reflux Disease. Digestive Diseases and Sciences 2002; 47: 652-656. Disponible en: http://link.springer.com/10.1023/A:1017992808762
- Mathew G, Watson DI, Myers JC, Holloway RH, Jamieson GG. Oesophageal motility before and after laparoscopic Nissen fundoplication. Br J Surg 1997; 84 (10): 1465-1469.
- Yang H, Watson DI, Kelly J, Lally CJ, Myers JC, Jamieson GG. Esophageal Manometry and Clinical Outcome After Laparoscopic Nissen Fundoplication. Journal of Gastrointestinal Surgery 2007; 11: 1126-1133. Disponible en: http://dx.doi.org/10.1007/s11605-007-0224-x
- Montenovo M, Tatum RP, Figueredo E, Martin AV, Vu H, Quiroga E, et al. Does combined multichannel intraluminal esophageal impedance and manometry predict postoperative dysphagia after laparoscopic Nissen fundoplication? Dis Esophagus 2009; 22 (8): 656-663.
- Savarino E, de Bortoli N, Bellini M, Galeazzi F, Ribolsi M, Salvador R, et al. Practice guidelines on the use of esophageal manometry – A GISMAD-SIGE-AIGO medical position statement. Digestive and Liver Disease 2016; 48: 1124-1135. Disponible en: http://dx.doi.org/10.1016/j.dld.2016.06.021
- Lee KJ, Kim JH, Cho SW. Prevalence of Ineffective Esophageal Motility and Its Relevance to Symptoms and Esophageal Acid Exposure in Korean Patients Referred for Foregut Symptoms. Digestion 2006; 73: 171-177. Disponible en: http://dx.doi.org/10.1159/000094525
- Saleh CMG, Bredenoord AJ. Utilization of Esophageal Function Testing for the Diagnosis of the Rumination Syndrome and Belching Disorders. Gastrointestinal Endoscopy Clinics of North America 2014; 24: 633-642. Disponible en: http://dx.doi.org/10.1016/j.giec.2014.06.002
- Tucker E, Knowles K, Wright J, Fox MR. Rumination variations: aetiology and classification of abnormal behavioural responses to digestive symptoms based on high-resolution manometry studies. Alimentary Pharmacology & Therapeutics. 2013; 37: 263-274. Disponible en: http://dx.doi.org/10.1111/apt.12148
- Tack J, Talley NJ, Camilleri M, Holtmann G, Hu P, Malagelada J-R, et al. Functional Gastroduodenal Disorders. Gastroenterology. 2006; 130: 1466-1479. Disponible en: http://dx.doi.org/10.1053/j.gastro.2005.11.059
- Kessing BF, Bredenoord AJ, André J P. Objective Manometric Criteria for the Rumination Syndrome. American Journal of Gastroenterology 2014; 109: 52-59. Disponible en: http://dx.doi.org/10.1038/ajg.2013.428
- Kessing BF, Govaert F, Masclee AAM, Conchillo JM. Impedance measurements and high-resolution manometry help to better define rumination episodes. Scandinavian Journal of Gastroenterology 2011; 46: 1310-1315. Disponible en: http://dx.doi.org/10.3109/00365521.2011.605467
- Rommel N, Tack J, Arts J, Caenepeel P, Bisschops R, Sifrim D. Rumination or belching-regurgitation? Differential diagnosis using oesophageal impedance-manometry. Neurogastroenterology & Motility 2010; 22: e97-e104. Disponible en: http://dx.doi.org/10.1111/j.1365-2982.2009.01431.x
- Tack J, Blondeau K, Boecxstaens V, Rommel N. Review article: the pathophysiology, differential diagnosis and management of rumination syndrome. Alimentary Pharmacology & Therapeutics 2011; 30: 782-788. Disponible en: http://dx.doi.org/10.1111/j.1365-2036.2011.04584.x
- Kidambi T, Toto E, Ho N, Taft T, Hirano I. Temporal trends in the relative prevalence of dysphagia etiologies from 1999-2009. World J Gastroenterol 2012; 18 (32): 4335-4341.
- Perretta S, McAnena O, Botha A, Nathanson L, Swanstrom L, Soper NJ, et al. Acta from the EndoFLIP® Symposium. Surg Innov 2013; 20 (6): 545-552.
- Hirano I, Pandolfino JE, Boeckxstaens GE. Functional Lumen Imaging Probe for the Management of Esophageal Disorders: Expert Review From the Clinical Practice Updates Committee of the AGA Institute. Clinical Gastroenterology and Hepatology 2017; 15: 325-334. Disponible en: http://dx.doi.org/10.1016/j.cgh.2016.10.022
- Savarino E, di Pietro M, Bredenoord AJ, Carlson DA, Clarke JO, Khan A, et al. Use of the Functional Lumen Imaging Probe in Clinical Esophagology. Am J Gastroenterol 2020. Disponible en: http://dx.doi.org/10.14309/ajg.0000000000000773
- Carlson DA, Kou W, Lin Z, Hinchcliff M, Thakrar A, Falmagne S, et al. Normal Values of Esophageal Distensibility and Distension-Induced Contractility Measured by Functional Luminal Imaging Probe Panometry. Clinical Gastroenterology and Hepatology 2019; 17: 674-681.e1. Disponible en: http://dx.doi.org/10.1016/j.cgh.2018.07.042
- Su B, Novak S, Callahan ZM, Kuchta K, Carbray J, Ujiki MB. Using impedance planimetry (EndoFLIPTM) in the operating room to assess gastroesophageal junction distensibility and predict patient outcomes following fundoplication. Surgical Endoscopy 2020; 34: 1761-1768. Disponible en: http://dx.doi.org/10.1007/s00464-019-06925-5
- Donnan EN, Pandolfino JE. Applying the Functional Luminal Imaging Probe to Esophageal Disorders. Curr Gastroenterol Rep 2020; 22 (3): 10.
- Drossman DA. Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology 2016. Disponible en: http://dx.doi.org/10.1053/j.gastro.2016.02.032
- Aziz Q, Fass R, Gyawali CP, Miwa H, Pandolfino JE, Zerbib F. Functional Esophageal Disorders. Gastroenterology 2016. Disponible en: http://dx.doi.org/10.1053/j.gastro.2016.02.012
- Carlson DA, Kahrilas PJ, Lin Z, Hirano I, Gonsalves N, Listernick Z, et al. Evaluation of Esophageal Motility Utilizing the Functional Lumen Imaging Probe. American Journal of Gastroenterology 2016; 111: 1726-1735. Disponible en: http://dx.doi.org/10.1038/ajg.2016.454
- Carlson DA, Prakash Gyawali C, Kahrilas PJ, Triggs JR, Falmagne S, Prescott J, et al. Esophageal motility classification can be established at the time of endoscopy: a study evaluating real-time functional luminal imaging probe panometry. Gastrointestinal Endoscopy 2019; 90: 915-923.e1. Disponible en: http://dx.doi.org/10.1016/j.gie.2019.06.039
Acta Gastroenterol Latinoam – Vol 50 – Sup N° 3 (AMTME – Noviembre 2020)
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE