Sebastián Fernando Niño Ramírez1 ID· Laura Osorio2 ID· Marco Santisteban3 ID· Luis Fernando Roldán3 ID· Sandra León3 ID· Luis Gonzalo Guevara1 ID
1 Universidad CES, Instituto Gastroclinico, Colombia.
2 Hospital Pablo Tobón Uribe, Colombia.
3 Instituto Gastroclinico, Colombia.
Acta Gastroenterol Latinoam 2024;54(3):247-253
Recibido: 06/07/2024 / Aceptado: 22/09/2024 / Publicado online el 30/09/2024 /
https://doi.org/10.52787/agl.v54i3.422
Resumen
Introducción. La respuesta al tratamiento en dispepsia funcional con inhibidor de bomba de protones es variable. Una herramienta de decisión que identifique la probabilidad de respuesta utilizando datos clínicos podría optimizar el manejo en estos pacientes. Objetivo. Desarrollar y validar internamente un modelo predictivo pronóstico fácil de usar que permita establecer clínicamente la probabilidad de respuesta al inhibidor de bomba de protones en dispepsia funcional. Material y métodos. Realizamos un estudio de cohorte retrospectiva con base en la recolección de datos de historias clínicas de adultos con dispepsia funcional. Un estudio piloto permitió identificar las variables relacionadas con la respuesta al inhibidor de bomba de protones. Realizamos la validación interna por división de muestra, 70% desarrollo y 30% validación. Desarrollamos el modelo por regresión logística multivariable utilizando el mejor subconjunto para el número y la selección de variables. El modelo final se transformó en una regla de puntuación. Evaluamos la capacidad predictiva con área bajo la curva (AUC) y estadístico Hosmer-Lemshow. Resultados. Se incluyeron 192 pacientes. El mejor subconjunto identificó 4 variables con mejor desempeño. El modelo logístico demostró buena calibración y discriminación con AUC de 0,89 y chi-cuadrado de Hosmer-Lemshow con p = 1. La regla de puntuación asignó los valores: síntomas de ansiedad 3 puntos; fibromialgia 2 puntos; depresión 1 punto; sexo femenino se resta un punto. La suma de puntuaciones inferiores a 4 puntos se relacionaron con una buena respuesta al manejo con inhibidor de bomba, con una sensibilidad del 96,5% y especificidad del 56,6%. Conclusiones. Presentamos una herramienta novedosa que permite la identificación temprana de pacientes con mejor respuesta terapéutica al manejo de dispepsia funcional.
Palabras claves. Dispepsia funcional, inhibidores de la bomba de protones.
Development and Internal Validation of a Predictive Model for Prognostic Response to Proton Pump Inhibitors in Adults with Functional Dyspepsia
Summary
Introduction. The response to proton pump inhibitor treatment in functional dyspepsia varies among patients. A decision tool that identifies the probability of response based on clinical data could optimize management in these patients. Objective. To develop and internally validate an easy-to-use predictive model that enables clinicians to establish the probability of response to proton pump inhibitors in patients with functional dyspepsia. Material and methods. We conducted a cross-sectional study on adults with functional dyspepsia. A pilot study identified variables related to response to proton pump inhibitors. Internal validation was performed by split-sample method, with 70% for model development and 30% for validation. We developed the model using multivariable logistic regression, and selected variables based on the best subset method. The final model was subsequently transformed into a scoring rule. Predictive ability was assessed using the area under the curve (AUC) and Hosmer-Lemeshow statistic. Results. A total of 192 patients were included. The best subset identified 4 variables with the best performance. The logistic model showed good calibration and discrimination with an AUC of 0.89 and a Hosmer-Lemeshow chi-square test with p = 1. The scoring rule assigned the following values: anxiety symptoms (3 points), fibromyalgia (2 points), depression (1 point), and female sex (− 1 point). A total score of 4 points or less was associated with a good response to proton pump inhibitor treatment, with a sensitivity of 96.5% and specificity of 56.6%. Conclusions. We present a novel tool that facilitates the early identification of patients with a better therapeutic response to the management of functional dyspepsia.
Keywords. Functional dyspepsia, proton pump inhibitors.
Introducción
La dispepsia es un término amplio que describe un complejo de síntomas gastroduodenales tales como dolor epigástrico, saciedad precoz y llenura posprandial.1 Según los criterios Roma IV para los trastornos del eje intestino-cerebro, la dispepsia funcional (DF) se define como la presencia de al menos uno de los siguientes criterios: plenitud posprandial, saciedad temprana, dolor epigástrico y/o ardor epigástrico,2 en ausencia de una enfermedad estructural que pueda explicar los síntomas. Es un trastorno que afecta la calidad de vida de los pacientes, específicamente el dominio físico, mental y social.3
El abordaje de tratamiento incluye terapia de supresión de ácido, proquinéticos y neuromoduladores centrales.1,4,5 Los inhibidores de bomba de protones (IBP) son la terapia supresora de ácido de elección, especialmente si predomina el dolor epigástrico. Un metaanálisis publicado en 2017 por Pinto-Sanchez et al. encontró una mayor efectividad de los IBP para lograr la ausencia de síntomas o síntomas mínimos, en comparación con placebo (31,1% vs. 25,8%), con un número necesario a tratar (NNT) de 11.6
Existen publicaciones que destacan la importancia de establecer cuál puede ser la respuesta al tratamiento con inhibidor de bomba de protones en dispepsia funcional; sin embargo, no se pueden considerar estos esfuerzos como modelos pronósticos desarrollados con la metodología recomendada.7-9
Hasta la fecha y para nuestro conocimiento, no se han desarrollado modelos de predicción validados con una adecuada metodología que permitan establecer de manera pronóstica la respuesta al IBP.
Tendiendo esto en consideración, el objetivo de nuestro trabajo fue desarrollar y validar internamente un modelo predictivo pronóstico fácil de usar que permita establecer clínicamente la probabilidad de respuesta al IBP en dispepsia funcional.
Material y métodos
Utilizamos como referencia la guía para la realización de informes transparentes en modelos de predicción multivariable para diagnóstico individual (TRIPOD), tanto para el desarrollo metodológico como para la publicación.10
El diseño del estudio fue de tipo cohorte retrospectiva con base en la recolección de datos de historias clínicas, tanto para el desarrollo como para la validación interna del modelo. La población objetivo del estudio fueron pacientes adultos con diagnóstico de dispepsia funcional establecido por criterios de Roma IV que consultaron en la institución participante entre agosto de 2021 y marzo de 2022, y que recibieron manejo exclusivo con IBP para el control de síntomas dispépticos por un período mínimo de ocho semanas. Fueron excluidos del estudio los pacientes en estado de gestación, los menores de 18 años y aquellos con trastornos cognitivos graves. En todos los pacientes se realizaron endoscopía digestiva superior y ecografía de abdomen. Fueron excluidos del estudio los pacientes en los que se documentó infección por Helicobacter pylori, lesiones erosivas o úlceras esofágicas, gástrico o duodenal, litiasis biliar o pancreatopatía. Los casos de información incompleta o inconsistencias en los registros de historia clínica fueron eliminados de los análisis.
La institución participante es un centro de referencia para el manejo de enfermedades digestivas, ubicada en el área urbana de la ciudad de Medellín, Colombia.
Variables analizadas: para identificar las variables más relacionadas con la respuesta favorable al tratamiento con IBP, así como el porcentaje de respuesta, realizamos un estudio piloto de 50 pacientes. Las variables identificadas fueron: distrés posprandial; dolor epigástrico; intensidad del dolor epigástrico por escala visual análoga del dolor; saciedad precoz; síntomas típicos de reflujo gastroesofágico (pirosis o regurgitación); bloating, definido como la percepción no objetiva por parte del paciente de distensión o aumento de gas abdominal; fibromialgia, según criterios del Colegio Americano de Reumatología;11 edad; sexo; limitación funcional, definida como la necesidad de asistencia para llevar a cabo sus actividades cotidianas; dolor crónico no digestivo, definido como la necesidad de toma regular de analgésicos por más de 3 meses para control de síntomas. Además, dada la frecuente asociación con dispepsia de síntomas de ansiedad o depresión y su frecuente subdiagnóstico, se estableció en el modelo la presencia de trastorno de ansiedad o depresión, establecido por psiquiatra; también se incluyó como otra variable la manifestación de síntomas ansiosos o depresivos por parte del paciente. Esta última se definió como presente en caso de responder positivamente a las preguntas: ¿en las últimas semanas se ha sentido más preocupado/a de lo normal?; ¿en las últimas semanas se ha sentido más triste de lo normal?. No se incluyeron escalas validadas de ansiedad o depresión, ya que incluirlas obligaría a su realización en el momento de aplicar el modelo, haciéndolo más difícil de ejecutar en la práctica clínica diaria. Las seis variables con mayor asociación fueron seleccionadas para ser evaluadas en el modelo. La variable dependiente fue respuesta adecuada al manejo con IBP y se definió como resolución completa de síntomas dispépticos tras 8 semanas de tratamiento con esomeprazol a dosis mínima de 40 mg día. La mejoría parcial o no mejoría fue definida como mala respuesta al manejo con IBP.
La evaluación y el registro de las variables predictoras se realizó por medio de formularios de Google, en el cual se incluyeron de manera clara la definición de variables y el método de registro. Las personas encargadas fueron entrenadas en el registro del formato.
La evaluación de predictores no fue ciega con respecto a la variable dependiente.
Análisis estadístico: comparamos variables continúas utilizando la prueba de la t de Student para variables con distribución normal y la prueba U de Mann-Whitney para variables con distribución no normal; las variables categóricas se evaluaron con la prueba de Chi2. Calculamos razones de probabilidad (OR) y los intervalos de confianza (IC) del 95% para evaluar la fuerza de cualquier asociación con la variable dependiente. El tamaño de la muestra se estableció de acuerdo con la fórmula de Freeman. Para el desarrollo del modelo, el cálculo del tamaño muestral estimó una proporción de 40% de pacientes con mala respuesta al IBP, lo cual para la evaluación de seis variables indicó un tamaño de muestra de 150 pacientes. Para la validación interna se segmentó el total de la muestra en un 70% para el desarrollo del modelo y un 30% para la validación interna.
Resolvimos valores perdidos aleatorios < 5% con imputación múltiple; valores mayores excluían la variable del análisis. Se supuso que los datos faltantes se produjeron completamente al azar, por lo que se usó el método de imputación múltiple para abordar los datos faltantes, realizando la imputación con el mismo método de análisis de datos.
Desarrollamos el modelo por regresión logística utilizando el método del mejor subconjunto para el número y selección de variables; basándonos en criterios de información Bayesiano se incluyeron los conjuntos de variables con el mejor ajuste dándole prioridad al modelo más parsimonioso. Usamos la regresión logística multivariable con un valor de p mayor que 0,05 para la eliminación de variables no significativas en el modelo. Debido a las restricciones por el tamaño de muestra no se realizó evaluación de interacciones.
Todos los análisis estadísticos se realizaron utilizando el programa R versión 4.1.3.
Validación interna: evaluamos la validez interna realizando un proceso de remuestreo (dejar uno afuera) y estimamos nuevamente los coeficientes. Evaluamos el desempeño del modelo según la capacidad de discriminación y calibración con área bajo la curva ROC y estadístico de Hosmer Lemeshow. Definimos el punto de la curva ROC que brindaba un mejor desempeño en términos de sensibilidad y especificidad, según las probabilidades predichas por el modelo.
Transformamos el modelo final en una regla de puntuación.12 Las puntuaciones asignadas a cada variable se obtuvieron dividiendo cada coeficiente de regresión por la mitad del coeficiente más pequeño y redondeándolo al entero más cercano.
Consideraciones éticas
La investigación fue aprobada por el Comité de Ética del Institucional y fue considerada como de riesgo mínimo por ser de carácter observacional. No se realizaron ningún tipo de intervenciones o experimentos en humanos. El estudio siguió las directrices establecidas en la Declaración de Helsinki y no fue necesaria la solicitud de consentimiento informado. Los datos de los participantes fueron anonimizados.
Resultados
Participantes
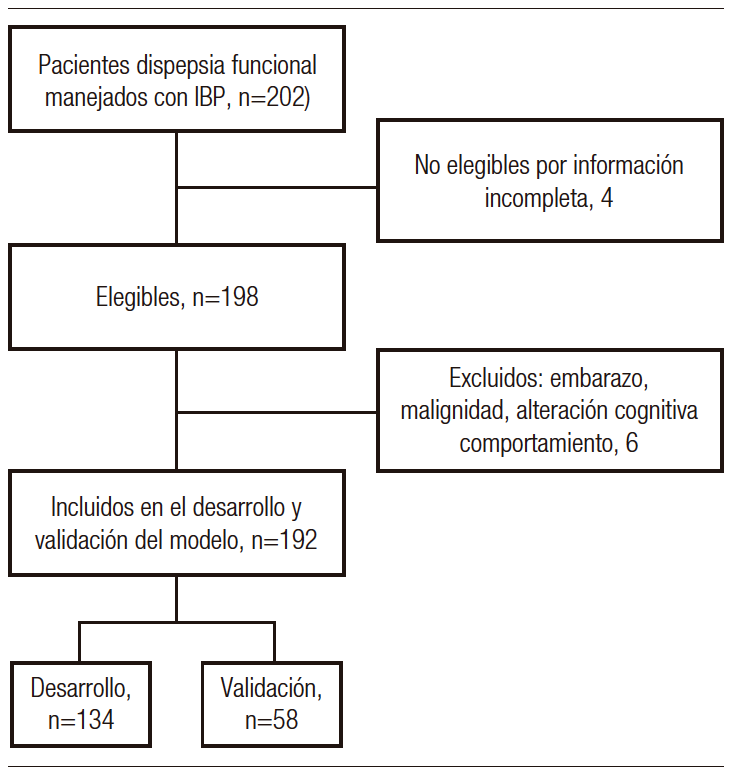
Un total de 202 pacientes cumplieron los criterios de Roma IV para DF; cuatro pacientes fueron inelegibles por información incompleta y 6 por criterios de exclusión. Los detalles de la selección de participantes se detallan (Figura 1).
Figura 1. Flujograma de selección de participantes
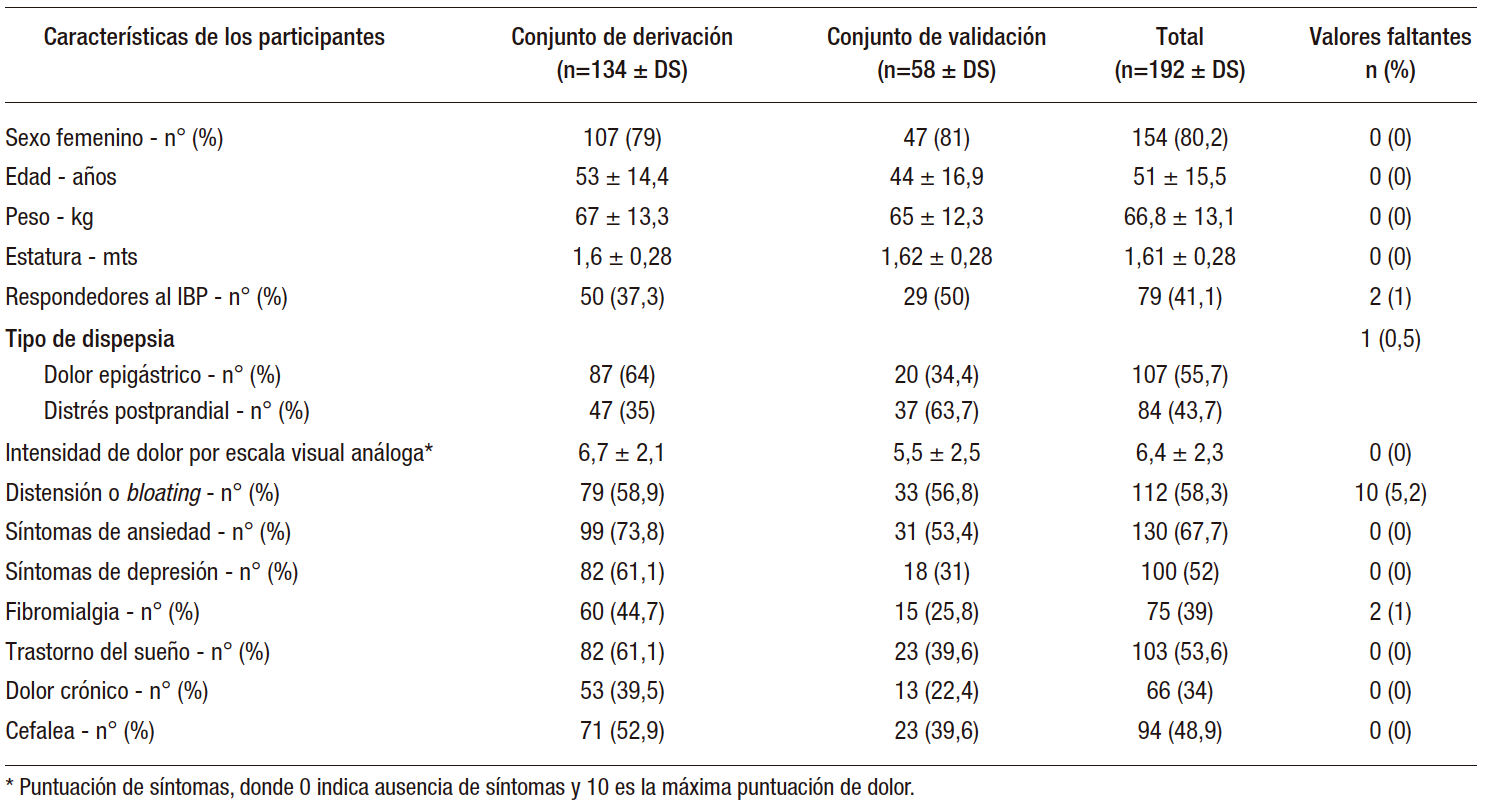
Las características clínicas y demográficas de los pacientes junto con el valor de datos perdidos se resumen (Tabla 1). Se excluyó del análisis por datos perdidos > 5% la variable bloating y saciedad temprana.
Tabla 1. Características clínicas y demográficas de los pacientes
Análisis bivariado
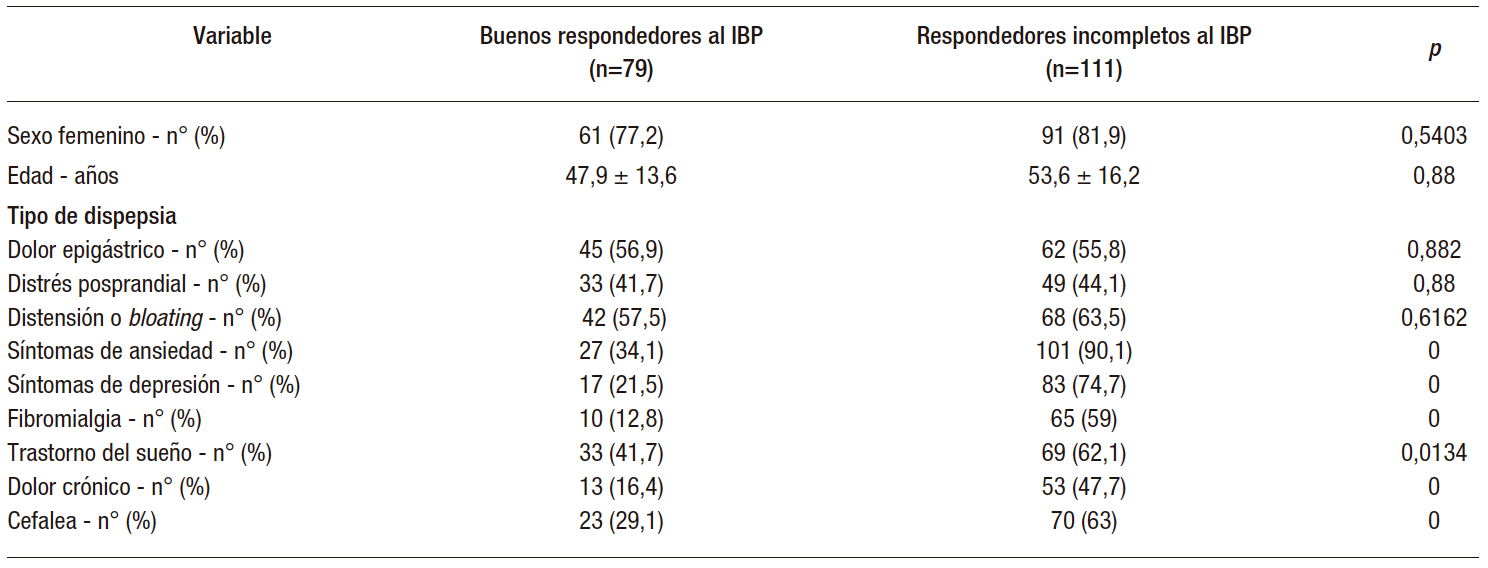
Del total de la muestra, 79 pacientes tuvieron buena respuesta al IBP (41,1%) y 111 (57,8%) presentaron respuesta incompleta o no respuesta. El 77,2% de los respondedores fueron de sexo femenino y esta proporción se elevó a 81,9% en los no respondedores. El promedio de edad en los pacientes con buena respuesta al IBP fue 47,9 años ± 13,6 vs. 53,6 años ± 16,2 en los pacientes con respuesta incompleta. De manera significativa los pacientes sin respuesta al IBP reportaban más síntomas de ansiedad (90,9% vs. 34,1%), depresión (74,1% vs. 21,5%), fibromialgia (58,5% vs 12,6%), trastornos del sueño (62,1% vs. 41,7%), dolor crónico (48,6% vs. 16,4%) y cefalea (63% vs. 29,1%). Los detalles del análisis bivariado se muestran (Tabla 2).
Tabla 2. Análisis bivariado. Asociación no ajustada con la variable independiente buena respuesta al manejo con IBP
Construcción y validación del sistema de puntuación predictiva
Para el desarrollo del modelo predictivo, empleando el método de mejor subconjunto, se identificaron cuatro variables con el mejor desempeño en términos de los criterios de información de Akaike. El modelo logístico demostró una adecuada calibración y discriminación con AUC de 0,89, IC 95%: 0,854-0,944 (Figura 2) y un resultado de la prueba de chi-cuadrado de Hosmer-Lemshow con p = 1.
Los detalles de los coeficientes de regresión se resumen (Tabla 3).
Tabla 3. Modelo logístico, coeficientes de regresión y puntaje asignado a cada variable
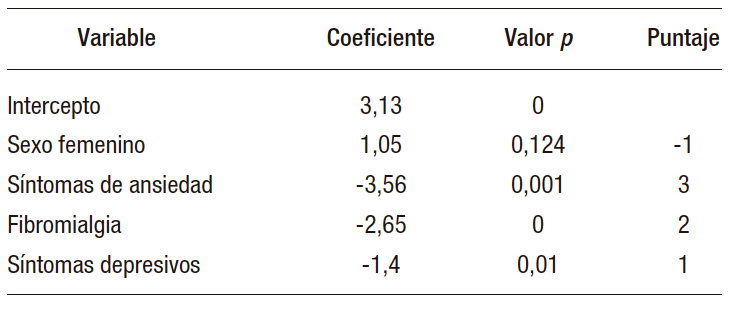
El sistema de puntuación final asignó un valor a cada variable; por ansiedad 3 puntos; fibromialgia 2 puntos; depresión 1 punto, y sexo femenino resta 1 punto (Figura 2).
Se estableció un corte de 4 puntos, al presentar una mayor capacidad de discriminación para establecer la respuesta favorable al IBP por estadístico AUC. La suma de puntuaciones inferior a 4 puntos se relacionó con una respuesta favorable al IBP, con una sensibilidad del 96,5%, (95% IC, 88,1 a 100), especificidad de 56,6% (95% IC, 37,2 a 76), valor predictivo positivo de 68,2% (95% IC, 52,8 a 83,7) y valor predictivo negativo de 94,4% (95% IC, 81 a 100).
Como usar el modelo
La regla de puntaje establece valores entre -1 y 6; para cada atributo se establece el valor 0 en caso de ausencia y el valor asignado en caso de estar presente. Para el caso de mujeres al valor final se le resta uno. Puntajes menores a 4 se van a relacionar con una respuesta favorable al IBP; para puntajes mayores se espera una respuesta parcial, por lo cual recomendamos considerar cointervenciones para optimizar la respuesta.
Discusión
Desarrollamos y validamos internamente un modelo de pronóstico fácil de usar e implementar que permite establecer la probabilidad de respuesta al manejo con IBP.
Se logró identificar una fuerte asociación de ansiedad y depresión con la mala respuesta al tratamiento con IBP. Previamente se ha destacado la complejidad de dicha asociación y la necesidad de tomar en consideración la influencia de estos síntomas en la dispepsia funcional.13
Como limitaciones del estudio se destacan la construcción y la validación del modelo en una misma población de un solo centro de atención en gastroenterología, lo cual limita la validez externa del modelo. Dado el diseño del estudio, las variables ansiedad y depresión fueron tomadas como la autopercepción general de tales síntomas por parte del paciente y no se utilizó una escala validada para la evaluación precisa de dichas variables. Asimismo, la naturaleza del estudio no permitió establecer un control adecuado de sesgos potenciales, como gastroparesia o coexistencia de SIBO, que pudieran afectar la percepción del paciente a la respuesta al tratamiento con inhibidor de bomba de protones. Tampoco existió un método para definir la adherencia al tratamiento con IBP, el cual se constituye en un sesgo al momento de definir la respuesta al tratamiento. Es importante considerar una escala de evaluación de adherencia farmacológica en los estudios de validación externa.
Existieron variables con un elevado valor de datos perdidos, las cuales se excluyeron en el desarrollo del modelo y que podrían haber tenido un desempeño importante en la definición de predictores.
Como ventajas, nuestro trabajo brinda un modelo pronóstico fácil de utilizar en el consultorio, con un rendimiento diagnóstico decente. Su empleo puede optimizar los manejos en dispepsia funcional, identificando los pacientes en quienes es necesario una evaluación y un manejo multidisciplinario para optimizar la respuesta clínica.
Es necesario realizar la validación externa de nuestros hallazgos, empleando el modelo en diferentes tipos de población, así como la correlación de síntomas ansiosos con escalas validadas para dicho fin; corregir de manera prospectiva sesgos como la coexistencia de gastroparesia o SIBO, e incluir una evaluación con escalas de adherencia farmacológica, con el propósito de evaluar de la manera más objetiva el desempeño de nuestro modelo.
Conclusiones
En conclusión, nuestro modelo de medicina de precisión para la dispepsia representa un avance significativo al permitir la identificación de subgrupos de pacientes según su respuesta a terapias de primera línea. No obstante, para garantizar su aplicabilidad clínica, es fundamental llevar a cabo una validación externa en diferentes tipos de población, así como correlacionar los síntomas ansiosos con escalas validadas para este fin. Además, es necesario corregir prospectivamente sesgos como la coexistencia de gastroparesia o SIBO, e incluir una evaluación mediante escalas de adherencia farmacológica. Esto nos permitirá evaluar de manera más objetiva el desempeño de nuestro modelo y optimizar su precisión en la práctica clínica.
Consentimiento para la publicación. Para la confección de este manuscrito, se utilizaron datos anonimizados que no han distorsionado su significado científico.
Propiedad intelectual. Los autores declaran que los datos, las figuras y las tablas presentes en el manuscrito son originales y se realizaron en sus instituciones pertenecientes.
Financiamiento. Los autores declaran que no hubo fuentes de financiación externas.
Conflicto de interés. Los autores declaran no tener conflictos de interés en relación con este artículo.
Aviso de derechos de autor
© 2024 Acta Gastroenterológica Latinoamericana. Este es un artículo de acceso abierto publicado bajo los términos de la Licencia Creative Commons Attribution (CC BY-NC-SA 4.0), la cual permite el uso, la distribución y la reproducción de forma no comercial, siempre que se cite al autor y la fuente original.
Cite este artículo como: Niño Ramírez S F, Osorio L, Santisteban M y col. Desarrollo y validación interna de un modelo predictivo pronóstico de respuesta al inhibidor de la bomba de protones en adultos con dispepsia funcional. Acta Gastroenterol Latinoam. 2024;54(3):247-253. https://doi.org/10.52787/agl.v54i3.422
Referencias
- Ford AC, Mahadeva S, Carbone MF, Lacy BE, Talley NJ. Functional dyspepsia. The Lancet. 2020;396(10263):1689-702.
- Stanghellini V, Chan FKL, Hasler WL, Malagelada JR, Suzuki H, Tack J, et al. Gastroduodenal Disorders. Gastroenterology. 2016;150(6):1380-92.
- Aro P, Talley NJ, Agréus L, Johansson SE, Bolling-Sternevald E, Storskrubb T, et al. Functional dyspepsia impairs quality of life in the adult population: Functional dyspepsia and quality of life. Aliment Pharmacol Ther. 2011;33(11):1215-24.
- Harer KN, Hasler WL. Functional Dyspepsia: A Review of the Symptoms, Evaluation, and Treatment Options. Gastroenterol Hepatol. 2020;16(2):66-74.
- Wauters L, Talley NJ, Walker MM, Tack J, Vanuytsel T. Novel concepts in the pathophysiology and treatment of functional dyspepsia. Gut. 2020;69(3):591-600.
- Pinto-Sanchez MI, Yuan Y, Hassan A, Bercik P, Moayyedi P. Proton pump inhibitors for functional dyspepsia. Cochrane Upper GI and Pancreatic Diseases Group, editor. Cochrane Database Syst Rev [Internet]. 21 de noviembre de 2017 [citado 27 de enero de 2019]; Disponible en: http://doi.wiley.com/10.1002/14651858.CD011194.pub3
- Nagahara A, Miwa H, Asaoka D, Shimada Y, Sasaki H, Matsumoto K, et al. Pretreatment prediction of symptom response to proton pump inhibitor therapy. J Gastroenterol Hepatol. 2015;30 Suppl 1:25-30.
- Hsu YC, Liou JM, Yang TH, Hsu WL, Lin HJ, Wu HT, et al. Proton pump inhibitor versus prokinetic therapy in patients with functional dyspepsia: is therapeutic response predicted by Rome III subgroups? J Gastroenterol. 2011;46(2):183-90.
- Bolling-Sternevald E, Lauritsen K, Talley NJ, Junghard O, Glise H. Is it possible to predict treatment response to a proton pump inhibitor in functional dyspepsia? Aliment Pharmacol Ther. 2003;18(1):117-24.
- Collins GS, Reitsma JB, Altman DG, Moons KGM. Transparent Reporting of a multivariable prediction model for Individual Prognosis Or Diagnosis (TRIPOD): The TRIPOD Statement. Ann Intern Med. 2015;162(1):55-63.
- Wolfe F, Clauw DJ, Fitzcharles MA, Goldenberg DL, Häuser W, Katz RS, et al. Fibromyalgia Criteria and Severity Scales for Clinical and Epidemiological Studies: A Modification of the ACR Preliminary Diagnostic Criteria for Fibromyalgia. J Rheumatol. 2011;38(6):1113-22.
- Sullivan LM, Massaro JM, D’Agostino RB. Presentation of multivariate data for clinical use: The Framingham Study risk score functions. Stat Med. 2004;23(10):1631-60.
- Kugler TE. [ANXIETY AND DEPRESSIVE DISORDERS IN FUNCTIONAL DYSPEPSIA: CAUSE OR CONSEQUENCE?]. Eksp Klin Gastroenterol Exp Clin Gastroenterol. 2015;(9):29-35.
Correspondencia: Sebastián Fernando Niño Ramírez
Correo electrónico: sfnesp@gmail.com
Acta Gastroenterol Latinoam 2024;54(3):247-253
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE