Roberto Salgado (h), Marcelo Oliva, Federico Rovegno, Nicolás Avellaneda, Tomás Lancelotti, Ricardo Oddi
Servicio de Cirugía General, Hospital CEMIC. Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2018;48(1):13-22
Recibido: 29/12/2016 / Aprobado: 23/10/2017 / Publicado en www.actagastro.org el 19/03/2018
Resumen
El uso de la colangiografía intraoperatoria (CIO) de forma rutinaria vs. selectiva durante la colecistectomía ha sido controversial en las últimas décadas. Objetivo. Analizar nuestra experiencia en la realización de CIO selectiva para identificar lesiones quirúrgicas de la vía biliar (LQVB) y comparar nuestra prevalencia con otras instituciones. Diseño. Estudio observacional, descriptivo, retrospectivo. Material y métodos. Sobre 1799 colecistectomías laparoscópicas (CL) en un período de 6 años (2010-2015) en un solo centro, se analizaron las causas que llevaron a realizar una CIO y se identificaron aquellos pacientes que tuvieron LQVB. Resultados. Se realizaron 1817 colecistectomías, 1545 se realizaron de forma programada y 272 de urgencia. El 95,8% se realizó de forma laparoscópica y el 3,1% necesitó ser convertida. Se indicó CIO de forma selectiva al 22,9%. El porcentaje de LQVB grave representa el 0,22% de la muestra. Hubo 8 lesiones en total, 4 de ellas fueron tipo A de la clasificación de Strasberg. Las 4 restantes fueron lesiones graves (2 tipo D, 1 tipo E1 y 1 tipo E3) identificadas en el mismo acto operatorio y resueltas por otro miembro del servicio. Conclusiones. El porcentaje de lesiones quirúrgicas graves de la vía biliar realizando una CIO de forma selectiva fue de 0,22%. Todas las lesiones fueron identificadas por CIO y resueltas en el mismo acto operatorio. No existe diferencia significativa en la prevalencia de LQVB comparándola con centros donde se utiliza la CIO de forma rutinaria.
Palabras claves. Colangiografía intraoperatoria, litiasis vesicular, estudio retrospectivo, lesión quirúrgica de la vía biliar.
Cystic Selective intraoperative cholan-giography and bile duct injury during laparoscopic cholecystectomy
Summary
The use of routinely vs selective Intraoperative cholangiography (IOC) during cholecystectomy has been controversial in the last decades. The aim of the present study is to analyze our experience in the use of selective IOC to identify bile duct injuries and compare our incidence of Bile Duct Injury (BDI) with that in other institutions. Material and methods. Observational, descriptive and retrospective analysis performed in 1,799 Laparoscopic Cholecystectomies (LCs) during a 6-year period (2010-2015) in a single center in Buenos Aires. Causes that led to the use of IOC were analyzed and patients who suffered from BDI were identified. Results. We performed 1,817 cholecystectomies, 1,545 were elective and 272 were emergency cholecystectomies. 95.8% were laparoscopic and 3.1% had to be converted. Selective IOC was indicated in 22.9% of the cases. Severe BDI represented 0.22% of the study population. There were 8 injuries in total, 4 of them were Type A according to the Strasberg classification. The remaining 4 were severe injuries (2 Type D, 1 Type E1 and 1 Type E3), identified during the same surgical act and repaired by a different specialist. Conclusion. Of 1,799 cholecystectomies performed during the 6 year period, the study yielded 0.22% severe BDI detected by selective IOC. All injuries were repaired during the same surgical act. There is no significant difference in the incidence of injuries when compared with institutions where the IOC is performed routinely.
Key words. Intraoperative cholangiography, gall bladder lithiasis, retrospective study, surgical lesion of the bile duct.
La introducción de la laparoscopía ha aumentado la prevalencia de la lesión quirúrgica de la vía biliar (LQVB).1, 2
La utilización de la colangiografía intraoperatoria (CIO) en la colecistectomía laparoscópica (CL) realizada en forma rutinaria es debatible.3, 5-7
La CIO fue descripta inicialmente en 1937 y se estableció como una herramienta para la identificación de la litiasis coledociana en 1960.8 Otro rol de suma importancia durante la colecistectomía es el reconocimiento temprano de las lesiones de la vía biliar y, en ocasiones, la prevención de lesiones mayores.
El empleo de la CIO puede ser selectivo o de rutina, y diversas publicaciones muestran las preferencias y experiencias de los distintos centros.3, 5, 7, 9-14
Los objetivos de este trabajo son 1) analizar retrospectivamente los resultados obtenidos en una serie de 1799 colecistectomías laparoscópicas realizadas durante el período comprendido entre enero de 2010 y diciembre de 2015 en un hospital universitario de la Ciudad Autónoma de Buenos Aires, identificando las LQVB y relacionándolas con las CIO selectivas realizadas, 2) comparar los resultados con series de grupos que realizan CIO de forma rutinaria.
Material y métodos
Se recolectó de forma retrospectiva la información sobre 1817 pacientes de un hospital universitario de la Ciudad de Buenos Aires, a los cuales se les realizó una colecistectomía entre 2010 y 2015.
Se tomaron en cuenta solo a aquellos pacientes en los cuales se inició la cirugía en forma laparoscópica, independientemente de si fue convertida o no, por lo cual el número de pacientes se redujo a 1799. El tiempo de seguimiento de los pacientes fue de 1 año.
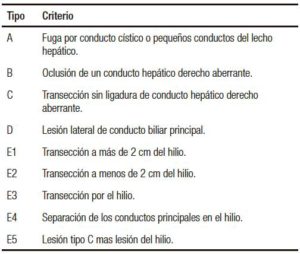
Se utilizó la clasificación de Strasberg para describir el tipo de lesión quirúrgica de vía biliar (Tabla 1).15
Tabla 1. Clasificación de Strasberg.
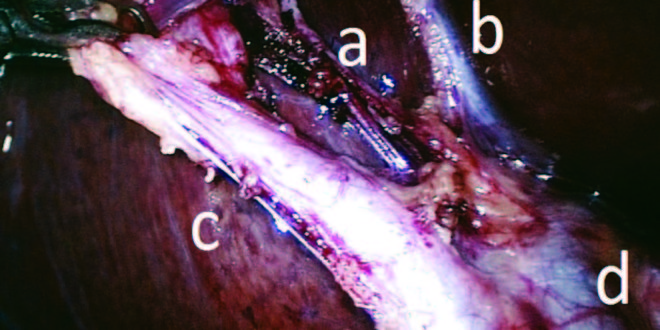
En nuestro servicio utilizamos la técnica americana para la colecistectomía laparoscópica con el paciente en decúbito dorsal, el cirujano y el 2do ayudante a la izquierda del paciente y el 1er ayudante a la derecha.16 Se comienza la cirugía realizando el neumoperitoneo con aguja de Veress en aquellos casos en los cuales no hay antecedentes de cirugías abdominales previas. En caso contrario, el ingreso se realiza por disección. Se colocan 4 trócares (2 x 12 mm: umbilical y epigástrico; 2 x 5 mm: flanco derecho) según la técnica americana. Se realiza la exploración de la cavidad abdominal reconociendo la vesícula y el estado de la misma, la vía biliar principal y el duodeno. Se procede a la exposición del triángulo de Calot, traccionando el fondo vesicular y el bacinete (Figuras 1 y 2). Se comienza la disección de los elementos: conducto cístico, arteria cística y placa cística hasta lograr el “critical view of safety” (CVS) descripto por primera vez en 1995 por Strasberg.17, 18 El mismo consta de tres pasos. El primero es la liberación de tejido graso y fibroso del triángulo de Calot. El segundo es la separación de la porción inferior vesicular de la placa cística y, por último, el reconocimiento de solo dos estructuras ingresando a la vesícula. Una vez logrado este objetivo, se procede a clipar y seccionar la arteria cística y conducto cístico, para luego continuar con el lecho vesicular. La ectomía vesicular se realiza a través de la incisión del trocar epigástrico. En todos los casos se controla la hemostasia y bilistasia. Cuando la disección es dificultosa debido a un proceso inflamatorio extenso, o bien la identificación correcta de la anatomía se encuentra en duda debido a variaciones anatómicas, se realiza también una CIO.19
Figura 1. Punto crítico de seguridad, vista anterior. Arteria cística (a), borde hepático (b), conducto cístico (c), conducto hepático común (d).
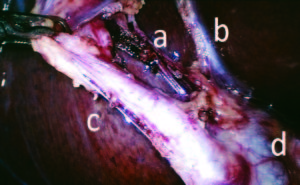
Figura 2. Punto crítico de seguridad, vista posterior. Arteria cística (a), conducto cístico (c), conducto hepático común (d).
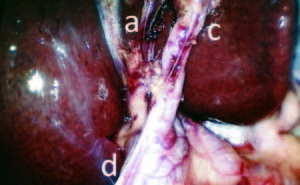
Para realizarla se procede en primer lugar con la cisticotomía lo más cercana posible al bacinete. Se coloca una sonda K-33 / K-30 según el diámetro del conducto. Se utilizan de 5 a 10 ml de Iotalamato de Meglumina al 60% como contraste (Conray). De esta forma se identifica de forma clara y precisa la anatomía de la vía biliar.15, 17, 20
De obtener una colangiografía normal: contraste completo del árbol biliar, conducto cístico, colédoco, conducto hepático común (CHC), conducto hepático derecho (CHD), conducto hepático izquierdo (CHI) y sectoriales, correcto pasaje del contraste a duodeno, ausencia de fuga de contraste y una vía biliar expedita, se procede al clipado del conducto cístico, luego la arteria cística, y luego se continúa con idéntica técnica descripta para la CL sin CIO.21
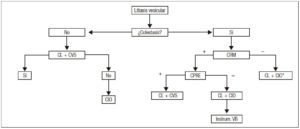
El manejo de la litiasis coledociana asociada a la colecistectomía laparoscópica y la realización de la CIO es un tema importante, pero no es motivo de análisis en este trabajo. El análisis retrospectivo con seguimiento a un año nos impide realizar la evaluación en un lapso adecuado para dar datos fidedignos sobre litiasis residual. La Figura 3 muestra el algoritmo diagnóstico y terapéutico utilizado por el servicio.22
Figura 3. Algoritmo diagnóstico y terapéutico. Cuando se presenta un paciente con litiasis vesicular sintomática, en primer lugar se debe descartar la presencia de litiasis coledociana asociada: según el cuadro clínico, el laboratorio y la ecografía abdominal inicial. En caso de sospecha de ocupación de la vía biliar extrahepática por alteración de alguna de las pruebas iniciales, se realiza rutinariamente una CRM de abdomen. Si se identifica un cálculo en la vía biliar mediante una CRM, se intentará su extracción mediante una CPRE previa a la cirugía y luego se procederá a realizar la CL, con o sin CIO de acuerdo con la técnica descripta. Si no se pudo extraer el cálculo mediante CPRE, se realizará la CL con instrumentación de la vía biliar e intentará solucionarse mediante dicho abordaje.
CL: Colecistectomía laparoscópica; CVS: Critical View of Safety; CRM: colangioresonancia magnética.
*En aquellos casos en que la CRM es negativa pero quedan dudas sobre la existencia de litiasis coledociana, se realizará CIO.
Resultados
Dentro de las 1817 colecistectomías realizadas, 1545 se realizaron de forma programada y 272 de urgencia.
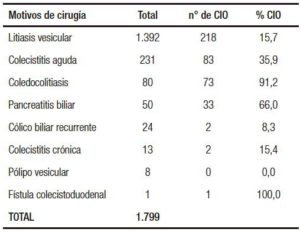
La edad mediana fue de 50 años (rango: 8-93). La proporción hombre mujer fue de 1:1,5. De las 1817 colecistectomías, se realizaron por vía laparoscópica 1742 (95,8%), se convirtieron 57 (3,1%), y por vía convencional 18 (1,0%). Por lo tanto, el número total de pacientes a analizar es 1799, ya que se descartan aquellas realizadas por vía convencional. El mayor porcentaje de cirugías se debió a litiasis vesicular (77,4%). Luego sigue en frecuencia la colecistitis aguda con 13% (Tabla 2).
Tabla 2. Motivos de cirugía y % de CIO.
La totalidad de las CL fueron realizadas por residentes acompañados siempre por un médico de planta.
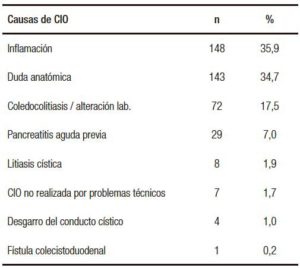
En el período comprendido entre 2010 y 2015 se indicaron 412 CIO, de las cuales 109 fueron programadas en pacientes con antecedentes de litiasis coledociana no resuelta por CPRE, alteración en el hepatograma prequirúrgico, o bien pancreatitis aguda biliar. En 303 pacientes se indicó realizar CIO por no poder cumplir con los principios de Strasberg. En 7 de esos 303 no se pudo realizar CIO por dificultades técnicas, lo que representa un 98% de efectividad en la realización de la misma. El servicio realiza CIO al 22,9% de las colecistectomías laparoscópicas. En la Tabla 3 se detallan las causas que llevaron a realizar la CIO.
Tabla 3. Causas de CIO selectiva y porcentajes.
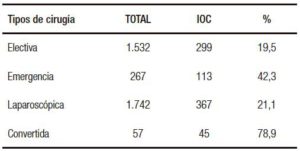
En las cirugías laparoscópicas se realiza CIO al 21% y en aquellas que fueron convertidas ese porcentaje aumenta a 78%, lo cual se comprende ya que las razones que llevan a modificar la técnica quirúrgica habitualmente son la gran inflamación y la dificultad en la disección por laparoscopia. En cirugías de urgencia: 42% de CIO y en programadas 19,5%; las causas de esa diferencia de porcentajes obedecen a que las urgencias suelen ser cuadros de colecistitis aguda (Tabla 4).
Tabla 4. Tipos de colecistectomías.
En la Tabla 5 se analizan los motivos de internación de los pacientes operados y los porcentajes de CIO.
Tabla 5. Motivos de la cirugía.
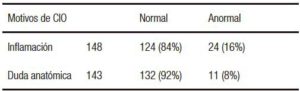
Tomando como referencia un resultado de CIO normal cuando el contraste tiñe por completo el árbol biliar (conducto cístico, colédoco, CHC, CHD, CHI y sectoriales), existe buen pasaje del contraste a duodeno sin imágenes negativas en su interior, ausencia de fuga de contraste y una vía biliar expedita. En caso de duda anatómica los resultados fueron normales en el 92% vs. 84% cuando existía un gran componente inflamatorio.
El número total de lesiones de la vía biliar fue de 8 y en todos los casos fueron lesiones advertidas durante el procedimiento. Se utilizó la clasificación de Strasberg para identificarlas (Tabla 1).15
Se produjeron 4 lesiones tipo A, las cuales no se han tenido en cuenta en el análisis de este trabajo ya que no tuvieron ninguna implicancia clínica de importancia. Las 4 lesiones restantes son: 2 del tipo D, una E1 y una E3 (Tabla 6). El resultado es un porcentaje de lesión de 0,22% sobre el total de CL en el período estudiado.
En todos los casos fueron resueltas en el mismo procedimiento quirúrgico por otro cirujano especialista en HPB del servicio de cirugía general.23-26
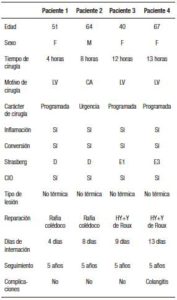
Los principales factores contribuyentes en la producción de las lesiones son la inflamación y las variaciones en la anatomía de la vía biliar. El mecanismo de lesión fue sección con tijera de la vía biliar. No hubo lesiones térmicas. La reparación requirió la conversión en todas las lesiones graves. Se realizó mediante una rafia al colédoco en el caso de las lesiones tipo D y una hepático y bihepáticoyeyuno anastomosis en el tipo E1 y E3 respectivamente. No hubo lesiones vasculares asociadas (Tabla 7).
Tabla 7. Pacientes con LQVB grave.
Discusión
Este trabajo está basado en un análisis retrospectivo del Servicio de Cirugía General de un hospital universitario de Buenos Aires, teniendo en cuenta el uso selectivo de la CIO durante la CL y el impacto en las LQVB.
La colecistectomía en nuestro servicio es realizada en todos los casos por residentes, acompañados por médicos de planta.
La litiasis vesicular es una patología frecuente, con una prevalencia del 21,6% en la ciudad de Buenos Aires.27
Desde el año 1993 la colecistectomía laparoscópica es el tratamiento de elección para la litiasis vesicular sintomática.28
Desde el comienzo de la CL, se han descripto técnicas para identificar correctamente el conducto cístico:13-15, 29
- Técnica cístico-infundibular: se basa en el reconocimiento de la unión del cístico con el infundíbulo vesicular.
- Técnica que identifica la unión cístico-coledociana.
- La colangiografía intraoperatoria.
- El Critical View of Safety.12, 15, 29
Actualmente en la literatura existen diversos estudios que avalan la técnica de colecistectomía descripta por Strasberg (CVS), demostrando que la misma no tiene mayor incidencia de LQVB.12-15, 30
Nuestra técnica se basa en una disección meticulosa del triángulo de Calot, intentando identificar el critical view of safety en el 100% de nuestras cirugías. Esto, realizado correctamente, permite identificar variantes anatómicas y favorece la prevención de las LQVB.
Aún hoy es un tema de debate el uso de CIO selectivo o de rutina.3-7, 31 De acuerdo con nuestro criterio, lo que previene la LQVB es una disección minuciosa del CVS, usando la CIO como una herramienta fundamental cuando el CVS no puede ser logrado. En nuestra serie le realizamos CIO al 22,9%, casi a 1 paciente de cada 4 operados.
Daly y col. en un interesante trabajo publicado en el año 2015 analizaron las encuestas realizadas a 374 cirujanos del Midwest Surgical Association (MSA) y de la American Gastrointestinal and Endoscopic Surgeons (SAGES), los cuales realizan en promedio 100 colecistectomías al año. Según la encuesta, la gran mayoría no describió el CVS durante la CL, solo el 27% lo hizo. El mayor porcentaje de cirujanos utilizó la técnica infundibular y solo un 16% de los 374 realizó CIO de rutina.32
El porcentaje de LQVB en nuestra serie fue de 0,22%, realizándose CIO al 22,9%. Las principales causas por las cuales no pudimos seguir los criterios de Strasberg y por lo tanto nos llevaron a realizar CIO fueron: inflamación (35 %) y duda anatómica (34%).
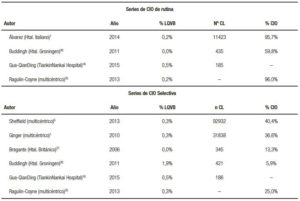
Nuestra prevalencia de LQVB es similar a los centros que realizan CIO de forma rutinaria (Tabla 8). Es amplia la literatura que avala nuestra conducta.
Tabla 8. Cuadro comparativo con otros centros.
La Asociación Europea de Estudio del Hígado (EASL), en las guías de práctica clínica sobre prevención, diagnóstico y tratamiento en litiasis vesicular publicadas recientemente, hace mención sobre el uso de la CIO.33 En ellas publican que el uso selectivo o rutinario de la CIO no es necesario en aquellos pacientes con bajo riesgo de litiasis coledociana (recomendación débil; evidencia de baja calidad). En un estudio sistemático comparando uso de la CIO (rutina o selectivo) vs. el no uso de la CIO se demuestra que no existen diferencias significativas en la frecuencia de las LQVB.9 Incluso menciona mayores complicaciones en aquellos pacientes donde se realizó la CIO de rutina y mayor tiempo operatorio.9 Debido a esas razones no existe evidencia suficiente para recomendar el uso rutinario de la CIO.33
En las guías se hace referencia al manejo de litiasis residual postcolecistectomía, actualmente no se dispone de ningún ensayo clínico randomizado que evidencie beneficio de la utilización de la CIO de rutina en los pacientes de bajo riesgo para tener coledocolitiasis. Se entiende por bajo riesgo pacientes sin alteraciones en el hepatograma, sin pancreatitis agudas biliares previas o datos en la ecografía que la hagan sospechar.33
Ford publica en el año 2012 una revisión sistemática de estudios randomizados controlados y no encuentra diferencias significativas con respecto a lesión quirúrgica de vía biliar, y la litiasis residual. Sí menciona las complicaciones secundarias a la CIO de rutina: el aumento del tiempo de cirugía, entre otras.9
Nosotros también consideramos que la radiación a la que se exponen los cirujanos, residentes y personal de quirófano no es un tema menor y debe ser motivo de análisis a futuro. Ninguna serie estudia este punto y sería útil analizarlo a la hora de decidir realizar la CIO sistemática.
En la actualidad hay autores que consideran que utilizando la CRM y la CPRE la realización de la CIO no es indispensable, y su utilización sería menos frecuente en lo que respecta a la litiasis coledociana.34
De las 409 CIO realizadas en nuestra serie, 303 fueron realizadas por no cumplir los criterios de Strasberg. En 109 pacientes se realizó CIO por presentar litiasis coledociana no resuelta por CPRE, alteración en el hepatograma prequirúrgico o bien por pancreatitis aguda biliar previa.
Metcalfe y col. realizan una revisión de la literatura comparando la incidencia de LQVB entre CL con CIO de rutina vs. CL sin CIO. Los resultados de sección completa de la vía biliar fueron 0,02% y 0,09% respectivamente. Esta diferencia no es considerada estadísticamente significativa.10
En el año 2012 se publicaron las guías europeas. En ellas también mencionan que el uso de CIO rutinario es controversial. El panel de expertos concluyó que no se puede recomendar de manera rutinaria la CIO basándose en la literatura actual. Pero sí permite diagnosticar precozmente la LQVB siempre y cuando esté bien interpretada.35
Giger y col. analizaron 31.838 pacientes a los cuales se les realizó una CL por colecistitis aguda o crónica en un período de 10 años. Se indicó CIO al 36,6%, de los cuales 40 pacientes presentaron LQVB. No se realizó CIO en el 63,4% y se reportaron un total de 61 LQVB. Esta diferencia no fue estadísticamente significativa en cuanto a la incidencia de LQVB.3
En nuestra serie se realizó diagnóstico intraoperatorio de LQVB en el 100% de los casos y se decidió la conversión en todos ellos. Somos partidarios de que la resolución se lleve a cabo en ese momento por otro cirujano con experiencia en cirugía hepatobiliar que no haya intervenido en la lesión. Es importante mencionar que no hubo lesiones vasculares asociadas en ningún caso. La reparación de la LQVB en el mismo acto operatorio o en forma diferida es discutida actualmente en la bibliografía.23 En los 4 casos que tuvimos LQVB pudimos hacer un correcto diagnóstico mediante colangiografía, en ninguno de los casos fueron lesiones térmicas y contamos con un cirujano HPB entrenado en el hospital en ese momento.
Recientemente B. Tornqvist y col. publican en BJS una serie que engloba 51.041 pacientes del registro nacional sueco en 5 años. Su conclusión luego del análisis es que la CIO estaría restringida a casos de colecistitis aguda.36 En nuestro servicio la mayor indicación de CIO fue en los casos donde se encontró procesos inflamatorios. Esto se ve reflejado en el número de CIO en cirugías de urgencia: 113 CIO de 267, lo que representa un 42%. Avalamos la utilidad de la CIO en los cuadros inflamatorios.13 Nuestra conducta es operar los cuadros de colecistitis agudas una vez hecho el diagnóstico, en las primeras 24 h.37, 38
La CIO utilizada durante la CL es utilizada con dos objetivos: para identificar la anatomía de la vía biliar y para detectar cálculos.4, 9, 39 La evidencia es inconsistente en cuanto a la efectividad de la CIO en la prevención de lesiones de la vía biliar y el manejo de la litiasis.4, 9
CEMIC es un Hospital Universitario y dispone de la carrera de especialización en Cirugía General desde el año 1965. Con respecto al aprendizaje de la anatomía de la vía biliar y el manejo transcístico, es cierto que la CIO selectiva es un factor negativo para la formación de residentes, pero disponemos de medios para atenuar dicha situación.
Se realizaron en el período evaluado 409 CIO, con un promedio de 80 CIO por año. A este número se suman las colangiorresonancias preoperatorias que se realizan en pacientes con sospecha de litiasis coledociana, las colangiografías transparietohepáticas, las tomografías computadas trifásicas y resonancias magnéticas de hígado, y todo el estudio de los pacientes de la unidad de Cirugía Hepatobiliar de CEMIC en la cual los residentes tienen una participación activa. Todo lo mencionado hace que el residente de Cirugía General de CEMIC tenga, luego de 4 años de formación, un conocimiento profundo de la anatomía de la vía biliar.
Conclusión
El porcentaje de lesiones quirúrgicas graves de la vía biliar de nuestro centro en 6 años analizados fue de 0,22%, realizándose CIO de forma selectiva. Todas las lesiones fueron identificadas en el intraoperatorio por medio de CIO y luego resueltas. No existe diferencia significativa de la incidencia de lesión al comparar con aquellos centros donde se utiliza CIO de forma rutinaria. Por lo tanto, concluimos que la CIO selectiva puede ser una opción, si se respetan en forma estricta los pasos de la CL y el Critical View of Safety descripto por Strasberg, considerando la colangiografía como una herramienta fundamental cuando el CVS no es logrado.
Conflicto de intereses. Los autores declaran no presentar conflicto de interés.
Referencias
- Adamsen S, Hansen OH, Jensen PMF, Schulze S, Stage JG, Wara P, Jensen LP. Enprospektivregistrering. Ugeskrift for Læger 1995; 157: 4449-4454.
- Kirstine Moll Harboe, Linda Bardram. The quality of cholecystectomy in Denmark: outcome and risk factors for 20,307 patients from the national database. SurgEndosc 2011; 25: 1630-1641.
- Giger U, Ouaissi M, Schmitz SF, Krähenbühl S, Krähenbühl L. Bile duct injury and use of cholangiography during laparoscopic cholecystectomy. Br J Surg 2011; 98: 391-396.
- Sheffield K, Han Y, Kuo Y, Townsend CM Jr, Goodwin JS, Riall TS. Variation in the use of intraoperative cholangiography during cholecystectomy. J Am Coll Surg 2012; 214: 668-679.
- Álvarez FA, de Santibañes M, Palavecino M, Sánchez Clariá R, Mazza O, Arbues G, de Santibañes E, Pekolj J. Impact of routine intraoperative cholangiography during laparoscopic cholecystectomy on bile duct injury. Br J Surg 2014; 101: 677-684.
- Ding GQ, Cai W, Qin MF. Is intraoperative cholangiography necessary during laparoscopic cholecystectomy for cholelithiasis? World J Gastroenterol 2015; 21: 2147-2151.
- Khaira HS, Ridings PC, Gompertz HK. Routine Laparoscopic Cholangiography: A means of avoiding unnecessary endoscopicretrograde cholangiopancreatography. Journal of Laparoendoscopic & Advanced Surgical Techniques 2009; 9: 17-22.
- Mirizzi PL. Operative cholangiography. Surg Gynecol Oncol 1937; 65: 702-710.
- Ford J, Soop M, Du J, Loveday BP, Rodgers M. Systematic review of intraoperative cholangiography in cholecystectomy. Br J Surg 2012; 99: 160-167.
- Metcalfe MS, Ong T, Bruening MH, Iswariah H, Wemyss-Holden SA, Maddern GJ. Is laparoscopic intraoperative cholangiogram a matter of routine? Am J Surg 2004; 187: 475-481.
- Massarweh NN1, Flum DR. Role of intraoperative cholangiography in avoiding bile duct injury. J Am Coll Surg 2007; 204: 656-664.
- Avgerinos C, Kelgiorgi D, Touloumis Z, Baltatzi L, Dervenis C. One Thousand Laparoscopic Cholecystectomies in a Single Surgical Unit Using the “Critical View of Safety” Technique. J Gastrointest Surg 2009; 13: 498-503.
- Sanjay P, Fulke JL, Exon DJ. ‘Critical View of Safety’ as an Alternative to Routine Intraoperative Cholangiography During Laparoscopic Cholecystectomy for Acute Biliary Pathology J Gastrointest Surg 2010; 14: 1280-1284.
- Yegiyants S, Craig Collins J. Operative Strategy Can Reduce the Incidence of Major Bile Duct Injury in Laparoscopic Cholecystectomy Presented at the 19th Annual Scientific Meeting of the Southern California Chapter of the American College of Surgeons in Santa Barbara, CA, January 18-20, 2008.
- Strasberg S, Hertl M, Soper N. Analysisof theproblem of biliary injury during laparoscopic cholecystectomy. J Am Coll Surg 1995; 180: 101-125.
- Asbun H, Rossi R. Techniques of laparoscopic cholecystectomy, The difficult operation. Surg Clin North Am 1994; 74: 755-775.
- Strasberg SM, Brunt ML. Rationale and Use of the Critical View of Safety in Laparoscopic Cholecystectomy. J Am Coll Surg 2010; 211: 132-138.
- Strasberg SM. A teaching program for the ‘culture of safety in cholecystectomy’ and avoidance of bile duct injury. J Am Coll Surg 2013; 217: 751.
- Stremple J. The need for careful operative dissection in Moosman´s area during cholecystectomy. Surgery Gynecology & Obstetrics 1986; 163: 169-173.
- Strasberg SM, Helton WS. An analytical review of vasculobiliary injury in laparoscopic and open cholecystectomy. HPB 2011; 13: 1-14.
- Livingston EH, Miller JA, Coan B, Rege RV. Indications for selective intraoperative cholangiography. J GastrointestSurg 2005; 9: 1371-1377.
- Barkun JS, Fried GM, Barkun AN, Sigman HH, Hinchey J, Garzon J, Wexler MJ, Meakins JL. Cholecystectomy Without Operative Cholangiography Implications for Common Bile Duct Injury and Retained Common Bile Duct Stones. Annals of Surg 1993; 218: 371-379.
- Iannelli A, Painea J, Hamy A, Schneck AS, Schaaf C, Gugenheiml J. Primary versus delayed repair for bile duct injuries sustained during cholecystectomy: results of a survey of the Association Francaise de Chirurgie. HPB 2013; 15: 611-616.
- Flum DR, Cheadle A, Prela C, Patchen Dellinger E, Chan L. Bile Duct Injury During Cholecystectomy and Survival in Medicare Beneficiaries. JAMA 2003; 290: 2168-2173.
- Hamad MA, Nada AA, Abdel-Atty MY, Kawashti AS. Major biliary complications in 2,714 cases of laparoscopic cholecystectomy without intraoperative cholangiography: amulticenter retrospective study Surg Endosc 2011, 25: 3747-3751.
- Waage A, Nilsson M. Iatrogenic Bile Duct InjuryA Population-Based Study of 152 776 Cholecystectomies in the Swedish Inpatient Registry. Arch Surg 2006; 141: 1207-1213.
- Palermo M, Berkowski D, Gaynor F, Loviscek M, Verde JM, Cardoso Cúneo J, Herrera S, De la Vega S, Ferreres A, Córdoba P, Giménez M. Prevalencia de litiasis vesicular. Analisis preliminar Proyecto LIVE. Rev Argent Cirug 2011; 100: 85-99.
- Gollan JL, Bulkley GB, Diehl AM, Elashoff JD, Federle MP, Hogan WJ, Kelly KA, Massanari DL, Powell DW, Sorrell M, Wilson JAP, Barkun JST, Bass EB, Bernard H, Carr-Locke DL, Fitzgibbons RJ Jr, Friedman GD, Gadacz TR, Hofmann AF, Hunter JG, McSherry ChK, Meyers WC, Moody FG, Nahrwold DL, Olsen DO, Pellegrini CA, Perissat J, Petelin JB, Phillips EH, Pitt HA, Schoenfield LJ, Soper NJ, Strasberg SM, Traverso LW, White JV, Zucker KA, Kaiser SC, Bray EA, Burton BT, Everhart J, Ferguson JH, Foster WR, Gadacz TK, Hall WH, Hamilton FA, Hoofnagle JH, Meyers W. NIH Consensus conference. Gallstones and laparoscopic cholecystectomy. JAMA 1993; 269: 1018-1024.
- Strasberg SM, Eagon ChJ, Drebin JA. The “Hidden Cystic Duct” Syndrome and the Infundibular Technique of Laparoscopic Cholecystectomy – the Danger of the False Infundibulum. J Am Coll Surg 2000; 191: 661-667.
- Pekolj J, Álvarez FA, Palavecino M, Sánchez Clariá R, Mazza O, de Santibañes E. Intraoperative management and repair of bile duct injuries sustained during 10,123 laparoscopic cholecystectomies in a high-volume referral center. J Am Coll Surg 2013; 216: 894-901.
- Shively EH, Wieman TJ, Adams AL, Romines RB, Garrison RN. Operative cholangiography. Am J Surg 1990; 159: 380-384.
- Daly SC, Deziel DJ, Li X, Thaqi M, Millika KW, Myers JA, Bonomo S, Luu MB. Current practices in biliary surgery: Do we practice what we teach? Surg Endosc. 2016; 30: 3345-3350.
- EASL Clinical Practice Guidelines bvvmtreatment of gallstones. European Association for the Study of the Liver (EASL). Journal of Hepatology 2016; 65: 146-181.
- Sirinek KR, Schwesinger WH. Has intraoperative cholangiography during laparoscopic cholecistectomy become obsolete in the era of preoperative endoscopic retrograde and magnetic resonance cholangiopancreatography? Journal of the American College of Surgeons 2015; 220: 522-528.
- Eikermann M, Siegel R, Broeders I, Dziri C, Fingerhut A, Gutt C, Jaschinski T, Nassar A, Paganini AM, Pieper D, Targarona E, Schrewe M, Shamiyeh A, Strik M, Neugebauer EAM. Prevention and treatment of bile duct injuries during laparoscopic cholecystectomy: the clinical practice guidelines of the European Association for Endoscopic Surgery (EAES). Surgical Endoscopy 2012; 26: 3003-3039.
- Tornqvist B, Stromberg C, Akre O, Enochsson L, Nilsson M. Selective intraoperative cholangiography and risk of bile duct injury during cholecystectomy. BJS 2015; 102: 952-958.
- Gutt CN, Encke J, Koninger J, Harnoss JC, Weigand K, Kipfmuller K, Schunter O, Gotze T, Golling MT, Menges M, Klar E, Feilhauer K, Zoller WG, Ridwelski K, Ackmann S, Baron A, Schon MR, Seitz HK, Daniel D, Stremmel W, Buchler MW. Acute Cholecystitis Early Versus Delayed Cholecystectomy, A Multicenter Randomized Trial. Ann Surg 2013; 258: 385-393.
- Yamashita Y, Takada T, Strasberg SM, Pitt HA, Gouma DJ, Garden OJ, Büchler MW, Gomi H, Dervenis C, Windsor JA, Kim SW, de Santibanes E, Padbury R, Chen XP, Chan AC, Fan ST, Jagannath P, Mayumi T, Yoshida M, Miura F, Tsuyuguchi T, Itoi T, Supe AN; Tokyo Guideline Revision Committee. TG13 surgical management of acute cholecystitis. J Hepatobiliary Pancreat Sci 2013; 20: 89-96.
- Ludwig K, Bernhardt J, Steffen H, Lorenz D. Contribution of intraoperative cholangiography to incidence and outcome of common bile duct injuries during laparoscopic cholecystectomy. Surg Endosc 2002; 16: 1098-1104.
- Buddingh KT, Weersma RK, Savenije RA, van Dam GM, Nieuwenhuijs VB. Lower rate of major bile duct injury and increased intraoperative management of common bile duct stones after implementation of routine intraoperative cholangiography. J Am Coll Surg 2011; 213: 267-274.
- Ragulin-Coyne E, Witkowski ER, Chau Z, Ng SC, Santry HP, Callery MP, Shah SA, Tseng JF. Is routine intraoperative cholangiogram necessary in the twenty-first century? A national view. J Gastrointest Surg 2013; 17: 434-442.
- Sheffield K, Taylor S, Yimei H, Yong Fang K, Courtney M, James S. Association Between Cholecystectomy with vs. without Intraoperative Cholangiography and Risk of Common Duct Injury. JAMA 2013, 310: 812-820.
- Bregante M, Pirchi D, Castagneto G, Iribarren C. La colangiografía intraoperatoria selectiva en colecistitis aguda. Rev Argent Cirug 2006; 91: 100-104.
Correspondencia: Salgado Roberto
Intendente Becco 848 (CP: 1642). San Isidro, Provincia de Buenos Aires, Argentina. Tel.: + (54) 9 11 1562198233
Correo electrónico: salgadorober@yahoo.com.ar
Acta Gastroenterol Latinoam 2018;48(1): 13-22
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE