Julio Berreta,1 Mónica Marino,2 Daniel Kociak,1 Adrián Balducci,1 Julio Argonz,3 Gustavo Romero2
1 Servicio de Terapia Intensiva.
2 Sección de Hepatología.
3 Servicio de Endoscopía.
Acta Gastroenterol Latinoam 2016;46: 284-290
Recibido: 21/09/2016 / Aprobado: 23/11/2016 / Publicado en www.actagastro.org el 01/01/2017
Resumen
En los últimos 5 años se comunicó que hay riesgo de generar hiponatremia en los pacientes cirróticos con hemorragia por várices esofágicas (HVE) tratados con terlipresina. Objetivo. Encontrar los predictores para el desarrollo de hiponatremia en estos pacientes y los cambios evolutivos vinculables a la misma. Métodos. Se analizaron 60 pacientes cirróticos con HVE entre marzo de 2012 y enero de 2015 tratados con terlipresina y ligadura endoscópica. Se consideró hiponatremia al descenso en la natremia mayor que 5 mEq/L hasta 1 día después de finalizado el tratamiento. Los enfermos fueron agrupados en: 1) cohorte A: los que no desarrollaron hiponatremia, y 2) cohorte B: los que desarrollaron hiponatremia. Se enfrentaron 24 variables de ingreso clínicas y de laboratorio, y 4 variables evolutivas en ambas cohortes a fin de detectar predictores de hiponatremia y posibles consecuencias evolutivas. Resultados. La cohorte A fue integrada por 43 pacientes, en tanto 17 pertenecieron a la cohorte B. Entre las variables al ingreso, la natremia ≥ que 137,5 mEq/L y la pertenencia a la clase A de Child-Pugh se asociaron con evolución a hiponatremia (p = 0,0001 y 0,0485, respectivamente). Analizados por regresión logística solo la natremia basal ≥ 137,5 mEq/L fue predictora independiente de evolución a hiponatremia. Las variables evolutivas no fueron diferentes en ambas cohortes. Conclusiones. La natremia basal mayor o igual que 137,5 mEq/L es predictora independiente de desarrollo de hiponatremia durante el tratamiento con ligadura endoscópica y terlipresina. La hiponatremia observada no modificó la evolución.
Palabras claves. Hemorragia digestiva por várices esofágicas, hiponatremia, terlipresina.
Terlipressin and hyponatremia in cirrhotic patients with variceal bleeding. Predictors and clinical significance
Summary
In the past 5 years it was reported that treatment with terlipressin in cirrhotic patients with esophageal variceal bleeding (EVB) may cause hyponatremia. Objective. to find predictors of hyponatremia in cirrhotic patients with EVB treated with terlipressin and endoscopic ligation. Methods. since january 2013 to march 2015, 60 cirrhotic patients were admitted because of EVB and treated with terlipressin plus endoscopic ligation. Hiponatremia was defined as a decrease of serum sodium concentration greater than 5 mEq/L until 1 day after terlipressin treatment was concluded. Thus 2 cohorts were formed. Cohort A: patients who did not develop hyponatremia, and cohort B: patients who developed hyponatremia. 24 clinical and analytic variables present at admission, and 4 evolutive variables were statistically confronted each other in both cohorts in order to identify predictors of developing hyponatremia during treatment, and changes in evolution related to it. Results. cohort A was composed for 43 patients, while 17 made up the cohort B. Among the variables on admission, the natremia at admission ≥ 137.5 mEq/L, and Child-Pugh A were significantly associated with hyponatremia development (p = 0.0001 and 0.0485 respectively). In multivariate analysis only the natremia ≥ 137.5 mEq/L was independent predictor. The outcome was not different in the both cohorts. Conclusions. A serum sodium level of 137.5 mEq/L or greater at admission is independent predictor of hyponatremia development in cirrhotic patients with esophageal variceal bleeding treated with endoscopic ligation plus terlipressin. The level of hyponatremia reached in our study did not change the results.
Key words. Gastrointestinal bleeding esophageal varices, hyponatremia, terlipressin.
La glipresina (terlipresina) es un fármaco ampliamente utilizado para el tratamiento de la hemorragia por várices esofágicas (HVE) y es recomendada como una de las drogas de primera línea asociada a la ligadura endoscópica para el tratamiento de esta complicación de la cirrosis.1-4 La terlipresina es una prodroga de la vasopresina que una vez inyectada por vía endovenosa tiene un rápido efecto vasoconstrictor sistémico y esplácnico y luego se metaboliza por peptidasas a vasopresina, responsable de su acción prolongada.5-6 Este fármaco ejerce su acción vasoconstrictora por efecto agonista sobre los receptores V1 de vasopresina en el músculo liso vascular, produciendo una reducción del flujo de entrada a la vena porta que se traduce en una reducción de la presión portal5 y variceal, extendiéndose esta última hasta una hora.7 La terlipresina también estimula los receptores V2 que se hallan en las células tubulares renales, lo que da cuenta de su efecto antidiurético a través del aumento de la expresión de acuaporina 2.8-9
El incremento de la actividad de los receptores V2 mediado por la terlipresina se considera responsable de la producción de hiponatremia por reabsorción de agua libre de electrolitos hacia la circulación sanguínea. Diversos estudios han evaluado el descenso de la natremia en pacientes cirróticos con hemorragia variceal tratados con terlipresina describiendo reducciones en el rango de 5 mEq/l o mayores en el 22,8 al 70%, y reducciones en más 10 meq/L en 12,6 al 38% de los pacientes.10-12 Las manifestaciones neurológicas se han referido en estos trabajos a aquellos pacientes en los que la natremia descendió más que 10 mEq/L respecto a la del ingreso. La reciente reunión de consenso de Baveno VI4 ha recomendado monitorear la natremia en los pacientes con hemorragia variceal tratados con terlipresina. No existen hasta el momento series en América que hayan evaluado esta complicación.
El objetivo de este trabajo fue evaluar, en pacientes cirróticos con HVE tratados con ligadura endoscópica y terlipresina la prevalencia de hiponatremia, y las variables clínicas y de laboratorio al ingreso del paciente que se asocian con esta complicación, identificar los predictores independientes para su desarrollo y evaluar su impacto evolutivo.
Material y métodos
Desde una base de datos iniciada en 2001 en el Hospital de Gastroenterología Dr. Carlos Bonorino Udaondo, se analizó en forma retrospectiva a todos los pacientes con cirrosis hepática ingresados por HVE y que fueron tratados con terlipresina y ligadura endoscópica entre marzo de 2012 y enero de 2015.
Se consideró HVE a todo episodio de hemorragia digestiva alta manifestada por la presencia de hematemesis y/o melena cuando la endoscopía digestiva alta realizada dentro de las 24 hs mostró: 1) visualización del sangrado de una várice, considerado en este caso sangrado activo; 2) coágulo fresco sobre la superficie de la várice; 3) tapón de fibrina sobre la várice; y 4) sangre fresca en estómago en presencia de várices esofágicas sin otra lesión que pueda justificar el sangrado.1
Se refirió como fracaso de la terapéutica hemostática inicial a la presencia de uno o más de los siguientes hechos: 1) hemorragia variceal persistente constatada por el endoscopista luego de finalizada la terapia inicial con terlipresina y ligadura endoscópica, en presencia de signos clínicos de sangrado persistente, 2) imposibilidad de elevar la presión arterial sistólica 20 mm Hg o de mantenerla en un valor de 80 mm Hg o mayor a pesar de una correcta reanimación con fluidos y hemoderivados en ausencia de shock séptico o cardiogénico.
Para el caso en que se hubiere detenido la hemorragia en las primeras 6 horas, se consideró resangrado a la presencia de: 1) nueva hematemesis de sangre fresca, 2) inestabilidad hemodinámica y caída de la presión sistólica 20 mm Hg o más, que se repite en una medición efectuada una hora después y a pesar de una correcta reanimación con fluidos.13
La reanimación inicial con fluidos se efectuó con suero fisiológico y albúmina al 20%, y glóbulos rojos, procurando mantener una concentración de hemoglobina en sangre [Hb] alrededor de 8 g%.14
Los planes de hidratación una vez conseguido el control hemostático y la estabilidad hemodinámica se efectuaron con criterio de restricción moderada de volumen intentando balances neutros. Se tomó como normal al valor de natremia entre 135 y 145 mEq/L. Se consideró hiponatremia atribuible al tratamiento, a un descenso de la natremia superior a 5 mEq/L en relación al basal hasta un día después de finalizado el mismo.
De este modo se constituyeron 2 cohortes: 1) Cohorte A: formada por aquellos pacientes cuya natremia no descendió o cuyo descenso no superó los 5 mEq/L respecto al valor basal; y 2) Cohorte B: formada por los pacientes que desarrollaron hiponatremia con un descenso mayor que 5 mEq/L respecto al basal durante el tratamiento y hasta un día después.
Con el fin de identificar variables al ingreso que pudieran predisponer al desarrollo de hiponatremia durante el tratamiento se analizaron en ambas cohortes: edad, sexo, etiología alcohólica o no alcohólica, clase de Child-Pugh, score de MELD (Model for End-Stage Liver Disease), [Hb], recuento de plaquetas, kalemia, valores de bilirrubina total, alanino aminotransferasa (ALAT), aspartato aminotransferasa (ASAT), fosfatasa alcalina, albuminemia, RIN, KPTT, urea, creatinina, glucemia, [Na] sérica basal, frecuencia cardíaca, presión arterial media, presencia o no de ascitis, sangrado variceal activo al momento de la endoscopía, y éxito o fracaso hemostático inicial. El valor de natremia basal se dicotomizó al valor seleccionado por la curva ROC que mejor discriminó la evolución hacia hiponatremia, e ingresó al análisis como el valor basal mayor o igual así seleccionado. Además, se evaluó como posible variable asociada a desarrollo de hiponatremia a la duración del tratamiento con terlipresina.
Para evaluar posibles cambios evolutivos asociados a hiponatremia se enfrentaron las siguientes variables en ambas cohortes: mortalidad intrahospitalaria, resangrado, requerimiento de transfusiones y presencia de encefalopatía.
La terlipresina se suministró según el siguiente protocolo: bolo de 2 mg endovenoso previo a la endoscopía diagnóstica-terapéutica realizada antes de 4 horas a partir del ingreso del paciente al hospital, seguida por bolos de 2 mg siempre endovenosos cada 4 horas hasta el control del sangrado, y luego por bolos de 1 mg cada 4 horas por 3 a 5 días.
Los criterios de exclusión para el tratamiento con terlipresina en nuestro hospital son: edad menor de 17 años, portador de insuficiencia cardíaca, o de cardiopatía hipertensiva con valores de presión arterial sistólica al ingreso de 150 mm Hg o mayores, arteriopatía periférica, enfermedad cerebrovascular y embarazo.
Métodos estadísticos
Se utilizó el software estadístico G – Stat 2.0.1 (Departamento de Biometría GlaxosmithKline – Universidad de Barcelona).
Para evaluar el descenso de natremia en el total de los pacientes, y en cada una de las 2 cohortes en particular, se utilizó el test t de Student para muestras apareadas. Para encontrar el punto de corte de natremia al ingreso que mejor discriminó desarrollo hacia hiponatremia durante el tratamiento se utilizó la curva Reciever Operator Characteristics (ROC) tomando el desarrollo de hiponatremia como estado de naturaleza y valor de natremia basal como variable testeada. Para evaluar asociación entre variables cuantitativas en ambas cohortes se utilizaron los test t de Student para muestras independientes y de Mann Whitney (rangos medios de Wilcoxon). Para evaluar asociación entre variables cualitativas en ambas cohortes se utilizó el test de Chi2 y cuando éste presentó una limitación técnica para su uso se utilizó el test no paramétrico exacto de Fisher. Las variables cuantitativas y cualitativas de ingreso, que en el análisis univariado tuvieron asociación significativa con evolución a hiponatremia durante el tratamiento, se evaluaron mediante regresión logística con el fin de detectar predictores independientes de evolución a hiponatremia en esta situación. El valor de natremia basal ingresó dicotomizado como mayor o igual al punto de corte que mejor discriminó hiponatremia. Un valor de p < 0,05 se consideró estadísticamente significativo.
Resultados
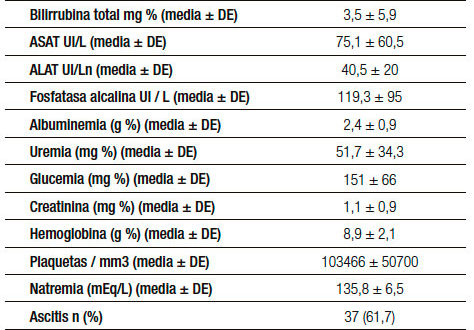
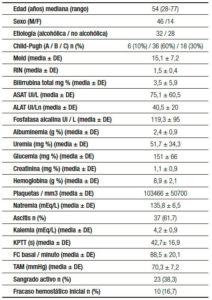
Entre marzo de 2012 y enero de 2015 sesenta pacientes con cirrosis hepática ingresados con diagnóstico de HVE fueron tratados con terlipresina y ligadura endoscópica de acuerdo al protocolo mencionado. La edad mediana de los enfermos fue de 54 años (rango: 28-77), 46 hombres (77%), 32 (53,3%) de etiología alcohólica, 6 (10%) pertenecían a la clase A de Child-Pugh, 33 (60%) a la clase B y 18 (30%) a la clase C. Las características clínicas y de laboratorio basales se listan en la Tabla 1.
La duración del tratamiento con terlipresina fue de 3,6 ± 1,3 días. De los 60 pacientes tratados con terlipresina y ligadura endoscópica, 43 tuvieron un descenso de la [Na] sérica que no superó los 5 mEq/L durante el tratamiento y hasta 1 día después, integrando la cohorte A (no hiponatremia). La [Na] sérica basal fue de 134 ± 6 mEq/L (rango: 117-145). Los 17 pacientes restantes, que experimentaron un descenso de la natremia mayor que 5 mEq/L en igual tiempo, integraron la cohorte B (hiponatremia), en ellos la [Na] sérica basal fue de 141 ± 5 mEq/L (rango: 129-149). En 15 de éstos la natremia basal fue normal y 2 tuvieron valores menores que 135 mEq/L.
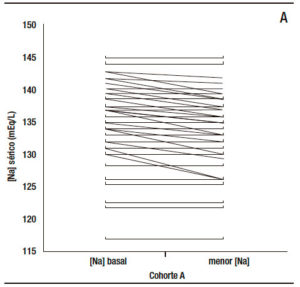
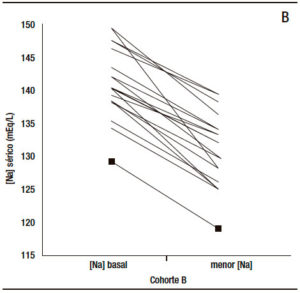
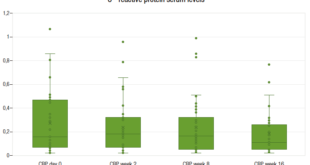
En el total de los paciente sometidos a ligadura endoscópica y terlipresina la natremia descendió 3,7 ± 4,8 mEq/L (p < 0,0001). En la Figura 1 A se grafica la evolución de la natremia en cada paciente de la cohorte A. En la Figura 1 B se hace lo propio con aquella correspondiente a los pacientes de la cohorte B.
Tabla 1. Se listan las variables presentes al ingreso (60) y sus valores. [Hb]: hemoglobina. FC: frecuencia cardíaca. TAM: presión arterial media. ALAT: aspartato aminotransferasa. ALAT: alanina aminotransferasa mEq: miliequivalente. DE: desvío estándar.
Un descenso de la [Na] sérica superior a 10 mEq/L respecto del basal se objetivó en 5 pacientes (29,4%) de los pacientes en la cohorte B. En este subgrupo la natremia basal fue 143,6 ± 5,1 mEq/L (rango: 138-149), y el valor más bajo de [Na] sérica durante la evolución fue 125 mEq/L. Ninguno de ellos tuvo manifestaciones neurológicas atribuibles a la hiponatremia.
La cohorte B tuvo más pacientes en clase A de Child- Pugh, 4 (23,5%) vs 2 (4,6%) p = 0,0485, y mayor natremia basal que la cohorte A (141 ± 5 mEq/L vs 134 ± 6 mEq/L, p = 0,003). En las demás variables de ingreso no hubo variación de significación entre ambas. Todos los valores de las variables de ingreso y sus diferencias en ambas cohortes se listan en la Tabla 2.
Figure 1. A: Modificación de la natremia en los pacientes de la cohorte A desde su ingreso hasta el menor valor durante el tratamiento con terlipresina y hasta 1 día después. B: Modificación de la natremia en los pacientes de la cohorte B en igual circunstancia.
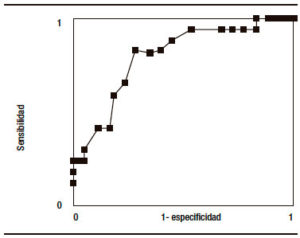
La curva ROC construida a partir de la [Na] sérica al ingreso como variable testeada y del desarrollo de hiponatremia por el tratamiento como estado de naturaleza, con un área bajo la curva (AUC) de 0,797, mostró que el valor de natremia basal ≥ 137,5 mEq/L fue el que mejor discriminó la evolución a hiponatremia con sensibilidad de 0,82 y especificidad de 0,72 para predecirla (Figura 2).
La [Na] sérica ≥ 137,5 mEq/L se asoció con desarrollo de hiponatremia durante el tratamiento (p = 0,0001) (Tabla 3).
Tabla 2. Se listan las diferencias cuantitativas y cualitativas en las variables de ingreso en ambas cohortes, y el nivel de significación de la diferencia. FC: frecuencia cardíaca. TAM: presión arterial media. Rec plaq: recuento de plaquetas. Creat: creatinina. Bil: bilirrubina. ALAT: aspartato aminotransferasa. ALAT: alanina aminotransferasa. FAL: fosfatasa alcalina. mEq: miliequivalente. min: minuto. [Na]: natremia. [K]: kalemia. DE: desvio estándar.
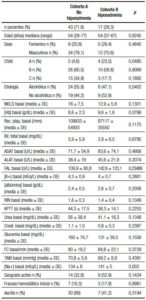
Tabla 3. Asociación entre natremia al ingreso ≥ 137,5 mEq/L y desarrollo de hiponatremia durante el tratamiento, Chi p = 0,0001.[Na]: natremia.
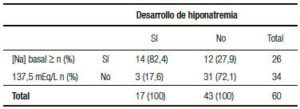
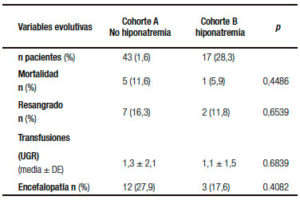
Tabla 4. Variables evolutivas en ambas cohortes. UGR: unidades de glóbulos rojos. DE: desvío estándar.
Figure 2. La curva ROC, construida a partir de los valores de natremia al ingreso de los pacientes y del desarrollo de hiponatremia durante el tratamiento con un AUC de 0,797, refirió al valor basal ≥ 137,5 mEq / L como el que mejor discriminó la evolución hacia la hiponatremia. Cada marca sobre la curva representa un valor de natremia medido en mEq/L.
Las variables de ingreso que correlacionaron con el desarrollo de hiponatremia durante el tratamiento fueron: la clase A de Child-Pugh y la [Na] sérica basal ≥ 137,5 mEq/L. Ambas fueron incluidas en el análisis de regresión logística, resultando la [Na] sérica basal ≥ 137,5 mEq/L la única que calificó como predictor independiente de evolución a hiponatremia con un OR (IC 95%) de 12,1 (2,9-49,6).
La duración del tratamiento con terlipresina fue de 3,4 ± 1,1 días en la cohorte A, y 4,1 ± 1,7 días en la cohorte B (p = 0,0605).
Durante la evolución no se observaron diferencias significativas en mortalidad hospitalaria, resangrado, requerimiento de transfusiones y presentación de encefalopatía en ambas cohortes (Tabla 4). No se presentaron manifestaciones neurológicas atribuibles a hiponatremia.
Discusión
El presente trabajo suma evidencia al hecho de que los pacientes cirróticos con HVE tratados con terlipresina presentan una reducción de la [Na] sérica. La hiponatremia por este tratamiento ocurrió en 28,3% de nuestros pacientes. Como en otras publicaciones, nuestro estudio evidencia una fuerte asociación entre los valores basales mayores de natremia al ingreso y el desarrollo de hiponatremia durante el tratamiento. La pertenencia a clase A de Child-Pugh también tuvo en el análisis univariado una significativa asociación con evolución a hiponatremia durante el tratamiento con terlipresina. La regresión logística mostró que la clase A de Child-Pugh pierde su valor predictivo cuando se incorpora al análisis multivariado el valor de natremia de 137,5 mEq/L o más al momento de ingreso del enfermo al hospital. Esta última es entonces predictor independiente de evolución a hiponatremia durante el tratamiento con esta droga.
La prevalencia comunicada de hiponatremia en esta situación es muy dispar y la proporción de pacientes que en nuestra serie la desarrolló (28,3%) es intermedia entre quienes no la mencionan15 o la refieren en 3 a 6% de los pacientes tratados16-17 y aquellos que la describen en el 41 a 70% de los casos.10-12
Se comunicó una asociación directa entre la evolución a hiponatremia y la eficacia de la terlipresina en el control del sangrado, y que esta complicación asociada al tratamiento de la HVE no es indicadora de pronóstico desfavorable12 como sí lo es en el paciente cirrótico en otras circunstancias.18-19
El primer trabajo que evaluó esta complicación en un número relevante de pacientes con HVE constató hiponatremia en el 67% de 58 enfermos tratados con terlipresina. Los pacientes incluidos en ese estudio presentaban características de mayor gravedad que los de nuestra serie, dado que ya habían fracasado o resangrado luego de recibir somatostatina más tratamiento endoscópico, y requirieron un número mayor de transfusiones de glóbulos rojos que los de nuestro grupo. Además, estos autores refieren a la solución de dextrosa 5% en agua como uno de los fluidos de reanimación.12 Todo esto podría tener relación con la elevada proporción con que se presentó esta complicación.
Nuestros pacientes no provenían de un fracaso hemostático previo y recibieron reanimación con suero fisiológico, albúmina, plasma cuando se lo consideró necesario, y con glóbulos rojos, intentando mantener la [Hb] en sangre en 7 a 8 g %.
Las manifestaciones neurológicas asociadas a la hiponatremia fueron referidas en la literatura en aquellos pacientes en los que la natremia descendió más de 10 mEq/L respecto a la de ingreso. Esto ocurrió en 3 de 21,12 1 de 40,10 y en 5 de 16 pacientes.11
En nuestra serie 5 pacientes tuvieron un descenso de la natremia superior a 10 mEq/L respecto al ingreso; en ellos la natremia basal fue 143,6 ± 5,1 mEq/L y el valor más bajo alcanzado fue de 125 mEq/L. Ninguno de ellos tuvo manifestaciones neurológicas atribuibles a hiponatremia.
En los tres trabajos que comunicaron hiponatremia asociada al tratamiento con terlipresina entre 41 y 70% de la población expuesta, ésta se asoció en el análisis univariado con los siguientes parámetros de ingreso: mayor [Na] sérica, menor score de MELD, menos antecedentes de encefalopatía hepática, de diabetes melitus y de uso de diuréticos, menor bilirrubina sérica, menor score de Child-Pugh, menor valor de RIN, menor índice de masa corporal, menor valor de creatinina. La mayor duración del tratamiento con terlipresina también se asoció a hiponatremia. El análisis multivariado entre los tres trabajos seleccionó como predictores independientes de evolución hacia hiponatremia a la presencia al ingreso de: mayor valor de natremia, menor score de MELD, menor edad, menor score de Child-Pugh, y durante el tratamiento a su mayor duración. Es de destacar que el predictor independiente común en todos éstos fue el mayor valor de la natremia al ingreso.10-12 En nuestro trabajo, la natremia al ingreso ≥ 137,5 mEq/L fue el único predictor independiente de evolución a hiponatremia OR: 12,1 (IC 95%: 2,9-49,6).
Se ha sugerido que el descenso de la natremia generado por la terlipresina sería mayor a menor grado de ocupación de los receptores V2 en los túbulos renales, permitiendo que la droga administrada estimule la retención de agua libre de solutos.12 El nivel de vasopresina circulante es mayor en los cirróticos descompensados que en los compensados y20-21 la elevada secreción de vasopresina no mediada por la osmolaridad plasmática es uno de los mecanismos responsables de la retención de agua en cirróticos.18, 22 Esto daría argumento al hecho de que la natremia desciende más en pacientes con natremia previa normal y está acorde con la baja prevalencia de hiponatremia reportada durante el tratamiento del síndrome hepatorenal con terlipresina y albúmina.22
Conclusión: El único predictor independiente de hiponatremia en cirróticos con HVE tratados con ligadura endoscópica y terlipresina fue el mayor valor de la natremia al ingreso, dicotomizado como una natremia basal de 137,5 mEq/L o mayor. El grado de hiponatremia observado no modificó los resultados de la terapéutica, no hallándose diferencias entre ambas cohortes en mortalidad intrahospitalaria, resangrado, número de transfusiones requeridas, ni encefalopatía. No observamos manifestaciones neurológicas que pudieran atribuirse a la hiponatremia.
Referencias
- de Franchis R. Updating consensus in portal hypertension: report of the Baveno III Consensus Workshop on definitions, methodology and therapeutic strategies in portal hypertension. J Hepatol 2000; 33: 846-852.
- Abraldes JG, Bosch J. The treatment of acute variceal bleeding. J Clin Gastroenterology 2007; 41: S312-S317.
- Garcia-Tsao G, Sanyal AJ, Grace ND, Carey W; Practice Guidelines Committee of the American Association for the Study of Liver Diseases; Practice Parameters Committee of the American College of Gastroenterology. Prevention and management of gastroesophageal varices and variceal hemorrhage in cirrhosis. Hepatology 2007; 46: 922-938.
- de Franchis R. Expanding consensus in portal hypertension: Report of the Baveno VI Consensus Workshop: Stratifying risk and individualizing care for portal hypertension. J Hepatol 2015; 63: 743-752.
- Escorsell A, Bandi JC, Moitinho E, Feu F Garcia-Pagan JC, Bosch J, Rodes J. Time profile of the haemodynamic effects of terlipressin in portal hypertension. J Hepatol 1997; 26: 621-627.
- Merkel C, Gatta A, Bolognesi M, Finucci G, Battaglia G, Angeli P, Zuin R. Hemodynamic changes of systemic, hepatic, and splenic circulation following triglycyl-lysine-vasopressin administration in alcoholic cirrhosis. Dig Dis Sci 1988; 33: 1103-1109.
- Romero G, Kravetz D, Argonz J, Bildozola M, Suárez A, Terg R. Terlipressin is more effective in decreasing variceal pressure than portal pressure in cirrhotic patients. J Hepatol 2000; 32: 419-425.
- Machova´ Antidiuretic activity of terlipressin (triglycyl-lysine vasopressin) – role of pressure natriuresis. Physiol Res 1992; 41: 121-127.
- Krag A, Bendtsen F, Pedersen EB, Holstein-Rathlou NH, Møller S. Effects of terlipressin on the aquaretic system: evidence of antidiuretic effects. Am J Physiol Renal Physiol 2008; 295: F1295-F1300.
- Yim SY, Seo YS, Jung CH, Kim TH, Kim ES, Keum B, Kim JH, An H, Yim HJ, Yeon JE, Jeen YT, Lee HS, Chun HJ, Byun KS, Um SH, Kim CD, Ryu HS. Risk Factors for Developing Hyponatremia During Terlipressin Treatmen: A Retrospective Analyses in Variceal Bleeding. J Clin Gastroenterol 2015; 49: 607-612.
- Kang YJ, Bae EJ, Hwang K, Jeon DH, Jang HN, Cho HS, Chang SH, Park DJ. Initial serum sodium concentration determines the decrease in sodium level after terlipressinadministration in patients with liver cirrhosis. Springerplus 2013; 2: 519.
- Solà E, Lens S, Guevara M, Martín-Llahí M, Fagundes C, Pereira G, Pavesi M, Fernández J, González-Abraldes J, Escorsell A, Mas A, Bosch J, Arroyo V, Ginès P. Hiponatremia in patients treated with terlipressin for severe gastrointestinal bleeding due to portal hypertension. Hepatology 2010; 52: 1783-1790.
- Berreta J, Kociak D, Romero G, Balducci A, Amaya R, Argonz J. Endoscopic versus endoscopic plus octreotide treatment for acute variceal bleeding. Benefit according to severity at admission. Acta Gastroenterol Latinoam 2013; 43: 89-97.
- de Franchis R. Evolving consensus in portal hypertension. Report of the Baveno IV consensus workshop on methodology of diagnosis and therapy in portal hypertension. J Hepatol 2005; 43: 167-176.
- Abid S, Jafri W, Hamid S, Salih M, Azam Z, Mumtaz K, Shah HA, Abbas Z. Terlipressin vs. octreotide in bleeding esophageal varices as an adjuvant therapy with endoscopic band ligation: a randomized double-blind placebo-controlled trial. Am J Gastroenterol 2009; 104: 617-623.
- Escorsell A, Ruiz del Arbol L, Planas R, Albillos A, Bañares R, Calès P, Pateron D, Bernard B, Vinel JP, Bosch J. Multicenter randomized controlled trial of terlipressin versus sclerotherapy in the treatment of acute variceal bleeding: the TEST study. Hepatology 2000; 32: 471-476.
- Feu F, Ruiz del Arbol L, Bañares R, Planas R, Bosch J. Double-blind randomized controlled trial comparing terlipressin and somatostatin for acute variceal hemorrhage. Variceal Bleeding Study Group. Gastroenterology 1996; 111: 1291-1299.
- Lehrich RW, Ortiz-Melo DI, Patel MB, Greenberg A. Role of vaptans in the management of hyponatremia. Am J Kidney Dis 2013; 62: 364-376.
- Biggins SW, Rodriguez HJ, Bacchetti P, Bass NM, Roberts JP, Terrault NA. Serum sodium predicts mortality in patients listed for liver transplantation. Hepatology 2005; 41: 32-39.
- San-e Ishikawa, Schrier R. Pathogenesis of hyponatremia: the role of arginine vasopressin. En: Gines P, Arroyo V, Rodes J, Schrier R. Ascites and renal dysfunction in liver disease. Pathogenesis, diagnosis, and treatment. 2a edition. ed: Blackwell Publishing 2005: 305-314.
- Bichet D, Szatalowicz V, Chaimovitz C, Schrier RW. Role of vasopressin in abnormal water excretion in cirrhotic patients. Ann Intern Med 1982; 96: 413-417.
- Nazar A, Pereira GH, Guevara M, Martin-Llahi M, Pepin MN, Marinelli M, Solá E, Baccaro ME, Terra C, Arroyo V, Ginès P. Predictors of response to therapy with terlipressin and albumin in patients with cirrhosis and type 1 hepatorenal syndrome. Hepatology 2010; 51: 219-226.
Correspondencia: Julio Berreta
Caseros 2061. Ciudad Autónoma de Buenos Aires, Argentina
Tel./Fax. 4821-7569.
Correo electrónico: julioberreta@googlemail.com
Acta Gastroenterol Latinoam 2016;46(4): 284-290
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE