Carlos Miguel Lumi,1, 2 Juan Pablo Muñoz,1, 2 Omar Rubén Miravalle,1 Dolores Caffarena,1 Pablo Antonio Farina,1 Ubaldo Gualdrini,1, 2 Luciana La Rosa,1 Guillermo Masciangioli2
1 Centro Privado de Cirugía y Coloproctología.
2 Hospital de Gastroenterología “Dr Carlos Bonorino Udaondo”.
Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2016;46: 77-89
Recibido: 18/08/2015 / Aprobado: 11/02/2016 / Publicado en www.actagastro.org el 04/07/2016
Resumen
La neuromodulación sacra (NMS) consiste en la estimulación eléctrica de la vía aferente de las raíces nerviosas sacras para modular y restablecer el equilibrio entre los reflejos inhibitorios y facilitadores que controlan la actividad funcional del suelo pélvico. Mediante la estimulación de las vías nerviosas se logra restablecer la fisiología alterada ante determinados cuadros de patología funcional anorrectal, incontinencia fecal, constipación o proctalgia crónica. Objetivo. Presentar los resultados obtenidos con la utilización de la NMS para el tratamiento de pacientes con incontinencia fecal, constipación severa e intratable y con proctalgia crónica. Material y métodos. En un período de 11 años se realizaron 33 pruebas de estimulación eléctrica sacra transitoria, 25 en pacientes que presentaban incontinencia fecal, 5 con constipación y 3 con dolor anorrectal crónico. Todos los pacientes con incontinencia fecal se realizaron en el preoperatorio, ecografía esfinteriana de 360º y manometría anorrectal; en los casos de constipación severa e intratable como alternativa previa a la colectomía total. En pacientes con dolor pelviano crónico se utilizó la NMS sacra según el protocolo de tratamiento de dolor anorrectal sin respuesta a los tratamientos previos. En todos los casos se llevó a cabo la prueba de estimulación eléctrica transitoria y ante la presencia de resultados satisfactorios se colocó el implante definitivo. Resultados. Los resultados fueron evaluados luego de un seguimiento promedio de 69 meses (rango 6-130). Se colocó el implante definitivo para el tratamiento de la incontinencia fecal en 23 pacientes por test de prueba positivo, presentando una disminución en los scores de incontinencia fecal en el 98% de los pacientes con una tasa de éxito promedio del 66% (rango 45-92%). Para el tratamiento de la constipación se colocaron 3 implantes definitivos con un seguimiento promedio de 77 meses (rango 51-96) y una tasa de éxito entre 50%-80% medida por la frecuencia de las deposiciones. En casos de dolor anorrectal crónico, severo e intratable se utilizó el método en 3 pacientes. Las tasas de respuestas medidas por escala analógica visual fueron entre 40% y 70%. Conclusiones. La utilización de la estimulación eléctrica de las raíces sacras para obtener un mejor funcionamiento de los órganos pelvianos es un área en constante crecimiento, obteniendo cada vez mayor cantidad de indicaciones. La garantía de tener resultados favorables depende de la correcta indicación y es por eso que los pacientes deben ser evaluados minuciosamente, y dependiendo de la patología, tratados con los métodos habituales hasta llegar a la NMS.
Palabras claves. Neuromodulación sacra, resultados, largo plazo.
Sacral neuromodulation. Long-term results
Summary
Sacral neuromodulation involves electrical stimulation of afferent nerve roots to restore the balance between inhibitory and excitatory reflexes who improve the functional activity of the pelvic floor. With benefits in patients with fecal incontinence, constipation and chronic anorectal pain. Objective. The aim of this study is present the results obtained with sacral neuromodulation for the treatment of patients with fecal incontinence, severe and intractable chronic constipation and chronic anorectal pain. Patients and methods. 33 patients had indication for transitory electrical sacral stimulation, 25 patients performed transitory electrical stimulation for fecal incontinence, 5 with refractary constipation and 3 with chronic anorectal pain. In cases of fecal incontinence, the patients performed previous anorectal manometry and ultrasonography examination of anal sphincters. When the constipation is the indication, we performed stimulation in patients with severe and refractary constipation like step before total colectomy. In cases of chronic anorectal pain, the electrical transitory test was performed according to our treatment algorithm for management of functional anorectal pain. In all cases, if the patients had satisfactory results after 2 weeks period the definitive implant was placed. Results. Mean follow-up was 69 months (range 6-130). Definitve implant was placed for treatment of fecal incontinence in 23 patients with a decrease in fecal incontinence scores in 98%, with an average success rate of 66% (range: 45-92). In cases of constipation, 3 definitive implants were placed, the mean follow-up was 77 months (range: 51-96) with a success rate between 50%-80% as measured by bowel frequency. We performed definitive electrical stimulation in 3 patients wit chronic and intractable anorectal pain. Response rates as measured by visual analog scale were between 40%-70%. Conclusions. Sacral neuromodulation is an area in constant growth, with more indications. The success depends on the correct indication and the patients need to be treated with other therapeutic options before sacral neuromodulation.
Key words. Neuromodulation, long-term, results.
La neuromodulación engloba cualquier tecnología que afecte la interfaz nerviosa para producir un beneficio y es una de las áreas de mayor crecimiento en la medicina. En los últimos veinte años, la neuromodulación ha ganado gran apoyo como tratamiento de la incontinencia fecal por medio de la estimulación crónica de baja tensión de los órganos pélvicos para reclutar la función residual en los mismos. La neuromodulación sacra (NMS) es la estimulación eléctrica de la vía aferente de las raíces nerviosas sacras para modular y restablecer el equilibrio entre los reflejos inhibitorios y facilitadores que controlan la actividad funcional del suelo pelviano. Mediante la estimulación de las vías nerviosas se logra modificar la actividad esfintérica anal y la sensibilidad nociceptivarrectoanal patológica mediante interacciones sinápticas a través de estímulos eléctricos.1-4 La primera experiencia en neuromodulación mediante estimulación eléctrica de las raíces nerviosas pelvianas fue realizada por Caldwell en 1963.5 Matzel en el año 1995 comenzó a aplicar la NMS para tratar pacientes que tenían déficit funcional pero no anatómico del complejo muscular esfinteriano.6, 7
La incontinencia anal es una patología frecuente con una prevalencia aproximada que llega hasta el 10%.8, 9 Puede tener múltiples orígenes; es generalmente desencadenada por varios trastornos fisiopatológicos que incluyen trastornos de la sensorialidad anorrectal, la motilidad colorrectal, así como cambios estructurales en el piso pelviano y en el complejo esfínteriano.10, 11 Rao y Patel demuestran en un estudio prospectivo que el 80% de los pacientes con incontinencia tienen más de una anormalidad.12 El tratamiento en primera instancia se basa en medidas conservadoras como son la dieta, los formadores de materia fecal, la loperamida en algunos casos, hasta llegar al biofeedback.13-17 Las reparaciones quirúrgicas incluyen la reparación del esfínter anal (esfinteroplastias), la colocación de un esfínter anal artificial, las interposiciones musculares o las ostomías, las cuales tienen sus respectivas complicaciones y pérdida de la efectividad a largo plazo.18 A pesar de esto, las plásticas esfinterianas continúan siendo la primera elección cuando existe lesión muscular. Ante la falta de respuesta a cualquiera de estos tratamientos tiene indicación la NMS.
Los pacientes con constipación, definida por los criterios de Roma III,19 son generalmente respondedores a las terapéuticas convencionales. Si esto no sucediera, son sometidos a estudios específicos y se establecen nuevas pautas terapéuticas. Ante la falta de respuesta a esta segunda instancia se considera estar ante la presencia de una constipación severa intratable. La conducta terapéutica consiste en la colectomía total con ileorrectoanastomosis. Surge en los últimos años la NMS como tratamiento previo a la cirugía, ya que ésta produce ondas propulsivas de gran amplitud en todo el marco colónico en pacientes con constipación por tránsito lento revirtiendo la misma.20, 21
Los cuadros de dolor anorrectal funcional incluyen un grupo de patologías de prevalencia creciente, generalmente subdiagnosticados o mal diagnosticados, de difícil tratamiento y sin uniformidad en el mismo. Para la definición de estos síndromes se utilizan los criterios de Roma III19 que reconocen dos formas de dolor funcional anorrectal: el síndrome del elevador y la proctalgia fugax. Este sistema de clasificación no incluye a la coxigodinia, que se refiere a pacientes con dolor en la parte final del cóccix, ni a la neuralgia del nervio pudendo, la cual se debe a un atrapamiento del nervio en el canal pudendo.22 La proctalgia crónica puede ser el resultado de cirugías de la columna, generalmente por hernia de disco, traumatismos o ependimomas. Puede llegar a ser invalidante y refractaria a tratamientos analgésicos convencionales como así también a bloqueos radiculares. La NMS se transformó en una herramienta útil para el tratamiento de estos pacientes.23-25
Numerosas publicaciones sobre resultados obtenidos en el tratamiento de la incontinencia, la constipación y el dolor mediante NMS hacen de esta técnica una herramienta de gran valor. A partir de las distintas experiencias sus indicaciones se han ampliado implantando hoy a pacientes con injuria medular, anastomosis coloanales o colorrectales bajas, e incluso a pacientes con lesión esfinteriana sin reparar de hasta 120º por ecografía.
Es muy importante que la indicación sea precisa ya que de ella dependerá en gran parte el éxito de la terapéutica. Es por eso que los pacientes deben ser evaluados minuciosamente y, dependiendo de la patología, ser tratados con los métodos habituales, hasta llegar a la NMS.
Objetivo
Presentar los resultados obtenidos con la utilización de la NMS para el tratamiento de la incontinencia anal, la proctalgia crónica y la constipación severa e intratable.
Diseño
Estudio prospectivo y observacional.
Material y métodos
Criterios de inclusión
a) Incontinencia fecal (IF) de más de tres días demostrada en el diario de hábito intestinal basal de 21 días.
b) Falta de respuesta al tratamiento médico con fibra seca y/o loperamida.
c) Falta de respuesta al biofeedback luego de completar 6 sesiones semanales de 45 minutos de duración a cargo de un médico gastroenterólogo o coloproctólogo especializado en piso pelviano.
d) Esfínteres anales (interno y externo) indemnes o con lesión parcial reparada.
e) Respuesta muscular y sensorial adecuada demostrada por la prueba de evaluación transitoria.
f) Mejoría mayor o igual al 50% en el número total de episodios de incontinencia o en el número de días afectado por dichos episodios luego del test de prueba.
Criterios de exclusión
a) Malformaciones congénitas.
b) Cirugía rectal menor a 12 o 24 meses por cáncer.
c) Prolapso rectal.
d) Enfermedad inflamatoria intestinal.
e) Diarrea crónica inmanejable.
f) Embarazo.
g) Enfermedades neurológicas.
h) Alteraciones anatómicas que impidan la colocación del electrodo.
i) Enfermedades dermatológicas que provoquen riesgo de infección.
Todos los pacientes realizaron en el pre-operatorio una ecografía esfinteriana de 360º y una manometría anorrectal.
Incontinencia fecal. La severidad de la incontinencia fue evaluada en todos los pacientes mediante el score de Jorge & Wexner (Cleveland Clinic Incontinence Score),26 el formulario de calidad de vida en incontinencia fecal (FIQL),27 consignando el estilo de vida, el comportamiento, la vergüenza y la depresión. Diario de hábito evacuatorio de 21 días: registro de la cantidad de episodios de incontinencia, urgencia evacuatoria, número total de deposiciones, utilización de apósitos y características de la materia fecal.
Constipación. Se utilizó la NMS para el tratamiento de la constipación en aquellos pacientes que presentaban constipación severa que no mejoraron luego de al menos 6 meses de tratamiento médico (dieta, hidratación, fibra y laxantes) ni con biofeedback como opción previa a la colectomía.
Dolor pelviano crónico. Pacientes que completaron el protocolo de tratamiento del dolor según detalla la siguiente cita sin respuesta al mismo.22 El dolor y la respuesta al tratamiento fueron medidos por una escala analógica visual (EAV).
Descripción de la técnica. La NMS se realiza en dos etapas: a) Prueba de estimulación nerviosa percutánea (PENP) y b) Implante definitivo (ID).
a) Prueba de Estimulación Nerviosa Percutánea
El procedimiento se realiza en quirófano, con el paciente en decúbito prono, se elevan el sacro y las extremidades inferiores mediante la colocación de almohadillas a nivel de la pelvis y la región anterior de la pierna para exponer el ano y los pies, que no se deben cubrir con los campos quirúrgicos. Se utilizan reparos óseos para localizar los forámenes sacros II, III y IV de ambos lados. Posteriormente y bajo anestesia local se introduce una aguja (MedtronicInterstim®, Minnesota, EE.UU., 041828, 3.5 inch) con una inclinación entre 60 y 80 grados con respecto a la piel para que ingrese en dirección perpendicular al sacro en uno de los forámenes, comenzando habitualmente en S3. La colocación y la ubicación correcta de la aguja se realizan bajo visión radioscópica con incidencia lateral. Luego se estimula la raíz sacra con un generador externo con estímulos crecientes a partir de 1 Volt (máximo 10 Volts) hasta obtener la respuesta sensorial y/o motora adecuada que variará de acuerdo al foramen. La estimulación de la raíz S2 genera como respuesta motora la contracción esfintérica, la rotación de la pierna y la flexión plantar del pie y como respuesta sensitiva la sensación de contracción en base del pene o la vagina. La estimulación de S3 determina la flexión plantar del primer dedo del pie y la elevación del periné y el ano, y la sensación de presión rectal o parestesias en ano, pene, escroto o vagina. La estimulación de S4 genera contracción en fuelle del periné sin respuesta en las extremidades y la sensación de opresión rectal. Una vez elegido el sitio con mejor respuesta, se reemplaza la aguja por un electrodo cuatripolar (MedtronicInterstim® 3889 Quadripolar Lead Kit, Minneapolis, Minnesota, EE.UU.) bajo control radioscópico. Antes de ser implantado se impregna el material con una solución de gentamicina (80 mg en 500 cc de solución salina). El catéter se conecta a un neuroestimulador externo temporario (Medtronic 3625) con el que pueden modificarse la frecuencia, el ancho de pulso, la amplitud y la polaridad.
b) Implante definitivo
Luego de tres semanas de estimulación se evalúa la respuesta terapéutica y frente a una disminución del número de episodios de incontinencia mayor o igual al 50%, constatado a través del diario de hábito evacuatorio, se lleva a cabo el implante definitivo. En los casos de constipación frente una mejoría mayor al 50% medida por deposiciones/semana y en los casos de dolor ante una mejoría mayor al 50% según la escala analógica visual, se realiza el implante definitivo. El procedimiento puede realizarse bajo anestesia general o local y consiste en el reemplazo del cable proveniente del electrodo, el labrado de un túnel subcutáneo entre el glúteo y el abdomen y la creación de un bolsillo subcutáneo abdominal donde se alojará el marcapasos definitivo (Medtronic 3023).
Parámetros de estimulación. Los valores que utilizamos habitualmente son aquellos con los que hemos obtenido mejores respuestas, 210 μs para el ancho de pulso, frecuencia de 25 Hz y el voltaje se regula de acuerdo al umbral sensorial del paciente con un máximo de 10 Volts, manteniendo una estimulación continua. Durante el postoperatorio es posible modificarlos por telemetría de acuerdo a la respuesta clínica del paciente. En tres pacientes el electrodo se ubicó en el foramen S3 y en una en S4.
Tanto el implante transitorio como el definitivo fueron realizados por el mismo equipo de especialistas en trastornos del piso pelviano.
Análisis estadístico
Todos los datos fueron analizados mediante el software estadístico IBM SPSS versión 15.0.1. Para las variables continuas de distribución normal se utilizó la media con su desvío estándar y para las variables de distribución no paramétrica la mediana con percentilos. Los resultados obtenidos con la terapéutica fueron evaluados para datos continuos y con distribución normal con T Test y para las variables categóricas el análisis se realizó con Chi2. Los eventos adversos relacionados con el dispositivo fueron resumidos en número total de eventos y el porcentual. Se interpretó un valor de p < de 0,05 como estadísticamente significativo.
Resultados
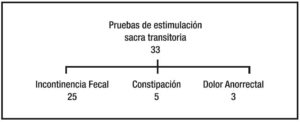
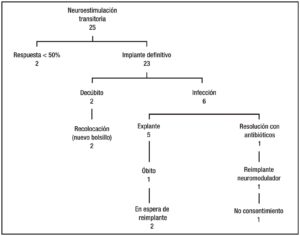
En el período comprendido entre julio de 2004 a marzo de 2015 se realizaron 33 pruebas de estimulación sacra transitoria. Como se muestra en la Figura 1, 25 en pacientes con diagnóstico de incontinencia fecal, 5 por constipación y 3 por dolor anorrectal crónico.
Figura 1. Distribución de los pacientes neuromodulados según indicación.
Incontinencia fecal
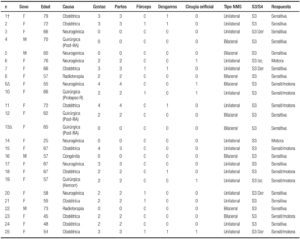
Se realizaron 25 pruebas de estimulación sacra transitoria (Tabla 1), en 2 pacientes no se logró una mejoría del 50% a las 3 semanas por lo que no se les colocó el implante definitivo. De los restantes 23 pacientes, el 84% fueron de sexo femenino (n= 19), con una edad promedio de 61 años (rango: 25-79). Las etiologías de la incontinencia fecal fueron: el trauma obstétrico (n= 10), neurogénica (n= 6), postquirúrgica (n= 4), actínica (n= 2) y la congénita en un solo caso. Las pacientes con causa obstétrica presentaron un promedio de 2,8 gestas (rango: 2-4), el 70% por desgarro obstétrico no reparado. Los 5 pacientes operados fueron en 3 casos por resección anterior del recto, un paciente por reparación de un prolapso rectal y una por hemorroidectomía.
Todos los pacientes fueron estimulados accediendo al plexo sacro a través del 3er foramen sacro presentando principalmente respuesta sensitiva en el 60%, sensitivo/ motora el 32% y sólo motora el 8% (Tabla 1). El tiempo de seguimiento fue de 69 meses (rango: 6-130). El primer implante definitivo fue realizado en julio de 2004.28 Los controles fueron semanales en el primer mes postoperatorio, mensuales hasta los 6 meses y luego trimestrales hasta cumplir el año; posteriormente anuales en conjunto con personal técnico para la evaluación del estado del generador y eventuales modificaciones de los parámetros de voltaje del dispositivo.
Tabla 1. Características clínicas de los pacientes que se sometieron a neuromodulación con indicación de incontinencia fecal. POST-RA: Postoperatorio de resección anterior de recto. Hemorr: Postoperatorio de hemorroidectomía. Prolapso R: Postoperatorio de rectopexia. Δ: pacientes que no se colocaron el implante definitivo por falta de mejoría.
Respecto a los resultados obtenidos, luego del seguimiento a largo plazo se observó una disminución en los scores de incontinencia en casi todos los pacientes, con una tasa promedio de éxito del 66% (rango: 45-92%).
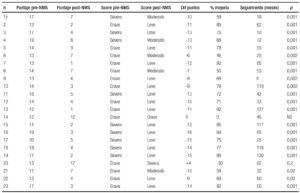
Un paciente no presentó cambios y empeoramiento de sus síntomas. En la Tabla 2 se muestran los resultados obtenidos según el score de incontinencia (CCIS).
Las complicaciones incluyeron dolor en el sitio de implante del generador, parestesias, dolor perineal o en miembros inferiores, decúbito del generador o infección de alguno de los componentes, con una morbilidad del 34% y sin mortalidad (Figura 3).
Las complicaciones más severas fueron el decúbito del generador y la infección. En los dos casos de decúbito se realizó un nuevo bolsillo sin inconvenientes ni interrupción de la estimulación eléctrica. Respecto a las infecciones, un paciente tuvo evolución favorable con la administración de antibióticos, el resto (5 casos) se les explantó el generador y los cables. Fue reimplantado un paciente, 2 se encuentran en espera de un nuevo implante. Un paciente falleció por causas no vinculadas al tratamiento y otro paciente rechazó el tratamiento (Figura 3).
Constipación
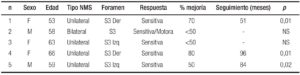
Cinco pacientes presentaron constipación crónica, severa e intratable con todos los tratamientos previos por lo que se indicó NMS como alternativa previa a la colectomía. En 2 casos no se observó mejoría > 50% por lo que no se realizó el implante definitivo (Tabla 3).
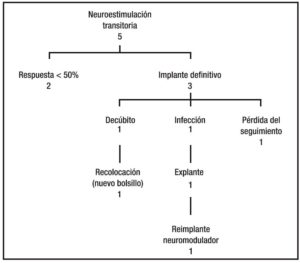
Tres pacientes presentaron mejoría > 50% tomando como parámetro el número de deposiciones semanales, por lo que se realizó el implante definitivo, presentando en un seguimiento promedio de 77 meses (rango: 51-96) una mejoría entre el 50% y 80% (promedio 64%) en la frecuencia de sus deposiciones. Un paciente presentó a los 12 meses decúbito del generador por lo que se confeccionó un nuevo bolsillo, otro se tuvo que explanar por infección realizándose posteriormente un 2do implante con buenos resultados funcionales. Un paciente se perdió del seguimiento a los 84 meses (Tabla 3) (Figura 4).
Tabla 2. Resultados de la NMS según puntaje en el score de incontinencia de Jorge & Wexner (CCIS).
Dolor anorrectal crónico
El dolor anorrectal severo, crónico y sin respuesta a otras terapéuticas fue indicación de NMS en 3 pacientes. El primer paciente fue por dolor neuropático se realizó implante bilateral con buena respuesta inicial y posteriormente una mejoría cercana al 40% según EAV. El segundo caso fue por fractura y lesión medular presentando para paresia, vejiga neurogénica, constipación y dolor intratable; con seguimiento de 19 meses presentó mejoría del dolor a corto plazo del 40%. El 3er paciente presentó una mejoría del 70% pero no cumplió 6 meses de seguimiento.
Discusión
Nuestra población tratada por incontinencia fecal fue con claro predominio del sexo femenino (relación 9/1) con una edad promedio de 60 años y como primera causa de la IF el trauma obstétrico, representativa de los pacientes que presentan mayor prevalencia de esta patología. Si bien la segunda causa de IF es postquirúrgica, en nuestra serie fue la 3ra causa seguida por la neurogénica. Correspondería a una distribución de frecuencias la explicación de este fenómeno, no existiendo tampoco en la bibliografía consultada una razón determinada.10 Los resultados obtenidos en los pacientes tratados por IF son equiparables a los citados por la mayoría de los estudios con seguimiento a largo plazo tanto por el porcentaje de éxito obtenido como por el prolongado tiempo de seguimiento (hasta 130 meses).29-32 Las tasas de éxito de la NMS en el tratamiento de la IF según el seguimiento son del 63% (33-66),33-37 58%(52-81)38-46 y 54% (50-58)47, 48 en el corto, mediano y largo plazo, respectivamente. Nuestra población presentó un promedio de 66% de mejoría con un seguimiento a largo plazo promedio superior a los 5 años. No existe un consenso al respecto y se considera seguimiento a corto plazo hasta 12 meses, mediano plazo 12-36 meses y largo plazo el mayor a los 36 meses.
La importancia que adquiere el seguimiento se ve reflejada en que la disminución de la efectividad de la neuromodulación entre el corto y el largo plazo es cercana al 10% tanto en nuestra serie como en las consultadas, manteniendo aun así su efectividad. La disminución de la misma puede ser debida a cambios de posición del electrodo, fibrosis alrededor del mismo que genera un aumento de la resistencia al pasaje del estímulo y a interrupciones producidas por secreciones dentro del conector. A su vez, estas situaciones requerirán un aumento del voltaje del generador con el consiguiente agotamiento más rápido de la batería.
Es muy importante el control postneuromodulación para la regulación de los parámetros de voltaje, frecuencia y ancho de pulso y también para controlar que el generador esté descargando en forma continua. Con respecto a esta situación merece destacarse que Kenefick presentó un trabajo en el cual comparó la efectividad de la neuromodulación apagando y prendiendo en forma secuencial el generador “modo on-off”.55 Los resultados obtenidos demostraron que no era necesaria una descarga continua, de todas formas, preferimos neuromodular los pacientes de forma continua.
Altomare y col reporta 52 pacientes con seguimiento mínimo de 5 años, obteniendo un 74% de los pacientes una mejoría mayor al 50% en disminución de los episodios de incontinencia.49 A pesar de no haber criterios comunes para la definición del éxito en distintos trabajos, nuestros resultados son comparables y superan a varios publicados ya que el 82% de los pacientes neuromodulados y seguidos presentaron una mejoría > 50%.
Dentro de los estudios pre- y postneuromodulación se encuentra la manometría anorrectal. Las publicaciones consultadas no han observado cambios significativos en los valores de las presiones de reposo y de contracción voluntaria, pese a que hubiera sido esperable un aumento de la presión en esta última ya que es la correspondiente al esfínter anal externo.50 En lo que respecta a la sensorialidad rectal y máximo volumen tolerable, Michelsen encuentra una diferencia significativa (p = <0,0001) en el incremento de la capacidad rectal, lo que se traduciría en una disminución de la urgencia evacuatoria.50 Si bien no fueron expuestos los resultados manométricos de nuestros pacientes por no ser el objetivo principal del trabajo, no encontramos diferencias en los pacientes de nuestra serie evaluados con manometría pre- y postoperatoria.
La ecografía esfinteriana de 3600 cobra valor para evaluar la indemnidad anatómica de la masa muscular. En nuestra serie todos los pacientes, respetando los criterios de inclusión, tenían esfínter anal indemne o lesión reparada quirúrgicamente. Se han descripto y comparado pacientes neuromodulados con y sin lesión esfinteriana obteniendo buenos resultados en el corto plazo sin explicar el mecanismo por el cual un esfínter anatómicamente incompleto podría responder desde el punto de vista funcional.51-54 Un número mayor de investigaciones en este tipo de pacientes serán los responsables de dar la respuesta a esta situación.
La NMS ha adquirido popularidad y aceptación por sus ventajas de ser mínimamente invasiva, con buenas tasas de éxito (70% aproximadamente),56 poca morbilidad (índice de complicaciones de 5-26%)57 y sin mortalidad reportada.58 Últimamente surgieron nuevas modalidades de neuromodulación con intención de ser menos costosas, menos invasivas y con la ventaja de ser ambulatorias. Al respecto, la estimulación del nervio tibial posterior (ENTP) percutánea utiliza un electrodo aguja para estimular a nivel retromaleolar interno el nervio tibial posterior y llevar el estímulo eléctrico a nivel medular. La ENTP requiere tratamientos repetidos para mantener la efectividad y distintas series refieren una tasa de éxito cercana al 60%.59-61 La ENTP transcutánea es aún menos invasiva, ya que utiliza electrodos adherentes para generar el estímulo eléctrico. Los índices de respuesta para la ENTP se encuentran descriptos principalmente en el corto plazo.62, 63 Dos estudios refieren mejorías, aunque realizando distintos protocolos de tratamientos (6 semanas de estimulación vs 3 meses). La ENTP percutánea ha demostrado presentar mejoría en el corto plazo en el score de incontinencia, FIQoL y en el número semanal de episodios de incontinencia, si bien al comparar la magnitud de estos cambios con la NMS, ellos son menores. Algunos autores sugieren, en función de esto, que la ENTP podría ser el tratamiento para pacientes con IF leve o moderada, o también como prueba de estimulación transitoria previa a la NMS. Respecto a la transcutánea, no hay resultados publicados a largo ni mediano plazo. Los pacientes de este protocolo tenían scores de incontinencia mayores por lo que la indicación fue la NMS.
En los pacientes que fueron sometidos a NMS con indicación de constipación severa e intratable, los resultados demuestran una mejoría en el 60%. Debido al pequeño tamaño de la muestra, no son comparables los resultados obtenidos con lo referido en la bibliografía, y como la NMS en constipación es más reciente, hay menos trabajos de seguimiento y con resultados a corto y mediano plazo.64, 65 En un trabajo publicado por Kenefick del St’Marks,64 se refiere que durante el implante transitorio y definitivo los pacientes presentaron una reducción en la intensidad de los síntomas y en el CCCS (Cleveland Clinic Constipation Score)66 con un incremento en la frecuencia evacuatoria. Rato y col reporta su experiencia con 16 pacientes neuromodulados por constipación severa intratable, mostrando a los 12 meses de seguimiento una mejoría del 60% CCCS.67 Holzer publica una tasa de éxito de 88% en 8 pacientes en los que se colocó el implante definitivo con un seguimiento de 11 meses.68 Naldini y col refiere una tasa de éxito del 60% con seguimiento a 42 meses.69 Kamm y col publicó un trabajo prospectivo y multicéntrico con un gran número de pacientes tratados con NMS por constipación.70 La frecuencia evacuatoria cambió de 3,5-7,1 episodios por semana (p < 0,001) y estos beneficios se mantuvieron durante el seguimiento. Describe una disminución en el tiempo de pujo, menos evacuación incompleta, menor tiempo en el baño, menor sensación de distensión y menor limitación en las actividades. Si bien nuestra serie tiene la limitación de ser con un bajo número de pacientes, de los 3 que se implantaron 2 tienen una tasa de éxito entre el 50 y el 80%.
En los pacientes neuromodulados por proctalgia los resultados obtenidos son de díficil interpretación ya que la muestra es muy pequeña. Un paciente presentó mejoría del 70% y los otros 2 mejoraron un 40% aproximadamente. La bibliografía refiere una tasa de éxito promedio de 50 a 70% en el seguimiento.
Como todo procedimiento quirúrgico, la NMS no está exenta de complicaciones, al contrario, presenta el factor agravante de dejar un dispositivo crónicamente en el paciente por lo que las complicaciones o eventos indeseados más frecuentes están relacionados con la presencia del mismo. La bibliografía describe el dolor en el sitio del implante definitivo, parestesias, cambios en la sensorialidad, incontinencia de orina, agotamiento de la batería, dolor glúteo, dolor en miembros inferiores, migración o decúbito del generador e infección del mismo.30 La mayoría de estos eventos (80%) pueden ser tratados satisfactoriamente con medicación u otra terapéutica no quirúrgica. Algunos autores mencionan cómo complicaciones tardías se producen luego de los 3 años del implante, a la migración y pérdida de la efectividad de forma casi exclusiva.30 En nuestra población las mayores complicaciones fueron la infección y el decúbito, siendo la primera la responsable de 4 explantes. Esto no condice con los descripto por la bibliografía que refiere que la principal causa de revisión en quirófano es la migración y la causa más común de explante del implante definitivo es el agotamiento de la batería o la pérdida de respuesta.71 Se estima que la probabilidad de que un paciente tenga que realizarse revisión o reemplazo del dispositivo, independientemente de la causa, es del 10,3% al año, aumentando a 24,4% a los 5 años. Igualmente, se estima que la probabilidad de que a un paciente se le explante el dispositivo al año es del 3,4%, incrementándose al 19% a los 5 años. En términos generales, luego de 5 años de NMS, los pacientes tienen 35,6% de posibilidades de tener alguna intervención, sea revisión, reemplazo o explante.
Se cuenta con el consenso general que el procedimiento debe ser efectuado con anestesia local para poder evaluar la respuesta sensitiva que experimenta el paciente con la estimulación eléctrica y que solo puede ser referida si el paciente no se encuentra sedado. En los casos que se realice con sedación solamente se cuenta con la respuesta motora como indicador. Todos nuestros pacientes se realizaron NMS con anestesia local evaluando así las respuestas motora y sensitiva.
En la mayoría de los pacientes se realizó NMS unilateral. Solo en 9 casos se colocaron implantes bilaterales. La principal indicación de la NMS bilateral es en pacientes irradiados o con incontinencia postresección rectal. Varios autores concluyen que la estimulación bilateral es superior en resultados funcionales.72, 73
Respecto a los costos de la NMS, si bien es un tratamiento con un costo elevado, fue sometido a múltiples estudios de costo-efectividad concluyendo que es una terapéutica costo-efectiva.74-76 La etapa de estimulación transitoria tiene un costo aproximado de 4.300 euros y la colocación del implante definitivo de 9.000 euros, un total aproximado de 15.000 euros.
Existe controversia en la medición de los resultados obtenidos y no hay un acuerdo de cuál sería la medición adecuada. Sería recomendable encontrar un consenso para estandarizar los indicadores de éxito.
La mayor fortaleza de este trabajo es la casuística que presenta y el prolongado tiempo de seguimiento, no existiendo experiencias similares publicadas en Latinoamérica, y es comparable con el resto de las publicaciones mundiales.
Conclusión
La utilización de la estimulación eléctrica de las raíces sacras para obtener un mejor funcionamiento de los órganos pelvianos es un área en constante crecimiento, teniendo cada vez mayor cantidad de indicaciones. Al igual que otros especialistas en NMS, nuestra experiencia fue inicialmente en pacientes con IF y con el incremento de la casuística y la experiencia se fueron incorporando pacientes con otras patologías. La garantía de tener resultados favorables depende de una correcta indicación, es por eso que los pacientes deben ser evaluados minuciosamente y, dependiendo de la patología, tratados con los métodos habituales hasta llegar a la NMS.
Conflictos de interés. Los autores declaran no presentar conflictos de interés.
Este manuscrito cuenta con un video de la técnica disponible en www.actagastro.org
Referencias
- Matzel K, Schmidt RA, Tanagho EA. Neuroanatomy of the striated anal continence mechanism: implications for use of neuroestimulation. Dis Colon Rectum 1990; 33: 666-673.
- Tanagho EA. Concepts of neuromodulation. Neurourol Urodyn 1993; 12: 487-488.
- Kenefick NJ, Emmanuel A, Nicholls RJ, Kamm MA. Effect of sacral nerve stimulation on autonomic nerve function. Br J Surg 2003; 90: 1256-1260.
- Ganio E, Masin A, Ratto C, Altomare D, Ripetti V, Clerico G, Lise M, Doglietto G, Memeo V, Landolfi V, Del Genio A, Arullani A, Giardello G, de Seta F. Short-term sacral nerve stimulation for functional anorectal and urinary disturbances: results in 40 patients. Evaluation of a new option for anorectal functional disorders. Dis Colon Rectum 2001; 44: 1261-1267.
- Caldwell KPS. The electrical control of sphincter incompetence. Lancet 1963; 2: 174.
- Matzel KE, Stadelmaier U, Gall FP, Hohenfellner M. Electrical stimulation of sacral spines nerves for treatment of fecal incontinence. Lancet 1995; 346: 1124-1127.
- Matzel KE, Stadelmaier U, Hohenfellner M, Gall FP. Permanent electrostimulation of sacral spines nerves with an implantable neuroestimulator in treatment of fecal incontinence. Chirurg 1995; 66: 813-817.
- Drossman DA, Li Z, Andruzzi E, Temple RD, Talley N, Grant Thompson W, Whitehead W, Janssens J, Funch-Jensen P, Corazziari E, Richter J, KocH G. U.S. Householder survey of functional gastrointestinal disorders. Prevalence, sociodemography, and health impact. Dig Dis Sci 1993; 38: 1569-1580.
- Nelson R, Norton N, Cautley E, Furner S. Comunity-based prevalence of anal incontinece. JAMA 1995; 274: 559-561.
- Rao SS. Diagnosis and management of fecal incontinence. Am J Gastroenterol 2004; 99: 1585-1604.
- Bharucha AE, Fletcher JG, Harper CM, Hough D, Daube JR, Stevens C, Seide B, Riederer SJ, Zinsmeister AR. Relationship between symptoms and disordered continence mechanisms in women with idiophaticfaecal incontinence. Gut 2005; 54: 546-555.
- Rao SS, Patel Rs. How useful are manometric tests of anorectal function in the management of defecation disorders. Am J Gastoenterol 1997; 92: 469-475.
- Madoff RD, Parker SC, Varma MG, Lowry AC. Faecal incontinence in adults. Lancet 2004; 364: 621-632.
- Sultan AH, Nugent K. Pathophysiology and nonsurgical treatment of anal incontinence. BJOG 2004; 111: 84-90.
- Wald A. Fecal incontinence. Curr Treat Options Gastroenterol 2005; 8: 319-324.
- Heymen S, Jones KR, Ringel Y, Scarlett Y, Whitehead WE. Biofeedback treatment of fecal incontinence: a critical review. Dis Colon Rectum 2001; 44: 728-736.
- Norton C, Kamm MA. Outcome of biofeedback for faecal incontinence. Br J Surg 1999; 86: 1159-1163.
- Brown SR, Wadhawan H, Nelson RL. Surgery for faecal incontinence in adults. Cochrane Database Syst Rev 2010; 9: CD001757.
- Bharucha A, Wald A, Rao SS. Functional anorectal disorders. Gastroenterology 2006; 130: 1510-1518.
- Dinning PG, Fuentealba SE, Kennedy ML, Lubowski DZ, Cook IJ. Sacral nerve stimulation induces pan-colonic propagating pressure waves and increases defecation frequency in patients with slow-transit constipation. Colorectal Dis 2007; 2: 123-132.
- Hirabayashi T, Matsufuji H, Yokohama J, Hagane K, Hoshino K, Morikawa Y, Kitajima M. Colorectal motility induction by sacral nerve electrostimulation in a canine model: implications for colonic pacing. Dis Colon Rectum 2003; 46: 809-827.
- Vazquez F, Miravalle OR, Bolino C, Gutierrez A, Arias J, Gualdrini U, Lumi CM, Muñoz J, La Rosa L, PiussI SV. Effectiveness of a therapeutic algorithm for functional anorectal pain: Experience in a private ambulatory coloproctology center in Buenos Aires, Argentina. Gastroenterology 2013; 144: S718.
- Siegel S, Paszkiewicz E, Kirkpatrick C, Hinkel B, Oleson K. Sacral nerve stimulation in patients with chronic intractable pelvic pain. J Urol 2001; 166: 1742-1745.
- Falletto E, Masin A, Lolli P, Villani R, Ganio E, Ripetti V, Infantino A, Stazi A, GINS (Italian Group for Sacral Neuromodulation). Is sacral nerve stimulation an effective treatment for chronic idiopathic anal pain? Dis Colon Rectum 2009; 52: 456-462.
- Govaert B, Melenhorst J, van Kleef M, van Gemert WG, Baeten CG. Sacral neuromodulation for the treatment of chronic functional anorectal pain: a single center experience. Pain Pract 2010; 10: 49-53.
- Jorge JM, Wexner SD. Etiology and management of fecal incontinence. Dis Colon Rectum 1993; 36: 77-97.
- Rockwood TH, Church JM, Fleshman JW, Kane RL, Mavrantonis C, Thorson AG, Wexner SD, Bliss D, Lowry AC. Fecal Incontinence Quality of Life Scale: quality of life instrument for patients with fecal incontinence. Dis Colon Rectum 2000; 43: 9-16.
- Lumi C, Muñoz J, La Rosa L. Neuromodulación sacra para el tratamiento de la incontinencia anal. Experiencia pilot oprospectiva en Argentina. Acta Gastroenterol Latinoam 2007; 37: 29-36.
- Thin N, Horrocks E, Hotouras A, Palit S, Thaha MA, Chan CL, Matzel KE, Knowles CH. Systematic review of the clinical effectiveness of neuromodulation in the treatment of faecal incontinence. British J Surg 2013; 100: 1430-1447.
- Hull T, Giese C, Wexner SD, Mellgren A, Devroede G, Madoff RD, Stromberg K, Coller JA, SNS Study Group. Long-term durability of sacral nerve stimulation therapy for chronic fecal incontinence. Dis Colon Rectum 2013; 56: 234-245.
- El-Gazzaz G, Zutshi M, Salcedo L, Hammel J, Rackley R, Hull T. Sacral neuromodulation for the treatment of fecal incontinence and urinary incontinence in female patients: long-term follow-up. Int J Colorectal Dis 2009; 24: 1377-1381.
- Uludag Ö, Melenhorst J, Koch SM, van Gemert WG, Dejong CH, Baeten CG. Sacral neuromodulation: long-term outcome and quality of life in patients with faecal incontinence. Colorectal Dis 2011; 13: 1162-1166.
- Tjandra JJ, Chan MK, Yeh CH, Murray-Green C. Sacral nerve stimulation is more effective than optimal medical theraphy for severe fecal incontinence: a randomized, controlled study. Dis Colon Rectum 2008; 51: 494-502.
- Gourcerol G, Gallas S, Michot F, Denis P, Leroi AM. Sacral nerve stimulation in fecal incontinence: are there factors associated with success? Dis Colon Rectum 2007; 50: 3-12.
- Boyle DJ, Knowles CH, Lunniss PJ, Scott SM, Williams NS, Gill KA. Efficacy of sacral nerve stimulation for fecal incontinence in patients with anal shincter defects. Dis Colon Rectum 2009; 52: 1234-1239.
- Hollingshead JR, Dudding TC, Vaizey CJ. Sacral nerve stimulation for fecal incontinence: results from a single centre over a 10 year period. Colorectal Dis 2011; 13: 1030-1034.
- Wexner SD, Coller JA, Devroede G, Hull T, McCallum R, Chan M, Ayscue JM, Shobeiri AS, Margolin D, England M, Kaufman H, Snape WJ, Mutlu E, Chua H, Pettit P, Nagle D, Madoff RD, Lerew DR, Mellgren A. Sacral nerve stimulation for fecal incontinence: results of a 120-patient prospective multicenter study. Ann Surg 2010; 251: 441-449.
- Matzel KE, Kamm MA, Stösser M, Baeten CG, Christinsen J, Madoff R, Mellgren A, Nicholls RJ, Rius J, Rosen H. Sacral spine nerve stimulation for faecal incontinence: multicentre study. Lancet 2004; 363; 1270-1276.
- Melenhorst J, Koch SM, Uludag O, van Gemert WG, Baeten CG. Sacral neuromodulation in patients with faecal incontinence: results of the first 100 permanent implantations. Colorectal Dis 2007; 9: 725-730.
- Dudding TC, Meng Lee E, Faiz O, Parés D, Vaizey CJ, McGuire A, Kamm MA. Economic evaluation of sacral nerve stimulation for faecal incontinence. Br J Surg 2008; 95: 1155-1163.
- Muñoz-Cuyos A, Navarro-Luna A, Brosa M, Pando JA, Sitges- Serra A, Marco-Molina. Clinical and cost effectiveness of sacral nerve stimulation for faecal incontinence. Br J Surg 2008; 95: 1037-1043.
- Govaert B, Melenhorst J, Van Gemert WG, Baeten CG. Can sensory and/or motor reactions during percutaneous nerve evaluation predict outcome of sacral nerve modulation? Dis Colon Rectum 2009; 52: 1423-1426.
- Govaert B, Melenhorst J, Nieman FH, Bols EM, van Gemert WG, Baeten CG. Factors associated with percutaneous nerve evaluation and permanent sacral nerve modulation outcome in patients with fecal incontinence. Dis Colon Rectum 2009; 52: 1688-1694.
- Oom DM, Steensma AB, van Lanschot JJ, Schouten WR. Is sacral neuromodulation for fecal incontinence worthwhile in patients with associated pelvic floor injury? Dis Colon Rectum 2010; 53: 422-427.
- Mellgren A, Wexner SD, Coller JA, Devroede G, Lerew DR, Madoff RD, Hull T; SNS Study Group. Long-term efficacy and safety of sacral nerve stimulation for fecal incontinence. Dis Colon Rectum 2011; 54: 1065-1075.
- Boyle DJ, Muprhy J, Gooneratne ML, Grimmer K, Allison ME, Chan CL, Williams. Efficacy of sacral nerve stimulation for the treatment of fecal incontinence. Dis Colon Rectum 2011; 54: 1271-1278.
- Matzel KE, Lux P, Heuer S, Basendörfer M, Zhang W. Sacral nerve stimulation for faecal incontinence: long-term outcome. Colorectal Dis 2009; 11: 636-641.
- Devroede G, Giese C, Wexner SD, Mellgren A, Coller JA, Madoff RD, Hull T, Stromberg K, Iyer S; SNS Study Group. Quality of life is markedly improved in patients with fecal incontinence after sacral nerve stimulation. Female Pelvic Med Reconstr Surg 2012; 18: 103-112.
- Altomare DF, Ratto C, Ganio C, Loli P, Masin A, Villani RD. Long-term outcome of sacral nerve stimulation for fecal incontinence. Dis Colon Rectum 2009; 52: 11-17.
- Michelsen H, Buntzen S, Krogh K, Laurberg S. Rectal volume tolerability and anal pressures in patients with fecal incontinence treated with sacral nerve stimulation. Dis Colon Rectum 2006; 49: 1039-1044.
- Melenhorst J, Koch S, Uludag O, van Germet WG, Baeten CG. Is a morphologically intact anal sphincter necessary for success with sacral nerve stimulation in patients with faecal incontinence? Colorectal Dis 2008; 10: 257-262.
- Ratto C, Litta F, Parello A, Donisi L, Doglietto GB. Sacral nerve stimulation is a valid approach in fecal incontinence due to shincter lesion when compared to sphincter repair. Dis Colon Rectum 2010; 53: 264-272.
- Jarret M, Dudding T, Nicholls RJ, Vaizey CJ, Cohen CR, Kamm MA. Sacral nerve stimulation for fecal incontinence related to obstetric anal sphincter damage. Dis Colon Rectum 2008; 51: 531-537.
- Brouwer R, Duthie G. Sacral nerve neuromodulation is effective treatment for fecal incontinence in the presence of a sphincter defect, pudendal neuropathy, or previous sphincter repair. Dis Colon Rectum 2010; 53: 273-278.
- Kenefick NJ, Vaizey CJ, Cohen RG, Nicholls RJ, Kamm MA. Medium-term results of sacral nerve stimulation for fecal incontinence. Br J Surg 2002; 89: 896-901.
- Matzel KE. Sacral nerve stimulation for faecal incontinence: its role in the treatment algorithm. Colorectal Dis 2011; 13: 10-14.
- Tjandra JJ, Lim JF, Matzel K. Sacral nerve stimulation: an emerging treatment for fecal incontinence. ANZ J Surg 2004; 74: 1098-1106.
- Wong MT, Meurette G, Rodat F,Regenet N, Wyart V, Lehur PA. Outcome and management of patients in whom sacral nerve stimulation for fecal incontinence failed. Dis Colon Rectum 2011; 54: 425-232.
- Shafik A, Ahmed I, El-Sibai O, Mostafa RM. Percutaneous peripheral neuromodulation in the treatment of fecal incontinence. Eur Surg Res 2003; 35: 103-107.
- Findlay JM, Yeung JM, Robinson R, Greaves H, Maxwell-Armstrong C. Peripheral neuromodulation via posterior tibial nerve stimulation -a potential treatment for faecal incontinence? Ann R Coll Surg Engl 2010; 92: 385-390.
- de la Portilla F, Rada R, Vega J, Gonzalez C, Cisneros N, Maldonado V. Evaluation of the use of posterior tibial nerve stimulation for the treatment of fecal incontinence: preliminary results of a prospective study. Dis Colon Rectum 2009; 52: 1427-1433.
- Boyle DJ, Prosser K, Allison ME, Williams NS, Chan CL. Percutaneous tibial nerve stimulation for the treatment of urge fecal incontinence. Dis Colon Rectum 2010; 53: 432-437.
- Govaert B, Pares D, Delgado-Aros S, La Torre F, Van Germert WG, Baeten CG. A prospective multicentre study to investigate percutaneous tibial nerve stimulation for the treatmnet of faecal incontinence. Colorectal Dis 2010; 12: 1236-1241.
- Kenefick NJ, Nicholls RJ, Cohen RG, Kamm MA. Permanent sacral nerve stimulation for treatment of idiophatic constipation. Br J Surg 2002; 89: 882-888.
- Masin A, Ratto C, Ganio E. Effect of sacral nerve stimulation for intractable constipation. Ital J Public Health 2005; 2: 305-307.
- Agachan F, Chen T, Pfeifer J, Reissman P, Wexner S. A constipation scoring system to simplify evaluation and management of constipated patients. Dis Colon Rectum 1996; 39: 681-685.
- Ganio E, Masin A, Ratto C, Basile M, Realis Luc A, Lise G, Doglietto GB, Gidaro S, Giardello G, De Seta F. Sacral Nerve Modulation for chronic outlet constipation. http://colorep.it
- Holzer B, Rosen H, Novi G, Ausch C, Hölbling N, Hofmann M, Schiessel R. Sacral nerve stimulation in patients with severe constipation. Dis Colon Rectum 2008; 51: 524-529.
- Naldini G, Martelluci J, Moraldi L, Balestri R, Rossi M. Treatment of slow-transit constipation with sacral nerve modulation. Colorrectal Dis 2010; 12: 1149-1152.
- Kamm MA, Dudding TC, Melenhorst J, Jarret M, Wang Z, Buntzen S, Johansson C, Laurberg S, Rosen H, Vaizey C, Matzel K, Baeten C. Sacral nerve stimulation for intractable constipation: Gut 2010; 59: 333-334.
- Maeda Y, Matzel K, Lundby L, Buntzen S, Laurberg S. Postoperative issues of sacral nerve stimulation for fecal incontinence and constipation: A systematic literature review and treatment guideline. Dis Colon Rectum 2011; 54: 1430-1460.
- Scheepens W, de Bie R, Weil E, van Kerrebroeck PE. Unilateral versus bilateral sacral neuromodulation in patients with chronic voiding dysfunction. J Urol 2002; 168: 2046-2050.
- van Kerrebroeck, Scheepens WA, de Bie R, Weil EH. European experience with bilateral sacral neuromodulation in patients with chronic lower urinary tract dysfunction. Urol Clin North Am 2005; 32: 51-57.
- Dudding TC, Meng Lee E, Faiz O, Parés D, Vaizey CJ, Mc Guire M, Kamm A. Economic evaluation of sacral nerve stimulation for faecal incontinence. Br J Surg 2008; 95: 1155-1165.
- Muñoz-Duyos A, Navarro-Luna A, Bross M, Pando JA, Sitges- Serra A, Marco-Molina C. Clinical and cost effectiveness of sacral nerve stimulation for faecal incontinence. Br J Surg 2008; 95: 1037-1043.
- Van Wunnik BPW, Visschers RGJ, van Asselt ADI, Baeten CGMI. Cost-effectiveness analysis of sacral neuromodulation for faecal incontinence in the Netherlands. Colorectal Dis 2012; 14: 807-814.
Correspondencia: Omar Rubén Miravalle
Dirección: Av Santa Fé 1589 1º (C1060AAB). Ciudad Autónoma de
Buenos Aires, Argentina
Tel: +54-911-4815-1403.
Correo electrónico: rubenmiravalle@gmail.com
Acta Gastroenterol Latinoam 2016;46(2): 82-94
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE