Luis Soifer
Unimot. Ciudad Autónoma de Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2016;46: 327-331
Recibido: 29/01/2016 / Aprobado: 12/10/2016 / Publicado en www.actagastro.org el 01/01/2017
Resumen
La pseudoobstrucción intestinal crónica (SOIC) es un cuadro clínico caracterizado por episodios recurrentes de oclusión o suboclusión intestinal, sin una alteración anatómica mecánica que pueda explicarlos. Se presenta el caso de una mujer de 80 años con antecedentes de enfermedad de Parkinson y episodios reiterados de SOIC. Refiere constipación crónica severa (pueden pasar más de 15 días sin evacuar), marcada distensión abdominal, asas intestinales visibles y marcado timpanismo percutorio. El empleo de un esquema secuencial de antibóticos y probióticos, no logró reducir la elevada excreción de metano en el aire espirado, sino que, al contrario, se incrementó en forma significativa. Solo la limpieza colónica con dosis elevadas de polietilengicol 3350, de modo semejante a la que se obtiene durante las preparaciones en los estudios endoscópicos del colon, logró reducir, aunque no suprimir totalmente la metanogénesis y mejorar la sintomatología de la paciente.
Palabras claves. Pseudoobstrucción intestinal crónica, test del aire espirado con lactulosa, flora metanogénica, PEG3350.
Methanogenic excretion in chronic intestinal pseudo-obstruction. Therapeutic response
Summary
The chronic intestinal pseudo-obstruction (CIPO) is a clinical condition characterized by recurrent episodes of occlusion or partial bowel obstruction without mechanical or anatomical changes. The case of a 80 year old woman with a long history of Parkinson’s disease and repeated episodes of CIPO is presented. She refers severe chronic constipation (it may take more than 15 days without a bowel movement), important abdominal distension, visible bowel loops and tympanic abdomen percussion. The use of a sequential scheme of antibiotics and probiotics, failed to reduce the high excretion of methane in breath lactulose test, but instead increase significantly. Only colonic cleansing with high doses of PEG 3350, similarly to that obtained during the preparations of the colon endoscopic studies, reduces, but not completely suppresses methanogenesis, and improves patient symptoms.
Key words. Chronic intestinal pseudo-obstruction, lactulose breath test, methanogenic flora, PEG3350.
Abreviaturas
SOIC: pseudoobstrucción intestinal crónica.
CIPO: chronical intestinal pseudoobstruction.
PEG: olietilenglicol.
FODMAP´S: oligosacáridos, disacáridos, monosacáridos y polioles fermentables.
LBT: test del aire espirado con lactulosa.
H2: hidrógeno.
CH4: metano.
ABC: área bajo la curva.
PPM: partes por millón.
VCC: videocolonoscopía.
La interrupción de la progresión distal del contenido intestinal recibe el nombre de íleo. Existen dos grandes grupos, el íleo mecánico u obstructivo y el íleo paralítico o adinámico.
La seudooclusión intestinal, íleo paralítico o adinámico consiste en un compromiso del tránsito, sin una causa mecánica que lo justifique, atribuyéndose, por lo tanto, a una alteración de la función motora del intestino. Es habitual reservar el término de íleo paralítico para la seudooclusión intestinal aguda que afecta globalmente al intestino delgado y al colon.
Existen dos formas clínicas de pseudooclusión intestinal que merecen una consideración específica: el síndrome de Ogilvie y la pseudoobstrucción intestinal crónica.1
La pseudoobstrucción cólica aguda (síndrome de Ogilvie) se caracteriza por una dilatación masiva del colon, de instauración aguda, en ausencia de obstrucción mecánica.
La pseudoobstrucción intestinal crónica (SOIC) es un cuadro clínico caracterizado por episodios recurrentes de oclusión o suboclusión intestinal, sin una alteración anatómica mecánica que pueda explicarlos. Las causas implicadas en la aparición de este síndrome son diversas: es posible detectar a menudo una causa neurológica (enfermedad de Parkinson, tumores cerebrales) o muscular (miositis, esclerodermia, amiloidosis). Asimismo, no es infrecuente identificar una enfermedad endocrinológica (hipotiroidismo, hipoparatiroidismo, feocromocitoma) o el consumo reciente o habitual de determinados fármacos (opiáceos y psicolépticos). Finalmente, en algunos casos no se logra identificar una causa aparente, considerándose a estas formas como idiopáticas. Entre ellas deben distinguirse esencialmente dos cuadros: la miopatía visceral y la neuropatía visceral.
En la miopatía visceral existe una alteración en la musculatura lisa del intestino, caracterizada por una degeneración de las células musculares lisas y su sustitución por tejido fibroso. Puede afectar a una o más capas del tejido muscular y se traduce en una contractilidad intestinal ordenada, aunque débil e inefectiva. La neuropatía visceral engloba procesos que pueden afectar a cualquier eslabón de la regulación del sistema nervioso cerebro-intestinal. Se caracteriza por presentar contracciones de magnitud normal pero con un patrón desorganizado y, por tanto, inefectivo en la propulsión.2
Caso clínico
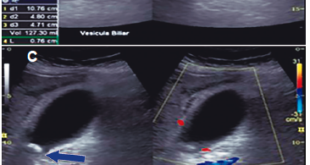
Mujer de 80 años que consulta por primera vez en noviembre de 2014. Antecedentes clínicos: enfermedad de Parkinson de varios años de evolución, varias internaciones por íleo, interpretadas como una pseudoobstrucción intestinal (se resuelve con enemas y aspirado mediante VCC). Antecedentes quirúrgicos: mastectomía radical por adenocarcinoma de mama, safenectomía por trombosis y cirugía de cataratas.
Refiere constipación crónica severa (pueden pasar más de 15 días sin evacuar), marcada distensión abdominal, asas intestinales visibles y marcado timpanismo percutorio. Requiere enemas evacuantes de 500 ml en forma frecuente. Al tacto rectal la ampolla se encuentra libre.
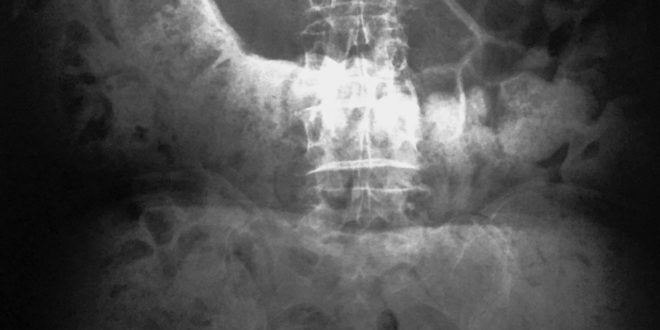
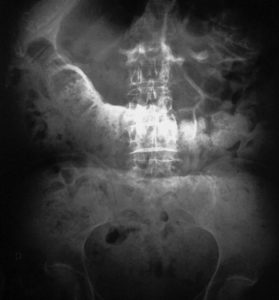
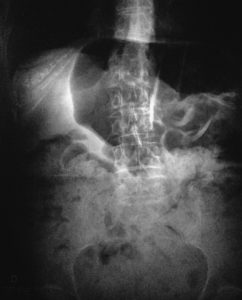
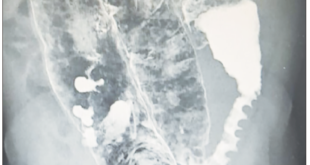
Se solicita una radiografía simple del abdomen que evidencia la presencia de un dolicocolon, con abundantes restos de materia fecal (Figuras 1 y 2).
Se inicia tratamiento con Polietilenglicol 17 gramos/ día, lincomicina 500 mg/día y dieta hipofermentable con bajo contenido en FODMAP´S (en inglés: oligosacáridos, disacáridos, monosacáridos y polioles fermentables). Ante la escasa respuesta a este tratamiento se incorpora a lo anterior una combinación de psyllium 190 mg + senósidos 7,5 mg, dos veces por día (Medilaxan-comprimidos) y picosulfato de sodio 5 mg + agar-agar 30 mg dos veces por día (Agarol-cápsulas).
Quince días después la paciente continúa muy distendida pese a lograr evacuaciones blandas y formadas, hasta 4 veces por día. Tres meses después, la paciente continúa distendida y se le propone un tratamiento con rifaximina 550 mg + neomicina 920 mg dos veces por día durante 10 días. Refiere mejoría clínica, estar menos distendida y con catarsis diaria de forma y consistencia normal.
No obstante, dos meses más tarde se presenta nuevamente muy distendida con marcado timpanismo percutorio y dolor abdominal generalizado. Se le solicita un test del aire espirado con lactulosa con determinación del área bajo la curva de las concentraciones de hidrógeno y metano, con muestras obtenidas en forma basal y cada 20 minutos luego de la ingesta de 10 mg de lactulosa por un lapso total de 180 minutos. El test reveló valores muy bajos de hidrógeno (450 ppm/h) pero sumamente elevados para metano (21.330 ppm/h). Se realiza por lo tanto el diagnóstico de sobrecrecimiento bacteriano metanogénico.
Se intenta en ese momento un esquema secuencial que se detalla a continuación:
- Lincomicina 500 mg/día durante 7 dí
- Probiótico con sacaromices boulardii (Floratil) 200 mg dos veces por día durante 7 dí
- Neomicina 920 mg/día + rifaximina 550 mg/día durante 7dí
- Probiótico con sacaromices boulardii (Floratil) 200 mg dos veces por día durante 7 dí
- Tetraciclina 500mg/d + metronidazol 500 mg dos veces por día 7 dí
- Probiótico con sacaromices boulardii (Floratil) 200 mg dos veces por día durante 7 dí
Se repite el test de H2 y CH4 en el aire espirado luego de finalizado el esquema secuencial (antibiótico-probiótico) con los siguientes valores del área bajo la curva de ambos gases.
- H2: 936 ppm/h.
- CH4: 13.968 ppm/h.
Se intenta un segundo esquema secuencial, pero esta vez con:
- Metronidazol 500 mg/día + ciprofloxacina 500 mg/d durante 7 dí
- Trimetoprima 80 mg + sulfametoxazol 200 mg + neomicina 920 mg dos veces por día durante 7 dí
Se repite el test de H2 y CH4 en aire espirado luego de finalizado el esquema secuencial (antibiótico-probiótico) con los siguientes valores del área bajo la curva de metano. CH4: ABC 25.974 ppm/h. Es decir que los esquemas secuenciales con antibióticos y prebióticos no solo no habían mejorado el sobrecrecimiento bacteriano matanógeno, sino que lo habían empeorado.
Luego de observar la respuesta metanógena incrementada se decide administrar PEG 3.350 en dosis semejantes a las empleadas en las preparaciones de limpieza colónica, 4 litros, 240 gramos, a razón de 250 ml cada 2 horas. Un nuevo test de H2 y CH4 al mes de administrado el PEG revela los siguientes valores del área bajo la curva de ambos gases.
- LBT H2: 918 ppm/h.
- CH4: 9.738 ppm/h.
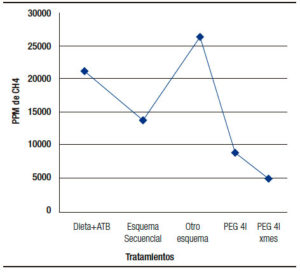
A partir de la evidencia positiva, con reducción significativa en la excreción de metano, se inicia mensualmente un esquema de PEG 3350/4 litros. Un control a los tres meses de iniciado el tratamiento revela los valores de metano en el aire espirado de 4.200 ppm/h con una reducción máxima estimada en 84% en el metano excretado desde el valor verificado luego de los esquemas secuenciales con antibióticos (Figura 3).
La paciente se mantiene estable, menos distendida y con evacuaciones semilíquidas a diario.
Figura 3. Respuesta metanogénica.
Discusión
El proceso fermentativo inducido por la microbiota intestinal, básicamente por bacteroides y firmicutes, da por resultado la producción de ácidos grasos de cadena corta (acetato, propionato y butirato), que representan hasta un 10% del aporte calórico.3 Por este motivo actualmente se sabe que los animales libres de gérmenes no engordan pese a ingerir alimentos con alto contenido calórico.4 También como resultado del proceso fermentativo se producen en gran cantidad el dióxido de carbono (CO2) y de hidrógeno (H2). El H2 es eliminado mediante tres mecanismos: flatos, absorción en la circulación sistémica y excreción respiratoria (aire espirado) y por el metabolismo de la microbiota colónica hidrogenotrófica, que es considerado el mecanismo de mayor eliminación de H2.5
El hidrógeno es metabolizado por microorganismos hidrogenotróficos que compiten intensamente por la utilización del mismo. Se trata de las arqueas metanogénicas que convierten el H2 en metano (CH4), siendo la principal el metanobrevibacter smithii, las bacterias reductoras de sulfato y las bacterias acetogénicas.
La presencia de flora metanogénica, más frecuente en el sexo femenino, independientemente de la edad, ha sido asociada a la constipación crónica con lento tránsito intestinal y con una significativa reducción en la actividad de las ondas motoras colónicas.6-8
Si bien se ha podido establecer una fuerte asociación entre constipación, tránsito enlentecido y metanogénesis, no queda claro si la relación es causal o incidental. En este sentido existen evidencias de que los laxantes y los lavajes colónicos reducen la excreción de metano.9 De otro modo, mediante experiencias en animales, la infusión directa de metano al intestino delgado produjo una reducción en el tiempo de tránsito del 59% comparativamente con la infusión de aire ambiental.10 Estos efectos del metano sobre el tránsito podrían estar mediados por una reducida producción de serotonina postprandial en sujetos con microbiota metanogénica.11
También es factible que el disbalance en la microbiota hidrogenotrófica a favor de las metanogénicas, en detrimento de las bacterias reductoras de sulfuro, pueda tener un efecto negativo en la sintomatología de los pacientes, debido al conocido efecto neuromodulador del sulfuro de hidrógeno.12 Por lo tanto, es posible que ante una alteración motora de causa neurológica, como en este caso es la enfermedad de Parkinson, se condicione un sobrecrecimiento de arqueas metanógenas, lo que a su vez establezca un mayor compromiso de la motilidad debido al efecto antiquinético del metano.
La detección de metano en el aire espirado en pacientes constipados, mediante la medición del área bajo la curva, luego de la ingesta de lactulosa, ha demostrado tener una adecuada reproducibilidad intrasujeto y las mediciones son además estables en el tiempo.13
Actualmente existen pocos datos sobre cómo modular terapéuticamente la flora metanógena. Son muy pocos los antibióticos sensibles para lograr vencer la resistencia del metanobrevibacter smithii. Reducciones en la excreción de metano, evaluadas mediante test del aire espirado con lactulosa, se han logrado mediante la combinación de neomicina y rifaximina.14
La neomicina, el ácido pseudomónico, la puromicina, los fluorometanos, los 2 cloro etano sulfonatos y algunas estatinas (mevastatin y lovastatin) han demostrado ser inhibidores metanogénicos.15
El empleo del S boulardii como probiótico terapéutico se basó en su mecanismo de acción, en su farmacoquinética y en su eficacia demostrada en trabajos realizados sobre modelos animales y clínicos. Además, debido a su buen perfil de seguridad, ha sido recomendado para el tratamiento de varios trastornos digestivos y para la prevención de las disbacteriosis y diarreas inducidas por antibióticos; éste útimo es el principal motivo por el que fue empleado en esta paciente.16
Asimismo, el empleo de un esquema secuencial de antibóticos y probióticos no logró reducir la excreción de metano en el aire espirado, sino que al contrario se incrementó en forma significativa. Solo la limpieza colónica con dosis elevadas de polietilengicol 3350, de modo semejante a la que se obtiene durante las preparaciones en los estudios endoscópicos del colon, logró reducir, aunque no suprimir totalmente, la metanogénesis.
Conclusiones
La medición del área bajo la curva en la excreción de metano en el aire espirado en esta paciente con pseudobstrucción intestinal, demostró un sobrecrecimiento metanogénico y asociación entre la severidad sintomática de la paciente y la excreción de metano. No se logró revertir la excreción de metano mediante el empleo secuencial de antibióticos y probióticos. Solo se logró reducir de un modo significativo la metanogénesis y mejorar la sintomatología mediante el empleo de PEG oral en dosis elevadas.
Referencias
- Bernardi MP, Warrier S, Lynch AC, Heriot AG. Acute and chronic pseudo-obstruction: a current update. ANZ J Surg 2015; 85: 709-714.
- De Giorgio R, Cogliandro RF, Barbara G, Corinaldesi R, Stanghellini V. Chronic intestinal pseudo-obstruction: clinical features, diagnosis, and therapy. Gastroenterol Clin North Am 2011; 40: 787-807.
- McNeil NI. The contribution of the large intestine to energy supplies in man. Am J Clin Nutr 1984; 39: 338-342.
- Turnbaugh PJ, Ley RE, Mahowald MA, Magrini V, Mardis ER, Gordon JI. An obesity-associated gut microbiome with increased capacity for energy harvest. Nature 2006; 444: 1027-1031.
- Sahakian AB, Jee SR, Pimentel M. Methane and the gastrointestinal tract. Dig Dis Sci 2010; 55: 2135-2143.
- Attaluri A, Jackson M, Valestin J Rao SS. Methanogenic flora is associated with altered colonic transit but not stool characteristics in constipation without IBS. Am J Gastroenterol 2010; 105: 1407-1411.
- Attaluri A, Valestin J, Rao SSC. Is small bowel and colonic motility altered in constipated patients with methanogenic flora? Neurogastroenterol Motil 2011; 22: 79.
- Kunkel D, Basseri RJ, Makhani MD, Chong K, Chang C, Pimentel M. Methane on breath testing is associated with constipation: a systematic review and meta-analysis. Dig Dis Sci 2011; 56: 1612-1618.
- Sahakian AB, Jee SR, Pimentel M. Methane and the gastrointestinal tract. Dig Dis Sci 2010; 55: 2135-2143.
- Pimentel M, Lin HC, Enayati P, Van den Burg B, Lee HR, Chen J, Park S, Kong Y, Conklin J. Methane, a gas produced by enteric bacteria, slows intestinal transit and augments small intestinal contractile activity. Am J Physiol Gastrointest Liver Physiol 2006; 290: G1089-G1095.
- Pimentel M, Kong Y, Park S. IBS subjects with methane on lactulose breath test have lower postprandial serotonin levels than subjects with hydrogen. Dig Dis Sci 2004; 49: 84-87.
- Distrutti E, Sediari L, Mencarelli A, Renga B, Orlandi S, Antonelli E, Roviezzo F, Morelli A, Cirino G, Wallace JL, Fiorucci S. Evidence that hydrogen sulfide exerts antinociceptive effects in the gastrointestinal tract by activating KATP channels. J Pharmacol Exp Ther 2006; 316: 325-335.
- Meduri K, Attaluri A, Valestin J, Summers RW, Rao SSC. Reproducibility of methane and hydrogen values in constipated patients with methanogenic flora. Gastroenterology 2011; 140: S530-S531.
- Low K, Hwang L, Hua J, Zhu A, Morales W, Pimentel M. A combination of rifaximin and neomycin is most effective in treating irritable bowel syndrome patients with methane on lactulose breath test. J Clin Gastroenterol 2010; 44: 547–550.
- Pimentel M, Gunsalus RP, Rao SSC, Zhang H. Methanogens in Human Health and Disease. Am J Gastroenterol 2012; 1: 28-33.
- Lynne V McFarland. Systematic review and meta-analysis of Saccharomyces boulardii in adult patients World J Gastroenterol 2010; 16: 2202–2222.
Correspondencia: Luis Soifer
Unimot, Santa Fe 1206, 4H (1059). Ciudad Autónoma de Buenos Aires, Argentina
Tel.: 5411-48111810
Correo electrónico: lsoifer@gmail.com
Acta Gastroenterol Latinoam 2016;46(4): 327-331
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE