Miguel A Valdovinos,1 Roberto AM Teutle,1 Jesús Sepúlveda,2 Juan M Gómez,1 Elisa N Saleme,1 Ilonka Zsolt,3 Thais Baleeiro
1 Departamento de Gastroenterología, Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. México DF, México.
2 Medicina Nuclear, Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán. México DF, México.
3 Departamento médico, Ferrer. Barcelona, España.
Acta Gastroenterol Latinoam 2017;47(4):277-287
Recibido: 30/01/2017 / Aprobado: 23/03/2017 / Publicado en www.actagastro.org el 18/12/2017
Resumen
La diabetes mellitus (DM) es la segunda causa de gastroparesia (GD). Los procinéticos son la piedra angular del tratamiento. Objetivo. Evaluar el efecto de levosulpirida vs. cinitaprida en el alivio de los síntomas gástricos en pacientes con GD. Material y métodos. Ensayo clínico piloto unicéntrico aleatorizado doble ciego y doblemente enmascarado. Se incluyeron 35 pacientes de 18 a 70 años con DM tipos 1 o 2 y diagnóstico de GD, con sintomatología clínica compatible. La variable principal de evaluación fue la diferencia en la puntuación global del cuestionario de síntomas (gastroparesis cardianal symptom index, GCSI) a los 6 meses del inicio del tratamiento. Adicionalmente, se evaluó la velocidad de vaciado gástrico (VG), la calidad de vida y la seguridad de ambos fármacos. Resultados. Al final del estudio (6 meses) la diferencia en la media de puntuación global del GCSI fue significativamente menor en el grupo tratado con levosulpirida (0,52 puntos; IC95%: 0,08-0,96; p = 0,043). Levosulpiride aceleró significativamente el VG mientras que no ocurrió así con cinitaprida. Ambos fármacos mejoraron la calidad de vida y fueron bien tolerados; únicamente se produjo la activación de un microadenoma hipofisario silente en un paciente tras el inicio del tratamiento con levosulpirida. Conclusiones. Los resultados muestran que levosulpirida es un procinético eficaz y seguro en el tratamiento de la GD. Al tratarse de un estudio piloto, los datos obtenidos deberían ser confirmados en posteriores estudios con un mayor tamaño muestral.
Palabras claves. Levosulpirida, cinitaprida, gastroparesia diabética, procinéticos, ensayo clínico aleatorizado.
Efficacy of levosulpiride versus cinitapride in symptom control, quality of life and gastric emptying in patients with diabetic gastroparesis. Double blind, randomized pilot study after 6 months of therapy
Summary
Diabetes mellitus (DM) is the second cause of diabetic gastroparesis (DG). Prokinetics are the cornerstone of DG therapy. Objective. The aim of this was to assess the efficacy of levosulpiride vs. cinitapride in the relief of gastric symptoms in DG patients. Material and methods. Single center, double blind, double dummy, randomized pilot clinical trial. Thirty five diabetic type 1 and 2 patients of 18 to 70 years diagnosed of DG and compatible clinical symptoms were included. The main outcome was the difference in the global score of the gastroparesis cardinal symptom index (GCSI) after 6 months of therapy. Additionally, the delay in gastric emptying (GE), quality of life and safety was assessed. Results. At the end of the study (6 months of follow up) the difference in the mean of the global score of the GCSI was significantly lower in the levosulpiride treated group (0.52 points, CI95%: 0.08-0.96; p = 0.043). Levosulpiride accelerated significantly the GE whereas it did not happen after cinitapride therapy. Both drugs improved quality of life and were well tolerated, but of one case of activation of a silent pituitary microadenoma in the levosulpiride group. Conclusions. These results show that levosulpiride is an efficacious and safe prokinetic for DG therapy. As it is a pilot study, these data should be confirmed in further studies with a broader simple size.
Key words. Levosulpiride, cinitapride, diabetic gastroparesis, prokinetic drugs, randomized clinical trial.
La GP es un síndrome caracterizado por síntomas gástricos y retraso del VG en ausencia de obstrucción mecánica. La DM es la segunda causa más frecuente de GP, después de la idiopática.1 La prevalencia de la gastropatía diabética (GD) es variable de acuerdo a la población estudiada. Los estudios en centros de tercer nivel de atención muestran una prevalencia de GD de 10 a 30% en pacientes con DM tipo 2,2 en contraste con los estudios en la comunidad que han estimado una prevalencia del 1%.3 En pacientes con DM tipo 1 la prevalencia observada es del 40% en centros de tercer nivel y del 5% en la comunidad.4, 5
La GD evoluciona con el tiempo. En un período de 10 años, aproximadamente 5,2% de los pacientes con DM tipo 1 y 1% de aquellos con DM tipo 2 desarrollarán GP.6 Los pacientes diabéticos con GP comúnmente tienen alguna de las complicaciones crónicas de la DM como retinopatía, nefropatía, neuropatía. En pocos pacientes, la GP es la primera manifestación de complicaciones neuropáticas de la DM. La tasa de admisión al hospital por GD se ha incrementado más del 100% en las últimas 2 décadas.7 La GD afecta significativamente la calidad de vida de los pacientes con DM, incrementa los costos de la atención médica y es un factor importante de descontrol de la glucemia.41
El tratamiento de la GD incluye apoyo nutricional, fármacos antieméticos y procinéticos, inyección de toxina botulínica en el píloro, neuroestimulación gástrica y uso de gastrostomía descompresiva. Los procinéticos son la piedra angular en el tratamiento de la GD.8
Levosulpirida, una benzamida sustituida con propiedades antidopaminérgicas D2 y serotoninérgicas 5-HT4, es un procinético que ha mostrado ser superior a placebo9, 10 y cisaprida11 en la mejoría de los síntomas y el VG en pacientes con GD. No existen ensayos clínicos aleatorios que comparen levosulpirida con cinitaprida, otro agonista 5-HT4, en pacientes con GD.
El objetivo principal de este estudio fue evaluar el efecto de levosulpirida versus cinitaprida en el alivio de los síntomas gástricos en pacientes con GD. Secundariamente, se evaluó la velocidad de VG, la calidad de vida del paciente, el control de la glucemia, la adherencia al tratamiento y la seguridad de ambos fármacos.
Material y métodos
Se trata de un ensayo clínico piloto, unicéntrico, aleatorizado, doble ciego y doblemente enmascarado de dos grupos paralelos y de 6 meses de duración. Se incluyeron pacientes de 18 a 70 años con DM tipos 1 o 2 según los criterios de la American Diabetes Association (ADA),12 con niveles de hemoglobina glicosilada (Hb1Ac) > 6,5% y diagnóstico de GD, con sintomatología clínica compatible y VG retrasado. Se excluyeron pacientes embarazadas o en lactancia, con condiciones médicas o psiquiátricas descontroladas, con cirugía gastrointestinal (excepto apendicectomía) y uso de fármacos que alteren la motilidad gastrointestinal 1 mes antes del inicio del estudio. Los pacientes fueron aleatorizados a recibir comprimidos de levosulpirida 25 mg (Dislep® Ferrer) t.p.d o cinitaprida 1 mg (Rogastril®, Siegfried Rhein, S.A.) t.p.d vía oral, 20 minutos antes de las comidas durante 6 meses, usando el método de doble enmascaramiento.
La variable principal fue la puntuación total en el cuestionario de síntomas gastroparesis cardinal symptom index (GCSI)13 evaluada a los 6 meses de tratamiento. De forma complementaria a la puntuación total, también se evaluó el porcentaje de mejoría respecto a la visita basal: [(Puntuación inicio – puntuación 6 meses)/puntuación al inicio * 100].
El cuestionario GCSI consiste en nueve items extraídos del cuestionario Patient Assessment of Upper Gastrointestinal Disorders-Symptom Severity Index (PAGI-SYM)13 que están validados al español14 y que cubren los siguientes dominios semiológicos: nauseas/vómitos (3 ítems), llenura (4 ítems) e hinchazón (2 ítems) y se evaluó de acuerdo con lo descripto por Revicki y col.13 a los 1, 3 y 6 meses durante el tratamiento. Secundariamente se evaluaron los datos demográficos, Hb1Ac, parámetros analíticos y datos clínicos. La calidad de vida se midió mediante la escala Dyspepsia-Related Health Scale (DRHS) al inicio del estudio y a los 1, 3 y 6 meses durante el tratamiento. La DRHS consta de 19 ítems que cubren los siguientes dominios: sintomatología (9 ítems), intensidad del dolor (3 ítems), incapacidad por el dolor (3 ítems) y satisfacción con la salud (4 ítems). Todas las escalas fueron transformadas a una escala de 0 a 100, donde 0 indica el estado de calidad de vida menos favorable y 100 el estado más favorable.15
A todos los pacientes se les midió el tiempo de VG con comida marcada (sandwich de huevo y vaso de leche) marcado con 1 mCi 99Tc en condiciones basales y a los 6 meses de tratamiento. Esta variable se midió en una escala de 0 a 100, donde un valor de 100% indica contenido completo de 99Tc marcado en el estómago, mientras que un valor del 0% indica ausencia de marcador y por tanto un vaciado gástrico total.16
La adherencia al tratamiento se evaluó al tercer y sexto mes mediante el método de registro de medicación sobrante (RMS),17 considerándose como buena adherencia al tratamiento un cumplimiento de la medicación de entre un 80-100%; una adherencia media un cumplimiento de la medicación de entre un 60-80%, y una mala adherencia un cumplimiento de la medicación inferior al 60%. La seguridad se evaluó a los 1, 3 y 6 meses del inicio del estudio.18
Análisis estadístico
El tamaño de muestra está basado en la variable principal, definida como la puntuación total GCSI a los 6 meses de tratamiento. El análisis principal consistió en comparar la variable principal entre los brazos de tratamiento. La hipótesis alternativa asumió una menor puntuación total GCSI a los 6 meses en el brazo de levosulpirida que en el brazo cinitaprida, por lo que se consideró un contraste de hipótesis unilateral. De acuerdo con estudios previos,19 se consideró como clínicamente relevante una diferencia mayor de 0,5 (± 0,55) en la puntuación total GCSI. Se asumió una tasa de pérdida de pacientes del 10% a los 6 meses de seguimiento. Por lo que se predefinieron 17 pacientes por brazo (total de 34 pacientes) para asegurar una potencia del 80% con un nivel de significación del 5%.
Para las variables cuantitativas, se compararon las diferencias entre los 2 brazos de tratamiento mediante la prueba U de Mann-Whitney. Para evaluar las diferencias entre diferentes visitas se utilizó la prueba de Wilcoxon. También se estimaron las diferencias de medias entre los diferentes brazos o períodos de tratamiento, mediante los intervalos de confianza del 95% (IC95%) derivados de la distribución T. Se utilizó la D de Cohen20 para evaluar la magnitud de la diferencia de la puntuación total GCSI entre los dos brazos de tratamiento. Se calculó dividiendo la diferencia de medias de los grupos por la desviación estándar conjunta. Se consideró como significativo un p-valor ≤ 0,05. De acuerdo al tamaño de muestra, los contrastes de hipótesis fueron de tipo unilateral para el análisis principal, y bilateral para los secundarios.
Resultados
Este estudio fue aprobado por el Comité Institucional de Investigación Biomédica en Humanos del Instituto Nacional de Ciencias Médicas y Nutrición “Salvador Zubirán” y se desarrolló siguiendo las normas de buena práctica clínica entre marzo de 2011 y diciembre de 2014.
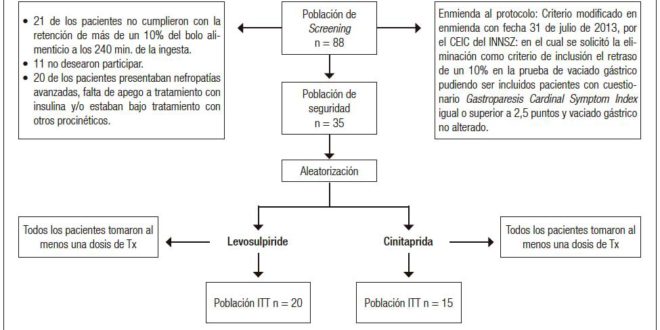
Se incluyeron 35 pacientes, 20 en el grupo de levosulpirida y 15 en el de cinitaprida. El flujo de pacientes se puede observar en la Figura 1.
Un 24% de los pacientes evaluados no pudieron participar en el estudio por no presentar retraso en el VG. Puesto que ello dificultaba en gran medida la inclusión de pacientes, se enmendó el protocolo de forma que pudiesen participar en el estudio pacientes que cumplían los requisitos clínicos de GD aunque no tuviesen el VG retrasado.
Las características basales eran similares entre grupos y la mayoría (60%) de los pacientes incluidos tenían obesidad y diabetes de larga duración (> 15 años) (Tabla 1).
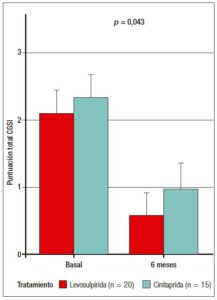
Al final del estudio (6 meses) la diferencia en la media de la puntuación global del cuestionario GCSI fue significativamente menor en el grupo tratado con levosulpirida (0,52 puntos; IC95%: 0,08-0,96; p = 0,043) (Figura 2, Tabla 2).
Figura 1. Flujo de pacientes en el estudio aleatorizado doblemente enmascarado para comparar la eficacia y la seguridad de levosulpirida vs. cinitaprida (Estudio LEVEL).
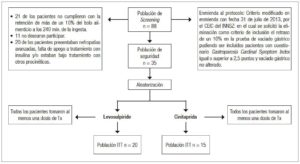
Tabla 1. Datos demográficos de los pacientes incluidos en el estudio.
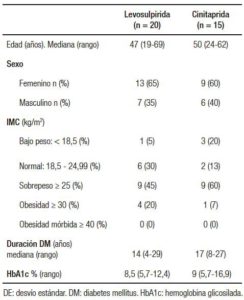
Tabla 2. Valores de la puntuación del cuestionario GCSI al inicio y al final del estudio. La variable principal de comparación fue la diferencia entre tratamientos en la puntuación del GCSI tras 6 meses de tratamiento.
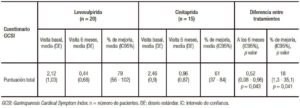
Figura 2. Puntuación del cuestionario GCSI en el momento basal y tras 6 meses de tratamiento con levosulpirida o cinitaprida. La variable de comparación fue la diferencia en la puntuación media global del GCSI a los 6 meses favorable a levosulpirida en 0,52 puntos (IC95%: 0,08-0,96; p = 0,043).
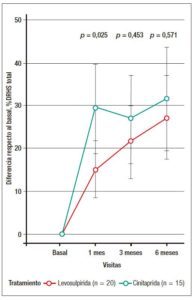
La puntuación en el cuestionario GCSI disminuyó con ambos tratamientos. La reducción de los síntomas fue progresiva en el grupo de levosulpirida, alcanzando un 79% de reducción en el puntaje de síntomas respecto de la visita basal (basal: 2,12 ± 1,03; final: 0,44 ± 0,68) mientras que en el grupo que recibió cinitaprida, la disminución de síntomas fue máxima al mes del tratamiento (reducción del 76%), observándose un incremento en el puntaje sintomático al final del tratamiento que revirtió hasta un 61% de mejoría (basal: 2,46 ± 0,9; final: 0,96 ± 0,87) (Figura 3A y 3B). El porcentaje de mejoría en la puntuación del GCSI al final del estudio también fue significativamente mayor en los pacientes tratados con levosulpirida (Figura 4).
En los pacientes tratados con levosulpirida, todos los ítems individuales del cuestionario GCSI mejoraron significativamente en relación al momento basal. En el grupo de cinitaprida el único ítem que no se redujo significativamente desde el momento basal fue la pérdida de apetito.
Figura 3. Evolución de la media de puntuación del cuestionario GCSI a lo largo de las visitas del estudio. 3A. Valores absolutos de la puntuación global del cuestionario GCSI y comparaciones por cada visita. 3B. Porcentaje de mejoría respecto del nivel basal. Ambos análisis muestran resultados equivalentes por lo que se descarta que la superioridad de levosulpirida sobre el brazo de cinitaprida fuese debido a las diferencias en la puntuación GCSI al inicio del estudio.
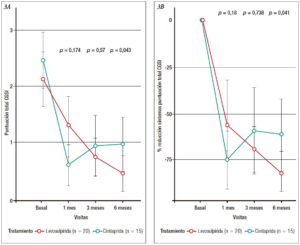
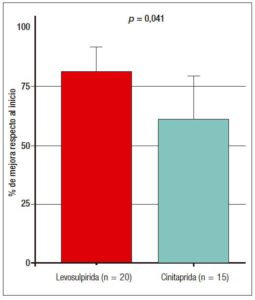
Figura 4. Comparación del porcentaje de mejoría entre tratamientos. Tras 6 meses de tratamiento los pacientes tratados con levosulpirida mostraron una media de porcentaje de mejoría en la sintomatología de GD evaluada con el GCSI un 18% mayor (IC95%: 1,3 – 35,1%; p = 0,041) que los tratados con cinitaprida.
En general, levosulpirida y cinitaprida mejoraron la calidad de vida evaluada con la escala DRHS al final del tratamiento (puntuación media del DRHS en el grupo de levosulpirida: basal: 54,44 ± 22,02; final: 81,76 ± 10,77; 27% de mejoría). La puntuación media del DRHS en el grupo de cinitaprida fue basal: 43,64 ± 17,46; final: 75,25 ± 11,89; 32% de mejoría. A pesar de que no se hallaron diferencias estadísticamente significativas entre ambos tratamientos, el puntaje DRHS mostró una mejoría progresiva y sostenida con levosulpirida hasta el final del tratamiento, en contraste con cinitaprida, con la cual el puntaje de calidad de vida no aumentó ulteriormente después del primer mes de tratamiento (Figura 5).
La disminución global en el porcentaje de retención gástrica entre la visita inicial y final (6 meses) fue significativamente mayor para el grupo levosulpirida ya a partir de los 60 minutos del inicio de la prueba. La comparación de la diferencia hallada entre los resultados de la prueba basal y final (a los 6 meses) entre ambos tratamientos muestra que levosulpirida mejora significativamente el vaciado gástrico, mientras que cinitaprida no parece influir sobre esta variable (levosulpirida -4% vs cinitaprida + 1,97%; p = 0,014) (Figura 5). No hubo diferencias en la Hb1Ac entre los pacientes tratados con levosulpirida o cinitaprida. Para ambos tratamientos el grado de apego fue elevado, superando el 80% (levosulpirida 94% y cinitaprida 97%).
Figura 5. Evolución del porcentaje de mejora en la calidad de vida respecto del momento basal. Ambos tratamientos produjeron una mejora significativa desde el momento basal en todos los parámetros del DRHS, excepto en la subescala de satisfacción con la salud. No hubo diferencias significativas al final del tratamiento. DRHS: Dispepsia-Related Health Scale.
Durante el estudio, 7 pacientes (35%) en el grupo de levosulpirida y 3 (20%) en el grupo de cinitaprida presentaron acontecimientos adversos de intensidad mayoritariamente leve y moderada, dos de los cuales, uno en el grupo de levosulpirida y otro en el de cinitaprida, estuvieron relacionados con la medicación en estudio.
En el caso de levosulpirida un paciente presentó un acontecimiento adverso severo por el hallazgo de un microadenoma hipofisiario silente manifestado por ginecomastia, disfunción eréctil e hiperprolactinemia que requirió suspensión de la levosulpirida y tratamiento médico con cabergolina 0,5 mg dos veces por semana hasta que revirtió la sintomatología luego de tres años de tratamiento. No requirió intervención quirúrgica. En el grupo de cinitaprida un paciente presentó aumento de la irritabilidad que se consideró relacionado con la medicación del estudio. El resto de los acontecimientos adversos se describen en la Tabla 3. Cinco pacientes abandonaron el estudio por acontecimientos adversos. Durante el estudio no se produjo ningún caso de muerte o acontecimiento adverso grave.
Figura 6. Diferencias en la velocidad de vaciado gástrico entre levosulpirida y cinitaprida. Un valor de 100% indica contenido completo de 99Tc marcado en el estómago, mientras que un valor del 0% indica ausencia de marcador y por tanto un vaciado gástrico total. A partir de los 60 minutos del inicio de la prueba ya se evidencian diferencias significativas a favor de levosulpirida entre ambos grupos de tratamiento y persiste hasta los 6 meses.
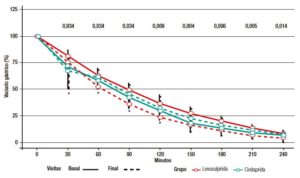
Tabla 3. Acontecimientos adversos (AA) notificados durante el estudio.

Discusión
Este es el primer ensayo clínico piloto que ha comparado directamente la eficacia y seguridad de dos procinéticos, levosulpirida y cinitaprida, en pacientes con GD. Levosulpirida, perteneciente a la clase farmacológica de las benzaminas sustituidas con actividad antidopaminérgica por acción inhibitoria selectiva sobre los receptores D221 y agonista de los receptores de 5-HT4 localizados en las terminaciones presinápticas de las neuronas colinérgicas del plexo mientérico,22 ha mostrado en estudios previos superioridad en el incremento del vaciado gástrico comparado con placebo10 y cisaprida,11 sobre el control de la glucemia23 o sobre la sintomatología de la gastroparesia en pacientes diabéticos.9, 23 Cinitaprida también es un agonista selectivo de los receptores serotoniérgicos 5-HT4 y antagonista de los receptores dopaminérgicos D2 y ha mostrado mejorar la sintomatología frente a placebo en pacientes con dispepsia funcional, pero su eficacia no ha sido nunca estudiada previamente en pacientes con GD.24, 25
Los resultados del presente estudio nos muestran que levosulpirida mejora significativamente la sintomatología de los pacientes con GD tras 6 meses de tratamiento cuando se compara con cinitaprida. A pesar de que se trata de un estudio piloto, es llamativo que cinitaprida reduce durante el primer mes de tratamiento la puntuación de la mayoría de ítems del cuestionario GCSI, pero posteriormente revierte su efecto mientras que, en el caso de levosulpirida, se aprecia una mejoría sintomática constante y sostenida hasta el final del estudio. La mejoría clínica alcanzada por levosulpirida fue un 18% superior a la alcanzada por cinitaprida (levosulpirida 79% vs. cinitaprida 61%; p = 0,041) tras 6 meses de tratamiento.
En estudios previos,26 en condiciones de práctica clínica habitual, se observaron tamaños del efecto de 0,52 (D de Cohen)20 tras un mes de tratamiento. En nuestro estudio, el tamaño del efecto de levosulpirida respecto de cinitaprida fue de 0,68 (D de Cohen), lo que sugiere que estas diferencias entre tratamientos son clínicamente relevantes. Levosulpirida ya había mostrado eficacia en la disminución de síntomas dispépticos durante 6 meses en un estudio comparativo con placebo en pacientes con GD.23 La mayoría de estudios comparativos con placebo realizados con los distintos procinéticos9, 27 o las comparaciones entre sí,28, 29 han tenido mayormente una duración de 4 semanas.30 Por ello, esta persistencia del efecto gastrocinético a largo plazo parece ser una característica peculiar de levosulpirida, ya que otros procinéticos como metoclopramida o domperidona pierden dicho efecto con el tiempo30-32 y nuestros resultados muestran que esto último también ocurre con el tratamiento con cinitaprida.
En una revisión sistemática llevada a cabo por Janssen y col.33 en la que se estudió la correlación entre la mejoría sintomática y la velocidad de VG se concluye que, dada la falta de correlación entre ambos parámetros, no parece necesario realizar la prueba de vaciado gástrico cuando existe sintomatología de GD evidente previamente a la prescripción de un procinético y, por supuesto, tampoco es necesario realizar pruebas de vaciado gástrico de control tras el tratamiento.33 De hecho, en nuestro estudio, un 24% de los pacientes evaluados no pudieron participar por no presentar prueba de vaciado gástrico alterada, a pesar de presentar clara sintomatología clínica de GD. Levosulpirida ya había mostrado en un estudio previo de 6 meses de duración que el vaciado gástrico se aceleró significativamente frente al tratamiento con placebo,23 mientras que en el caso de cinitaprida un único estudio que evaluó el efecto sobre el vaciado gástrico en pacientes con dispepsia funcional no mostró diferencias significativas respecto de placebo a las 4 semanas.34
En relación a la seguridad de ambos tratamientos, únicamente dos pacientes, uno en el grupo de levosulpirida y otro en el de cinitaprida, presentaron acontecimientos adversos relacionados con la medicación del estudio. Un paciente presentó hiperprolactinemia con disfunción eréctil y ginecomastia. Los fármacos que bloquean el sistema dopaminérgico central, como los antipsicóticos (fenotiacinas, butirofenonas, haloperidol), antieméticos (metoclopramida, domperidona) y algunos antidepresivos (metildopa, reserpina) han sido descriptos como causa importante de hiperprolactinemia,35, 36 ya que son capaces de evidenciar la presencia de un adenoma hipofisiario. Los adenomas pituitarios constituyen el trastorno hipofisiario más frecuente.37 Son neoplasias benignas que constituyen un 10-15% de todas las masas intracraneales y su prevalencia promedio es de 16,7% en autopsias y estudios radiológicos. Esta alta prevalencia hace pensar que entre un 10-20% de estos tumores no tienen traducción clínica, sino que se descubren por hallazgo casuales o durante la autopsia.38, 39 Este era el caso que se descubrió de forma casual durante el estudio. Al paciente se le diagnosticó un microadenoma hipofisario por RMN, fue retirado del estudio y tratado médicamente con cabergolina 0,5 mg/día durante 3 años hasta la normalización de la hiperprolactinemia, sin requerir tratamiento quirúrgico. Por ello, todos los fármacos que bloquean el sistema dopaminérgico central son tributarios de provocar este tipo de sintomatología en pacientes con adenomas silentes.
En la literatura, los estudios realizados para evaluar la eficacia de diversos procinéticos en pacientes con GD tanto vs. placebo9, 27, 40 como estudios de comparación28 han tenido un seguimiento de 4 semanas y un tamaño de muestra que ha oscilado de 19 a 93 pacientes. El estudio previo que evaluó la eficacia y seguridad de levosulpirida frente a placebo incluyó 40 pacientes que fueron seguidos durante 6 meses.9 Debido a la falta de datos previos sobre la comparación entre levosulpirida y cinitaprida se diseñó este estudio como piloto, por lo que los datos obtenidos tienen un carácter exploratorio y deberían ser confirmados en posteriores estudios con un mayor tamaño muestral. Los resultados obtenidos también recomendarían la realización de futuros estudios con una mayor duración de seguimiento.
Conclusiones
En este primer estudio piloto aleatorizado, doblemente enmascarado, se demuestra que levosulpirida y cinitaprida mejoran significativamente los síntomas y la velocidad de vaciado gástrico de los pacientes con GD. Levosulpirida mejora progresiva y sostenidamente estos parámetros a lo largo de 6 meses de tratamiento. Después de un mes de tratamiento con cinitaprida, el efecto sobre síntomas y calidad de vida permanece estable, sin mejoría de estos parámetros a los 3 y 6 meses de tratamiento. Al final del tratamiento, levosulpirida muestra una mejora significativamente superior en la sintomatología clínica medida por GCSI respecto de cinitaprida. Levosulpirida es un procinético eficaz y seguro para mejorar los síntomas y la calidad vida en pacientes con GD que requieren tratamiento a largo plazo.
Sostén financiero. Este estudio ha sido realizado gracias al patrocinio de Ferrer, Barcelona, España.
Referencias
- Camilleri M, Bharucha AE, Farrugia G. Epidemiology, mechanisms, and manage- ment of diabetic gastroparesis. Clin Gastroenterol Hepatol 2011; 9: 5-12.
- Intagliata N, Koch KL. Gastroparesis in type 2 diabetes mellitus: prevalence, etiology, diagnosis, and treatment. Curr Gastroenterol Rep 2007; 9: 270-279.
- Jung HK, Choung RS, Locke GR 3rd, Schleck CD, Zinsmeister AR, Szarka LA, Mullan B, Talley NJ. The incidence, prevalence and outcomes of patients with gastroparesis in Olmsted County, Minnesota, from 1996 to 2006. Gastroenterology 2009; 136: 1225-1233.
- Horowitz M, O’Donovan D, Jones KL, Feinle C, Rayner CK, Samsom M. Gastric emptying in diabetes: clinical significance and treatment. Diabet Med 2002; 19: 177-194.
- Choung RS, Locke GR 3rd, Schleck CD, Zinsmeister AR, Melton LJ 3rd, Talley NJ. Risk of gastroparesis in subjects with type 1 and 2 diabetes in the general population. Am J Gastroenterol 2012; 107: 82-88.
- The effect of intensive diabetes therapy on measures of autonomic nervous system function in the Diabetes Control and Complications Trial (DCCT). Diabetologia 1998; 41: 416-423.
- Wang YR, Fisher RS, Parkman HP. Gastroparesis-related hospitalizations in the United States: trends, characteristics, and outcomes, 1995-2004. Am J Gastroenterol 2008; 103: 313-322.
- Acosta A, Camilleri M. Prokinetics in gastroparesis. Gastroenterol Clin North Am 2015; 44: 97-111.
- Mansi C, Savarino V, Vigneri S, Perilli D, Melga P, Sciaba L, De Martini D, Mela GS. Gastrokinetic effects of Levosulpiride in dyspeptic patients with diabetic gastroparesis. Am J Gastroenterol 1995; 90: 1989-1993.
- Arienti V, Corazza GR, Sorge M, Boriani L, Ugenti F, Biagi F, Maconi G, Sottili S, Van Thiel DH, Gasbarrini G. The effects of Levosulpirida on gastric and gall-bladder emptying in functional dyspepsia. Aliment Pharmacol Ther 1994; 8: 631-638.
- Mansi C, Borro P, Giacomini M, Biagini R, Mele MR, Pandolfo N, Savarino, V. Comparative effects of Levosulpirida and cisapride on gastric emptying and symptoms in patients with functional dyspepsia and gastroparesis. Aliment Pharmacol Ther 2000; 14: 561-569.
- American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care 2011; 34: S62-S69.
- Revicki DA, Rentz AM, Dubois D, Kahrilas P, Stanghellini V, Talley NJ, Tack J. Gastroparesis Cardinal Symptom Index. Qual Life Res 2004; 13: 833-844.
- Tobón S, Vinaccia S, Sandín B. Estudio preliminar de la validez y confiabilidad del cuestionario PAGI-SYM para determinar síntomas de dispepsia acorde con la calidad de vida. Rev Col Gastroenterol 2006; 21: 268-274.
- Ruiz M, Villasante F, León F, Gonzales V, Gonzales C. Cuestionario sobre calidad de vida asociada a dispepsia. Adaptación española y validación del cuestionario Dyspepsia Related Health Scale. Medicina Clínica 2001; 17: 567-573.
- Szarka LA, Camilleri M. Gastric emptying. Clin Gastroenterol Hepatol 2009; 7: 823-827.
- Codina C, Martínez M, Tuset M, del Cacho E, Martín MT, Miró JM, Mallolas J, de Lazzari E, García F, Martínez E, Gatell JM, Ribas J. [Comparison of three methods to calculate adherence in patients receiving antiretroviral treatment]. Enferm Infecc Microbiol Clin 2002; 20: 484-490.
- Karch FE, Lasagna L. Towards the operational identification of adverse drug reactions. Clin Pharmacol Ther 1977; 21: 247-254.
- Revicki DA, Camilleri M, Kuo B, Norton NJ, Murray L, Palsgrove A, Parkman HP. Development and content validity of a gastroparesis cardinal symptom index daily diary. Aliment Pharmacol Ther 2009; 30: 670-680.
- Cohen J. Statistical Power Analysis for the Behavioural Sciences. Hillsdale, NJ: Lawrence Erlbaum Associates (Eds.). New York, 2nd edition 1988.
- Spano PF. Stereospecific of sulpiride on striatal and nonstriatal dopamine receptor. En: Spano PF, Trabucchi M, Corsini GU (Eds.), Sulpiride and Other Benzamides. New York, Raven Press 1979: 3-9.
- Tonini M, De Ponti F, Di Nucci A, Crema F. Review article: cardiac adverse effects of gastrointestinal prokinetics. Aliment Pharmacol Ther 1999; 13: 1585-1591.
- Melga P, Mansi C, Ciuchi E, Giusti R, Sciaba L, Prando R. Chronic administration of Levosulpiride and glycemic control in IDDM patients with gastroparesis. Diabetes Care 1997; 20: 55- 58.
- Fernández AG, Roberts DJ. Cinitapride hydrogen tartrate. Drugs of the Future 1991; 16: 885-892.
- Robert M, Salvà M, Segarra R, Pavesi M, Esbri R, Roberts D, Golor G. The prokinetic cinitapride has no clinically relevant pharmacokinetic interaction and effect on QT during coadministration with ketoconazole. Drug Metab Dispos 2007; 35: 1149- 1156.
- Revicki DA, Camilleri M, Kuo B, Szarka LA, McCormack J, Parkman HP. Evaluating symptom outcomes in gastroparesis clinical trials: validity and responsiveness of the Gastroparesis Cardinal Symptom Index-Daily Diary (GCSI-DD). Neurogastroenterol Motil 2012; 24: 456-463.
- Perkel MS, Moore C, Hersh T, Davidson ED. Metoclopramide therapy in patients with delayed gastric emptying: a randomized, double-blind study. Dig Dis Sci 1979; 24: 662-666.
- Patterson D, Abell T, Rothstein R, Koch K, Barnett J. A double-blind multicenter comparison of domperidone and metoclopramide in the treatment of diabetic patients with symptoms of gastroparesis. Am J Gastroenterol 1999; 94: 1230-1234.
- Dilengite MA, Loria P, Digrisolo A, Crulli N. Effeto de L-sulpiride e metoclopraminde sulla cinetica colecistitca nel diabético. Argomenti Gastroenterol Clin 1993; 6: 165-171.
- Lata PF, Pigarelli DL. Chronic metoclopramide therapy for diabetic gastroparesis. Ann Pharmacother 2003; 37: 122-126.
- Schade RR, Dugas MC, Lhotsky DM, Gavaler JS, Van Thiel DH. Effect of metoclopramide on gastric liquid emptying in patients with diabetic gastroparesis. Dig Dis Sci 1985; 30: 10-15.
- Horowitz M, Harding PE, Chatterton BE, Collins PJ, Shearman DJ. Acute and chronic effects of domperidone on gastric emptying in diabetic autonomic neuropathy. Dig Dis Sci 1985; 30: 1-9.
- Janssen P, Harris MS, Jones M, Masaoka T, Farré R, Törnblom H, Van Oudenhove L, Simrén M, Tack J. The relation between symptom improvement and gastric emptying in the treatment of diabetic and idiopathic gastroparesis. Am J Gastroenterol 2013; 108: 1382-1391.
- Portincasa P, Mearin F, Robert M, Plazas MJ, Mas M, Heras J. Efficacy and tolerability of cinitapride in the treatment of functional dyspepsia and delayed gastric emptying. Gastroenterol Hepatol 2009; 32: 669-676. Spanish. Erratum in: Gastroenterol Hepatol 2010; 33: 345.
- Verhelst J, Abs R. Hyperprolactinemia. Pathophysiology and Management. Treat Endocrinol 2003; 2: 23-32.
- La Torre D, Falorni A. Pharmacological causes of hyperprolactinemia. Ther Clin Risk Management 2007; 3: 929-951.
- Famini P, Maya MM, Melmed S. Pituitary magnetic resonance imaging for sellar and parasellar masses: ten-year experience in 2598 patients. J Clin Endocrinol Metab 2011; 96: 1633-1641.
- Hall WA, Luciano MG, Doppman JL, Patronas NJ, Oldfield EH. Pituitary magnetic resonance imaging in normal human volunteers: occult adenomas in the general population. Ann Intern Med 1994; 120: 817-820.
- Ezzat S, Asa SL, Couldwell WT, Barr CE, Dodge WE, Vance ML, McCutcheon IE. The prevalence of pituitary adenomas: a systematic review. Cancer 2004; 101: 613-619.
- Snape WJ Jr, Battle WM, Schwartz SS, Braunstein SN, Goldstein HA, Alavi A. Metoclopramide to treat gastroparesis due to diabetes mellitus: a double-blind, controlled trial. Ann Intern Med 1982; 96: 444-446.
- Talley NJ, Young L, Bytzer P, Hammer J, Leemon M, Jones M, Horowitz M. Impact of chronic gastrointestinal symptoms in diabetes mellitus on health-related quality of life. Am J Gastroenterol 2001; 96: 71-76.
Correspondencia: Miguel A Valdovinos
Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán, Vasco de Quiroga 15, Sección XVI, Tlalpan. Ciudad de México 14000, México – Tel: 5255 55733418
Correo electrónico: miguelvaldovinosd@gmail.com
Acta Gastroenterol Latinoam 2017;47(4): 277-287
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE