Andrés E Ruf,1 Nora G Cejas,2 Eduardo de Santibañez,3 Federico G Villamil,1, 4 en representación de la Sociedad Argentina de Trasplantes
1 Unidad de Trasplante Hepático del Hospital Británico de Buenos Aires. Ciudad Autónoma de Buenos Aires, Argentina.
2 Unidad de Trasplante Hepático del Hospital Cosme Argerich, Buenos Aires. Ciudad Autónoma de Buenos Aires, Argentina.
3 Unidad de Trasplante Hepático del Hospital Italiano de Buenos Aires. Ciudad Autónoma de Buenos Aires, Argentina.
4 Unidad de Trasplante Hepático del Hospital El Cruce de Florencio Varela. Buenos Aires, Argentina.
Acta Gastroenterol Latinoam 2016;46: 230-236
Recibido: 01/03/2016 / Aprobado: 08/08/2016 / Publicado en www.actagastro.org el 03/10/2016
Colaboradores
Oscar Andriani, Horacio Aziz, Laura Barcán, Liliana Bisignano, Gustavo Braslavsky, Fernando Cairo, Paola Casciato, Miguel Ciardullo, Luis Colombato, Valeria Descalzi, Eduardo Fassio, Sebastián Ferretti, Adrián Gadano, Omar Galdame, Teresa García, Sergio Gianassi, Gabriel Gondolesi, Rosana Jordán, Shigeru Kozima, Pablo Maidana, Alfredo Martínez, Marta Martinuzzo, Francisco Mattera, Lucas McCormack, Claudia Nagel, Luis Podestá, Emilio Quiñonez, Rodolfo Quirós, Marcelo Silva, Juan Carlos Spina, Rubén Terg, Rogelio Traverso, Alejandra Villamil, Fernanda Zingale.
Resumen
Desde la adopción del modelo MELD (Model for End-Stage Liver Disease) para la distribución de órganos en el trasplante hepático en julio del año 2005, Argentina no ha introducido modificaciones sustanciales a la normativa que rige la procuración y distribución hepática. En el contexto de los recientes avances en las diferentes áreas relacionadas con el trasplante hepático, la Sociedad Argentina de Trasplantes patrocinó el Primer Consenso Argentino de Trasplante Hepático cuyas conclusiones se resumen en este artículo. Seis grupos de trabajo integrados por hepatólogos, cirujanos, infectólogos, radiólogos, bioquímicos y representantes del Organismo Nacional de Procuración y Trasplante (INCUCAI) abordaron la problemática de la selección de los donantes hepáticos, la transmisión de infecciones bacterianas por el donante, las situaciones especiales no contempladas (ascitis y encefalopatía hepática), la optimización del diagnóstico radiológico del hepatocarcinoma y la reproducibilidad del MELD. Las conclusiones del consenso fueron elevadas al Organismo Nacional de Procuración y Trasplante para modificar la normativa vigente.
Palabras claves. Donante cadavérico, situaciones especiales del MELD, hepatocarcinoma.
Argentine Consensus on Liver Transplantation
Summary
Ever since the adoption of the MELD score for liver allocation in July 2005 in Argentina, there have been no further modifications in liver procurement and allocation policies. Due to the recent innovations in different liver transplant-related areas, the Argentinean Transplant Society sponsored the First Argentinean Consensus on Liver Transplantation. The Consensus was integrated by six different working groups of hepatologists, transplant surgeons, infectious disease specialists, radiologists, biochemistry specialists and experts from the National Procurement and Transplantation Office (INCUCAI) who dealt with the problematic of liver donor selection, donor transmitted bacterial infection, MELD exceptions (ascites and encephalopathy), novel imaging diagnostic criteria for hepatocellular carcinoma and MELD reproducibility. Consensus final statements have been submitted to the National Procurement and Transplantation Office for consideration and modification of current regulations.
Key words. Deceased donor, MELD exceptions, hepatocellular carcinoma.
Abreviaturas
INCUCAI: Instituto Nacional Central Único Coordinador de Ablación e Implante.
TH: trasplante hepático.
DRI: donor risk index.
MELD: Model for End-Stage Liver Disease.
PELD: Pediatric End-Stage Liver Disease.
HCC: hepatocarcinoma.
PaO2: presión parcial de oxígeno en sangre arterial.
EPS: encefalopatía portosistémica.
Na: sodio sérico.
MELD-Na: MELD-Sodio.
TC: tomografía computada.
RM: resonancia magnética.
LI-RADS: Liver Imaging Reporting and Data System.
RIN: Razón Internacional Normatizada.
ISO: International Organization for Standardization.
CAP: College of American Pathologists.
OAA: Organismo Argentino de Acreditación.
ISI: International Sensitivity Index.
El 1 de diciembre de 2013, en el marco del XII Congreso Argentino de Trasplante y del XXII Congreso Latinoamericano y del Caribe de Trasplante, se realizó el Primer Consenso Argentino de Trasplante Hepático. Se constituyeron seis grupos de trabajo, integrados por expertos en cada uno de los temas a desarrollar. Durante la mañana los coordinadores presentaron las propuestas de trabajo y un breve resumen sobre lo publicado de cada tema. Posteriormente se pasó a una reunión cerrada para finalizar la redacción de las propuestas. Finalmente, en la sesión vespertina, los coordinadores de cada grupo presentaron las conclusiones que fueron discutidas en forma abierta con los asistentes al Consenso para generar las conclusiones que se resumen en este manuscrito y que fueron elevadas a la Dirección Científico Técnica del Instituto Nacional Central Único Coordinador de Ablación e Implante (INCUCAI) para solicitar las modificaciones a la norma de distribución hepática vigente.
-
Selección de los donantes hepáticos
La mayor limitación para el acceso al trasplante hepático (TH) en todo el mundo es la falta de un número adecuado de donantes. Datos del Registro Nacional de Trasplante Hepático muestran que durante el período 2005-2011 la aplicabilidad del TH en Argentina (número de trasplantes/ número de pacientes en lista de espera) fue del 43% y que la remoción de la lista de espera (por muerte o enfermedad avanzada) fue del 28%. El uso de donantes con criterios extendidos, también llamados donantes marginales, aumenta la aplicabilidad del TH pero acarrea un mayor riesgo de fallo primario del injerto. Los criterios usados para definir a un donante como marginal han cambiado a lo largo del tiempo. En Estados Unidos, y en base a un trabajo que incluyó 20.023 donantes, se desarrolló un índice de riesgo del donante (DRI o donor risk index en inglés) cuya fórmula contiene las variables que fueron predictoras independientes de la disfunción postoperatoria del injerto hepático. Un estudio reciente ha demostrado que en Argentina el hígado fue obtenido en solo la mitad de los operativos de trasplante en los que se ablacionó al menos un órgano vascularizado, algo difícil de explicar. Los beneficios del DRI no pueden extrapolarse directamente a nuestro país debido a que su fórmula incluye algunos parámetros como la raza que no son aplicables. Sin embargo, el análisis de las variables más representativas del DRI (edad, tipo de injerto y causa de muerte) en los donantes no aceptados de nuestro país sugiere que en muchos casos el rechazo del hígado fue inadecuado. Históricamente, se sabe que en muchos donantes con características clínicas y bioquímicas “desfavorables” (criterios extendidos) el hígado presenta un aspecto macroscópico normal en la cirugía de la ablación. En este caso, el buen juicio y experiencia del cirujano permite su aceptación y posterior implante con alta chance de éxito. Por lo tanto, ningún hígado debería ser rechazado por vía telefónica sin “ir a verlo”. El mayor problema para implementar esta estrategia en Argentina son las largas distancias que deben recorrerse en muchos casos para que un cirujano con experiencia pueda examinar el hígado en forma directa. Debido a esto, el traslado por vía aérea del equipo de ablación para evaluar órganos en zonas alejadas del centro de trasplante y con alta chance de ser rechazados no parece ser costo-efectivo.
Propuesta 1.1: Distribución hepática
– Solicitar a todos los Organismos Provinciales de Procuración distribuir el hígado en todos los operativos sin excepción alguna.
– Cumplir con los tiempos estipulados, no solo para la aceptación o rechazo del órgano sino también para la ablación, especialmente en el caso de donantes multiorgánicos.
Propuesta 1.2: Ablación regional
– Implementar un sistema de ablación regional comenzando en las provincias con mayor volumen de procuración y que además cuenten con cirujanos que acrediten formación y experiencia previa en TH.
– Los resultados de esta política de ablación regional deberán ser evaluados al año de su implementación.
Propuesta 1.3: Índice de riesgo del donante
– Iniciar en forma prospectiva la recolección de variables del donante que permitan desarrollar un índice propio para Argentina.
-
Transmisión de infecciones bacterianas por el donante
Actualmente, y en todo el mundo, existe una desproporción creciente y progresiva entre el número de candidatos en lista de espera y el número de trasplantes realizados. Este hecho ha llevado a la necesidad de maximizar la utilización de los donantes cadavéricos disponibles para aumentar así la aplicabilidad del TH. El mayor riesgo de usar donantes marginales o con criterios extendidos es el incremento de la incidencia de fallo primario del injerto, una complicación grave pero infrecuente en nuestro país. Es importante tener en cuenta que para muchos pacientes que tienen escasa chance de acceder a un órgano con el sistema MELD (Model for End-Stage Liver Disease), un “mal donante” puede ser su mejor o única opción. La contribución de las infecciones bacterianas del donante a la marginalidad del injerto y el impacto de utilizar hígados obtenidos de donantes bacteriémicos en los resultados del TH son aún motivo de controversia. En forma similar, la eficacia de la transmisión de gérmenes virulentos o multirresistentes del donante al receptor y la necesidad de adecuar el tratamiento antibiótico a los rescates bacteriológicos del donante no han sido investigadas en estudios controlados.
Durante el consenso se discutieron diversos aspectos vinculados a la bacteriología de los donantes cadavéricos de los cuales los más importantes fueron evaluar la necesidad de: 1) Contraindicar la ablación por infecciones bacterianas severas del donante, 2) Obtener sistemáticamente hemocultivos del donante y cultivos de la solución de transporte del órgano, y 3) Adaptar la antibioticoterapia (tipo y duración) a los rescates bacteriológicos del donante o de la solución de transporte.
Propuesta 2.1: Transmisión de infecciones bacterianas por el donante
Al no obtenerse consenso, este documento no incluye conclusiones o recomendaciones sobre el tema.
-
Situaciones especiales no contempladas
En Argentina el sistema MELD/PELD (Pediatric End- Stage Liver Disease) contempla la posibilidad de otorgar puntos suplementarios en situaciones especiales en las cuales el valor real (calculado) del MELD no refleja el riesgo de muerte o de ser removido de la lista de espera por progresión de la enfermedad. Las situaciones contempladas actualmente por la norma, para los pacientes adultos, son el hepatocarcinoma (HCC) dentro de los criterios de Milán, la polineuropatía amiloidótica familiar con disautonomía y el síndrome hepatopulmonar con hipoxemia severa (PaO2< 60 mmHg). Fuera de estas tres situaciones contempladas y regladas, todo equipo de TH puede solicitar una “vía de excepción” para situaciones especiales no incluidas en la norma toda vez que se considere que el valor de MELD no se condice con el riesgo de muerte o de salida de la lista. Según datos del Registro Argentino de Trasplante Hepático, entre julio del 2005 y julio del 2012 se solicitaron 403 vías de excepción por situaciones especiales, lo que representa el 13% del total de candidatos en lista de espera durante dicho período (n=3083). De las 403 vías de excepción, 263 (65%) fueron situaciones especiales contempladas (HCC 226, síndrome hepatopulmonar 27 y polineuropatía amiloidótica familiar 10), y las 140 restantes (35%) situaciones especiales no contempladas en la norma. Los motivos más frecuentes para solicitar excepciones no contempladas fueron la ascitis refractaria (35 casos, 25%) y la encefalopatía portosistémica (EPS) severa (22 casos, 16%). Es importante destacar que el 59% de estas solicitudes fueron rechazadas (ascitis 66% y encefalopatía 73%) y que la mortalidad en lista de este grupo fue de 46% en comparación al 7% observado en los pacientes cuyas vías de excepción fueron aceptadas y al 26% de los candidatos sin solicitud de vías de excepción. En forma similar, la aplicabilidad del TH fue significativamente menor en los pacientes en los que se rechazaron las vías de excepción no contempladas (42%) que en aquellos en los que fueron aceptadas (88%). Estos datos sugieren, en primer lugar, que la percepción del equipo de trasplante sobre la severidad de la enfermedad (riesgo de muerte en lista) suele ser mejor que la ofrecida por el score de MELD. En segundo lugar, estos hallazgos nos obligan a contemplar la inclusión en la norma vigente de situaciones especiales adicionales a las que deberían otorgarse puntos suplementarios de MELD para favorecer un acceso más rápido al TH.
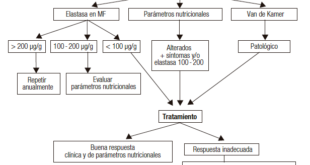
3.1 Ascitis y sus complicaciones
La ascitis es la complicación más frecuente de la cirrosis y se asocia a una elevada mortalidad, independientemente del valor del MELD. No es de extrañar entonces que en el Registro Argentino de Trasplante Hepático la ascitis refractaria fuera el motivo más frecuente de solicitud de vías de excepción para situaciones especiales no contempladas. El rechazo de la vía de excepción por ascitis en el 66% de los casos resultó en una elevada e inaceptable mortalidad en lista de espera (46%). El diseño e implementación de un score cuantitativo aplicable a la generalidad de los pacientes con ascitis es difícil debido a que muchos de los parámetros pasibles de utilización son subjetivos, inespecíficos, no auditables o manipulables. Algunos ejemplos de ello son el número de paracentesis terapéuticas, el número de internaciones, la calidad de vida y el estado nutricional. Sin embargo, existen algunas variables objetivas como la hiponatremia, la peritonitis bacteriana espontánea y el síndrome hepatorrenal que pueden ser de utilidad para evaluar la severidad de la ascitis. Estas variables son además predictores del riesgo de muerte en pacientes con cirrosis y por lo tanto resulta atractivo utilizarlas para modificar o complementar el MELD, mejorando así su eficacia para establecer la urgencia del TH y para priorizar la adjudicación de los órganos. Numerosos estudios han demostrado en forma categórica que la incorporación del sodio sérico (Na) a la fórmula del MELD incrementa significativamente su eficacia para predecir el riesgo de muerte a los 90 días en pacientes con cirrosis avanzada. A partir de enero de 2016 el MELD-Na (MELD-Sodio) ha reemplazado al MELD para la adjudicación de los hígados obtenidos de donantes cadavéricos para TH en Estados Unidos.
Propuesta 3.1.1: Hiponatremia
– Reemplazar al MELD por el MELD-Nay. Aplicarlo a la totalidad de los pacientes con cirrosis en lista de espera según la fórmula: MELD-Na = MELD + 1,32 x (137-Na) – [0,033 x MELD*(137-Na)]. (Rango de Na: 125 a 137 mEq/L).
– El valor del sodio sérico para la renovación del MELD se solicitará a iguales intervalos que los demás componentes de la fórmula.
– El valor más bajo de Na para ingresar a la fórmula será fijado en 125 mEq/L para no priorizar en exceso a pacientes con hiponatremia severa.
Propuesta 3.1.2: Peritonitis bacteriana espontánea
– Priorizar en lista de espera a los pacientes que hayan presentado peritonitis bacteriana espontánea en los últimos 12 meses adicionando 2 puntos al score de MELD-Na con el primer episodio documentado y 1 punto adicional por cada episodio subsiguiente.
– Deberá enviarse la documentación respaldatoria del diagnóstico de peritonitis bacteriana espontánea acorde a los criterios aceptados internacionalmente.
Propuesta 3.1.3: Síndrome hepatorrenal
– Mantener el valor del MELD-Na al ingreso en lista o el valor más elevado hasta la realización del TH, independientemente de la respuesta a la terapia con vasoconstrictores como la terlipresina o noradrenalina.
– Deberá enviarse documentación respaldatoria del diagnóstico de síndrome hepatorrenal acorde a criterios aceptados internacionalmente.
3.2 Encefalopatía hepática
El desarrollo de EPS incrementa 4 veces el riesgo de muerte en pacientes con cirrosis hepática y puede afectar notablemente la calidad de vida. Al ser una variable subjetiva, resulta muy difícil incorporar la severidad de la EPS a la fórmula de los índices pronósticos cuantitativos. Al igual que con la ascitis refractaria, la mayoría de los pedidos de excepción por EPS (73%) fueron rechazados, lo que se asoció a una elevada mortalidad en lista de espera. Existen sin embargo una serie de parámetros que permiten identificar las formas más graves o invalidantes de EPS a las que se les debería otorgar prioridad para la adjudicación de los órganos, independientemente de la severidad de la insuficiencia hepatocelular o de la presencia de otras complicaciones mayores de la cirrosis. Un buen ejemplo es la degeneración hepatolenticular no Wilsoniana que es una forma degenerativa, grave e infrecuente de EPS que puede progresar hasta generar grados de lesión cerebral no completamente reversibles con el TH.
Propuesta 3.2.1: Encefalopatía hepática severa (Grado 3 y 4 de la clasificación de West Haven)
– Adjudicar 20 puntos de MELD-NA a los pacientes con EPS severa que, a pesar de recibir los tratamientos más efectivos disponibles (lactulosa y rifaximina), hayan presentado al menos uno de los siguientes: 1) un episodio con requerimiento de asistencia respiratoria mecánica; 2) dos episodios con requerimiento de internación, pero sin requerimiento de ARM, durante los 6 meses previos a la solicitud de la excepción; 3) Internación continua por más de 30 días debido a la EPS severa.
– A partir de los dos meses de otorgados los puntos suplementarios se adjudicará 1 punto adicional de MELD-Na por mes hasta que se realice el TH.
– Deberá enviarse documentación respaldatoria (epicrisis o resumen de ingreso hospitalario) sobre diversos aspectos de la EPS como internaciones, factores precipitantes, duración y detalles del tratamiento farmacológico utilizado.
Propuesta 3.2.2: Degeneración hepatolenticular no Wilsoniana
– Adjudicar 22 puntos de MELD-Na a los pacientes en los que el diagnóstico de esta forma grave de EPS sea bien fundamentado.
– A partir de los dos meses de otorgados los puntos suplementarios se adjudicará 1 punto adicional de MELD-Na por mes hasta que se realice el TH.
– Deberá enviarse documentación respaldatoria sobre esta forma infrecuente de EPS (lo más detallada posible) incluyendo imágenes del sistema nervioso central y material audiovisual que refleje las típicas anormalidades neurológicas que presentan estos pacientes como ser temblor, trastornos de la palabra y/o de la marcha.
-
Optimización del diagnóstico de hepatocarcinoma
Los candidatos a TH con cirrosis y HCC que cumplen los Criterios de Milán reciben actualmente un MELD suplementario de 22 puntos y luego un punto cada tres meses hasta el trasplante o hasta ser removidos de la lista de espera por muerte o progresión tumoral. Datos del Registro Argentino de Trasplante Hepático han demostrado que el HCC es el motivo más frecuente (86%) de solicitud de situaciones especiales contempladas. A diferencia de lo ocurrido con las situaciones especiales no contempladas, la solicitud de puntos suplementarios por HCC fue aceptada en el 92% de los casos. La mortalidad en lista de espera fue significativamente menor (7%) y la aplicabilidad del TH significativamente mayor (83%) en los candidatos con HCC y puntos suplementarios otorgados que en aquellos pacientes en lista de espera con MELD real, sin solicitud de vías de excepción. El acceso al puntaje suplementario, y por lo tanto al TH trasplante, depende casi exclusivamente de una correcta caracterización del HCC en los estudios por imágenes. El análisis de los explantes en los candidatos trasplantados por HCC con puntaje suplementario mostró que 22% tenían un estadio mayor que T2, y por lo tanto fuera de los Criterios de Milán, y que un porcentaje no despreciable (9%) no tenían tumor evidenciable. Por lo tanto, para asignar los órganos en forma justa y equitativa a los pacientes con cirrosis y HCC resulta necesario optimizar y homogeneizar el equipamiento y la interpretación de los estudios contrastados trifásicos como la tomografía computada (TC) y la resonancia magnética (RM) entre los distintos centros de TH.
Propuesta 4.1: Equipamiento y detalles técnicos
– Disponer de un equipamiento mínimo compuesto por un tomógrafo computado multidetector de ocho o más pistas y/o un resonador magnético de por lo menos 1.5 Tesla.
– Realizar el estudio respetando criterios previamente establecidos y validados para los estudios contrastados trifásicos de hígado.
Propuesta 4.2: Diagnóstico de hepatocarcinoma en pacientes con cirrosis hepática
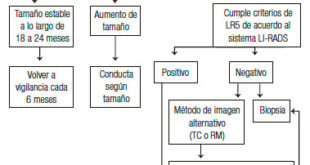
– Adoptar la clasificación de LI-RADS (Liver Imaging Reporting and Data System), un sistema propuesto recientemente por el American College of Radiology que permite estandarizar los informes de los estudios dinámicos (TC o RM) de lesiones hepáticas en pacientes cirróticos o con factores de riesgo para el desarrollo de HCC.
– Un nódulo hepático en pacientes con cirrosis debe considerarse como HCC cuando cumple criterios de LR-5.
– Se define como LR-5 a un nódulo de 10 a 20 mm de diámetro, con wash-in (realce) en la fase arterial y al menos dos de los siguientes tres criterios: cápsula en la fase portal o tardía, wash-out (lavado) en fase portal o tardía o crecimiento del nódulo (>50% en <6 meses o >100% en >6 meses). Si el nódulo es >20 mm de diámetro, se lo considera LR-5 si muestra wash-in en fase arterial y al menos uno de los tres criterios antes mencionados.
– Un solo estudio dinámico con estos hallazgos debe ser considerado como suficiente para el diagnóstico de HCC.
– En caso de duda diagnóstica deben realizarse dos estudios trifásicos contrastados y enviar los informes por separado.
– De existir dos estudios dinámicos, para evaluar el otorgamiento de puntaje suplementario se tendrá en cuenta el informe con mayor número y tamaño de lesiones de acuerdo a la clasificación de LI-RADS.
– Para evaluar si un paciente con HCC cumple o no los Criterios de Milán, solo se considerarán los nódulos catalogados como LR-5. El radiólogo no debe informar si el paciente cumple o no los criterios de Milán.
– Finalmente, los nódulos <1 cm deben ser informados cuando no tienen la misma densidad /señal que los considerados como nódulos de regeneración en cualquiera de las fases.
Propuesta 4.3: Estadificación del hepatocarcinoma
– Debido a la importancia de las imágenes para el diagnóstico y estadificación del HCC, sería conveniente que al solicitar los puntos suplementarios los centros de TH remitan, además del informe radiológico, un disco o dispositivo de almacenamiento con las imágenes (TC y/o RM). De ser así, el INCUCAI debería incluir un radiólogo en el Comité de expertos que otorga las vías de excepción.
– Para obtener puntos suplementarios adicionales, la estadificación radiológica del HCC deberá actualizarse cada tres meses. De no cumplirse con este requisito, el paciente perderá el puntaje de MELD otorgado por excepción (22 puntos).
– Luego de lograrse una regresión del tamaño tumoral del HCC con terapias adyuvantes (dowstaging) se sugiere considerar como candidatos a recibir puntos suplementarios solo a los pacientes que en la evaluación previa al tratamiento instrumentado cumplieran con los criterios de la Universidad de California San Francisco (UCSF) y que luego del tratamiento cumplan con los Criterios de Milán o que, manteniendo el tamaño inicial, tengan respuesta completa al tratamiento de acuerdo a las imágenes (criterios RECIST-Modificado).
-
Reproducibilidad del MELD
La falta de reproducibilidad en la determinación de las tres variables del modelo MELD, creatinina, bilirrubina y protrombina expresada como RIN (Razón Internacional Normatizada) puede generar variaciones significativas en los valores obtenidos en los diferentes centros de TH. Esto a su vez tiene un claro impacto en el acceso al trasplante ya que los pacientes pueden ascender o descender en la lista de espera por un problema metodológico en el cálculo del MELD y no por la mejoría o empeoramiento de su enfermedad o riesgo de muerte, lo cual resulta injusto e inaceptable.
Propuesta 5.1: Referido a los laboratorios de los centros de trasplante hepático
– Exigir que todo centro de TH tenga su laboratorio debidamente certificado y/o acreditada su calidad mediante el International Organization for Standardization (ISO 9000), el College of American Pathologists (CAP) o el Organismo Argentino de Acreditación (OAA).
– Exigir que en los pacientes del grupo sanguíneo “O” con valores de MELD ≥25 o de otros grupos sanguíneos con valores de MELD ≥20 los análisis de laboratorio se realicen exclusivamente en el centro de TH tanto para los ingresos a lista como para las renovaciones.
Propuesta 5.2: Determinación del RIN
– Exigir la utilización de tromboplastinas con un valor de International Sensitivity Index (ISI) <1,4 (idealmente <1,2) y específico para el instrumento utilizado en la detección del coágulo.
– Tomar la muestra con una concentración de citrato de 3,2%.
– Solicitar a los laboratorios de los centros de TH que expresen los valores del tiempo de protrombina en porcentaje de actividad además del RIN.
Propuesta 5.3: Determinación de la bilirrubina y creatinina
– Solicitar a los centros de TH que informen sobre el método de determinación de la creatinina (enzimático o Jaffe modificado) y bilirrubina, el instrumental utilizado y los valores de referencia para cada prueba en mg/dL.
Propuesta 5.4: Utilización del MELD en pacientes anticoagulados
– Exigir la notificación sobre la indicación de anticoagulación en pacientes con cirrosis, incluyendo la droga utilizada.
– Establecer un valor “techo” de 3.0 para el RIN en los pacientes anticoagulados, independientemente de la indicación o de la enfermedad de base.
– Realizar determinaciones de factor 5 y factor 11 en las muestras auditadas por el INCUCAI.
– Evaluar alternativas para reemplazar al MELD en cirróticos anticoagulados como ser el MELD sin RIN, el MELD-factor V o el MELD-factor 11.
Sostén financiero. Los autores no recibieron ningún aporte de becas u otro sostén financiero.
Referencias
- Sistema Nacional de Información de Procuración y Trasplante de la República Argentina (SINTRA); Central de Reportes y Estadísticas (CRESI). En: https://cresi.incucai.gov.ar/IniciarCresiFromSintra.do [Accesed 07/16/2015].
- Registro Argentino de Trasplante Hepático. En: http://sat.org.ar/ index.php/component/content/article/27-contenido-web/165- registro-argentino-de-trasplante-hepatico-sat-incucai [Accesed 07/16/2015].
- Cejas NG, Villamil FG, Lendoire JC, Tagliafichi V, López A, Krogh DH, Soratti CA, Bisigniano L. Improved waiting-list outcomes in Argentina after the adoption of a model for end-stage liver disease-based liver allocation policy. Liver Transpl 2013; 19: 711-720.
- Feng S, Goodrich NP, Bragg-Gresham JL, Dykstra DM, Punch JD, Deb Roy MA, Greenstein SM, Merion RM. Characteristics associated with liver graft failure: the concept of a donor risk index. Am J Transplant 2006; 6: 783-790.
- Dirchwolf M, Ruf AE, Biggins SW, Bisigniano L, Hansen Krogh D, Villamil FG. Donor selection criteria for liver transplantation in Argentina: are current standards too rigorous? Transpl Int 2015; 28: 206-213.
- Braat AE, Blok JJ, Putter H, Adam R, Burroughs AK, Rahmel AO, Porte RJ, Rogiers X, Ringers J. European Liver and Intestine Transplant Association (ELITA) and Eurotransplant Liver Intestine Advisory Committee (ELIAC). The Eurotransplant donor risk index inliver transplantation: ET-DRI. Am J Transplant 2012; 12: 2789-2796.
- Green M, Covington S, Taranto S, Wolfe C, Bell W, Biggins SW, Conti D, DeStefano GD, Domínguez E, Ennis D, Gross T, Klassen-Fischer M, Kotton C, LaPointe-Rudow D, Law Y, Ludrosky K, Menegus M, Morris MI, Nalesnik MA, Pavlakis M, Pruett T, Sifri C, Kaul D. Donor-derived transmission events in 2013: a report of the Organ Procurement Transplant Network Ad Hoc Disease Transmission Advisory Committee. Transplantation 2015; 99: 282-287.
- Miller R, Covington S, Taranto S, Carrico R, Ehsan A, Friedman B, Green M, Ison MG, Kaul D, Kubak B, Lebovitz DJ, Lyon GM, Nalesnik MA, Pruett TL, Teperman L, Vasudev B, Blumberg E. Communication gaps associated with donor-derived infections. Am J Transplant 2015; 15: 259-264.
- Ruf AE, Kremers WK, Chavez LL, Descalzi VI, Podesta LG, Villamil FG. Addition of serum sodium into the MELD score predicts waiting list mortality better than MELD alone. Liver Transpl 2005; 11: 336–343.
- Kim WR, Biggins SW, Kremers WK, Wiesner RH, Kamath PS, Benson JT, Edwards E, Therneau TM. Hyponatremia and mortality among patients on the liver-transplant waiting list. N Engl J Med 2008; 359: 1018-1026.
- Kalra A, Wedd JP, Biggins SW. Changing prioritization for transplantation: MELD-Na, hepatocellular carcinoma exceptions, and more. Curr Opin Organ Transplant 2016 Jan 27. [Epub ahead of print]
- Lim KH, Potts JR, Chetwood J, Goubet S, Verma S. Long-term outcomes after hospitalization with spontaneous bacterial peritonitis. J Dig Dis 2015; 16: 228-240.
- França AV, De Souza JB, Silva CM, Soares EC. Long-term prognosis of cirrhosis after spontaneous bacterial peritonitis treated with ceftriaxone. J Clin Gastroenterol 2001; 33: 295-298.
- Nadim MK, Durand F, Kellum JA, Levitsky J, O’Leary JG, Karvellas CJ, Bajaj JS, Davenport A, Jalan R, Angeli P, Caldwell SH, Fernández J, Francoz C, Garcia-Tsao G, Ginès P, Ison MG, Kramer DJ, Mehta RL, Moreau R, Mulligan D, Olson JC, Pomfret EA, Senzolo M, Steadman RH, Subramanian RM, Vincent JL, Genyk YS. Management of the critically ill patients with cirrhosis: A multidisciplinary perspective. J Hepatol 2016; 64: 717-735.
- Wong RJ, Gish RG, Ahmed A. Hepatic encephalopathy is associated with significantly increased mortality among patients awaiting liver transplantation. Liver Transpl 2014; 20: 1454-1461.
- Wedd J, Bambha KM, Stotts M, Laskey H, Colmenero J, Gralla J, Biggins SW. Stage of cirrhosis predicts the risk of liver-related death in patients with low Model for End-Stage Liver Disease scores and cirrhosis awaiting liver transplantation. Liver Transpl 2014; 20: 1193-1201.
- Servin-Abad L, Tzakis A, Schiff ER, Regev A. Acquired hepatocerebral degeneration in a patient with HCV cirrhosis: complete resolution with subsequent recurrence after liver transplantation. Liver Transpl 2006; 12: 1161-1165.
- Stracciari A, Baldin E, Cretella L, Delaj L, D’Alessandro R, Guarino M. Chronic acquired hepatocerebral degeneration: effects of liver transplantation on neurological manifestations. Neurol Sci 2011; 32: 411-415.
- The Liver Imaging Reporting and Data System (LI-RADS), LI-RADS v2014. En: http://www.acr.org/~/media/ACR/Documents/PDF/QualitySafety/Resources/LIRADS/LIRADS%20 2014%20Flash%20Cards.pdf [Accesed 09/02/2016].
- Mitchell DG, Bruix J, Sherman M, Sirlin CB. LI-RADS (Liver Imaging Reporting and Data System): summary, discussion, and consensus of the LI-RADS Management Working Group and future directions. Hepatology 2015; 61: 1056-1065.
- Trotter JF, Brimhall B, Arjal R, Phillips C. Specific laboratory methodologies achieve higher model for endstage liver disease (MELD) scores for patients listed for liver transplantation. Liver Transpl 2004; 10: 995-1000.
- Lisman T, van Leeuwen Y, Adelmeijer J, Pereboom IT, Haagsma EB, van den Berg AP, Porte RJ. Interlaboratory variability in assessment of the model of end-stage liver disease score. Liver Int 2008; 28: 1344-1351.
- Ruf AE, Martinuzzo ME, Cerrato GS, Chávez LL, Descalzi VI, Yantorno SE, Andriani OC, Podesta LG, Villamil FG. Impact of different thromboplastins on the international normalized ratio and meld score in patients with cirrhosis listed for liver transplantation. Am J Transplant 2004; 4: 515.
- Ruf AE, Martinuzzo M, Cerrato G, Chavez L, Descalzi V, Yantorno S, Podestá L, Villamil F. Factor V is less thromboplastin dependant than INR and is a significant predictor of waitlist mortality. Liver Transpl 2007; 13: S159.
- Cholongitas E, Marelli L, Kerry A, Senzolo M, Goodier DW, Nair D, Thomas M, Patch D, Burroughs AK. Different methods of creatinine measurement significantly affect MELD scores. Liver Transpl 2007; 13: 523-529.
- Goulding C, Cholongitas E, Nair D, Kerry A, Patch D, Akyol M, Walker S, Manas D, Mc Clure D, Smith L, Jamieson N, Oberg I, Cartwright D, Burroughs AK. Assessment of reproducibility of creatinine measurement and MELD scoring in four liver transplant units in the UK. Nephrol Dial Transplant 2010; 25: 960-966.
Correspondencia: Andrés E Ruf
Unidad de Trasplante Hepático. Hospital Británico de Buenos Aires.
Perdriel 74 – CP 1280AEB. Ciudad Autónoma de Buenos Aires, Argentina.
Correo electrónico: aruf@fundieh.org.ar
Acta Gastroenterol Latinoam 2016;46(3): 230-236
 Revista ACTA Órgano Oficial de SAGE
Revista ACTA Órgano Oficial de SAGE